Широкая распространенность ишемической болезни сердца (ИБС), сохраняющаяся на достаточно высоком уровне смертность от ИБС, инвалидизация, снижение качества жизни больных ИБС инициируют поиск и внедрение в клиническую практику новых методов лечения и эффективных фармакологических препаратов. Принципиально новым направлением в терапии ИБС представляется применение кардиоцитопротекторов.
Ишемия миокарда сопровождается дисбалансом между потребностью кардиомиоцитов в кислороде и его реальным обеспечением, что ведет к гипоксии миокарда, и ассоциируется с двумя патологическими нарушениями внутриклеточного метаболизма: снижением продукции молекул АТФ и активацией процессов свободнорадикального окисления (СРО), ведущих к угнетению функциональной активности кардиомиоцитов и непосредственному разрушению клеточных структур [1–4]. Активация СРО обусловлена снижением активности мембранных антиоксидантных энзимов и дефицитом природных антиоксидантов, наличием дислипидемии, при которых содержащиеся в крови в высокой концентрации липопротеиды низкой плотности, триглицериды служат легким субстратом для перекисного окисления [5, 6]. В свою очередь перекисно модифицированные липопротеиды обладают многократно большей атерогенной активностью и ускоряют прогрессирование атеросклероза [7, 8]. В процессе гипоксии создается парадоксальная ситуация: дефицит кислорода инициирует образование большого количества перекисных соединений из недоокисленных вследствии дефицита кислорода жирных кислот, промежуточных метаболитов цикла Кребса [9, 10]. Высокая токсичность перекисей определяется их способностью инактивировать тканевые ферменты, разрушать клеточные и митохондриальные мембраны, инициировать процессы гиперкоагуляции, ускорять распад эндотелиального оксида азота (с образованием токсичного пероксинитрита) [11, 12], что стимулирует дисфункцию сосудистого эндотелия, ангиоспазм [13], уменьшает терапевтическую эффективность антиангинальных средств [14, 15], провоцирует повышение аритмической активности миокарда [16], ведет к поврежданию кардиомиоцитов, способствует расширению зоны некроза [17, 18].
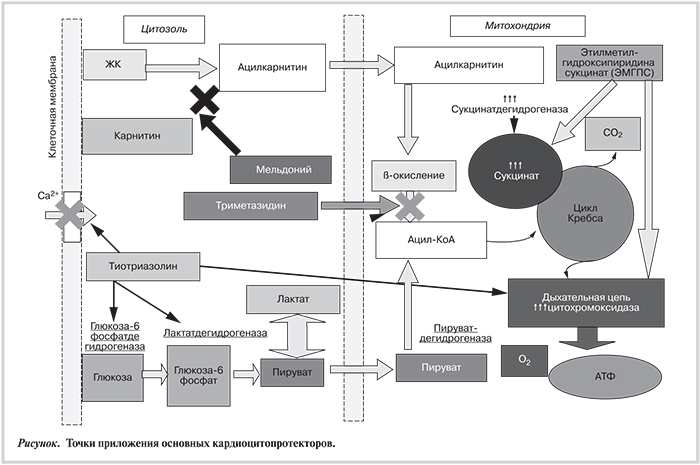
В норме кардиомиоциты получают АТФ за счет расщепления ацетил-КоА (аКоА) в цикле Кребса (см. рисунок), где основными источниками энергии выступают глюкоза и свободные жирные кислоты (СЖК). При достаточной оксигенции в условиях адекватного кровоснабжения большая часть (около 60–80%) КоА образуется за счет β-окисления CЖК, а остальные 20–40% – за счет окисления глюкозы (гликолиза) или лактата, поступающих в клетку из крови. При нормальной оксигенации СЖК служат основным источником АТФ, хотя и потребляют на синтез каждой молекулы на 30–35% кислорода больше, чем при ее синтезе за счет окисления глюкозы. Гликолизный путь синтеза АТФ дополняет жирнокислотный, он способен оперативно и менее кислородозатратно восполнить внезапный дефицит АТФ [19].
Таким образом, при гипоксии синтез АТФ за счет гликолиза представляется более выгодным, в связи с чем действие большинства современных кардиоцитопротекторов основано на стимуляции гликолиза и торможении окисления СЖК.
Использование кардиоцитопротекторов при стабильной стенокардии позволяет улучшить энергообеспеченность кардиомиоцитов, что в условиях хронической ишемии миокарда ведет к увеличению физической толерантности, урежению частоты ангинозных приступов, сокращению суточной потребности в нитроглицерине, повышению эффективности антиангинальных средств [20].
В основе фармакодинамики современных цитопротекторов лежит их способность повышать устойчивость миокарда к гипоксии, увеличивать способность ишемизированных тканей переносить ишемию, сохранять в этих условиях жизнеспособность кардиомиоцитов и восстанавливать их функциональную активность при реоксигенации [21].
История создания кардиопротективных препаратов насчитывает несколько десятилетий. Первые попытки цитопротекции сводились к применению энергоемких субстратов, занимающих промежуточное положение в цикле окисления глюкозы, других энергетических цепей, и потому требующих меньше кислорода для своего окисления и получения молекул АТФ. Опробовалось непосредственное введение в кровоток молекул АТФ и их предшественников (инозин-рибоксин, аденозинамонофосфат) или других соединений, имеющих макроэргические фосфорорганические связи (фосфокреатин – неотон). Позднее была подтверждена бесперспективность такого пути цитопротекции в связи с невозможностью доставки достаточного объема энергоемких субстратов в митохондрии клеток, где происходит энергообмен, или необходимостью постоянного введения огромных доз таких препаратов для обеспечения ишемизированных клеток непосредственно энергетическим субстратом (фосфокреатин).
Современные кардиоцитопротекторы реализут свою активность путем оптимизации синтеза АТФ за счет снижения потребности клетки в кислороде и запуске кислородсберегающих механизмов энергообразования, а также стимуляции анаэробных участков в цепи метаболического синтеза АТФ. Вторым путем реализации цитопротективной активности этих препаратов служат их антиоксидантные свойства, позволяющие снизить интенсивность свободнорадикальных процессов, сократить число свободных активных радикалов кислорода, образующихся в процессе окислительного стресса в период ишемии.
Следует подчеркнуть, что, с учетом фармакодинамики кардиопротекторов, их следует применять исключительно в составе комплексной терапии ИБС, что позволит повысить эффективность проводимой терапии. Монотерапия кардиопротекторами представляется нецелесообразной [22, 23].
Начало широкого клинического использования кардиопротекторов было положено в 1986 г. с появлением триметазидина, который в настоящее время служит «золотым стандартом» среди препаратов кардиопротективного ряда. В основе его действия лежит угнетение β-окисление жирных кислот (ЖК) в митохондриях за счет ингибирования 3-кетоацил-КоА-тиолазы, что стимулирует менее кислородозатратное окисления глюкозы. Препарат снижает продукцию протонов и ограничевает внутриклеточное накопление Na+ и Ca2+, что ингибирует мембранные фосфолипазы, препятствуя разрушению мембранных фосфолипидов, и определяет его мембранстабилизирующие свойства. Аналогичным действием обладает ранолазин, относящийся к неспецифическим блокаторам мембранных натриевых каналов и β-окисления ЖК [24–26].
Применение триметазидина может сопровождаться небольшим накоплением в митохондриях недоокисленных ЖК, служащих потенциальным субстратом для свободнорадикального окисления. Ряд авторов не подтвердили негативность таких процессов, обнаружив способность препарата снижать перекисную модификацию внутриклеточных липидов [27, 28], другие рассматривают такое «замусоривание» митохондрий как нежелательное явление [29].
Таких эффектов лишен кардиоцитопротектор мельдоний, тормозящий образование карнитина (из γ-бутиробетаина за счет конкурентного ингибирования γ-бутиробетаингидроксилазы), который, в свою очередь, обеспечивает транспорт СЖК в митохондрии клетки. В результате активируется менее кислородозатратный цикл получения АТФ путем гликолиза, а в митохондриях опосредованно угнетается β-окисление СЖК и не накапливаются их недоокисленные субстраты. При этом препарат не препятствует транспорту короткоцепочечных ЖК в митохондриии, что исключает дефицит субстрата окисления в случае умеренной гипоксиии [30].
Важно, что увеличение в крови γ-бутиробетаина сопровождантся активацией экспрессии NO-синтазы, индуцирующей генерацию NO, что определяет эндотелийпротективную активность мильдония [31]
Другим представителем кардиопротекторов является этилметилгидроксипиридина сукцинат (ЭМГПС), который в митохондриях стимулирует ключевые сукцинатзависимые фрагменты цикла Кребса, гликолиз, элементы цитохромной цепи, обеспечивая максимальную утилизацию глюкозы. Важно, что ЭМГПС непосредственно не угнетает окисление ЖК (см. рисунок) – так как блокада окисления ЖК при нормальной либо частично сниженной оксигенации может привести к дефициту субстрата окисления и нарушению синтеза АТФ в неишемизированных сегментах миокарда. [32, 33].
Отличительной чертой мельдония и ЭМГПС служит их способность тормозить процессы свободнорадикального окисления, что позволяет использовать его для защиты ишемизированного миокарда от последствий окислительного стресса [34–36].
В настоящее время кардиопротекторы служат важным дополнением комплексной терапии ИБС, отдельные препараты имеют IIb класс В уровень доказательности своей эффективности, входят в качестве средств второй линии в Европейские рекомендации по диагностике и лечению стабильной стенокардии [37].
Одним из новых перспективных кардиопротекторов, появившихся в клинической практике, является тиотриазолин (производное триазола – морфолиний 3-метил-1,2,4 –триазолил-5-тиоацетат). В основе действия препарата лежит комплексный механизм оптимизации энергетического внутриклеточного обмена, направленный на уменьшение потребности в кислороде при синтезе молекул АТФ. Основные точки приложения тиотриазолина:
- интенсификация гликолитического пути синтеза АТФ за счет активации лактатдегидрогеназы, обеспечивающей трансформацию имеющегося в избытке при гипоксии лактата в пируват, включающийся в энергетический цикл в качестве готового промежуточного субстрата, не требующего для своего синтеза кислорода, что относится к анаэробным эффектам препарата;
- активация глюкозо-6-фосфатдегидрогеназной реакции, увеличивающей уровень глюкозо-6-фосфата, что стимулирует первый этап гликолиза и гликолизный путь синтеза АТФ;
- активация малат-аспартатного челночного механизма транспорта через митохондриальную мембрану NADH-зависимых коферментных систем в дыхательную цепь, что способствует активации дыхательной цепи, в частности, цитохром-С-оксидазы в системе окислительного фосфорилирования;
- стабилизация клеточных мембран, восстановление мембранных тиоловых структур и их антиоксидантная защита от свободнорадикального окисления, активирующегося при ишемии (это обеспечивает как непосредственную целостность клеточных мембран, так и препятствует повышенному поступлению в клетку ионов кальция, которые повышают чувствительность β-адренорецепторов миокарда к катехоламинам, что увеличивает потребность миокарда в кислороде, оказывает проаритмогенное действие);
- непосредственная антиоксидантная активность препарата [38–40].
В ряде клинико-экспериментальных исследований установлена способность тиотриазолина повышать активность ключевых антиоксидантных ферментов крови (супероксиддисмутаза, глютатиопероксидаза), оптимизировать метаболизм природного антиоксиданта α-токоферола, в результате в организме снижается интенсивность свободнорадикальных процессов, о чем свидетельствует уменьшение в крови продуктов деградации липопероксидов – диеновых коньюгатов и малонового диальдегида [41, 42], снижается уровень перекисномодифицированного белка. При экспериментальных токсических кардиомиопатиях, вызванных доксорубицином у кроликов, тиотриазолин оказывал кардиопротективное действие, улучшая показатели центральной гемодинамики [43]. Клиническое применение препарата у больных ИБС показало улучшение качества жизни (согласно опросникам), его хорошую переносимость, отсутствие каких-либо существенных побочных эффектов [44].
При оценке активности ряда метаболических ферментов в полиморфноядерных лейкоцитах (сходных по ферментативному спектру с кардиомиоцитами) на фоне приема тиотриазолина у больных с хронической сердечной недостаточностью (ХСН) в сочетании с сахарным диабетом (СД) 2-го типа было отмечено повышение активности лактатдегидрогеназы, сукцинат-дегидрогеназы, α-глицерофосфатдегидрогеназы и никотинамидадениндинуклеотида диафоразы крови, что свидетельствует об энергопротективной активности препарата даже в условиях выраженного угнетения внутриклеточного энергообмена у больных с тяжелой коморбидной патологией [45, 46].Наряду с этим, описана специфическая, не присущая другим кардиоцитопротекторам, способность тиотриазолина активировать транскрипцию ядерного фактора NF-kB, путем стабилизации и защиты от окисления тиореданина, обеспечивающего реализацию механизма транскрипции, что препятствует каскаду апоптозных реакций клетки [47].
Уникальность сочетания указанных выше качеств препарата, определяет яркую, достаточно выраженную кардиоцитопротективную активность тиотриазолина в клинической практике.
Противоишемическое действие тиотриазолина было доказано у больных с постинфарктной стенокардией: в процессе госпитальной реабилитации препарат ускорял восстановление сократительной способности левого желудочка, способствовал ограничению зоны некроза, в том числе и при повторных инфарктах [48]. Отмечена высокая противоишемическая эффективность препарата у лиц пожилого возраста, страдающих стабильной стенокардией [49], при этом препарат улучшал результаты теста с 6-минутной шаговой ходьбой (ТШХ), сокращал частоту ангинозных приступов, потребность в нитроглицерине, что сочеталось с улучшением качества жизни [50].
Клинически доказана эффективность препарата при остром коронарном синдроме: тиотриазолин ускорял регресс ангинозных болей, сокращал число рецидивов инфаркта, ранних и поздних осложнений, снижал частоту желудочковых аритмических эпизодов в острый и подострый периоды инфаркта, ускорял физическую реабилитацию больных в постинфарктном периоде [51, 52].
Как показало наблюдение за 3052 больными с хроническими формами ИБС (стабильная стенокардия, транзиторные экстрасистолии) и сопутствующей артериальной гипертонией (АГ)терапия тиотриазолином в течение 1,5 мес приводила к сокращению доли больных с суправентрикулярными (с 11,4% до 1,3%) и желудочковыми (с 9,1% до 0,83%) экстрасистолами, с синусовой тахикардией (с 3% до 0,4%); существенного влияния на характер фиблилляции предсердий препарат не оказывал [53].
Тиотриазолин улучшал качество жизни больных хронической ИБС, повышал физическую толерантность, сокращал число ангинозых приступов, улучшал праметры систолической функции левого желудочка (ЛЖ) [54].
При сравнительной оценке эффективности тиотриазолина и триметазидина у больных стабильной стенокардией (112 человек) II–III функционального класса, выполненной в международном многоцентровом рандомизированном исследовании [55] было установлено, что при 2-месячном применении тиотриазолин не уступает триметазидину по степени сокращения частоты приступов стенокардии, числу принятых за неделю таблеток нитроглицерина, увеличению продолжительности физической нагрузки при велоэргометрии. Показана способность препарата улучшать у больных стенокардией показатели сократительной функции ЛЖ.
У лиц, страдающих ИБС в сочетании с АГ на фоне приема тиотриазолина, отмечается повышение эффективности ингибиторов АПФ и сартанов, что связывают с улучшением функции сосудистого эндотелия [56]. При стабильной и постинфарктной стенокардии терапия тиотриазолином сопровождалась повышением эффективности антиангинальных средств, что позволяло снижать суточную дозу пролонгированных нитратов [57–60].
Препарат сохраняет свою антиоксидантную активность при коморбидных состояниях – сочетании цереброваскулярной и коронарной патологии атеросклеротического генеза [61].
Получены данные о способности тиотриазолина в составе комплексной терапии улучшать параметры центральной гемодинами и физическую толерантность у больных ХСН ишемического генеза [62]. Тиотриазолин как антиоксидант и стимулятор внутриклеточного энергетического обмена, сохраняет свою эффективность и в состояниях с крайне выраженным нарушением энергетического метаболизма и проявлением окислительного стресса, в частности, при сочетании ХСН вследствии перенесенного Q-инфаркта миокарда (Q-ИМ) с сахарным диабетом 2-го типа в фазе субкомпенсации [63, 64]. В результате плацебо-контролируемого исследования [65] 74 больных ИБС, перенесших Q-ИМ с ХСН II–III функционального класса в сочетании с СД 2-го типа (субкомпенсация), получавших в составе комплексной терапии тиотриазолин (600 мг/сут) в течение 1 мес, установлено увеличение фракции выброса ЛЖ, а также прироста соотношения скоростей раннего и позднего трансмитрального потока (Е/А) и сокращение времени изоволюмического расслабления ЛЖ (IVRT). У больных, получавших тиотриазолин, через 2 мес после отмены препарата сохранялся прирост средней дистанции при ТШХ, не наблюдалось изменений в размере полости ЛЖ и индекса массы миокарда, в то время как у пациентов, принимавших плацебо, наблюдалось прогрессирование ХСН – прогрессивное увеличение полости ЛЖ и отсутствие динамики параметров ТШХ, что свидетельствует о кардиопротективной эффективности препарата у больных с тяжелыми нарушениями сердечной гемодинамики, а также наличии у тиотриазолина достаточно устойчивого, продолжительного эффекта метаболического последействия.
Показана способность тиотриазолина улучшать рузультаты реабилитации больных ИБС [66].
Длительная терапия тиотриазолином оказывает гиполипидемическое действие у больных хроническими формами ИБС на фоне гиперхолестеринемии [67–69].
Анализ полученных на сегодняшний день данных клинических исследований [70, 71] показывает реальную эффективность тиотриазолина в лечении различных проявлений ИБС [72] коморбидных состояний при поражении сердечно-сосудистой системы. Имеющиеся результаты научных исследований позволяют более широко внедрять кардиоцитопротекторы, в частности тиотриазолин, в комплексную терапию ИБС на различных этапах лечебно-профилактических и реабилитационных программ.



