Инсулинорезистентность (ИР) в настоящее время рассматривается не только как состояние, предшествующее развитию сахарного диабета (СД) 2-го типа, но и как один из основных патогенетических звеньев дисфункции эндотелия и атеросклеротического поражения сосудистой стенки [1].
Поскольку измерение уровня инсулина в крови является дорогостоящей методикой, в клинической практике состояние ИР оценивается по наличию совокупности метаболических факторов риска: абдоминальное ожирение, артериальная гипертензия (АГ), нарушения углеводного обмена и дислипидемия с увеличением уровня триглицеридов (ТГ) и снижением уровня холестерина (ХС) липопротеидов высокой плотности (ЛВП) [2, 3].
Известно, что наследственные факторы, наряду с факторами окружающей среды, играют важную роль в развитии метаболических нарушений. Так, по результатам разных исследований, наследственные факторы обусловливают от 10 до 50% всех случаев развития МС [4—6] и связаны с наличием дефекта в генах, регулирующих жировой, углеводный и липидный обмены. Одним из возможных генов-кандидатов является ген аполипопротеина С-III (апо С-III), регулирующий обмен ТГ.
Апо С-III служит структурным компонентом ЛВП и липопротеидов, содержащих ТГ (хиломикроны, липопротеиды очень низкой — ЛОНП и промежуточной плотности) [7]. Основная функция этого апобелка — регуляция метаболизма липопротеидов, богатых ТГ. Под воздействием апо С-III подавляется активность липопротеинлипазы, в результате чего уменьшается липолиз ТГ, что препятствует их обратному поглощению печенью. Это в свою очередь обеспечивает доставку ТГ к периферическим тканям [8, 9]. Повышенная экспрессия гена апо С-III ассоциировалась с развитием гипертриглицеридемии (ГТГ) как в экспериментальных, так и в клинических исследованиях [10, 11]. Увеличение концентрации апо С-III отмечено при некоторых клинических состояниях, включая ожирение, МС, СД 2-го типа и прогрессирование сердечно-сосудистых заболеваний (ССЗ) [12—15].
В то же время регуляция концентрации апо С-III в крови осуществляется при помощи экзогенных и эндогенных факторов, основным из которых является инсулин. Инсулин через участок IRE (insulin responsive element) в промоутерной зоне гена апо С-III подавляет транскрипцию белка и снижает экспрессию белка на 40—50%. При наличии мутации по полиморфизму Т455С гена апо С-III нарушается связывание участка IRE гена с инсулином, что снижает его ингибирующее влияние на экспрессию гена и приводит к накоплению апо С-III и липопротеидов, содержащих ТГ, в крови [16]. В некоторых исследованиях показано, что аллель 455С ассоциировался с увеличением концентрации апо С-III в крови, ГТГ и увеличением риска развития коронарной болезни сердца [17, 18].
Цель исследования — изучить ассоциацию полиморфизма Т455С гена апо С-III с ИР, МС и его компонентами в киргизской этнической группе.
Материал и методы
В исследование были включены 259 пациентов в возрасте от 35 до 70 лет, из которых 162 (108 мужчин, 54 женщин) имели МС. Группу контроля составили 97 сопоставимых по полу и возрасту практически здоровых лиц (75 мужчин, 22 женщин), не наблюдавшихся у кардиолога, без признаков МС, СД 2-го типа и ССЗ. Из исследования исключались лица с тяжелыми ССЗ (тяжелая сердечная недостаточность, мозговой инсульт, злокачественная артериальная гипертензия, инфаркт миокарда) и соматическими заболеваниями (хронические гепатиты, печеночная, почечная недостаточность, диффузные заболевания соединительной ткани); хроническим алкоголизмом; онкологическими заболеваниями; дисфункциями щитовидной железы; беременные женщины.
Всем пациентам было проведено клиническое исследование для уточнения диагноза, включающее сбор жалоб, анамнеза, объективное обследование с измерением систолического (САД) и диастолического (ДАД) артериального давления (АД) и антропометрических показателей (масса тела, рост, окружность талии и бедер). Индекс массы тела (ИМТ) высчитывали по формуле: ИМТ=масса тела (кг)/рост2 (м); ожирение констатировали при ИМТ≥30 кг/м2.
Диагноз МС устанавливали при наличии как минимум трех следующих критериев: артериальная гипертензия (АД≥130/80 мм рт.ст. или прием антигипертензивных препаратов); абдоминальное ожирение (окружность талии≥102 см у мужчин и ≥88 см у женщин); ГТГ (ТГ≥1,7 ммоль/л или прием препаратов, снижающих уровень ТГ); низкий уровень ХС ЛВП (ХС ЛВП<1,03 ммоль/л у мужчин и <1,29 ммоль/л у женщин или прием препаратов, повышающих уровень ХС ЛВП); нарушение углеводного обмена (глюкоза крови натощак ≥5,6 ммоль/л или прием гипогликемических препаратов) [2, 19].
Диагноз коронарной болезни сердца устанавливали на основании данных клинического осмотра (положительный опросник Роуза), наличия изменений на электрокардиограмме (ишемические или рубцовые изменения) и положительного результата нагрузочных проб (по показаниям). Кроме того, у всех включенных в исследование лиц оценивали наличие клинически значимых проявлений нарушений мозгового (дисциркуляторная энцефалопатия, очаговая симптоматика; при необходимости проводили консультацию невропатолога) и периферического кровообращения (жалобы, объективные данные и ослабление пульсации на артериях нижних конечностей с проведением ультразвуковой допплерографии).
Забор крови для определения биохимических показателей и генетического анализа проводили из локтевой вены натощак после 12-часового голодания. Определение глюкозы в крови, общего холестерина (ОХС), ТГ, ХС ЛВП в сыворотке крови осуществляли фотометрическим методом на автоанализаторе Sinhron СХ4-DELTA («Beckman», США). Содержание ХС липопротеидов низкой плотности (ЛНП) вычисляли по формуле Фридвальда [20]. У 140 пациентов проведено определение иммунореактивного инсулина (ИРИ) в сыворотке крови в Hospital Saint-Vincent De Paul Laboratory Hormonologie Pediatrique et Maladies Metaboliques (Париж, Франция), для чего после забора крови отделяли сыворотку и замораживали в жидком азоте и в последующем транспортировали в лабораторию. Определение уровня инсулина проводили методом ELISA. Индекс ИР НОМА высчитывали по формуле: НОМА=(инсулин в сыворотке крови, мкЕД/мл ×глюкоза в плазме, ммоль/л)/22,5. ИР констатировали при индексе НОМА 2,77 и выше.
Кровь для генетического анализа брали одновременно с образцами крови для определения биохимических показателей. ДНК выделяли из клеток крови с использованием набора для экстракции ДНК Nucleon BACC3. Определение полиморфизма Т455С гена апо С-III осуществляли с помощью полимеразной цепной реакции на амплификаторе Hybaid с использованием специфических праймеров (F-5'GGCTGTGAGAGCTCAGCCCT-3′, R-5'TCACACTGGAATTTCAGGCC-3′) и последующей рестрикцией продуктов полимеразной цепной реакции ферментом Fok-1. В результате рестрикции были получены следующие фрагменты: СС — 196 пн, TC — 196+133+129 пн и ТТ — 133+129 пн. Сканирование рестрикционных фрагментов в 3% агаровом геле и анализ полученных результатов осуществляли на денситометре GelDoc-It.
Статистическую обработку данных проводили с помощью программы приложения Statistiсa 8.0 и пакета стандартных программ PRIZM 5. Сравнение переменных с нормальным распределением выполняли при помощи t-критерия Стьюдента (2 группы) и однофакторного дисперсионного анализа (ANOVA) с последующим вторичным анализом данных Ньюмена—Кейлса (3 группы); данные представлены как среднее±стандартное отклонение. Переменные с непараметрическим распределением сравнивали с использованием ANOVA Крускала—Уоллиса (3 группы). Последующий вторичный анализ данных и сравнение 2 групп осуществляли при помощи критерия Манна—Уитни, данные представлены как медиана (25-й процентиль; 75-й процентиль). Соответствие распределения генотипов ожидаемым значениям при равновесии Харди—Вайнберга и наличие связи между качественными переменными оценивали при анализе таблиц сопряженности с использованием χ2-критерия, вычислением отношения шансов (ОШ) и соответствующего 95% доверительного интервала (ДИ). Критерием статистической значимости считали значения р<0,05.
Результаты
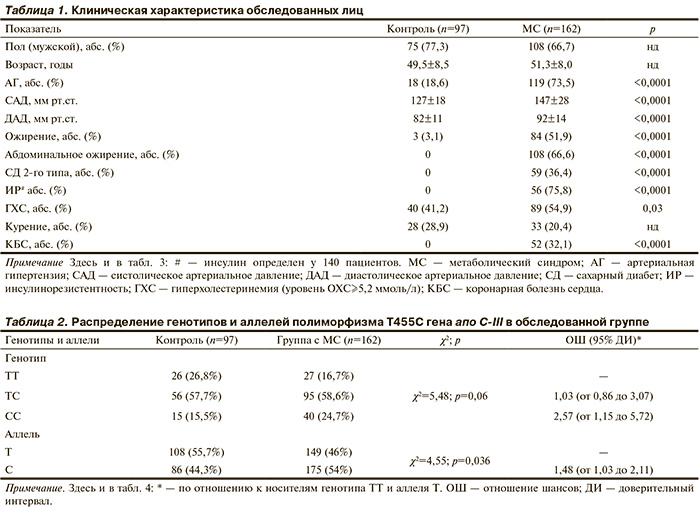
Клиническая характеристика обследованных лиц представлена в табл. 1. По полу, возрасту и таким факторам риска развития ССЗ, как курение и отягощенная наследственность пациенты с МС и группа контроля не различались. Согласно критериям включения пациентов в исследование, в группе с МС показатели, составляющие критерии МС, были достоверно выше.
В обследованной выборке как в группе контроля, так и у пациентов с МС наиболее часто встречался гетерозиготный генотип ТС. Распространенность генотипов в обеих группах находилась в равновесии Харди—Вайнберга. Частота мутантного аллеля 455С составила 0,44 в группе контроля и 0,54 у лиц с МС (р=0,036; табл. 2). Различия в частоте генотипов между группами были близки к достоверным (р=0,06).
Тем не менее вероятность обнаружения МС у носителей генотипа СС была в 2,57 раза выше, чем у гомозигот ТТ (р=0,019).
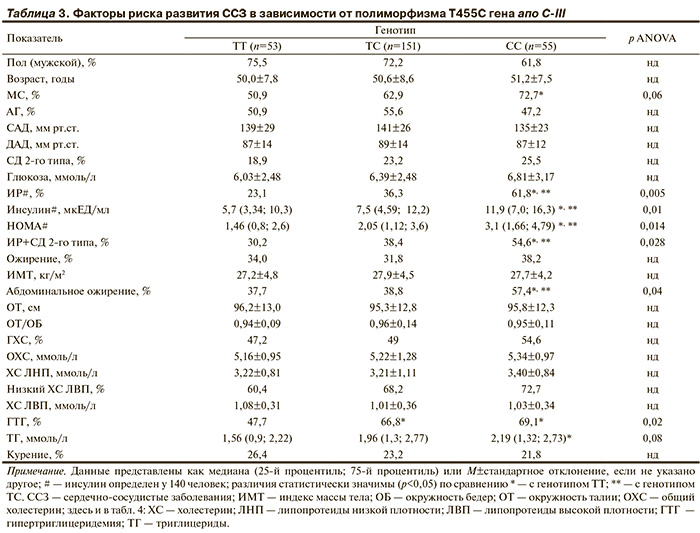
При анализе частоты компонентов МС и факторов риска у носителей различных генотипов отмечено, что у лиц с генотипом СС достоверно чаще обнаруживалась ИР с более высокими уровнями ИРИ в сыворотке крови и индексом НОМА по сравнению как с гомозиготами ТТ, так и с гетерозиготами ТС (табл. 3).
При этом достоверные различия по частоте МС отмечалась только между генотипами СС и ТТ. Частота СД 2-го типа в сравниваемых группах существенно не различалась, однако комбинированный показатель, объединяющий лиц с нарушениями углеводного обмена (ИР+СД) был значительно выше у носителей генотипа СС. Из других составляющих МС статистически значимые различия между генотипами выявлены только для абдоминального ожирения и ГТГ.
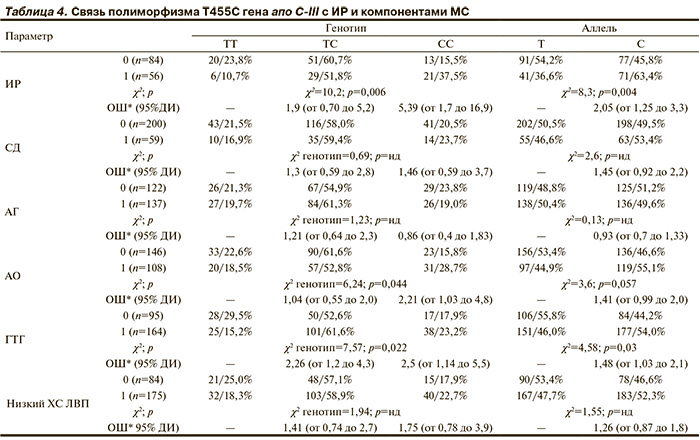
Ассоциация между генотипом Т455С гена апо С-III и наличием ИР, абдоминального ожирения и ГТГ также подтверждена при анализе таблиц сопряженности.
При этом при наличии гомозиготного генотипа СС вероятность обнаружения ИР возрастала в 5,39 раза (р=0,0028), абдоминального ожирения — в 2,21 раза (р=0,04) и ГТГ — в 2,5 раза (р=0,021) по сравнению с таковыми у носителей ТТ.
При сравнении гетерозигот ТС с генотипом ТТ достоверные различия отмечены только по частоте ГТГ (ОШ 2,26; р=0,011; табл. 4).
Обсуждение
В обследованной нами этнически однородной выборке частота мутантного аллеля С455 была достаточно высокой (0,44—0,54) и превалировал гетерозиготный генотип Т455С (0,58). По данным литературы, распространенность аллеля 455С варьируется в различных популяциях.
Так, в европейских исследованиях частота мутантного аллеля составила 0,28—0,37 [17, 21—23]. Ее распространенность была несколько выше в Южной Америке (0,41—0,47) и в азиатских популяциях (0,47 в Китае и 0,54 в Южной Азии) [24—26]. Наибольшая частота аллеля 455С отмечена в Южной Индии — 0,80 [27]. Таким образом, полученные нами данные по распространенности аллеля 455С примерно совпадают с результатами, полученными в других азиатских популяциях.
В нашем исследовании обнаружена связь между носительством генотипа СС гена апо С-III и наличием ИР, МС, а также такими его компонентами, как абдоминальное ожирение и ГТГ. По данным литературы, связь между уровнем апо С-III и развитием ИР неоднозначна. С одной стороны, апо C-III является одним из основных компонентов, содержащих ТГ липопротеидов, и увеличение его концентрации приводит к увеличению концентрации свободных жирных кислот в крови. С другой стороны, инсулин является одним из основных регуляторов секреции апо С-III.
Ген апо С-III локализован в хромосоме 11q23 в одном кластере с апо A-IV и апо А-I; сайт 455 находится в промоутерном участке гена апо С-III, отвечающем за взаимодействие с инсулином [16]. В норме экспрессия гена апо С-III подавляется инсулином через воздействие на IRE и, таким образом, активность гена апо С-III регулируется чувствительностью к инсулину [28]. Показано, что при наличии ИР супрессивное влияние инсулина на экспрессию гена апо С-III снижается и это приводит к повышению концентрации данного апобелка в крови. В исследовании с применением изотопов показано, что концентрация апо С-III в крови у лиц с ИР и ожирением повышается в основном за счет увеличения содержания ЛОНП [29].
Другим возможным механизмом связи между ИР и изучаемым полиморфизмом является регуляция транскрипции гена апо С-III под воздействием PPAR (peroxisome proliferator activated receptor) [30]. В частности, индукция PPARα снижает транскрипцию гена апо С-III [31, 32]. Известно, что состояние ИР ведет к снижению активности PPARs, что также уменьшает супрессивное воздействие на ген апо С-III и приводит к увеличению его концентрации в крови.
Мы не определяли концентрацию апо С-III в крови, тем не менее в других клинических исследованиях обнаружена тесная связь между носительством аллеля 455С и увеличением концентрации апо С-III в сыворотке крови [17, 33]. Известно, что основная физиологическая функция апо С-III в организме — регуляция метаболизма ТГ, поскольку апо С-III является одним из основных белковых компонентов липопротеидов, содержащих ТГ (хиломикроны, ЛОНП, ЛПП) и ЛВП, причем в норме основная часть апо С-III в крови находится в частицах ЛВП, в то время как при наличии ГТГ соотношение меняется в пользу частиц, содержащих ТГ [7, 11, 34]. Ингибирующее влияние апо С-III на липопротеинлипазу приводит к уменьшению липолиза количества частиц, содержащих ТГ, и снижению обратного захвата ТГ печенью. Кроме того, апо С-III может увеличивать синтез и секрецию апо-В и ЛОНП в гепатоцитах [35]. Таким образом, в норме происходит регуляция распределения ТГ и свободных жирных кислот с целью обеспечения доставки энергетического материала к периферическим тканям.
В то же время избыток апо С-III приводит к нарушению выведения ТГ из кровотока. Помимо угнетения поглощения липопротеидов, содержащих ТГ, в печени повышение уровня апо С-III способствует задержке катаболизма и матурации содержащих апо-В частиц [36]. Показано, что в больших концентрациях апо С-III подавляет активность не только липопротеинлипазы, но и печеночной липазы [37], а также может изменять конформационную структуру апо В и апо Е, снижая связывание липопротеидов с соответствующими рецепторами [38].
Кроме того, замедление катаболизма липопротеидов, содержащих ТГ, приводит к нарушению процесса переноса ТГ на частицы ЛВП и формированию нестабильных, богатых ТГ частиц ЛВП, что ускоряет их распад и ассоциируется со снижением концентрации апо А-I и ХС ЛВП в крови [39, 40].
Избыток апо С-III играет также ключевую роль в развитии постпрандиальной ГТГ у лиц с МС. Некоторые исследования обнаружили, что воздействие факторов окружающей среды, в частности диеты и курения, различно у лиц с генетическими вариантами апо С-III [22, 41]. Так, в исследовании О. Olivieri и соавт. [22] показано, что у носителей генотипов Т455Т и Т455С уровень апо С-III в крови снижался при увеличении концентрации w-3 полиненасыщенных жирных кислот, в то время как в подгруппе гомозигот С455С отмечалась противоположная ситуация.
Таким образом, избыток апо С-III приводит к увеличению концентрации ТГ и атерогенных липопротеидов в крови и их аккумуляции в жировой ткани, что способствует возникновению ожирения и запускает механизмы развития ИР. Повышение концентрации ТГ в крови приводит к увеличению энергетического потока к гепатоцитам и снижению чувствительности последних к инсулину и, таким образом, к развитию системной гиперинсулинемии. Нарушение ауторегуляции периферических инсулиновых рецепторов приводит к развитию системной ИР. В то же время избыточное содержание ТГ и свободных жирных кислот в воротной вене приводит к усилению стимуляции β-клеток поджелудочной железы, что приводит к нарушению секреции инсулина и усугубляет ИР [42, 43].
Заключение
Таким образом, в обследованной группе этнических киргизов наиболее часто встречался гетерозиготный генотип ТС.
Носительство мутантного гомозиготного генотипа СС ассоциируется с наличием инсулинорезистентности, метаболического синдрома, повышенным уровнем триглицеридов и абдоминальным ожирением.



