Сердечно-сосудистые заболевания (ССЗ) являются серьезной медико-социальной проблемой, поскольку приводят к высокой инвалидизации и смертности населения. За 2002—2011 гг. отмечено снижение смертности от болезней системы кровообращения во всех субъектах Российской Федерации [1]. Закономерным итогом улучшения качества и своевременности хирургического лечения больных ССЗ является увеличение числа пациентов трудоспособного возраста, подвергшихся коронарному шунтированию (КШ). В связи с этим оказание высокотехнологической специализированной кардиохирургической помощи неизбежно должно сопровождаться этапом послеоперационной реабилитации, главный итог которого заключается в возвращении к жизни и труду полноценного члена общества.
Однако несмотря на доказанную эффективность кардиологической реабилитации [2], только немногие (менее 32% пациентов во всем мире) получают эту жизненно важную медицинскую помощь. В нашей стране ситуация еще более сложная. По результатам международного многоцентрового исследования EUROASPIRE III, в котором принимали участие 22 страны европейского региона, менее 3% российских пациентов с ишемической болезнью сердца (ИБС) проходят курс восстановительного лечения, и этот результат оказался самым плохим среди всех стран-участниц [3].
Проблема отсутствия эффективных программ реабилитации относится не только к пациентам, проживающим в городах и селах, в которых отсутствуют реабилитационные центры, но и к пациентам, проживающим на территориях, где эти центры существуют. Основные причины неучастия пациентов в реабилитационных программах — отсутствие желания посещать реабилитационный центр; проблемы, связанные с транспортом, и другие [4].
Итогом этого у пациента после КШ являются низкие показатели качества жизни, нежелание возвращаться к труду и, соответственно, высокий уровень послеоперационной инвалидности [5].
Таким образом, программы реабилитации должны быть максимально удобными и доступными для пациента. Решение данной проблемы возможно с помощью проведения физических домашних тренировок (ДТ), что позволит включить большее число пациентов в программу физической реабилитации, существенно повысить ее доступность. Однако до сих пор отсутствуют убедительные данные об эффективности и безопасности такого вида реабилитации.
Цель исследования состояла в оценке эффективности и влияния ДТ амбулаторного этапа реабилитации на приверженность к лечению у пациентов, подвергшихся КШ.
Материал и методы
Обследованы 112 мужчин с ИБС, подвергшихся КШ в ФГБНУ НИИ комплексных проблем сердечно-сосудистых заболеваний в 2012 г. Средний возраст пациентов составил 56,4±6,2 года. Всем больным выполнялось плановое КШ в условиях искусственного кровообращения. Исследование соответствовало этическим стандартам биоэтического комитета, разработанным в соответствии с Хельсинкской декларацией Всемирной ассоциации «Этические принципы проведения научных медицинских исследований с участием человека». Пациентами подписано информированное согласие на участие в исследовании.
В исследование не включались больные с неполной реваскуляризацией миокарда, с приступами стенокардии, с низкой (менее 50 Вт) толерантностью к физической нагрузке (ТФН), с артериальной гипертензией (АГ) с уровнем диастолического артериального давления (АД) выше 100 мм рт.ст., со сложными нарушениями ритма и проводимости (пароксизмальной тахикардией, мерцательной аритмией, политопными и групповыми желудочковыми экстрасистолами, атриовентрикулярной блокадой II—III степени), с хронической сердечной недостаточностью (ХСН) III, IV функционального класса (ФК), с подострым течением хронических неспецифических заболеваний легких, послеоперационным тромбофлебитом нижних конечностей, с разнообразными неврологическими нарушениями, которые могли бы препятствовать проведению велотренировок (ВТ).
Все пациенты прошли стационарный (10—12 дней) и санаторный (18 дней) этапы восстановительного лечения. На санаторном этапе реабилитации пациенты получали базисную медикаментозную терапию, лечебную гимнастику, дозированную ходьбу, суховоздушные углекислые ванны, массаж, психотерапию, посещали занятия школы здоровья. Всем больным при окончании санаторного этапа реабилитации представлена информация об оптимальном двигательном режиме, питании, образе жизни и лекарственной терапии.

После окончания санаторного этапа реабилитации (через 1 мес после КШ) пациенты были рандомизированы с помощью таблицы случайных чисел на 3 сопоставимые по основным анамнестическим и исходным клинико-функциональным показателям группы (табл. 1): группа пациентов с контролируемыми ВТ (n=35), группа пациентов с ДТ (n=36) и группа сравнения (n=41) — в этой группе больные получали только медикаментозную терапию и выполняли рекомендации по двигательной активности, представленные при выписке из санатория.
Отказались от участия в исследовании по семейным обстоятельствам 7 (8%) пациентов, попавших при рандомизации в группы с контролируемыми и ДТ.
Всем пациентам на амбулаторном этапе реабилитации назначали статины, антиагрегантную терапию, ингибиторы ангиотензинпревращающего фермента (АПФ), β-адреноблокаторы, при необходимости — антагонисты медленных кальциевых каналов, диуретики. Оценивали состояние больных через 1 и 4 мес, а также через 1 год после КШ.
Пациентам группы с ВТ на амбулаторном этапе реабилитации на базе ФГБНУ НИИ КПССЗ проводили ВТ, используя велотренажер фирмы «Kettler». ВТ начинали с 35—36-го дня после операции и проводили с использованием индивидуально контролируемого метода в положении больного сидя [6]. Процедура тренировки состояла из подготовительного, основного и заключительного периодов. В подготовительный и заключительный периоды проводилось педалирование без включения нагрузки по 5 мин. Мощность основного периода определяли по данным велоэргометрической пробы как 50% от мощности пороговой нагрузки. При адекватной реакции сердечно-сосудистой системы мощность тренирующей нагрузки повышали на 10 Вт до достижения частоты сердечных сокращений (ЧСС) 50—75% от пиковой (максимально достигнутой во время проведения нагрузочного теста). ВТ проводили 3 раза в неделю в течение 3 мес в утренние часы, не ранее чем через 2 ч после еды. Продолжительность основного периода первой процедуры составляла 5 мин, затем ее увеличивали каждый день на 5 мин и доводили до 30 мин. ВТ проводили под контролем АД и ЧСС. В дни, когда ВТ не проводили, рекомендовали самостоятельные тренировки в виде дозированной ходьбы (ДХ) с той же тренирующей мощностью в отсутствие нежелательных явлений и при хорошей переносимости физической нагрузки.
Пациентам группы с ДТ (n=36) рекомендовали ДХ с частотой не менее 3 раз в неделю. Оптимальный темп ходьбы определяли для каждого пациента после велоэргометрии (ВЭМ) по формуле: P=0,042Х + 0,15Y + 65,5, где Х — пороговая мощность нагрузки (кгм/мин); Y — ЧСС на высоте нагрузки. За величину Х принимали мощность последней ступени нагрузки, если больной выполнял ее не менее 1 мин в отсутствие признаков непереносимости. В случае, если выполнение нагрузки последней ступени продолжалось менее 1 мин, в качестве величины Х использовали мощность предыдущей ступени. После выхода из дома сначала рекомендовалось пройти не менее 100 м более медленным темпом, на 10—20 шагов в минуту медленнее темпа ходьбы, который в настоящее время осваивается, а затем перейти на осваиваемый темп. Закончить ходьбу рекомендовалось более медленным темпом. Продолжительность основного периода первой процедуры составляла 5 мин, затем увеличивалась каждый день на 5 мин и доводилась до 30 мин. Целевой считали ЧСС в интервале 50—75% порогового пульса по данным ВЭМ. Оптимальный темп ходьбы пациенты контролировали с помощью шагомера. Контроль за выполнением ДТ осуществлялся с помощью телефонных визитов с периодичностью 1 раз в месяц, во время визитов выясняли выполнение рекомендаций по физическим нагрузкам и их переносимость. Пациенты группы сравнения с рекомендациями по ФН (выполнение аэробных физических тренировок (ФТ) средней интенсивности и длительностью по 30 мин ≥3 раза в неделю) наблюдались в лечебных учреждениях по месту жительства.
 Всем пациентам через 1 мес (перед началом ФТ амбулаторного этапа), через 4 мес (после их окончания) и через 1 год после КШ проводили комплексное обследование. Оценивали клиническое состояние пациента, включавшее оценку наличия и степени выраженности коронарной недостаточности, ХСН, наличие модифицируемых факторов риска (ФР), проводили исследования уровня липидов в крови; эхокардиографию (ЭхоКГ), ТФН определяли при помощи ВЭМ без отмены лекарственной терапии, качество жизни определяли при помощи опросника SF 36. Через 1 год после КШ оценивали клиническое состояние с регистрацией первичных конечных точек. В качестве анализируемых первичных конечных точек были выбраны случаи повторных атеротромботических осложнений: инфаркт миокарда (ИМ), эпизоды нестабильной стенокардии, ишемический инсульт, летальные исходы.
Всем пациентам через 1 мес (перед началом ФТ амбулаторного этапа), через 4 мес (после их окончания) и через 1 год после КШ проводили комплексное обследование. Оценивали клиническое состояние пациента, включавшее оценку наличия и степени выраженности коронарной недостаточности, ХСН, наличие модифицируемых факторов риска (ФР), проводили исследования уровня липидов в крови; эхокардиографию (ЭхоКГ), ТФН определяли при помощи ВЭМ без отмены лекарственной терапии, качество жизни определяли при помощи опросника SF 36. Через 1 год после КШ оценивали клиническое состояние с регистрацией первичных конечных точек. В качестве анализируемых первичных конечных точек были выбраны случаи повторных атеротромботических осложнений: инфаркт миокарда (ИМ), эпизоды нестабильной стенокардии, ишемический инсульт, летальные исходы.
Для статистического анализа использовали компьютерное программное обеспечение Statistica 6.0. Гипотезу о нормальном распределении проверяли с помощью критерия Шапиро—Уилка. Для каждой из непрерывных величин, имевших нормальное распределение, приведены среднее значение (М) и стандартное отклонение (SD). Для величин с ненормальным распределением результаты представлены в виде медианы (Ме) и интерквартильного размаха (25-й процентиль; 75-й процентиль). Анализ таблиц сопряженности проводили с использованием критерия Пирсона (χ²). Сравнение 3 групп выполняли с использованием критерия Крускала—Уоллиса, парное сравнение групп — с помощью теста Манна—Уитни с применением поправки Бонферрони. Для оценки динамики параметров использовали критерий Вилкоксона. Статистически значимыми признавали различия при р<0,05.
Результаты
В течение года ни у одного из пациентов не отмечено ИМ, нарушения мозгового кровообращения, смертельных исходов, увеличения ФК ХСН. В сравниваемых группах не выявлено различий по числу госпитализаций в связи с прогрессированием ИБС. В группе с контролируемыми в медицинском учреждении ВТ один пациент был госпитализирован в связи с прогрессирующей стенокардией, однако по результатам ВЭМ, суточного мониторирования электрокардиограммы (СМ ЭКГ) ишемических изменений у данного пациента выявлено не было, что позволило расценить его как пациента низкого риска по шкале GRACE. В группе пациентов с ДТ также была отмечена одна госпитализация в связи с прогрессирующей стенокардией, и одна — по поводу впервые возникшей фибрилляции предсердий. Из группы пациентов без ВТ у 2 развилась прогрессирующая стенокардия, у 1 из них проведена коронарошунтография с последующим стентированием коронарной артерии.
При анализе результатов ЭхоКГ через 4 мес после КШ отмечалась положительная динамика фракции выброса левого желудочка (ФВ ЛЖ): в группе пациентов с ВТ — с 55,7±3,8 до 62,2±3,9% (p=0,01), в группе с ДТ — с 55,0±5,4 до 61,0±5,7% (p=0,03) и в группе сравнения — с 54,5±4,9 до 58,9±5,7% (p=0,04). У пациентов с контролируемыми ВТ и ДТ динамика этого показателя была более выраженной. Однако различий в сравниваемых группах не было. Через 1 год после КШ достоверных изменений внутрисердечных гемодинамических показателей во всех группах не отмечалось и различий между сравниваемыми группами также не выявлено.
При оценке влияния различных видов реабилитации на показатели ТФН по результатам ВЭМ оказалось, что у пациентов, перенесших КШ, данный показатель через 4 мес после КШ также увеличился во всех 3 группах. У пациентов с ВТ — с 82,7±16,3 до 108,8±19,2 Вт (p=0,01), в группе пациентов с ДТ — с 81,4±17,5 до 99,0±15,3 Вт (p=0,03), в группе сравнения — с 83,1±16,3 до 96,3±12,7 Вт (p=0,04). Однако у пациентов с ВТ через 4 мес данный показатель был достоверно выше (на 12%), чем у пациентов группы сравнения (p=0,04). У пациентов с ДТ отмечалась только тенденция к более высокой ТФН через 4 мес после КШ по сравнению с пациентами группы сравнения (p=0,06). Через 1 год после КШ статистически значимых изменений ТФН по сравнению с показателями через 4 мес во всех группах не отмечалось: у пациентов с ВТ ТФН изменилась со 108,8±19,2 до 100,8±19,6 Вт, в группе с ДТ — с 99,0±15,3 до 103,1±14,2 Вт, в группе сравнения — с 96,3±12,7 до 102,4±16,4 Вт. Таким образом, через 1 год различия по ТФН между группами с различными видами реабилитации нивелировались.
При оценке динамики выраженности модифицируемых кардиоваскулярных ФР установлено, что число курящих пациентов снизилось достоверно только в группе занимающихся ВТ в условиях амбулаторного реабилитационного центра — с 45 до 28% (p=0,02). В группе занимающихся ДТ отмечалась лишь тенденция к снижению количества курящих пациентов (с 46 до 33%; p=0,05). В группе пациентов без ВТ только 3 отказались от курения после операции (с 48 до 39%; p=0,21).
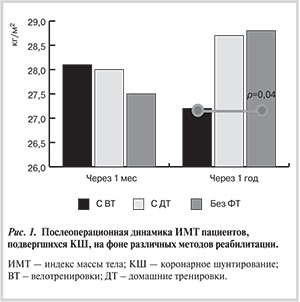
Средний показатель индекса массы тела (ИМТ) в течение года после КШ имел тенденцию к уменьшению только в группе пациентов с ВТ (p=0,05). А в группах с ДТ и сравнения этот показатель имел тенденцию к увеличению, причем более выраженную в группе сравнения. Через 1 год после КШ данный показатель в группе с ВТ был достоверно ниже (рис. 1), чем в группе сравнения (p=0,04).
Среднее значение окружности талии после КШ в группе с ВТ статистически значимо не изменилось (с 98,5±11,3 до 98,0±10,9 см), а в группе с ДТ и без ВТ отмечалась тенденция к его увеличению (c 97,0±10,2 до 99,0±11,6 см и с 97,5±11,1 до 11,0±11,7 см соответственно).
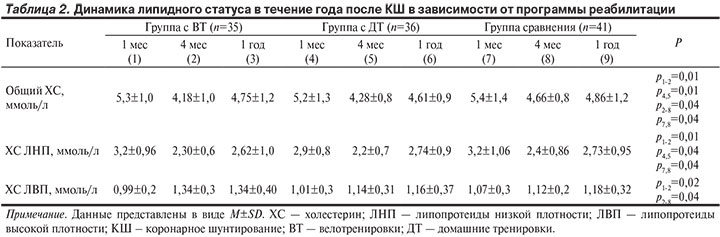
Морфологической основой стенокардии является атеросклероз коронарных артерий. Даже при успешной реваскуляризации пациентам необходимо постоянное лечение с целью предотвращения прогрессирования атеросклероза и развития тромбоза. При оценке влияния различных видов реабилитации на показатели липидного статуса у пациентов, перенесших КШ, оказалось, что через 4 мес после КШ такие показатели, как общий холестерин (ХС), ХС липопротеидов низкой плотности (ЛНП), достоверно снизились во всех 3 группах, однако более выраженно в группах с ВТ и ДТ (табл. 2).
Так, у пациентов с ВТ уровень ХС уменьшился на 21%, в группе с ДТ на 18%, а в группе сравнения только на 14%. Через 4 мес в группе с ВТ уровни ХС были достоверно более низкими, чем в группе сравнения, а по сравнению с группой с ДТ достоверных различий не отмечалось. Содержание ХС ЛНП более выраженно снизилось в группе пациентов, занимавшихся ВТ (на 28%), чем у пациентов с ДТ и в группе сравнения (на 24 и 25% соответственно), однако достоверных различий в сравниваемых группах не отмечалось. Через 1 год после КШ отмечалась тенденция к повышению уровней общего ХС и ХС ЛНП во всех 3 группах, и различия между группами нивелировались. Уровень ХС липопротеидов высокой плотности (ЛВП) увеличился через 4 мес только у пациентов в группе с контролируемыми ВТ (на 26%). В группе с ДТ отмечалась лишь тенденция к его увеличению (на 11%). При этом в группе сравнения данный показатель не изменился. Через 4 мес достоверно лучшие результаты были также в группе с ВТ в сравнении с группой сравнения, а в сравнении с группой с ДТ достоверных различий не отмечалось. Через 1 год различия между группами нивелировались.
При оценке приверженности к медикаментозной терапии до начала амбулаторного этапа реабилитации практически все пациенты принимали β-адреноблокаторы, ингибиторы АПФ/блокаторы рецепторов ангиотензина II (БРА), антитромботические препараты, статины, что, безусловно, связано с пребыванием пациентов в стационарном реабилитационном отделении.
Через 4 мес после операции в группе пациентов с ВТ уменьшилось число принимавших β-адреноблокаторы (с 97 до 82%; p=0,005), антитромботические препараты (со 100 до 88%; p=0,0004), статины (с 97 до 82%; p=0,0005). Число пациентов, принимавших ингибиторы АПФ/БРА, осталось на прежнем уровне. В группе с ДТ также статистически значимо уменьшилось число пациентов, принимающих β-адреноблокаторы (с 97 до 84%; p=0,001), антитромботические препараты (с 97 до 88%; p=0,01), статины (с 9 до 80%; p=0,001). Число пациентов, принимавших ингибиторы АПФ/БРА, уменьшилось незначительно — с 77 до 73%. В группе без ФТ отмечалось еще более выраженное уменьшение числа пациентов, принимавших β-адреноблокаторы (с 100 до 70%; p=0,00001), антитромботические препараты (с 100 до 71%; p=0,00001), статины (с 98 до 65%; p=0,00001). Количество пациентов, принимавших ингибиторы АПФ/БРА, также имело тенденцию к снижению (с 75 до 66%; p=0,12). Необходимо отметить, что через 4 мес после КШ в группе как с ВТ, так и с ДТ, число пациентов, принимавших статины (p=0,007 и p=0,02 соответственно), антитромботические препараты (p=0,003 и p=0,003 соответственно), β-адреноблокаторы (p=0,01 и p=0,04 соответственно), было достоверно больше, чем в группе пациентов без ФТ.
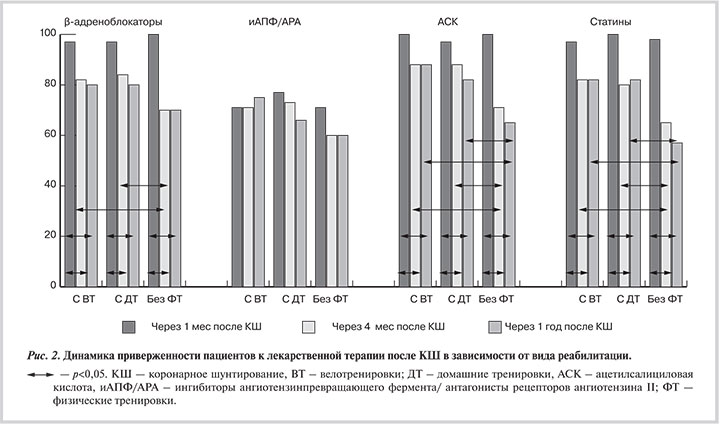
Через 1 год после КШ во всех 3 группах число пациентов, принимавших препараты основных групп, статистически значимо не изменилось по сравнению с результатами через 4 мес. Однако в группе без ФТ отмечалась тенденция к уменьшению числа пациентов, принимавших ацетилсалициловую кислоту (АСК) и статины. В группе с ДТ отмечалась тенденция к уменьшению числа пациентов, принимавших только АСК. У пациентов с ВТ такой тенденции не отмечалось. Кроме того, в группах с ВТ и ДТ было статистически значимо больше пациентов, принимавших АСК и статины, чем у пациентов, не занимавшихся ФТ (рис. 2).
Одной из целей любой реабилитационной программы является сохранение приверженности пациента к активному образу жизни и после завершения контролируемого амбулаторного этапа реабилитации. В связи с этим через 1 год после КШ была проведена оценка приверженности пациентов к выполнению ФТ. Оказалось, что в группе с ВТ 28% пациентов продолжали заниматься ФТ в виде ВТ или ДХ, в группе с ДТ только 9%, а в группе сравнения таких пациентов не было.
Не отмечено ни одного случая осложнений или отказа пациента от предложенной программы физической реабилитации.
Обсуждение
Низкая приверженность к выполнению врачебных назначений и рекомендаций является основным барьером на пути успешного лечения. По данным литературы, каждый четвертый пациент не придерживается предписанной лечащим врачом терапии [7]. Очевидно, что недостаточная приверженность может иметь серьезные и дорогостоящие последствия. Доказано, что она является причиной значительного количества смертельных исходов при ССЗ [8]. Для пациентов, подвергшихся КШ, также доказана важность соблюдения рекомендаций врача как по приему лекарственных препаратов, так и по немедикаментозному контролю ФР развития сердечно-сосудистых осложнений (ССО). В исследовании REACH показано, что несоблюдение пациентами после КШ рекомендаций врача ассоциировалось с более чем в 2 раза высоким риском развития ИМ и смертельного исхода в течение 1 года после проведения КШ [9].
Реабилитация после операции на сердце улучшает самооценку пациентов, клиническую картину [10], способствует изменению ФР развития ССО, повышает ТФН. Ранее доказано, что пациенты, не посещающие программы кардиореабилитации, хуже контролируют АД, показатели липидного статуса, реже отказываются от курения [11]. При участии в программах реабилитации отмечается снижение смертности от всех причин на 20% и сокращение смертности от ССО на 27% [12—14]. Однако, несмотря на доказанную эффективность кардиореабилитации, доля пациентов, участвующих в реабилитационных программах, остается небольшой [4, 15, 16]. Основная масса пациентов выписывается домой после хирургического вмешательства без реабилитации [17].
В связи с этим актуально «перемещение» программы реабилитации в домашние условия пациента, что позволит расширить доступность реабилитационных программ и, соответственно, увеличить число их участников. Кроме того, такая программа реабилитации может оказаться менее дорогостоящей альтернативой традиционным программам на базе лечебно-профилактических учреждений.
По данным ряда авторов, ДТ у больных ИБС дают эффект, аналогичный контролируемым тренировкам [18]. При сравнении влияния ДТ и контролируемых, проводимых на базе лечебно-профилактических учреждений, у пациентов после перенесенного ИМ и/или реваскуляризации миокарда не выявлено различий по показателям смертности и заболеваемости, качества жизни и выраженности основных модифицируемых ФР развития ССО. Однако отсутствие стандартизированных реабилитационных программ на базе лечебно-профилактических учреждений и ДТ делает прямое сравнение этих методик весьма затруднительным [19]. Тем не менее есть основания полагать, что ДТ являются безопасными и эффективными для тех, кто не может участвовать в контролируемых тренировках [20]. Приведенные факты продемонстрированы в зарубежных и единичных отечественных исследованиях [21], Однако ввиду известных различий отечественной и зарубежной медицины, а также различий менталитета жителей разных стран необходимы создание и апробация отечественных программ реабилитации.
Результаты проведенного нами исследования позволили придти к выводу о безопасности ДТ. Так, не было выявлено различий в сравниваемых группах по числу госпитализаций в связи с прогрессированием ИБС. Данные настоящего исследования позволяют сделать вывод о большей эффективности контролируемых ФТ в условиях амбулаторного реабилитационного отделения. У больных всех 3 групп через 4 мес после КШ отмечены положительные изменения внутрисердечной гемодинамики, однако у пациентов с контролируемыми ВТ эти изменения были более выражены. При оценке влияния различных видов реабилитации на показатели ТФН по ВЭМ оказалось, что только контролируемые ВТ способствовали значимому увеличению ТФН, но это преимущество оказалось недолговременным, и через 1 год после хирургического вмешательства различия нивелировались. Однако ДТ оказались более эффективными по модификации основных ФР развития ССО по сравнению с реабилитацией без ФТ. Так, выяснено, что число курящих достоверно сократилось только в группе пациентов, занимавшихся контролируемыми ВТ, у пациентов с ДТ отмечена лишь тенденция к снижению этого показателя, в группе же без ВТ от курения отказались после операции только 3 (p=0,21).
Средний показатель ИМТ в течение 1 года после КШ имел тенденцию к уменьшению только в группе пациентов с ВТ, а в группах с ДТ и без ФТ он имел тенденцию даже к увеличению, причем более выраженную в группе без ФТ. Среднее значение окружности талии после КШ только в группе с ВТ статистически значимо не изменилось, а в группе как с ДТ, так и в группе сравнения отмечалась тенденция к увеличение данного показателя.
При оценке влияния различных видов реабилитации на показатели липидного статуса, такие как ХС, ХС ЛНП, у пациентов, перенесших КШ, не отмечалось достоверных преимуществ при ФТ в отличие от пациентов без ФТ. Такой показатель, как ХС ЛВП, только на фоне 3-месячного курса ВТ стал статистически значимо выше в сравнении с исходными данными, и был выше в сравнении с пациентами без ФТ. Однако эффект ВТ оказался недолговременным, и через 1 год после КШ различия между группами нивелировались.
При оценке приверженности пациентов к продолжению ФТ после КШ оказалось, что самые высокие показатели были в группе с контролируемыми ВТ (28%), у пациентов с ДТ — только 9%, а у пациентов группы сравнения она отсутствовала.
При оценке приверженности к медикаментозной терапии через 4 мес после операции во всех 3 группах отмечалось значительное уменьшение числа принимавших препараты основных групп, а в группе сравнения эта динамика была еще более значимой. Кроме того, через 4 мес после КШ в группе как с ВТ, так и с ДТ число пациентов, принимавших статины, антитромботические препараты, β-адреноблокаторы, было достоверно больше, чем в группе пациентов без ФТ. Через 1 год в группах с ВТ и ДТ также было значимо больше пациентов, принимавших антитромботические препараты и статины, в сравнении с пациентами, не занимавшимися ФТ.
Важным итогом настоящего исследования явился факт краткосрочности эффектов реабилитации. Так, через 1 год после КШ основные различия пациентов с физической реабилитацией и без нее нивелировались. С одной стороны, возможной причиной данной закономерности является небольшая по срокам продолжительность реабилитационных программ, с другой — низкая мотивированность их участников на достижение и сохранение эффекта. Представленные результаты должны явиться основой для совершенствования программ реабилитации даже в условиях медицинских учреждений. Ведь основная задача таких программ состоит в обучении пациентов подходам к эффективной и безопасной вторичной реабилитации. По-видимому, необходимо уделять большее внимание мероприятиям, повышающим мотивированность пациентов соблюдать рекомендации врача.
Вторым итогом исследования явился вывод о более низкой эффективности ДТ, в том числе и в отношении приверженности к медикаментозному и немедикаментозному лечению. Причины таких различий многообразны. Во-первых, в отсутствие непосредственного взаимодействия пациента и медицинского сотрудника в процессе реабилитации, по-видимому, большую роль играет низкая информированность пациентов, выполняющих ДТ, о важности такой реабилитации. Во-вторых, причиной представленных различий могут выступать и отличия методов физической реабилитации (ВТ и ДТ). И, наконец, требуют разработки подходы к дистанционному контролю эффективности таких реабилитационных программ. В зарубежных исследованиях оценивают эффективность ДТ в условиях использования принципов телемедицины, информационно-коммуникационных технологий, а также при активном участии среднего медицинского персонала для контроля эффективности и безопасности такого рода реабилитационных программ, что нами полноценно не использовалось. Еще одним подходом, обеспечивающим повышение эффективности ДТ, является сочетание реабилитации в условиях медицинского учреждения и домашних программ [22, 23].
Заключение
Домашние физические тренировки умеренной интенсивности безопасны, эффективны, легко выполнимы и доступны для большого числа больных. Однако по эффективности влияния на показатели толерантности к физической нагрузке и приверженность к немедикаментозной терапии домашние тренировки уступают контролируемым физическим тренировкам, но имеют преимущество в сравнении с таковыми у пациентов, не занимавшихся физическими тренировками. Домашние физические тренировки должны быть рекомендованы пациентам после коронарного шунтирования при невозможности посещения ими реабилитационного центра. Однако предложенная программа нуждается в усовершенствовании в виде интенсивного мониторинга выполнения рекомендаций для повышения мотивации и приверженности пациентов к лечению.



