Гипертрофическая кардиомиопатия (ГКМП) — наследственное заболевание с генетической предрасположенностью и распространенностью в популяции 0,2% [1, 2]. Вариативность гипертрофии желудочков при ГКМП многообразна [2]. Наиболее неблагоприятной является обструктивная форма ГКМП, при которой часто требуется хирургическое или интервенционное вмешательство [2, 3]. Обструкция выходного отдела левого желудочка (ВОЛЖ) с высоким внутрижелудочковым давлением увеличивает риск внезапной смерти (в результате фибрилляции желудочков), уменьшает отдаленную выживаемость и ухудшает клинический статус у пациентов данной когорты [2—4]. Одним из анатомических вариантов обструктивной ГКМП служит среднежелудочковый тип, распространенность которого достигает 9,4% [5]. «Золотым стандартом» лечения пациентов с обструктивной ГКМП и рефрактерностью к медикаментозной терапии является миоэктомия по Morrow или расширенная (септальная) миоэктомия [2]. Эффективность расширенной миоэктомии при хирургическом лечении больных с обструкцией ВОЛЖ описана в многочисленных исследованиях [2, 6, 7]. Среди пациентов с ГКМП, имеющих показания к хирургической коррекции, обструкция на уровне средней трети межжелудочковой перегородки (МЖП) является анатомически малопригодной для септальной спиртовой абляции и технически сложным вариантом для процедуры миоэктомии ВОЛЖ по Morrow [2, 3]. Данные литературы по применению расширенной миоэктомии при среднежелудочковой обструкции практически отсутствуют и представлены главным образом отдельными сообщениями [8—10].
Цель нашего исследования — оценка эффективности и безопасности применения расширенной миоэктомии у пациентов со среднежелудочковой обструкцией.
Материал и методы
Включение пациентов в исследование осуществляли по принципу «сплошного наблюдения», проспективно [11]. В качестве первичной конечной точки был выбран градиент давления на уровне ВОЛЖ, такие параметры, как отдаленная выживаемость и функциональный класс, определены как вторичные конечные точки. Показания к хирургическому лечению основывались на руководстве по ведению пациентов с обструктивной ГКМП. Проведение исследования было одобрено локальным этическим комитетом нашего института.
В период с января 2010 г. по апрель 2013 г. в Институте обследованы и получили хирургическое лечение 185 больных с обструктивной ГКМП. Среднежелудочковая обструкция наблюдалась в 32 (17,3%) случаях, в исследование включены 29 пациентов (3 отказались от участия в исследовании).
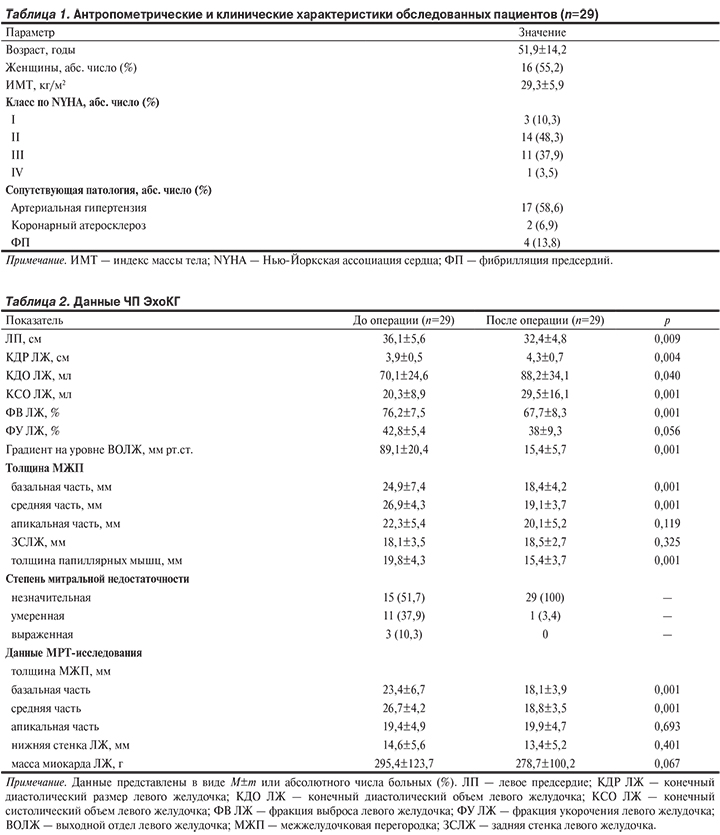
Средний возраст больных составил 51,9±14,2 года (от 22 до 74 лет, табл. 1). Пациенты, включенные в исследование, получали лечение согласно рекомендациям ACCF/AHA по лечению пациентов с ГКМП.
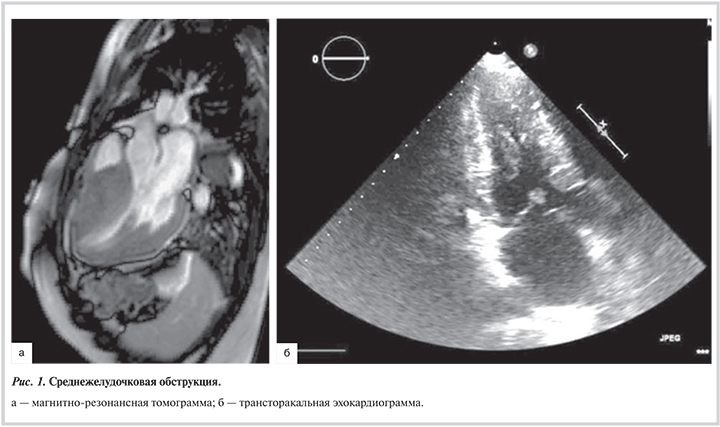
С целью оценки внутрисердечной анатомии всем обследуемым на до- и послеоперационнном этапе выполняли контрастную магнитно-резонансную томографию и чреспищеводную эхокардиографию (ЭхоКГ) (табл. 2, рис. 1).
Всем пациентам выполнен расчет риска внезапной сердечной смерти (ВСС) в течение 5 лет [4] по калькулятору, предложенному Европейским обществом кардиологов [7]. В среднем риск ВСС составил 5,2±0,8.
Технологическая карта операции. Операцию выполняли через срединную стернотомию в условиях искусственного кровообращения и бикавальной канюляции при умеренной гипотермии (33—34 °С). В качестве кардиоплегии использовали раствор кустодиола в объеме 2000 мл. Расширенную миоэктомию выполняли согласно предложенной B. Messmer методике [12]. Визуализацию гипертрофированного участка МЖП осуществляли через трансаортальный доступ.
Первым этапом скальпелем формировали боковые границы зоны резекции: справа — середина правой коронарной створки, слева — свободная стенка левого желудочка на 5 мм латеральнее комиссуры между коронарными створками. Основную линию резекции, соединяющую две предшествующие, проводили параллельно фиброзному кольцу аортального клапана, отступая от него 3—4 мм при базально-среднежелудочковой обструкции (рис. 2, см. цв. вклейку). При изолированной среднежелудочковой обструкции данную линию формировали по данным чреспищеводной ЭхоКГ, и эта линия могла начинаться ниже фиброзного кольца аортального клапана на 10 мм. В отличие от классической тоннелеобразной методики, предложенной Morrow, миокард МЖП иссекали в форме трапеции. Резекцию МЖП по возможности выполняли единым «блоком» миокардиальной ткани.
В ходе хирургической операции в 12 (41,4%) случаях выполнено сочетанное вмешательство на митральном клапане, в 4 (13,8%) случаях — радиочастотная абляция и криодеструкция предсердий по поводу фибрилляции предсердий (ФП) и в одном (3,5%) случае — коронарное шунтирование.
Во всех случаях удалось сохранить митральный клапан. Вмешательства на митральном клапане включали резекцию хорд второго порядка (от 2 до 4) с мобилизацией папиллярных мышц (высвобождение от всех аномальных предлежаний к стенкам ЛЖ) и продольную резекцию папиллярных мышц, если толщина мышцы была более 15 мм (рис. 3, см. цв. вклейку).
Абляцию во всех случаях выполняли по схеме Maze IV с использованием биполярного зажима и криозонда [13]. Особенность выполнения процедуры миоэктомии (в связи с глубоким расположением зоны обструкции) заключалась в использовании длинных эндоскопических инструментов. Эффективность операции оценивали по результатам интраоперационной чреспищеводной ЭхоКГ. Среднее время пережатия аорты составило 84,7±32,2 мин, средняя масса иссеченного миокарда — 7,5±3,6 г.
Всем пациентам после операции проводили электрокардиостимуляцию в режиме DDD или AOO (при сохраненном адекватном атриовентрикулярном проведении), через эпикардиальные электроды с частотой стимуляции от 80 до 86 уд/мин.
До и после операции пациенты получали базисную медикаментозную терапию β-адреноблокаторами в максимально переносимых дозах (метопролол сукцинат в начальной дозе 25 мг/сут с постепенным титрованием до 100 мг/сут). Ориентирами для титрования дозы были артериальное давление не ниже 100/70 мм рт.ст., а также частота сердечных сокращений не ниже 60 уд/мин.
При пароксизмах ФП назначали амиодарон в насыщающей дозе 600 мг/сут в течение 7 дней с последующим приемом 200 мг/сут в течение 3 мес. Вопрос об отмене поддерживающей антиаритмической терапии решали по результатам 3-суточного холтеровского мониторирования электрокардиограммы.
В случаях хирургической абляции субстрата ФП в после-операционном периоде пациентам назначали антикоагулянтную терапию с достижением целевых значений международного нормализованного отношения 2,5—3,0 в течение 3 мес. В случаях изолированной расширенной миоэктомии ВОЛЖ была назначена только ацетилсалициловая кислота в дозе 75 мг в течение 3 мес (период формирования эндотелия в зоне резекции миокарда ВОЛЖ).
Статистический анализ данных проведен с помощью программного пакета Stata/SE 13.0 (StataCorp LP, США). Для проверки статистических гипотез о виде распределения был применен критерий Шапиро—Уилка. Количественные признаки представлены как арифметическое среднее ±SD, качественные признаки — в виде относительных частот в процентах. Анализ выживаемости выполнен по методу Каплана—Майера.
Результаты
Во время пребывания больных в стационаре летальные исходы у них отсутствовали. В 27 (93,1%) случаях расширенная миоэктомия позволила адекватно резецировать МЖП при однократном пережатии аорты. В 2 (6,9%) случаях потребовалось повторное подключение аппарата искусственного кровообращения и выполнение дополнительной резекции МЖП в результате резидуального SAM-синдрома (парадоксальное движение передней митральной створки во время систолы) и остаточной обструкции. Во всех случаях на основании чреспищеводной ЭхоКГ получено достоверное снижение градиента на уровне ВОЛЖ (в среднем до 15,4±5,7 мм рт.ст.; p<0,001). Средняя длительность пребывания больных в палате интенсивной терапии составила 2,2±2,0 (1—5) дня. Специфических осложнений, связанных с процедурой расширенной миоэктомии (дефектов МЖП, разрывов свободной стенки ЛЖ и аортальной недостаточности), зарегистрировано не было.
В 2 (6,9%) случаях выполнена имплантация двухкамерного электрокардиостимулятора из-за развития полной атриовентрикулярной блокады в ходе миоэктомии. Госпитальный период составил 14,2±4,3 дня.
На этапе отдаленного наблюдения обследованы 100% пациентов. Средний период наблюдения составил 18,7 мес (при 95% доверительном интервале — ДИ от 17,2 до 20,3 мес). Рецидивов обструкции ВОЛЖ, нарастания резидуальной митральной недостаточности ≤2+ в отдаленном периоде не отмечено. Анализ Каплана—Майера продемонстрировал 100% отдаленную выживаемость через 12 мес. На этапе отдаленного наблюдения (22 мес) выживаемость составила 95,6% (при 95% ДИ от 72,9 до 99,3%). В отдаленном периоде зарегистрирован 1 (6,9%) летальный исход: в результате ВСС без каких-либо причин по данным патологоанатомического вскрытии. Регрессионный анализ Кокса продемонстрировал отсутствие предикторов летальности.
На этапе отдаленного наблюдения у 92,6% пациентов отмечен I—II функциональный класс по классификации NYHA. Качество жизни оценивалось с использованием опросника SF-36. В отдаленном периоде оценки работоспособности в профессиональной сфере, выполнения работы по дому были статистически значимо выше по всем параметрам (p<0,001; рис. 4, см. цв. вклейку).
В контрольных обследованиях выполнялся повторный расчет риска ВСС в течение 5 лет, который снизился до 2,7±0,9 и свидетельствовал об отсутствии показаний к имплантации кардиовертера-дефибриллятора.
Обсуждение
В настоящей работе представлены результаты, демонстрирующие возможности применения расширенной миоэктомии в устранении среднежелудочковой обструкции у пациентов с ГКМП.
На настоящем этапе в хирургическом лечении больных с обструктивной ГКМП применяются два основных метода: спиртовая редукция миокарда и различные варианты септальной миоэктомии, а также протезирование митрального клапана [2, 7]. Транскатетерная спиртовая редукция миокарда снижает градиент на уровне ВОЛЖ на этапе непосредственного наблюдения, однако имеет высокий процент рецидива обструкции и ограниченные анатомические показания (наличие крупных септальных артерий, базальный непротяженный уровень обструкции, толщина МЖП в зоне обструкции менее 25 мм), что ограничивает использование данного метода у пациентов со среднежелудочковой обструкцией [2, 7, 14]. Классический вариант миоэктомии, предложенный A.G. Morrow, позволяет более адекватно устранять обструкцию, однако неглубокое (менее 3 см) продольное иссечение миокарда МЖП также влечет остаточную обструкцию в средней трети МЖП [2, 7, 12].
Разработанная B. Messmer методика «расширенной миоэктомии» позволяет устранять обструкцию не только в базальной части, но и в средней трети МЖП [12]. Опубликованные работы M.K. Dearani и S.K. Balaram отражают улучшение функционального статуса, увеличение продолжительности жизни и снижение риска ВСС [15, 16].
Обладая наибольшим опытом в хирургическом лечении пациентов с обструктивной ГКМП, коллеги из клиники Мейо предложили трансапикальный поход для пациентов со среднежелудочковой обструкцией с целью оптимальной визуализации и выполнения адекватной миоэктомии средней части МЖП [17, 18]. Авторы показали высокую эффективность методики [17, 18], однако мы считаем, что данная технология сопряжена с рядом недостатков. Создание достаточно большого (около 6 см) рубца на стенке ЛЖ снижает контрактильную функцию миокарда, а формирование линейного двухрядного шва дополнительно приводит к редукции объема ЛЖ, индекс которого и так меньше нормы.
В нашей группе пациентов со среднежелудочковым уровнем обструкции во всех запланированных случаях удалось адекватно выполнить процедуру миоэктомии, что делает ее сопоставимой по эффективности с трансапикальным подходом [18]. Для достижения труднодоступной зоны МЖП в средней и верхушечной части мы используем длинный эндоскопический инструментарий, разработанный для мини-инвазивной хирургии митрального клапана. Данная методика позволила выполнить глубокую миоэктомию (апикально, до 6—7 см ниже створок аортального клапана) с использованием стандартного трансаортального доступа, сохранив целостность миокарда ЛЖ. Процент осложнений, связанных с процедурой, не превышал опубликованные ранее данные, а также был сопоставим с результатами миоэктомии у пациентов, имеющих базальный уровень обструкции [2, 7].
Отдаленная выживаемость через 22 мес в нашей когорте пациентов составила 95,6%, что совпадает с данными европейского многоцентрового исследования [19]. Однако регрессионный анализ Кокса не выявил предикторов летального исхода, что может быть связано с ограниченным числом наблюдений и недостаточным по времени отдаленным периодом. Результаты отдаленного наблюдения показали статистически значимое улучшение функционального статуса и качества жизни пациентов, что также согласуется с основными публикациями по данной тематике [15, 16].
Учитывая, что при расчете риска ВСС основными критериями для имплантации кардиовертера-дефибриллятора являются толщина МЖП, градиент на уровне ВОЛЖ и анамнез (наличие синкопальных состояний или зарегистрированных угрожающих жизни нарушений ритма), а после хирургического вмешательства данные параметры значительно нивелируются, был выполнен перерасчет риска ВСС у пациентов данной когорты. Следует отметить, что в рекомендациях указывается на необходимость повторных расчетов ВСС после смены соматического статуса или 1 раз в полгода. При начальных расчетах средний риск ВСС у наших пациентов составил 5,2±0,8, что свидетельствует о возможной имплантации кардиовертера-дефибриллятора, однако после процедуры он составил 2,9±0,7, а на момент контрольного перерасчета — 2,7±0,9, что отражает отсутствие четких показаний к имплантации дефибриллятора. В настоящее время в литературе нет четких рекомендаций относительно расчета риска ВСС у пациентов, которым в анамнезе выполнялась миоэктомия по поводу обструктивной ГКМП.
Заключение
Гипертрофическая кардиомиопатия является сложным наследственным заболеванием, которое в ряде случаев может сопровождаться среднежелудочковой обструкцией с выраженными клиническими проявлениями. Процедура расширенной миоэктомии позволяет безопасно и эффективно устранить среднежелудочковую обструкцию, улучшая функциональный статус пациентов как в раннем, так и в отдаленном послеоперационном периодах.
Ограничение
Результаты применения расширенной миоэктомии, согласно полученным данным, могут рассматриваться для идентичной группы со сроком наблюдения не больше 2 лет. Для полноты исследования требуется оценка отдаленных результатов с периодом наблюдения в 5 лет.
Исследование выполнено при поддержке гранта Президента Российской Федерации МД-5046.2015.7.
Авторы заявляют об отсутствии конфликтов интересов, связанных исследованием.



