Число пациентов с сахарным диабетом (СД) продолжает увеличиваться в индустриальном обществе в силу главным образом изменений в образе жизни (чрезмерное потребление калорий и жиров, снижение физической активности). Предполагается, что во всем мире число заболевших СД взрослых будет превышать 200 000 000 в течение ближайших 10 лет [1]. Неблагоприятный прогноз для больных СД в основном связан с развитием хронической сердечной недостаточности (ХСН) [2]. Более 1/3 больных СД 2-го типа умирают от сердечной недостаточности (СН), при этом наличие СД связано с 2—5-кратным увеличением риска развития СН, которая является наиболее распространенным диагнозом при госпитализации у пациентов с СД [3—5]. Сердечная и почечная недостаточность служат основными факторами, определяющими исход у пациентов с сочетанием СД и ишемической болезни сердца (ИБС) [6].
Хотя понятно, что существует ассоциация между СД и СН и худшим прогнозом для пациентов с СД и СН, патофизиологическое объяснение этой ассоциации менее ясно. Наиболее вероятным объяснением является наличие кардиотоксической триады: диабетическая кардиомиопатия (КМП), ИБС и артериальная гипертензия (АГ) / гипертрофия желудочков. Однако и другие механизмы в виде измененной экспрессии генов, вегетативной дисфункции играют важную роль в развитии и прогрессировании СН у больных СД [7]. Становится все более ясно, что СД сам вызывает систолическую и диастолическую СН, независимо от сопутствующего заболевания коронарных артерий (КА).
Лечение ИБС у пациентов с СД 2-го типа остается большой проблемой для кардиологов [8]. Несмотря на значительные достижения терапевтических и инвазивных методов лечения, включая имплантацию стентов с лекарственным покрытием, эти пациенты все еще имеют высокую инвалидизацию и смертность в результате прогрессирования атеросклероза и ХСН даже после чрескожной или хирургической реваскуляризации [9]. Рандомизированные клинические исследования сообщают об уровне смертности более 19,6% после операции аортокоронарного шунтирования — маммарокоронарного шунтирования и до 35% после ангиопластики в этой популяции [10].
Однако пока не существует конкретных стратегий профилактики, диагностики и лечения СН у пациентов с СД. Данные об эффективности и переносимости препаратов, используемых при лечении пациентов с СН и СД, являются в основном ограниченным анализом подгрупп в рандомизированных клинических исследованиях с частыми проблемами недостаточной статистической мощности. Тем не менее этот анализ подгрупп последних исследований, проведенный у больных СД, которые были госпитализированы по поводу СН, показал разную эффективность стандартной терапии и большую склонность к развитию побочных эффектов по сравнению с таковыми у пациентов с той же степенью СН, но без СД. Необходимы дальнейшие исследования для разработки целенаправленной терапии у пациентов с сопутствующими СН и СД. Препараты, направленные на изменение метаболизма, являются потенциально многообещающими для лечения СН у больных СД.
У пациентов с СД и ИБС метаболические изменения, происходящие в результате несоответствия между кровоснабжением и метаболическими потребностями сердца, усугубляются метаболическими изменениями, вызванными СД [11, 12]. Энергетическими субстратами кардиомиоцитов служат глюкоза и свободные жирные кислоты (СЖК). При стрессе и ишемии происходит сдвиг метаболизма в сторону использования СЖК, что является неоптимальным с точки зрения использования кислорода. Именно увеличение поглощения и использования СЖК служит одной из основных причин повышенной восприимчивости «диабетического сердца» к ишемии миокарда и значительного снижения функции миокарда для данного количества ишемии по сравнению с «недиабетическим сердцем» [11]. Ожидаемое количество молей АТФ, производимых на 1 моль потребляемого кислорода, на 12% больше при окислении глюкозы, чем при окислении СЖК, поэтому улучшение метаболизма глюкозы может увеличить производство АТФ до 30% [13]. В связи с изложенным модуляция метаболизма миокардиальных СЖК представляет ключевую задачу метаболических вмешательств у пациентов с ИБС и СД.
Ранее было показано, что частичный ингибитор окисления СЖК в миокарде триметазидин обладает антиишемическим свойством, снижая частоту приступов стенокардии, потребность в короткодействующих нитратах, улучшая переносимость физических нагрузок в сочетании с антиангинальными препаратами гемодинамического действия [14, 15]. Триметазидин является ингибитором 3-кетоацилкоэнзим А тиолазы (3-КАТ), который сдвигает получение энергии в кардиомиоците от окисления СЖК к окислению глюкозы путем ингибирования митохондриальной длинноцепочечной 3-КАТ[13]. Кроме того, доказано, что триметазидин ослабляет окислительный стресс [16], уменьшает потребление кислорода и улучшает обмен веществ митохондрий и работу сердца в условиях ишемии [17]. Есть сообщения об ослаблении активности нейтрофилов под воздействием триметазидина, что защищает сердце от опосредованной нейтрофилами постишемической травмы [18].
По нашему мнению, с точки зрения сохранения функции левого желудочка (ЛЖ), наиболее перспективным является фармакоинвазивный подход к лечению пациентов со стенозирующим атеросклерозом КА на фоне нарушений углеводного обмена. Этот подход заключается в сочетании реваскуляризации миокарда и метаболической кардиопротекции, добавленной к стандартной терапии ИБС и ХСН.
Целью нашего исследования была оценка влияния препарата метаболического действия триметазидина модифицированного высвобождения на функцию ЛЖ у пациентов со стабильной ИБС на фоне нарушений углеводного обмена, перенесших плановые эндоваскулярные вмешательства на КА.
Материал и методы
Проведено открытое проспективное рандомизированное контролируемое клиническое исследование, включившее 63 пациентов со стабильной формой ИБС, которым на базе отделения реабилитации НИИ кардиологии СО РАМН в течение 2010—2011 гг. выполнено эндоваскулярное вмешательство на КА. Критериями включения в исследование было наличие показаний к эндоваскулярной реваскуляризации миокарда согласно Национальным рекомендациям по диагностике и лечению стабильной стенокардии за 2008 г. [19], наличие фоновых нарушений углеводного обмена в стадии компенсации (СД 2-го типа или нарушение толерантности к глюкозе по данным теста на толерантность к глюкозе). Методом закрытых конвертов пациенты, подписавшие добровольное информированное согласие на участие в исследовании, были распределены в 2 группы. Пациенты основной группы (1-я группа, n=32) в течение 2 нед перед вмешательством и в течение 1 года последующего наблюдения получали триметазидин модифицированного высвобождения (предуктал МВ, «Лаборатории Сервье», Франция) по 35 мг 2 раза в сутки в дополнение к стандартной терапии. Пациентам контрольной группы (2-я группа, n=31) чрескожное коронарное вмешательство (ЧКВ) и последующее наблюдение проводилось на фоне стандартной терапии без применения препаратов метаболического действия.
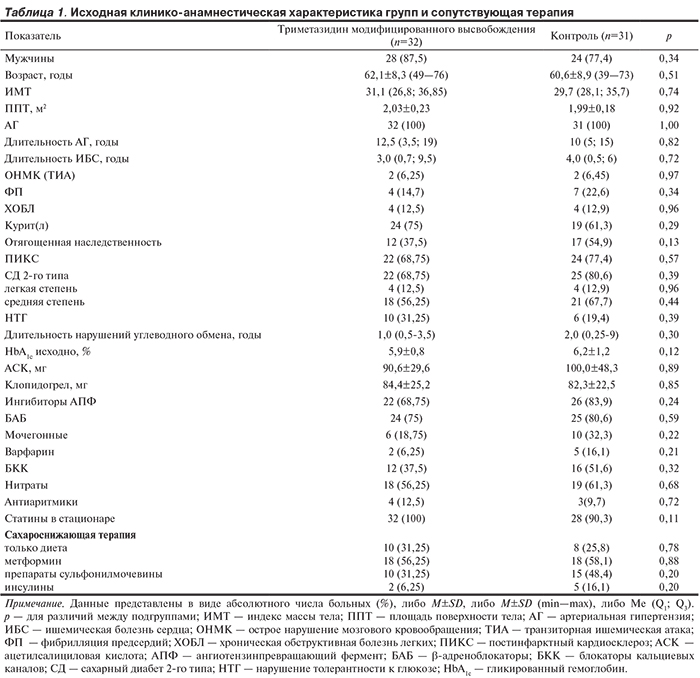
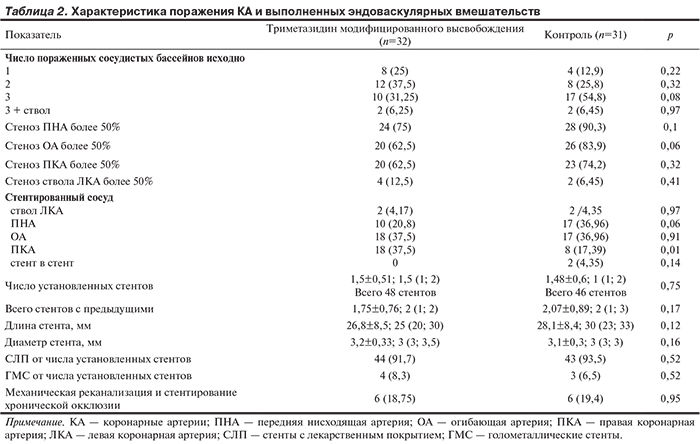
По тяжести ишемии миокарда, клинико-анамнестическим показателям, выраженности углеводных расстройств, сопутствующей терапии исходно группы не различались (табл. 1). Характеристика поражения КА и выполненных эндоваскулярных вмешательств представлена в табл. 2. Эхокардиографию (ЭхоКГ) проводили дважды: исходно и через 12 мес проспективного наблюдения. ЭхоКГ выполняли на аппарате Acuson Sequoja 512 в соответствии с рекомендациями Американской ассоциации эхокардиографии по стандартным методикам. Объемы ЛЖ измеряли с использованием бипланового метода дисков (модифицированный метод Симпсона) в апикальных 4- и 2-камерных позициях в конце диастолы и систолы с последующим вычислением конечного диастолического индекса (КДИ), конечного систолического индекса (КСИ), фракции выброса (ФВ) ЛЖ. Ударный объем ЛЖ определяли с помощью допплер-ЭхоКГ, затем индексировали к площади поверхности тела. Нарушение локальной сократимости ЛЖ оценивали с использованием 16-сегментарной модели по балльной системе в зависимости от степени сократимости с вычислением индекса нарушения локальной сократимости (ИНЛС) [20, 21].
Статистическую обработку данных проводили с помощью программы Statistica, версия 7,0. Правильность распределения выборки проверяли с помощью теста Колмогорова—Смирнова. Сжатие данных представлено в виде M±SD, где M — среднее арифметическое, SD — стандартное отклонение и Me (Q1; Q3), где Me — медиана, Q1 и Q3 — нижний и верхний квартили. Достоверность различий при нормальном распределении определяли с помощью критерия Стьюдента. В остальных случаях использовали критерии Манна—Уитни, Крускала—Уоллиса, Вилкоксона. Анализ различия частот проводили при помощи критерия Фишера. Критический уровень значимости р при проверке статистических гипотез принимали равным 0,05.
Результаты
Ангиографический успех ЧКВ в обеих группах составил 100%. Клинически значимых сердечно-сосудистых осложнений (смерть, острый коронарный синдром — ОКС, острое нарушение мозгового кровообращения — ОНМК) в течение госпитального периода и последующего 12-месячного периода наблюдения у пациентов обследуемых групп не было. Все больные выписаны из стационара в удовлетворительном состоянии. Статистически значимых различий между группами по количеству острых осложнений не выявлено.
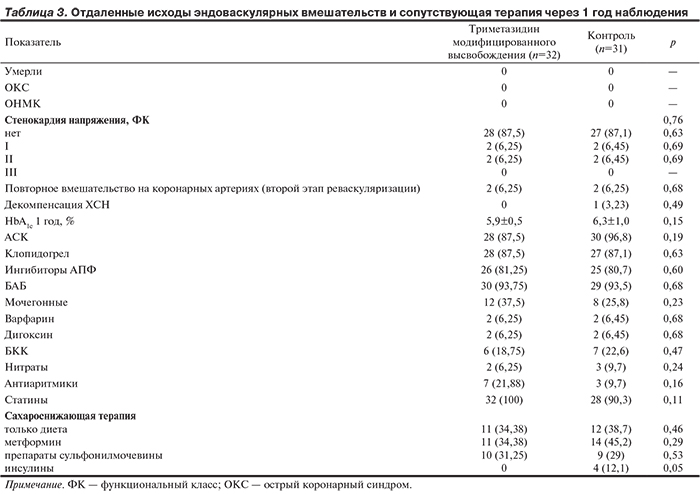
Отдаленные результаты ЧКВ в группах наблюдения представлены в табл. 3. Тяжесть клинических проявлений стенокардии напряжения в обеих группах через 12 мес достоверно не различалась. Повторные вмешательства на КА, как второй этап реваскуляризации, в течение года были выполнены 4 пациентам (по 2 в каждой группе), что составило 6,4% всех больных, включенных в исследование. Тяжелая декомпенсация ХСН, потребовавшая экстренной госпитализации, за время наблюдения произошла у 1 пациента в группе контроля.
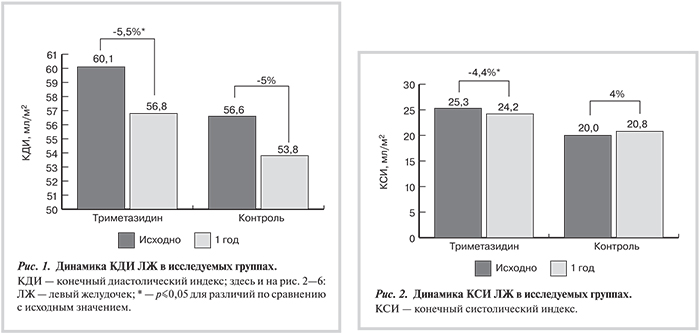
яКСИ оказался более чувствительным маркером положительного влияния метаболического цитопротектора после эндоваскулярной реваскуляризации. В 1-й группе выявлено достоверное снижение КСИ через 1 год после ЧКВ по сравнению с исходным — с 25,3 (19,8; 31,1) мл/м2 до 24,2 (7,8; 30,5) мл/м2 через 12 мес (р≤0,05). В контрольной группе выявлено недостоверное увеличение КСИ по абсолютным значениям к концу года проспективного наблюдения — с 20 (16,5; 26) мл/м2 до 20,8 (15,9; 25,9) мл/м2 через 12 мес (р>0,05). Динамика КСИ ЛЖ в исследуемых группах представлена на рис. 2.
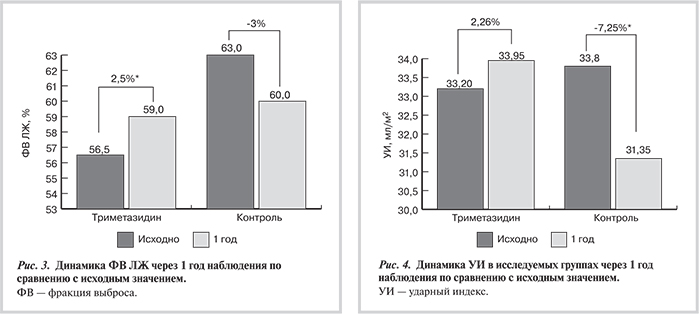
Интегральный показатель глобальной систолической функции миокарда — ФВ ЛЖ также статистически значимо увеличился в основной группе под влиянием длительной метаболической терапии триметазидином модифицированного высвобождения — с 56,5 (52; 63,5) % до 59 (55; 63) % через 12 мес (р≤0,05). Во 2-й группе, несмотря на выполненную реваскуляризацию миокарда, наблюдалось статистически незначимое снижение ФВ ЛЖ к концу 12-месячного периода наблюдения — с 63 (58; 65)% до 60 (55; 67) % через 12 мес (р>0,05). Динамика ФВ ЛЖ через 1 год наблюдения по сравнению с исходным значением представлена на рис. 3.
 Один из показателей насосной функции миокарда — ударный индекс (УИ, отражает объем крови, который выбросил ЛЖ в систолу, индексированный к площади поверхности тела), у пациентов контрольной группы достоверно снизился в течение года, несмотря на выполненное ЧКВ — с 33,8±5,87 мл/м2 до 31,35±4,87 мл/м2 через 12 мес (р≤0,05). Длительная терапия триметазидином способствовала увеличению УИ по абсолютным значениям, хотя статистическую значимость этого положительного влияния подтвердить не удалось — с 33,21±5,98 мл/м2 до 33,95±4,79 мл/м2 через 12 мес (р>0,05). Динамика УИ в исследуемых группах через 1 год наблюдения представлена на рис. 4.
Один из показателей насосной функции миокарда — ударный индекс (УИ, отражает объем крови, который выбросил ЛЖ в систолу, индексированный к площади поверхности тела), у пациентов контрольной группы достоверно снизился в течение года, несмотря на выполненное ЧКВ — с 33,8±5,87 мл/м2 до 31,35±4,87 мл/м2 через 12 мес (р≤0,05). Длительная терапия триметазидином способствовала увеличению УИ по абсолютным значениям, хотя статистическую значимость этого положительного влияния подтвердить не удалось — с 33,21±5,98 мл/м2 до 33,95±4,79 мл/м2 через 12 мес (р>0,05). Динамика УИ в исследуемых группах через 1 год наблюдения представлена на рис. 4.
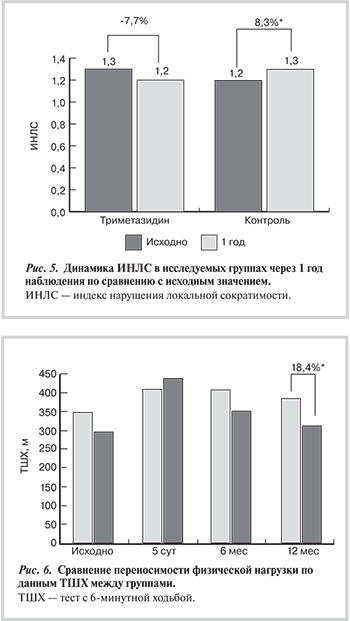
ИНЛС, использованный для количественной оценки локальной сократимости миокарда ЛЖ, недостоверно снизился в основной группе к концу исследования — с 1,3±0,3 до 1,2±0,3 через 12 мес наблюдения (р>0,05). Во 2-й группе отсутствие миокардиальной цитопротекции привело к ухудшению локальной сократимости через 1 год наблюдения, что проявилось статистически значимым увеличением ИНЛС по сравнению с исходным — с 1,2±0,3 до 1,3±0,4 через 12 мес (р≤0,05). Динамика ИНЛС в исследуемых группах через 1 год наблюдения по сравнению с исходным представлена на рис. 5.
Положительное влияние триметазидина модифицированного высвобождения на глобальную и локальную сократимость ЛЖ, выявленное в нашем исследовании, клинически реализовалось в лучшей переносимости пациентами физической нагрузки в основной группе по сравнению с контролем по данным теста с 6-минутной ходьбой (ТШХ) — исходно 348,8±114,8 м в 1-й группе по сравнению с 300,5±120,9 м во 2-й группе (р=0,12); через 12 мес 385,4±109,8 м в 1-й группе в сравнении с 314,7±141,6 м во 2-й группе (р=0,044). Сравнение переносимости физической нагрузки между группами по данным ТШХ представлено на рис. 6.
Обсуждение
Ранее рядом авторов было показано, что результатом эндоваскулярного вмешательства на КА в отдаленный период является достоверное снижение функционального класса стенокардии и недостаточности кровообращения, что подтверждается улучшением показателей сократительной и насосной функции миокарда по данным ЭхоКГ [22, 23]. Однако наличие сопутствующего СД у пациентов, подвергнутых эндоваскулярному лечению, сопряжено с отсутствием клинического улучшения течения ХСН и прогрессирующим снижением общей сократимости миокарда в отдаленный период [22].
Как отмечалось ранее, у пациентов с СД к снижению функции ЛЖ при острых и хронических ситуациях приводит кардиотоксическая триада: ИБС, АГ/гипертрофия ЛЖ и диабетическая КМП. Совместно эти 3 условия способствуют анатомическим, физиологическим и биохимическим изменениям в кардиомиоците. Снижение функции миокарда ЛЖ стимулирует ренин-ангиотензин-альдостероновую и симпатическую часть вегетативной нервной системы, что способствует дальнейшему повреждению миокарда и в отсутствие лечения приводит к ремоделированию миокарда, аритмиям, насосной недостаточности и смерти.
Основной причиной увеличения распространенности СН у больных СД является наличие специфической диабетической КМП, которая характеризуется гипертрофией клеток миокарда и фиброзом [24]. На физиологическом уровне диабетическая КМП проявляется снижением механической функции миокарда и электрофизиологическими нарушениями. На клеточном уровне она связана с дефектами в субклеточных органеллах и doun-регулированием рецепторов катехоламинов вследствие хронически повышенного уровня катехоламинов [25, 26].
Гипергликемия является одной из основных причин диабетической КМП. Хроническая гипергликемия приводит к необратимому гликированию коллагена, в результате чего увеличиваются «сшивание» коллагена и фиброз миокарда [27]. В исследованиях на животных с начальной гипергликемией было показано наличие изменений транспорта кальция в кардиомиоцитах и изменений сократительных белков, что приводит к систолической и диастолической дисфункции из-за увеличения содержания коллагена в миокарде [28].
Еще одним метаболическим фактором, кроме гипогликемии, который играет важную роль в развитии диабетической КМП, является липотоксичность, т. е. вне- и внутриклеточное повышение концентрации СЖК и триглицеридов. Избыток СЖК накапливается в миокарде. Продукты метаболизма СЖК, керамиды, индуцируют образование оксида азота до патологического уровня, что увеличивает образование митохондриального супероксида, который вызывает окислительный стресс. Последний путем изменения экспрессии генов приводит к апоптозу кардиомиоцитов [29].
Субклиническая дисфункция миокарда, вызванная диабетической КМП, усугубляется присоединением АГ, которая усиливает повреждение сократительных белков миокарда, фиброз и гипертрофию миокарда ЛЖ. Хотя у 70% пациентов пожилого возраста с СД 2-го типа имеется АГ, гипертрофия миокарда происходит также вследствие ростостимулирующего действия инсулина и выявляется у 71% больных СД на разных стадиях заболевания [30, 31].
При СД причиной ишемии миокарда и СН также является диабетическая микроангиопатия. Доказательством ее участия в патогенезе СН у больных СД является ассоциация между диабетической ретинопатией и нефропатией и увеличением кардиальных осложнений и смертности [32]. Диабетическая микроангиопатия характеризуется утолщением базальной мембраны капилляров и формированием микроаневризм. Эти структурные изменения вызывают функциональные изменения, такие как нарушение продукции оксида азота и проницаемости эндотелия с последующей его дисфункцией и снижением плотности сосудов [30]. Дисфункция эндотелиальная в свою очередь вызывает повторяющиеся эпизоды вазоконстрикции проксимальных сегментов КА и реперфузионные повреждения, интерстициальный отек и фиброз миокарда [33].
Кроме того, общим микрососудистым осложнением СД является автономная кардиальная невропатия. Ранним ее проявлением служит парасимпатическая денервация с дисбалансом в сторону относительно более высокого симпатического тонуса. Повышение кардиальной симпатической активности усиливает липолиз, повышает концентрацию СЖК, что влияет на утилизацию субстратов миокардом [34], митохондриальное разобщение [35] и окислительный стресс с последующей дисфункцией сердца.
Конечным результатом комбинации диабетической КМП, АГ/гипертрофии ЛЖ, макро- и микрососудистой болезни миокарда является фиброз, который клинически сначала проявляется как диастолическая дисфункция с последующей сначала мягкой, но позже тяжелой систолической дисфункцией. Кроме того, если фиброз распространяется на папиллярные мышцы, развивается митральная недостаточность, которая добавляет механическое бремя для неблагополучного миокарда [36].
Патофизиологически миокард пациентов с СД по многим параметрам напоминает ишемизированный миокард, в котором происходит уменьшение усвоения и окисления глюкозы и увеличение окисления жирных кислот. При этом изменяется метаболизм пирувата, который является продуктом гликолиза, в сторону синтеза гликогена. Так как АТФ, получаемая при гликолизе, используется для поглощения Са2+ в саркоплазматическом ретикулуме, снижение образования АТФ приводит не только к снижению поглощения Са2+ но и увеличению жесткости миокарда и диастолической дисфункции. Исследования in vitro показали, что при ингибировании гликолиза нарушается релаксация миокарда, особенно если миокард ишемизирован или была реперфузия. Кроме того, ингибирование гликолиза приводит к гипертрофии желудочков [37].
Дисфункция митохондрий играет ключевую роль при СН, так как митохондрии являются основным источником активных форм кислорода. Весьма вероятна правильность предположения, что основной причиной высокой частоты СН при инсулинорезистентности и СД является дисфункция митохондрий. Поэтому любое вмешательство, улучшающее функцию митохондрий, может быть спасительным при СН [38], особенно на фоне СД.
Триметазидин модифицированного высвобождения путем селективного ингибирования митохондриальной 3-КАТ и, возможно, карнитинпальмитолтрансферазы-1 уменьшает окисление жирных кислот и стимулирует использование глюкозы. При окислении глюкозы в митохондриях продуцируется больше энергетических субстратов в расчете на 1 моль кислорода, чем при использовании жирных кислот. Следовательно, триметазидин, способствуя синтезу большего количества молекул АТФ на одну потребляемую молекулу кислорода, улучшает баланс между потребностью миокарда в кислороде и его поступлением, что снижает общее ишемическое бремя и способствует более высокой механической эффективности миокарда. С точки зрения влияния на прогрессирование СН важно напомнить, что триметазидин модифицированного высвобождения улучшает активность натрий-калиевой АТФазы и поглощение кальция соответствующими насосами саркоплазматического ретикулума, которые несут ответственность за деполяризацию и диастолическое расслабление ЛЖ [39].
В предшествующих исследованиях было показано, что триметазидин модифицированного высвобождения модифицированного высвобождения улучшает ФВ ЛЖ и снижает функциональный класс СН у пациентов с ИБС и ХСН [40]. Однако в эти исследования было включено мало пациентов с СД. Еще меньше исследований изначально посвящено изучению эффективности триметазидина модифицированного высвобождения у пациентов с ИБС и/или СН на фоне СД. Так, в одном из них было показано, что у пациентов с ИБС на фоне СД триметазидин модифицированного высвобождения улучшает миокардиальный метаболизм в покое и на фоне нагрузки и уменьшает снижение ФВ ЛЖ, вызванное хронической гипоперфузией и повторяющимися эпизодами ишемии миокарда [12].
D. Rosano и соавт. показали, что триметазидин, добавленный к стандартной медикаментозной терапии, улучшает систолическую и диастолическую функцию ЛЖ у больных СД с ишемической КМП [41]. В другом исследовании показано снижение частоты совокупных неблагоприятных событий у пациентов с ишемической СН под влиянием триметазидина модифицированного высвобождения [42]. Наконец, недавно опубликованы данные о снижении смертности и заболеваемости при СН со сниженной функцией ЛЖ на фоне стандартной медикаментозной терапии с добавлением триметазидина модифицированного высвобождения [43].
Опубликованные в апреле 2014 г. данные X. Xu и соавт. свидетельствуют, что у пожилых пациентов с многососудистой ИБС и СД вспомогательная терапия триметазидином модифицированного высвобождения, назначаемая после имплантации стента с лекарственным покрытием, значительно снижает частоту рецидивов стенокардии и ее тяжесть, улучшает структуру и функцию ЛЖ [44].
В данной работе нами продемонстрировано клинически значимое улучшение общей сократительной функции ЛЖ у пациентов с ИБС на фоне нарушений углеводного обмена при сочетании эндоваскулярной реваскуляризации миокарда и длительного приема триметазидина. В то же время отсутствие миокардиальной цитопротекции, несмотря на выполненную реваскуляризацию миокарда, было сопряжено с нарастанием нарушений локальной сократимости и снижением насосной функции миокарда ЛЖ. Важно, что улучшение ультразвуковых показателей в группе триметазидина модифицированного высвобождения сопровождалось лучшей переносимостью физической нагрузки по данным ТШХ по сравнению с группой контроля через 12 мес после вмешательства на КА.
Существует несколько возможных причин сохранения и улучшения функции миокарда на фоне приема триметазидина. Прежде всего, это защитное действие триметазидина от ишемически-реперфузионного повреждения миокарда при выполнении реваскуляризации, что продемонстрировано нами в этих группах пациентов и опубликовано ранее. Положительную роль играет и доказанное многими авторами антиишемическое влияние исследуемого препарата. Кроме того, появляются сообщения о возможности профилактики рестенозов стентов с помощью триметазидина [45]. Все эти клинические возможности нуждаются в дальнейшем изучении.
Таким образом, применение фармакоинвазивного подхода, а именно добавление триметазидина модифицированного высвобождения — препарата метаболического действия — к стандартной терапии при плановой эндоваскулярной реваскуляризации миокарда у пациентов с нарушениями углеводного обмена способствует сохранению функции миокарда. Для оценки влияния триметазидина на отдаленную выживаемость этой категории больных необходимы крупные многоцентровые рандомизированные исследования.
Выводы
- Несмотря на выполненную эндоваскулярную реваскуляризацию миокарда, наличие нарушений углеводного обмена у пациентов с ишемической болезнью сердца сопряжено со значимым ухудшением локальной сократимости миокарда и снижением насосной функции левого желудочка при последующем наблюдении (увеличение индекса нарушения локальной сократимости на 8,3% и снижение ударного индекса левого желудочка на 7,25% через 12 мес после вмешательства по сравнению с исходным значением).
- Длительный прием миокардиального цитопротектора триметазидина в дозе 75 мг/сут за 2 нед до чрескожного коронарного вмешательства и в течение 12 мес после него у пациентов с ишемической болезнью сердца на фоне нарушений углеводного обмена приводит к достоверному улучшению сократительной функции миокарда левого желудочка в отдаленный период по данным эхокардиографии (снижение конечного диастолического индекса на 5,5% и конечного систолического индекса на 4,4%, увеличение фракции выброса левого желудочка на 2,5% через 12 мес после выполненной реваскуляризации миокарда по сравнению с исходным значением).
- Клинически улучшение функции миокарда на фоне длительного лечения триметазидином через 12 мес после чрескожного коронарного вмешательства проявляется увеличением расстояния, пройденного при выполнении теста с 6-минутной ходьбой, на 18,4% по сравнению с группой стандартной терапии.



