Введение. В настоящее время эндометриоз является довольно распространенным заболеванием. У женщин репродуктивного возраста данная патология встречается в 15% наблюдений [1, 2]. Эндометриоз мочевыделительной системы – одна из редких форм глубокого инфильтративного эндометриоза, доля которого составляет 1–5,5% случаев среди экстрагенитального эндометриоза всех локализаций [2, 3] и 14–20% случаев инфильтративных форм [4]. Мочеточники вовлекаются в процесс в 9% наблюдений, почки и уретра поражаются в 4 и 2% случаев соответственно. Однако чаще всего встречаются поражения мочевого пузыря – 85% наблюдений [4, 5].
Эндометриоз мочевого пузыря представляет собой доброкачественное разрастание ткани, по морфологическим и функциональным свойствам сходной с эндометрием, в стенке мочевого пузыря. Эндометриоидные очаги чаще локализуются в верхушке, по задней стенке или в области шейки мочевого пузыря [5]. По происхождению выделяют первичный (спонтанный) эндометриоз мочевого пузыря (11%) и вторичный, возникающий после оперативных вмешательств на органах малого таза [6, 7]. В 90% случаев он сочетается с другими формами эндометриоза малого таза [8].
Основными клиническими проявлениями эндометриоза мочевого пузыря могут быть симптомы вовлеченности в патологический процесс нижних мочевых путей: дизурия, гематурия, поллакиурия, боли внизу живота, ургентные позывы, усиливающиеся накануне или во время менструации. Однако в 30% случаев имеет место бессимптомное течение [2, 4, 5].
При наличии симптоматики последующая инструментальная диагностика очаговых форм эндометриоза мочевого пузыря, как правило, не вызывает затруднений. Для диагностики успешно используются УЗИ и МРТ. Специфичность ультразвукового метода диагностики составляет 100%, чувствительность – 25–50%, соответствующие показатели для МРТ составляют 88 и 99% [9, 10]. Таким образом, диагностическая ценность МРТ составляет 98%, поэтому данный метод служит «золотым» стандартом диагностики эндометриоза мочевого пузыря [9–12].
Метод лечения при данной патологии, как правило, хирургический. Используется два вида операций: трансуретральная и парциальная резекция мочевого пузыря (лапароскопическим или лапаротомным доступом). Часто эндометриоз может симулировать эндофитную опухоль мочевого пузыря, и лечение проводится в условиях урологических отделений. При этом необходимая дополнительная диагностика или гормональное лечение не проводится. С другой стороны, определение объема и доступа при резекции мочевого пузыря является непростой задачей для гинекологов.
Таким образом, целью статьи стало описание конкретных клинических примеров, позволяющих оценивать целесообразность междисциплинарного подхода к лечению пациенток с эндометриозом мочевыделительной системы с целью разработки корректной лечебной тактики. В центре урологии и гинекологии АНО «Клиника НИИТО» с 2014 по 2016 г. наблюдались две пациентки с эндометриозом мочевого пузыря.
 Клиническое наблюдение 1
Клиническое наблюдение 1
П а ц и е н т к а М. 30 лет обратилась в клинику в 2016 г. с жалобами на боли внизу живота, поллакиурию, рези при мочеиспускании за несколько дней до начала менструации и в течение 1–2 недель после ее окончания. Впервые симптомы появились в 2014 г., но в неоднократных анализах мочи не обнаруживалось ни гематурии, ни лейкоцитурии.
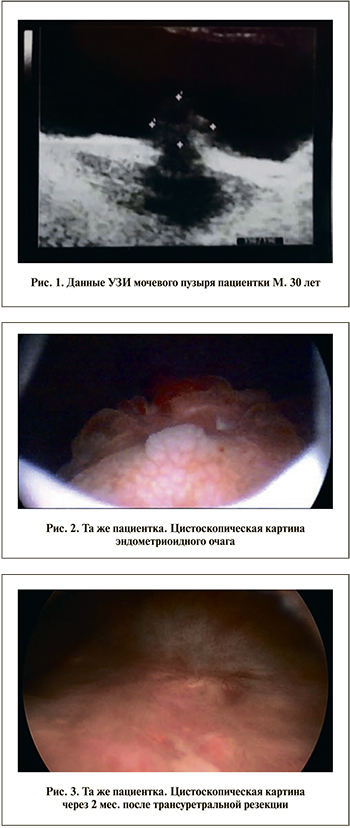
В условиях урологического отделения пациентке были проведены МРТ малого таза и УЗИ мочевого пузыря. Был обнаружен очаг инфильтративного эндометриоза 22×17×18 мм в проекции пузырно-маточной складки с инвазией в мочевой пузырь (рис. 1).
При цистоскопии в области межмочеточниковой складки (треугольник Льето) было обнаружено образование размером 2×1,5 см, не доходящее до устьев мочеточников. По данным биопсии, структура образования описана как «фрагмент мышечного слоя, обрывок пласта переходного эпителия». Пациентка была взята под наблюдение врачом-гинекологом. Из гинекологического анамнеза: беременностей 4, две из них закончились самопроизвольными срочными родами (2007 и 2012 гг.); дважды был сделан медицинский аборт по желанию, без осложнений. Менструации регулярные, умеренные, болезненные. По данным УЗИ органов малого таза в 2015 г. диагностирован аденомиоз II стадии, в связи с чем была установлена внутриматочная гормональная система с левоноргестрелом («Мирена»). На фоне проводимого лечения улучшения симптомов со стороны мочеиспускания не было.
При контрольном МРТ-исследовании малого таза в 2016 г. был обнаружен очаг инфильтративного эндометриоза размером 27×23×25 мм в проекции пузырно-маточной складки с инвазией в мочевой пузырь. Выполнена уретроцистоскопия: в области межмочеточниковой складки (треугольник Льето) обнаружено округлое ворсинчатое плотное образование размером 2,5×3 см, доходящее до устьев мочеточников с обеих сторон. Слизистая над ним была буллезно изменена (рис. 2, 3).
Гистологическое заключение: метаплазия слизистой мочевого пузыря с ангиоматозом стромы. При бимануальном осмотре по передней стенке влагалища ближе к переднему своду определялось округлое тугоэластическое безболезненное при пальпации образование до 3 см в диаметре.
Пациентке была проведена трансуретральная биполярная электрорезекция мочевого пузыря в пределах здоровых тканей после предварительного стентирования мочеточников, выполненного в связи с тем, что линия резекции проходила по устьям мочеточников. Интраоперационно потребовалась сквозная резекция задней стенки мочевого пузыря с последующей резекцией очага эндометриоза с «шейвингом» стенки влагалища, приподнятой с помощью пальца, введенного во влагалище.
В ходе диагностической лапароскопии дополнительных очагов эндометриоза в области малого таза обнаружено не было. По окончании операции при контрольном осмотре со стороны влагалища пальпаторно образование по передней стенке не определялось. Мочеточниковые стенты были удалены через 3 нед. Через 2 мес. была выполнена контрольная цистоскопия: очаговых образований обнаружено не было, в месте резекции – рубцовые изменения (рис. 3). Жалобы, предъявляемые пациенткой, полностью купированы.
Клиническое наблюдение 2
П а ц и е н т к а К. 59 лет обратилась в клинику в 2014 г. с жалобами на учащенное мочеиспускание, ноктурию до 4–5 раз, периодические рези при мочеиспускании, беспокоившие женщину с 2010 г. На момент обращения постменопауза длилась уже 16 лет, беременностей при регулярной половой жизни не было, у гинеколога по поводу бесплодия пациентка не обследовалась, не наблюдалась. В анализах мочи лейкоцитурии, гематурии, бактериурии не обнаружено. По данным УЗИ мочевого пузыря, в 2012 г. было выявлено образование задней стенки мочевого пузыря 15×9×5 мм.
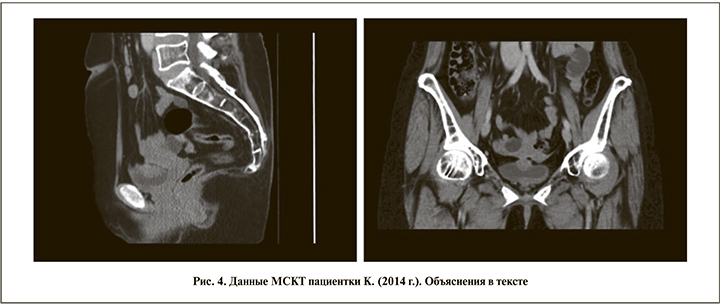
При цистоскопии в 2013 г. выявлено кистозно-солидное образование мочевого пузыря, гистологически – хронический цистит. При контрольном МСКТ-обследовании в 2014 г. выявлена опухоль задней стенки мочевого пузыря размером 35×18×28 мм на широком основании с инфильтрацией всех слоев, не выходившая за пределы мочевого пузыря (рис. 4). В ходе уретроцистоскопии в области верхушки мочевого пузыря выявлено подслизистое бугристое образование 3,5 см в диаметре, слизистая оболочка над которым кистозно изменена.
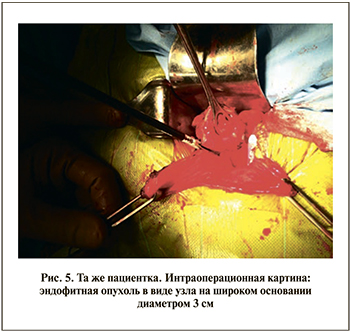 Гистологическое заключение по результатам исследования биоптатов: признаки хронического цистита. Пациентке был выставлен диагноз «опухоль мочевого пузыря T3bN0M0», в связи с чем проведено оперативное лечение: лапаротомия, ревизия, резекция мочевого пузыря. Интраоперационно по задней стенке мочевого пузыря на 5 см выше межмочеточниковой складки была обнаружена эндофитная опухоль в виде узла на широком основании диаметром 3 см с инвазией в паравезикальную клетчатку (рис. 5).
Гистологическое заключение по результатам исследования биоптатов: признаки хронического цистита. Пациентке был выставлен диагноз «опухоль мочевого пузыря T3bN0M0», в связи с чем проведено оперативное лечение: лапаротомия, ревизия, резекция мочевого пузыря. Интраоперационно по задней стенке мочевого пузыря на 5 см выше межмочеточниковой складки была обнаружена эндофитная опухоль в виде узла на широком основании диаметром 3 см с инвазией в паравезикальную клетчатку (рис. 5).
С учетом отсутствия гистологических данных о злокачественном процессе и локализации опухоли в верхушке мочевого пузыря операция была ограничена резекцией мочевого пузыря. Заключение по результатам гистологического исследования: эндометриоз мочевого пузыря, хронический цистит. В 2015 г. проведена контрольная цистоскопия, патологии не выявлено. Жалобы, предъявляемые пациенткой, полностью купированы.
Обсуждение. Единого подхода к лечению пациенток с эндометриозом мочевыделительной системы не существует. Это связано как с отсутствием крупных рандомизированных клинических исследований, так и с неспецифической клинической картиной, проявляющейся нарушениями мочеиспускания. Часто эндометриоз симулирует эндофитную опухоль мочевого пузыря, и лечение проводится в условиях урологических отделений. При этом необходимая дополнительная диагностика или гормональное лечение не проводятся. С другой стороны, определение объема и доступа при резекции мочевого пузыря является непростой задачей для гинекологов, а медикаментозная терапия, назначаемая гинекологами и включающая аналоги гонадотропин-рилизинг гормонов, гестагены и комбинированные оральные контрацептивы, часто становится причиной «рецидива» после недостаточно корректного лечения по поводу эндометриоза мочевого пузыря. То есть гормональная терапия женщин репродуктивного возраста может и должна сочетаться с одним из адекватно подобранных методов оперативного лечения [13, 14].
Выбор метода и объема хирургического вмешательства – трансуретральная резекция или парциальная резекция мочевого пузыря (лапароскопическим или лапаротомным доступом) – зависит от возраста пациентки, репродуктивных планов, локализации очагов, степени распространения и вовлечения соседних органов. Важно иметь возможность одновременного использования как эндоскопического трансуретрального, так и лапароскопического или лапаротомного доступа. И конечно, выбор операции будет зависеть от специализации отделения, в котором пациентка проходит лечение.
В представленных нами клинических наблюдениях пациенток одновременно вели уролог и гинеколог, также они входили в состав операционной бригады. В первом случае пациентке были выполнены трансуретральная резекция мочевого пузыря и диагностическая лапароскопия, которая помогла исключить наличие очагов другой локализации и необходимость дополнительного гинекологического вмешательства. Во втором случае с учетом возраста пациентки, постменопаузы продолжительностью 16 лет, отсутствия в анамнезе данных об эндометриозе, подозрения на опухоль мочевого пузыря выполнена лапаротомия и ревизия органов малого таза. В результате также были исключены другие локализации эндометриоза, в связи с чем объем операции был ограничен резекцией мочевого пузыря.
Заключение. Таким образом, для выбора корректной тактики ведения пациенток с эндометриозом мочевыделительной системы требуется междисциплинарный подход и взаимодействие врача-гинеколога и уролога. Это позволяет выбирать адекватный доступ и объем хирургического лечения, а также принимать решение о необходимости дополнительной гормональной терапии. Важность взаимодействия определяется тем, что назначение только гормональной терапии не приводит к полному регрессу очагов глубокого инфильтративного эндометриоза, а только хирургическое лечение не может гарантировать отсутствие рецидива.



