Вступление. Впервые перкутанная нефролитотомия (ПНЛ) как отдельный вид оперативного лечения была описана I. Fernström и B. Johansson в 1976 г. [1]. Благодаря J. Wickham et al., выполнившим первую успешную серию в 1981 г., ПНЛ практически полностью вытеснила лапаротомные, а затем и лапароскопические операции в лечении нефролитиаза [2]. За 40 лет активного выполнения ПНЛ как техники оперативного вмешательства неоднократно претерпевала модификации, что связывает научно-технологический прогресс с актуальностью данной операции. На сегодняшний день перкутанная нефролитотрипсия является операцией первой линии в лечении крупных и сложных камней почек [3].
Благодаря высокой частоте полного избавления от камней (stone free rate – SFR) ПНЛ наглядно демонстрирует свою эффективность, однако и не лишена осложнений [4]. Частота развития осложнений, по данным мировых и отечественных авторитетных источников, составляет от 20,5 до 23,3%. Наиболее распространены интраренальные осложнения: кровотечение, перфорация ЧЛС, инфекционные осложнения [4–6].
Одной из важных составляющих возникновения осложнений является непосредственно пункция ЧЛС, на долю которой приходится до 18% от всех причин возникновения осложнений ПНЛ [7]. Оптимальный почечный доступ является важнейшим начальным этапом операции. На сегодняшний день предложено множество методик и способов, помогающих минимизировать осложнения во время выполнения пункции ЧЛС: УЗ насадки для точного наведения иглы, лазерное и электромагнитное наведения, роботические системы размещения игл [8]. Все вышеперечисленное способствует снижению повреждения внутри- и внеорганных структур исключительно за счет повышения точности пункции. Несмотря на принятые за последние 30 лет меры с целью снижения травмирующей способности самой пункционной иглой, предложенные варианты заточек режущего кончика иглы не показали существенных различий.
В данной публикации мы описываем экспериментальные исследования и результаты пункции свиной почки новой малотравматичной иглой MG с патоморфологической сравнительной оценкой результатов.
Цель работы: определение эффективности и безопасности новой малотравматичной пункционной иглы МG в экспериментальных условиях.
Материалы и методы. С целью уменьшения травматизации структур почки во время пункции предложено модифицировать технику путем использования новой пункционной малотравматичной иглы MG (патент ПМ РФ № 201910), изображенной на рис. 1.
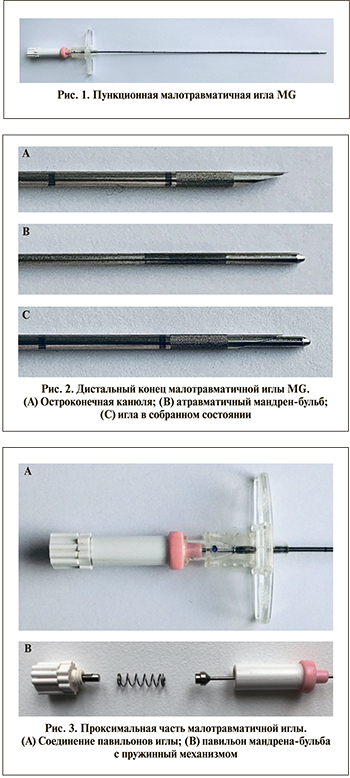
Игла является двукомпонентной (имеет канюлю и мандрен) с рабочей длиной 20 см и наружным диаметром канюли 18 Gauge (1.219 мм), что полноценно хватает для комфортной работы и соизмеримо с иглами, используемыми в рутинной практике для пункции ЧЛС при нефростомии или ПНЛ. Благодаря нанесенным меткам на рабочей поверхности иглы (шагом в 1 см) с утолщением на каждой 5-й (5см) метке достигается хорошая ориентация объема введенной иглы. Кроме этого на канюле и на мандрене нанесены ультразвуковые метки для лучшей визуализации колющей части иглы.
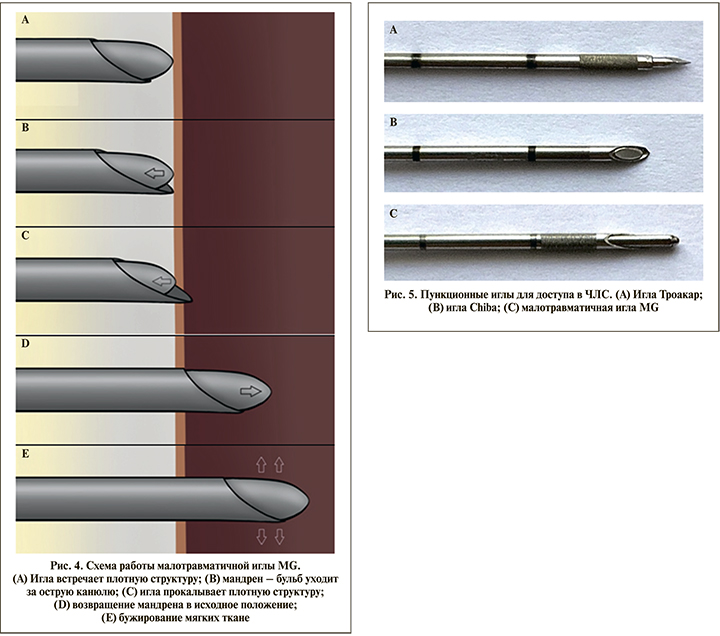
Инновационной отличительной особенностью иглы MG от аналогов является ее конструкция. Дистальный конец иглы состоит из остроконечной канюли, заточенной по типу Quinсke, и атравматичного (отсутствуют режущие грани) мандрена-бульба* (рис. 2). Благодаря принципиально отличающемуся строению мандрена, имеющего мобильный закругленный кончик – бульб, выступающего за пределы острой канюли, игла MG и приобрела малотравматичные свойства.
Проксимальная часть иглы представлена соединением павильонов со специальной рукояткой для пальцев с плотной фиксацией иглы во время пункции (рис. 3). Особенным отличием данной иглы является конструкция строения павильона мандрена, в котором спрятан пружинный механизм. Благодаря наличию пружины атравматичная часть мандрена-бульба получила способность возвратно-поступательных движений общей амплитудой в 5мм (рис. 3).
При выполнении пункции ЧЛС игла встречает на своем пути ряд анатомических структур разной толщины и плотности (кожа, апоневроз, фасция Герота, почечная капсула, вены, внутрипочечные структуры, слизистая ЧЛС).
В зависимости от конструкции кончика иглы (игла Chiba с заточкой типа Quinсke, игла Троакар с заточкой Pencil Point) по-разному происходит рассечение анатомических структур, попадающихся на пути иглы. Однако независимо от конструкций существующих игл ткани, встречающиеся по ходу прохождения иглы, рассекаются (разрезаются) независимо от своей структуры.
В отличие от своих аналогов во время пункции ЧЛС иглой MG первым плотных анатомических структур касается мандрен-бульб (рис. 4). Если плотность структур не позволяет их сместить в сторону (бужировать), мандрен-бульб смещается за остроконечную часть канюли, а последняя их прокалывает. Как только игла проходит плотные структуры за счет режущего кончика канюли, атравматичный конец автоматически возвращается в исходное положение. Благодаря прохождению иглы за счет мандрена-бульба мягкотканые структуры почки раздвигаются, а не разрезаются режущей частью иглы. Созданием эффекта бужирования мягких тканей осуществляется минимальная травматизация во время выполнения пункции.
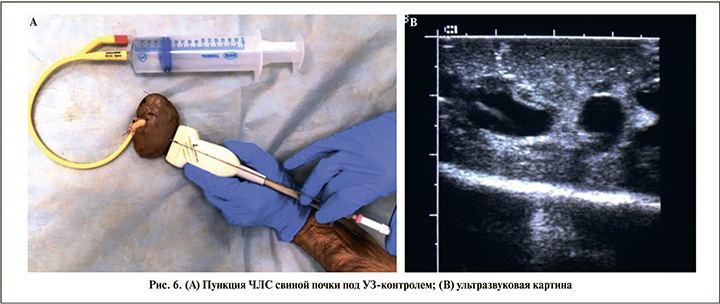
Для определения эффективности и безопасности пункционной иглы MG была выполнена сравнительная морфологическая оценка серий пункций свиной почки. В исследовании помимо иглы MG нами использовались стандартные пункционные иглы Chiba и Троакар (Coloplast A/S, Дания). Все иглы имели равный наружный диаметр канюли 18 Gauge (рис. 5).
Для осуществления патологоморфологического исследования первым этапом была подготовлена свиная почка. Для осуществления точной пункции ЧЛС (минуя попадание в межпирамидальное пространство) была создана искусственная дилатация путем введения 15 мл физиологического раствора под УЗ-контролем по герметично дренированному мочеточнику.
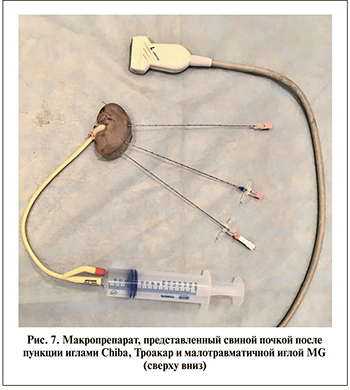
Вторым этапом под УЗ-навигацией с использованием линейного датчика поочередно выполнены пункции чашечек свиной почки тремя разными иглами (рис 6).
По окончании пункций свиная почка, пунктированная малотравматичной иглой MG, иглами Chiba и Троакар (рис. 7), залита 10%-ным раствором формалина и отправлена на морфологическое исследование.
После фиксации макропрепарата в 10%-ном растворе формалина с каждого пунктированного участка (иглами Chiba, Троакар, а также малотравматичной иглой MG) для дальнейшего гистологического исследования взято по три фрагмента ткани почки.
При заготовке гистологических препаратов выполнялась постепенная техника обезвоживания спиртовыми растворами для предотвращения сморщивания, затем заливка в парафин, предварительно пропитанного ксилолом при температуре 54–56ºС в трех порциях с формированием в парафиновый блок.
Для исследования с макропрепарата почки было изготовлено 9 парафиновых блоков, с которых произведены гистологические срезы. Каждый срез толщиной до 4 микрометров (4 микрона – 0,004 мм).
Окраска гистологических препаратов производится в три смены: окраска ядер гематоксилином Майера; окрашивание препарата эозином; просветление срезов карбол-ксилолом.
С целью полноценной патологоморфологической оценки паренхимы, пунктированной малотравматичной иглой MG, вторым этапом выполнена дополнительная оценка микропрепарата с окраской пикрофуксином по Ван- Гизону, позволяющая более объемно формировать картину структурных изменений ткани, в особенности коллагеновых волокон.
Окраска препаратов выполнена путем пропитывания срезов гематоксилином Вейгерта, затем промывка в воде, окраска пикрофуксином (раствор пикриновой кислоты и 1%-ный водный раствор кислого фуксина), по окончании окрашивания выполнена промывка в воде, 96%-ном спирте и растворе ксилола.
Материал представлен 15 препаратами. Оценка гистологической картины осуществлялась на микроскопе Leica DM2000. Представленные в публикации микрофотографии сделаны при помощи фотокамеры Leica EC3.
Результаты. На микропрепарах паренхимы свиной почки, пунктированной иглой Chiba (рис. 8), визуализируется место прохождения иглы, в просвете которого прослеживается участок паренхимы с мелкими фрагментами слущенного поврежденного эпителия и отдельных эритроцитов. Объемные фрагменты паренхимы в просвете пункционного хода, хорошо заметные уже при увеличении х50, являются результатом большой режущей плоскости пункционной иглы.

На макропрепаратах (рис. 9) с пункцией троакарной иглой в просвете хода иглы при увеличении х50 наблюдается слущенный паренхиматозный эпителий с неровными краями пункционного хода. При дополнительном увеличении х200 хорошо визуализируются поврежденные канальцы и крупные обрывки клубочков.
При исследовании микропрепарата паренхимы, пунктированной малотравматичной иглой MG (рис. 10), окрашенных гематоксилинои и эозином, при увеличении х50, х100 и х200, место прохождения иглы представлено четкими контурами с целостной структурой канальцев. В просвете практически отсутствует поврежденный эпителий, который представлен единичными мелкими обрывками.
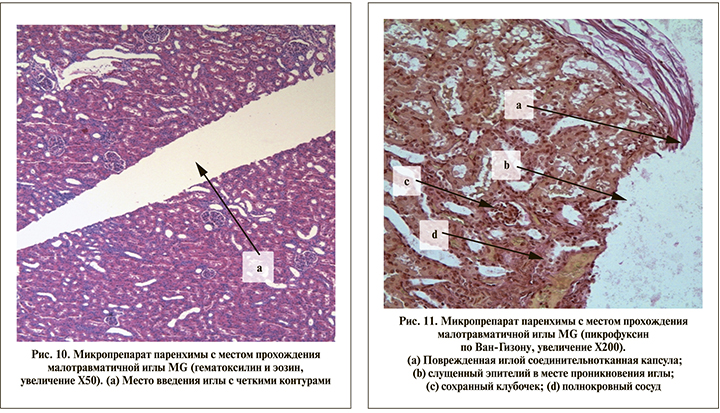
По результатам окраски пикрофуксином по Ван-Гизону (рис. 11) на микропрепаратах паренхимы в просвете дефекта (проникновения иглы), микроскопический препарат в двухсоткратном увеличении представлен невыраженным количеством слущенного эпителия. Дефект представлен четкими краями с сохраненной целостностью близлежащих структур. Почечная капсула, образованная соединительнотканными волокнами, незначительно обращена внутрь дефекта. При исследовании макропрепарата отчетливо визуализируется целостность структуры полнокровного сосуда рядом с пункционным ходом.
Благодаря атравматичному мандрену малотравматичной иглы MG пункция паренхимы осуществляется путем бужирования (раздвигания) структур. По сравнению с иглами Chiba и Троакар игла MG лучше сохраняет целостность паренхимы, избегая излишней травматизации близлежащих клубочков, канальцев, а также способствует сохранению целостности полнокровных сосудов.
Обсуждение. Перкутанная нефролитотрипсия является малоинвазивным оперативным лечением пациентов с конкрементами в почках. Однако, как и любое хирургическое вмешательство, имеет вероятность развития осложнений. Наиболее распространены интраренальные осложнения, к таковым относятся кровотечение, перфорация ЧЛС, инфекционные осложнения верхних мочевых путей (ВМП) [4].
Очень важно грамотно и полноценно планировать предстоящее операционное пособие, выполнив компьютерную томографию (КТ) [9]. В случае наличия у пациента сложного конкремента, а также анатомических особенностей строения, которые могут усложнять выполнение ПНЛ и пункции, в частности, возможно (на основании КТ с в/в контрастированием) выполнение 3D-моделирования. Трехмерная реконструкция почки с сосудами и ВМП позволяется грамотно планировать объем перкутанной операции [10].
Пристальное внимание к анатомии строения почек связано с их развитой системой крупных сосудов и сети капилляров, за счет которых эти органы обладают хорошим кровоснабжением с перфузией кровотока до 1200 мл (25% общего сердечного выброса поступает в почки) [11].
Кровотечение является одним из самых распространенных осложнений при выполнении ПНЛ, которое бывает интра- и послеоперационным в зависимости от времени наступления. Травмы крупных межсегмантарных сосудов во время операции могут приводить к возникновению массивного кровотечения. По данным С. Seitz et al., только гемотрансфузия в послеоперационном периоде достигает 7% [4].
Гемморагия, не требующая консервативной терапии, хоть и не является осложнением, однако способствует ухудшению видимости во время операции и сказывается на ее результатах (SFR) [12]. Такое кровотечение происходит по причине микротравм паренхимы во время бужирования, чрезмерном изгибе эндоскопа, а также пункции (особенно при многократных попытках) [13, 14].
Пункция чашечно-лоханочной системы (ЧЛС) является одной из самых ответственных этапов перкутанной нефролитотрипсии [7]. Суть техники была предложена Селдингером в 1953 г. для осуществления сосудистого доступа по струне-проводнику [15]. Для установки проводника в ЧЛС при ПНЛ доступ в почку осуществляется из заднебокового положения через аваскулярную зону Броделя. Благодаря пункции через зону невыраженной сосудистой архитектоники снижается частота травм крупных сосудов [16]. С целью снижения вероятности повреждения межпирамидальных артерий и излишнего надрыва паренхимы жестким нефроскопом траектория иглы, минуя бертиневые колоны, при попадании в чашечку должна быть направлена на центр лоханки [17].
С целью минимизации возникновения осложнений уменьшение чрезмерного числа попыток пункций способствует сохранению целостности паренхиматозных структур, благосклонно уменьшает вероятность развития кровотечения, а также повышает качество операции [18].
При осуществлении пункции описано множество техник с использованием рентгенологического и ультразвукового контроля. Одной из инновационных методик, выполняемой на С-дуге, стала гибридная техника. G. Sharma et al., объединив положительные качества бипланарных методов (триангуляция и «бычий» глаз), используя данную методику, достигли высочайшей точности пункции (однократная пункция ЧЛС >95%) [19].
Благодаря развитию современных технологий для повышения безопасности пункции разработаны вспомогательные средства направления и фиксации пункционной иглы:
- ультразвуковые навигационные системы, проектирующие объемную картинку за счет нескольких датчиков [20, 21];
- роботизированные навигационные системы, выполняющие автоматическое выравнивание пункционной иглы к нужной чашечке для дальнейшего выполнения комфортной и правильной пункции на C-дуге [22];
- электромагнитная система слежения, помогающая урологу выполнять прицеливание за счет заблаговременной ретроградной интраренальной установки датчика по мочеточниковому кожуху [23];
- устройства для комфортной фиксации иглы во время прицеливания на С-дуге [24] [25];
- мобильное устройство дополненной виртуальной реальности, накладывающее трехмерное изображение анатомии почки на пациента в режиме реального времени [26].
Вышеупомянутые методики минимизируют вероятность развития осложнений, помогая выполнить точный доступ в ЧЛС. Для снижения травматизации паренхимы во время выполнения пункции существует альтернатива в виде пункционной иглы Chiba с наружным диаметром 21G (0,8 мм).
С одной стороны, малый диаметр иглы способствует уменьшению площади травмы, что особенно полезно для начинающих урологов, испытывающих сложности с одномоментным доступом. Однако одним из ключевых недостатков такой иглы является особенность ее жесткости. За счет своих габаритов игла имеет более гибкую структуру, что влияет на ее траекторию (особенно у пациентов с ожирением или рубцовыми изменениям в почке). Еще одним минусом игл малого диаметра является отсутствие возможности использовать стандартные 0,035-дюймовые проводники. Для осуществления комфортного бужирования по стандартному проводнику хирург вынужден (после пункции иглой 21G) вначале устанавливать 0,018-дюймовый проводник, а затем его заменять на стандартный [27]. Малотравматичная игла MG лишена вышеуказанных недостатков, так как достигает пониженной травматизации паренхимы за счет атравматичного манрена-бульба, а стандартный диаметр наружной поверхности канюли (18G) дополнительно придает хорошую жесткость во время пункции.
Вывод. Пункция ЧЛС является важнейшим этапом перкутанной нефролитотрипсии. На сегодняшний день предложено множество методик, которые позволяют снижать травматизацию паренхимы во время пункции. Малотравматичная игла MG является инновационным инструментом, осуществляя бужирование мягкотканных структур за счет атравматичного мандрена-бульба. Обладая высокими результатами сохранения целостности структур паренхимы в экспериментальных условиях, игла представляет высокий интерес для дальнейшего выполнения клинического исследования.



