Пионером транскутанной биопсии собственной почки считается Alwall Nils, который в 1944 г. усовершенствовал методику транскутанной биопсии печени и использовал ее для биопсии почки, что позволило автору получить почечную ткань у 10 из 13 больных [1]. Тем не менее описание способа чрескожной биопсии собственных почек было тщательно описано в 1951 г. P. Irvesen et C. Brun [2].
Транскутанная биопсия почек (ТБП) остается золотым стандартом для определения этиологии заболевания почек и дальнейших методов лечения [3]. На основании проведенного исследования данных биопсии не только производится прогнозирование и выбор лечения собственных почек, но и является информативной процедурой для трансплантированных почек с последующей оценкой функционирующего пересаженного органа в послеоперационном периоде, для дифференциальной диагностики острого или хронического отторжения или развития гломерулонефрита de novo [4].
ТБП считается относительно безопасной процедурой, если она проводится в специализированных центрах и врачами, прошедшими соответствующий курс обучения. Однако данная манипуляция может приводить к формированию паранефральной гематомы различного объема, гематурии различной интенсивности, что требует в очень редких случаях серьезных вмешательств, таких как неф-рэктомия. ТБП может также приводить к смерти больного. [5, 6]. По данным К. М. Corapi и соавт., отмечено развитие транзиторной гематурии в 3,5%, необходимость ангиографии для выяснения источника кровотечения – в 0,6%, необходимость в нефрэктомии в связи с не корригируемым кровотечением – в 0,01% и смерть – в 0,02% наблюдений. Так как кровотечение с образованием гематомы является основным первичным осложнением, по этой причине всегда необходимо оценивать риск/польза ТБП для пациента и получать информированное согласие перед биопсией почки [7].
Приводим описание клинического наблюдения образования обширной гематомы после ТБП у больного хроническим диффузным гломерулонефритом.
Больной Л. 39 лет поступил c предварительным диагнозом «хронический диффузный гломерулонефрит, гематурическая форма, гиперлипидемия» в отделение трансплантологии и диализа для обследования и установления диагноза. Болен с февраля 2016 г. При обследовании выявлена протеинурия до 1,0 г/сут., микрогематурия и повышение сывороточного креатинина до 160,0 мкмоль/л, гиперлипидемия, корригируемая медикаментозно, общий белок – 71 г/л, альбумин – 43 г/л, мочевина крови – 8,0 ммоль/л, скорость клубочковой фильтрации (CКФ) по СKD–EPI (Chronic Kidney Disease Epidemiology Collaboration Formula) – 35,4 мл/мин. Больной госпитализирован для уточнения диагноза и проведения биопсии почки. 14.03.2017 больному под контролем ультразвукового исследования (УЗИ) (Philips iU-22) выполнена транскутанная толстоигольная биопсия нижнего полюса правой почки. Толщина биопсийной иглы – G16. Биопсийный материал представлен четырьмя столбиками почечной ткани. Была проведена световая и иммунофлюоресцентная микроскопия. По данным биопсии диагностированы IgA – нефропатия с картиной фокального сегментарного и глобального гломерулосклероза, гипертонический нефроангиосклероз.
Через два часа после выполненной ТКБ заподозрено забрюшинное кровотечение. У больного ухудшение самочувствия, выраженная слабость, боль в области пункции в поясничной области справа, холодный, липкий пот. Кожные покровы бледные. Артериальное давление – 70/40 мм рт.ст. Пульс – 115 ударов в 1 мин. Hb – 55 г/л. Ht – 0,18/л. По данным УЗИ правой биопсированной почки, имеется изоэхогенное образование с нечеткими контурами неправильной формы, охватившей нижний полюс и распространившееся по латеральному краю почки. Размер образования – 8,4×7,5х8,1 см. Примерный объем – 510,3 см3. Выявлена гематома в паранефральной клетчатке правой почки (рис. 1).
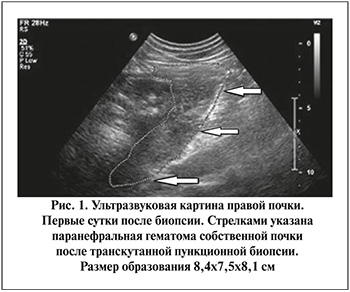
20.03.2017. Выполнена компьютерная томография (КТ) брюшной полости и забрюшинного пространства.
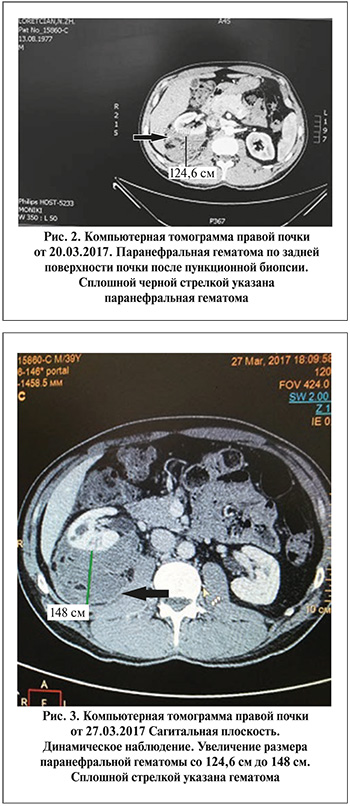
Визуализируется фрагментированное образование размером 58,1×78,3×127 мм (объем – 577,7 см3), которое смещает правую почку кпереди и кверху (рис. 2).
Больному назначена инфузионная гемостатическая терапия. Гемоглобин – 118 г/л, эритроциты – 4,48×1012/л, гематокрит – 0,36. лейкоциты – 7×109/л, тромбоциты – 325×109/л. Коагулограмма: AЧTB – 32,9 с, протромбиновое время – 12,1 с, МНО – 1,02 , фибриноген – 4,85 г/л, тромбиновое время – 25,8 с.
27.03.2017. Выполнена повторная КТ забрюшинного пространства (в динамике).
Визуализация паранефральной гематомы справа сохраняется. Определяется увеличение объема гематомы с 577,7 до 840 см3.
Правая почка оттеснена кпереди (рис. 3).
Несмотря на увеличение гематомы, по данным КТ, состояние больного не ухудшалось. Hb – 120 г/л, Ht – 0,39, А/Д – 120/75 мм рт.ст. Ps – 98 в 1 мин.
Ревизию забрюшинного пространства решено не выполнять, руководствуясь следующими соображениями: отсутствие болевого синдрома, снижение гемоглобина, гематокрита крови, лейкоцитоза, субфебрильной температуры как признак нагноившейся гематомы, удовлетворительное состояние самого больного. При оперативном вмешательстве имеется большая вероятность инфицирования гематомы, повторного кровотечения из-за отсутствия компрессионного момента гематомой места пункции с возможной потерей правой почки.
В дальнейшем при динамическом наблюдении за больным отмечалось уменьшение паранефральной гематомы.
При контрольном УЗИ на 37-е сутки после ТКБ правой почки паранефральная гематома значительно уменьшилась в размерах – с 877 до 177,7 см3 (рис. 4).
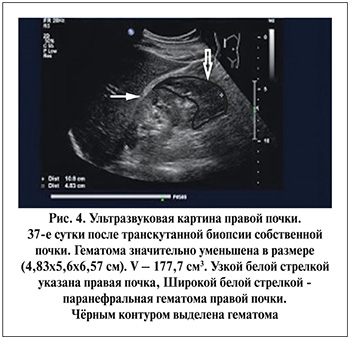
Состояние больного значительно улучшилось. Отсутствует боль в поясничной области справа. Температура тела – 36,8ºС. Артериальное давление – 135/90 мм рт.ст. Пульс – 84 уд. в 1 мин. Объем мочи за сутки – до 3 л. Hb – 13,5 г/л, Ht – 0,42 , тромбоциты – 386х109/л, креатинин – 4,4 мкммоль/л, мочевина – 10,7 ммоль/л. Больной выписан домой.
Несмотря на то что, по данным КТ, отмечалось увеличение гематомы с 577,7 до 840,1 см3, состояние больного не ухудшалось, не было снижения гемоглобина, гематокрита, артериального давления, отсутствовал лейкоцитоз, тест на эндотоксин отрицателен, было принято решение ревизию забрюшинного пространства не выполнять. Мы посчитали, что при вскрытии забрюшинного пространства возможно продолжение и/или усиление кровотечения, так как при эвакуации гематомы будет отсутствовать сдавливающий момент гематомой места пункции собственной почки, откуда, собственно, и продолжалось кровотечение. При невозможности остановки кровотечения, вероятно, будет необходима нефрэктомия. Также не исключается инфицирование гематомы, которая из асептической станет инфицированной, что может в дальнейшем привести к сепсису. Исходя из этих заключений, при отсутствие клинических симптомов продолжающего забрюшинного кровотечения и инфицирования гематомы ревизию забрюшинного пространства нами решено было не выполнять. Правильность нашей тактики подтвердило динамическое наблюдение за больным. Состояние больного клинически не ухудшалось. По данным УЗИ, размер гематомы уменьшился с 840,4 до 177,7 см3.
Чаще всего гематурические осложнения можно лечить, проводя инфузии жидкости и/или компонентов крови [8]. Кроме того, в некоторых случаях упорного кровотечения, перед проведением инвазивных процедур (эмболизации псевдоаневризмы или хирургического вмешательства), чтобы остановить кровотечение, можно прибегнуть к назначению рекомбинантного активированного VII фактора свертывания [9, 10].
Наличие небольшой бессимптомной гематомы до 50,0 см3 часто обнаруживается во время УЗИ почек после биопсии и не является само по себе осложнением. Что касается временного фактора появления гематомы, то исследования показали, что околопочечная гематома выявляется у 90% больных в первые 24–72 ч после процедуры. Большинство околопочечных гематом невелики и бессимптомны и исчезают спонтанно в течение нескольких месяцев. Только в 2% наблюдений гематомы могут иметь клинически значимые осложнения, такие как боль в пояснице, снижение концентрации гемоглобина сыворотки крови или потребность в переливании компонентов крови. Отсутствие гематомы в течении первого часа после биопсии является предиктором неосложненной процедуры [11].
Было показано, что у пациентов, у которых не была выявлена околопочечная гематома в течение часа после биопсии, не развивались серьезные осложнения в 95% наблюдений [12]. В то время как наличие гематомы прогнозировало серьезные осложнения в 43% наблюдений. Таким образом, регулярное использование ультразвукового исследования в течение первого часа после ТПБ может играть определенную роль в определении дальнейшей тактики лечения и прогнозировании осложнений. Однако, поскольку некоторые осложнения могут возникать позже, идеальное время наблюдения должно быть продолжено в течение 24 ч.
В серии из 750 биопсий нативной почки сообщалось, что 67% серьезных осложнений появились в течение первых 8 ч, поэтому наблюдение в течение 24 ч является гарантом безо-пасности при почечной биопсии [12].
Чрескожная биопсия почек (ЧБП) с использованием автоматических устройств для биопсии и ультрасонографии в режиме реального времени связана с относительно небольшим риском возникновения осложнений. Формирование обширной гематомы после ЧБП не является обязательным сигналом для выполнения ревизии. Следует комплексно оценивать клиническое состояние больного и риск при выполнении оперативного вмешательства.



