Введение. В настоящее время хронический простатит (ХП) остается одним из наиболее распространенных заболеваний среди мужчин независимо от возраста [1–3]. Согласно литературным данным, в нашей стране ХП выявляют у 19–42% мужчин, обратившихся к урологу [4–6].
Доля хронического абактериального простатита (ХАП) в структуре заболеваемости значительно превосходит долю бактериального простатита и может достигать 90% [1–3]. При этом как при абактериальном, так и при бактериальном вариантах заболевания первоначально воспаление в железе носит асептический характер, о чем свидетельствуют данные клинико-экспериментальных исследований [7]. Аутоиммунные процессы, химические воздействия при рефлюксе мочи и другие факторы могут приводить к «сбою» в системе неспецифической и специфической защиты организма, что создает условия для дальнейшего инфицирования простаты. Кроме того, возможно вторично-инфекционное происхождение заболевания, при котором инфекционный агент не определяется в секрете простаты/эякуляте вследствие механической обструкции протоков воспалительным отеком и фиброзом, сдавливающими их снаружи, и наличия фибринозных «пробок» внутри [6]. При этом продолжительность заболевания повышает вероятность перехода абактериальной формы простатита в бактериальную [8].
Лечение ХП также остается сложной задачей. В основе лечения бактериального простатита лежит длительное применение антибактериальной терапии [9–14]. Несмотря на отсутствие четких единых подходов к тактике лечения, по мнению многих ведущих зарубежных и отечественных специалистов, а также в соответствии с рекомендациями Европейскй ассоциации урологов (European Association of Urology, EAU), у больных ХАП обоснованно применение антибактериальной терапии в течение 4–6 нед., α-адреноблокаторов и нестероидных противовоспалительных средств [2, 13]. Тем не менее сохраняется проблема частых рецидивов заболевания [14].
Важное значение в развитии и рецидивировании ХП имеют иммунные защитные механизмы, как системные, так и локальные. Открытие системы цитокинов и определение их биологической роли в развитии и функционировании иммунной системы и в патогенезе большого спектра заболеваний человека привели к развитию нового направления в иммунотерапии – цитокинотерапии [15–20].
Отечественный препарат для проведения локальной цитокинотерапии Суперлимф® представляет собой естественный комплекс природных цитокинов, таких как фактор, угнетающий миграцию макрофагов, интерлейкин-1 (ИЛ-1), интерлейкин-6 (ИЛ-6), фактор некроза опухоли альфа (ФНО- α, TNF-α [tumor necrosis factor alpha], трансформирующий фактор роста TGF-β [transforming growth factor β]), а также антимикробные пептиды класса протегринов. Суперлимф® обладает противовирусным, противомикробным, противовоспалительным, иммуномодулирующим и репаративным действиями, подтвержденными результатами ряда исследований [21–29].
В 2022 г. нами было проведено исследование, целью которого стала оценка эффективности применения препарата Суперлимф® в составе комплексной терапии мужчин с ХАП [28]. Согласно полученным данным, наиболее высокие результаты продемонстрировала базовая комплексная терапия в сочетании с препаратом Суперлимф® 10 ЕД по 1 суппозиторию ректально 2 раза в сутки в течение 10 дней. Тем не менее полученные данные вследствие особенностей дизайна исследования не позволили оценить отдаленные результаты применения препарата Суперлимф® и его эффективность в профилактике рецидивов ХАП.
Цель исследования: оценить эффективность различных схем применения препарата Суперлимф® в профилактике рецидивов ХАП.
Материалы и методы. В исследование были включены 90 мужчин с ХП категории IIIa (National Institutes of Health, NIH, 1995) в стадии обострения [4].
Критерии включения в исследование: суммарный балл по шкале Международной системы суммарной оценки заболеваний предстательной железы в баллах (Internatiоnal Prоstate Symptоm Scоre, IРSS) от 8 до 19, Индекс шкалы симптомов ХП (National Institute Of Health Chronic Prostatitis Symptom Index, NIH-CPSI) более 10 баллов, объем остаточной мочи (Vом) менее 50 мл, уровень ПСА в крови не более 4 нг/мл, абактериальный характер воспаления, отсутствие сопутствующей медикаментозной терапии, подписанное информированное согласие на участие в исследовании.
Критерии невключения: конкременты мочевого пузыря и мочеточников, гематурия, подозрение на рак простаты или мочевого пузыря, отягощенный аллергический анамнез, оперативные пособия на органах малого таза, инфекции мочевыводящих путей, нейрогенная дисфункция мочевого пузыря, врожденные аномалии развития, онкологические и тяжелые сердечно-сосудистые заболевания, сахарный диабет.
В ходе визита 1 производилась оценка исходного состояния пациентов, выявлялось их соответствие критериям включения и невключения. Распределение пациентов на 3 группы по 30 человек производилось методом случайной выборки.
Всем пациентам была назначена базовая комплексная терапия ХАП, включившая поведенческую терапию, прием препарата из группы α1-адреноблокаторов (тамсулозин 0,4 мг 1 раз в день), антибактериального препарата из группы фторхинолонов (левофлоксацин 500 мг 1 раз в день) в течение 28 дней, а также препарат Суперлимф® 10 ЕД по 1 суппозиторию ректально 2 раза в сутки в течение 20 дней. Пациентам в группе сравнения (ГС) было рекомендовано динамическое наблюдение в последующие 12 мес. без проведения профилактических курсов.
В основной группе 1 (ОГ1) пациентам также проводилась базовая комплексная терапия, после которой были назначены профилактические курсы препарата Суперлимф ® 10 ЕД по 1 суппозиторию 1 раз в сутки в течение 10 дней каждые 3 мес. в течение 12 мес.
В основной группе 2 (ОГ2) пациентам была назначена аналогичная базовая терапия, после которой с целью профилактики были назначены курсы препарата Суперлимф® 10 ЕД по 1 суппозиторию 2 раза в сутки в течение 10 дней каждые 3 мес. в течение 12 мес.
Оценка эффективности лечения проводилась через 4 нед. (визит 2). Отдаленные результаты лечения оценивались через 3 (визит 3), 6 (визит 4) и 12 мес. (визит 5). Критериями эффективности служили средний балл по шкалам IPSS и оценки качества жизни (Quality of Life, QoL), средний балл по шкале NIH-CPSI, среднее значение максимальной скорости потока мочи (Qmax) и объема простаты (Vпж). Кроме того, был проведен анализ результатов микроскопического и бактериологического исследований секрета простаты.
Дополнительно в ходе исследования на визитах 1, 2 и 5 пациентам трех групп по данным трансректального ультразвукового исследования (ТРУЗИ) предстательной железы в дуплексном режиме сканирования была проведена оценка влияния проведенной терапии на гемодинамические показатели кровотока в простате. Оценивали пиковую систолическую (Vp), конечную диастолическую (Vd) и среднюю линейную скорости кровотока (Vm), а также индекс резистентности (RI) и пульсационный индекс (PI) при визуализации артерий простаты.
Для статистической обработки полученных данных были использованы программа MS Exel, 11.0 из стандартного пакета MS Office, 2013, а также программного обеспечения IBM SPSS Statistics, 21.0. При проверке статистических гипотез применяли методы параметрической (t-test Cтьюдента) статистики. При оценке достоверности выявленных различий между средними значениями выборок рассчитывали параметр р; вероятность справедливости нулевой гипотезы была принята равной 5% (р<0,05).
Результаты. Исходно у всех пациентов выявлены клинические симптомы, характерные для обострения ХП. Согласно результатам бактериологического исследования секрета простаты, рост возбудителей не зарегистрирован. Все пациенты соответствовали критериям включения, критериев невключения не выявлено.
Исследуемые группы были однородными, результаты обследований, полученные до лечения, статистически значимо не различались (р>0,05). В течение периода лечения комплаентность пациентов составила 100%, все пациенты соблюдали назначения врача, случаев отказа от терапии не было. Кроме того, нежелательных явлений, связанных с приемом препарата Суперлимф®, отмечено не было.
Результаты клинико-лабораторных и инструментальных исследований, полученных в трех исследуемых группах в течение 12 мес. терапии и наблюдения, представлены в табл. 1.
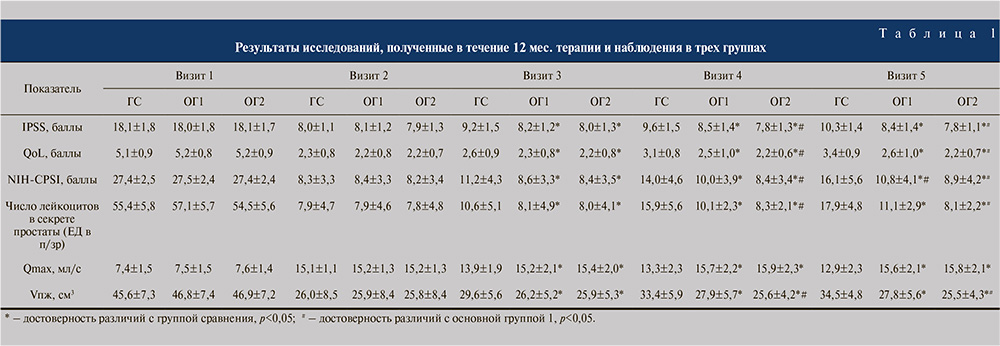
На визите 2 через 4 нед. терапии в трех группах зарегистрирована положительная динамика всех исследуемых показателей. Различия между показателями в трех группах были статистически не значимыми (p>0,05). Средний балл по шкале IPSS уменьшился на 10,2 балла (56,4% от исходного значения), по шкале Qol – на 2,9 балла (57,7% от исходного значения), а по шкале NIH-CPSI – на 19,2 балла (70,2% от исходного значения) (p<0,01). Число лейкоцитов в секрете простаты уменьшилось до уровня нормы в среднем с 57,1 до 7,9 в поле зрения (на 86,2% от исходного значения) (p<0,001). Среднее значение Qmax увеличилось до 15,2 мл/с (на 51,3% от исходного значения) (p<0,001). За 28 дней терапии Vпж уменьшился в среднем на 44,9% от исходного значения (p<0,001). Таким образом, результаты, полученные на визите 2, свидетельствуют об эффективности базовой комплексной терапии ХАБ во всех трех группах.
Через 3, 6 и 12 мес. терапии и наблюдения были зарегистрированы статистически значимые различия между результатами в ГС и основных группах.
Согласно данным, полученным по результатам заполнения шкалы IPSS на визите 3, средний балл в ГС увеличился на 1,2 (21,2% от исходного значения) (p<0,05). В ОГ1 и ОГ2 изменение данного показателя было статистически незначимым в пределах 0,1 балла (p>0,05). Различия между результатами в ОГ1 и ОГ2 были статистически не значимыми (p>0,05) и достоверно отличались от среднего балла по шкале IPSS в ГС (p<0,01).
Через 6 и 12 мес. на визитах 4 и 5 соответственно сохранялись статистически значимые различия между ГС и основными группами (p<0,05). При этом к концу периода наблюдения (визит 5) значение данного показателя в ГС увеличилось в среднем на 2,3 (22,3%) балла по сравнению с результатами, полученными после базовой комплексной терапии на визите 2 (p<0,05). Между результатами в ОГ1 и ОГ2 через 3 мес. терапии и наблюдения были зарегистрированы статистически значимые различия (p<0,05), которые сохранились до визита 5. При этом в ОГ1 средний балл по шкале IPSS увеличился в среднем на 0,3 балла – с 8,2 до 8,5 баллов, а в ОГ2, наоборот, уменьшился на 0,2 балла.
При оценке качества жизни по шкале, согласно опроснику QoL, в ГС в течение периода наблюдения также была зарегистрирована отрицательная динамика. Средний балл увеличился с 2,6 на визите 3 до 3,4 на визите 5 на 0,8 балла (23,5%) (p<0,05). Результаты в ОГ1 и ОГ2 статистически значимо отличались от таковых в ГС (p<0,05).
На визитах 4 и 5 сохранялись статистически значимые различия между ГС и основными группами (p<0,01). Однако в ОГ1 средний балл по шкале QoL увеличился с 2,3 на визите 3 до 2,6 на визите 5, тогда как в ОГ2 среднее значение данного показателя не изменилось и составило 2,2 балла. Различия между всеми тремя группами на визитах 4 и 5 были статистически значимыми (p<0,05).
В группах, в которых пациентам был назначен профилактический прием препарата Суперлимф®, результат по шкале NIH-CPSI на визитах 3–5 был статистически значимо лучше, чем в ГС (p<0,001). Средний балл в ГС за период наблюдения увеличился с 8,3 балла на визите 2 до 16,1 балла на визите 5 (на 7,8 балла, или 48,4%) (p<0,05).
В ОГ1 средний балл по шкале NIH-CPSI за этот период увеличился на 2,4 балла (22,2%) до 10,8 балла, а в ОГ2 – на 0,7 балла (7,8%). Между основными группами на визитах 4 и 5 были также выявлены статистически значимые различия (p<0,05).
При анализе секрета ПЖ ГС в течение периода наблюдения ГС было зарегистрировано увеличение числа лейкоцитов на визитах 3–5 с 7,9 в поле зрения до 17,9 в поле зрения (p<0,05). Полученные в ГС результаты также статистически значимо отличались от таковых в ОГ1 и ОГ2 (p<0,01).
В течение периода наблюдения и профилактического приема препарата Суперлимф® число лейкоцитов в ОГ1 в среднем увеличилось на 3,2 в поле зрения, а в ОГ2 на 1,3 в поле зрения. На визитах 4 и 5 различия между результатами в основных группах были статистически значимыми (p<0,05).
По данным микробиологического исследования секрета простаты на визитах 3–5 роста микрофлоры во всех группах выявлено не было.
За 12 мес. наблюдения в ГС была также зарегистрирована отрицательная динамика изменения Vпж. После значительного уменьшения на фоне проведенной базовой комплексной терапии с визита 2 по визит 5 данный показатель увеличился на 8,5 см3 (24,6%) (p<0,05). В ОГ2 среднее значение Vпж практически не изменилось, тогда как в ОГ1 была также зарегистрирована динамика уменьшения объема простаты. Значения показателя на визитах 3–5 в основных группах были статистически значимо меньше, чем в ГС (p<0,01). Между ОГ1 и ОГ2 были зарегистрированы статистически значимые различия на визитах 4 и 5 (p<0,05).
Среднее значение Qmax в ГС статистически значимо отличалось от результатов в ОГ1 и ОГ2 на визитах 3–5 (p<0,01). За период наблюдения средняя максимальная скорость потока мочи в ГС снизилась на 2,2 до 12,9 мл/с на визите 5 (p<0,05). Данный показатель в ГС статистически значимо отличался от результатов в основных группах (p<0,01). Между показателями в ОГ1 и ОГ2 достоверных различий за период терапии и наблюдения выявлено не было (p>0,05).
Показатели гемодинамики в сосудах простаты в течение 12 мес. терапии и наблюдения в трех группах представлены в табл. 2.
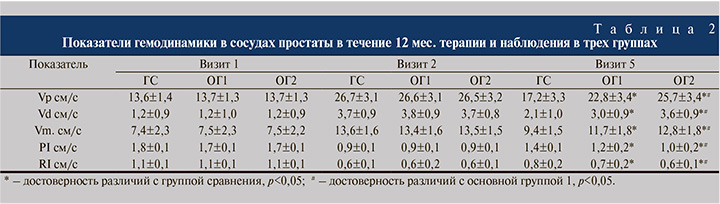
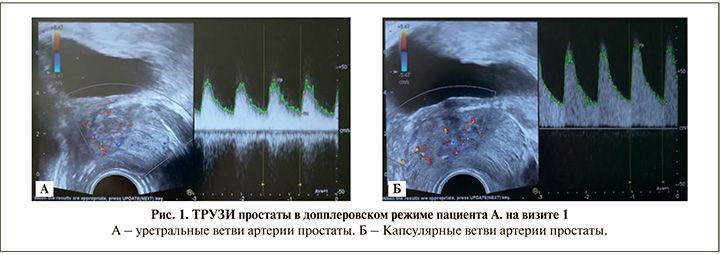
Исходно у пациентов трех групп выявлено нарушение гемодинамики в предстательной железе, о чем свидетельствуют низкие значения Vp, Vd и Vm, а также высокие значения PI и RI (см. табл. 2). Между результатами в ГС и основных группах статистически значимых различий на визите 1 не выявлено (p>0,05). Пример ТРУЗИ простаты в допплеровском режиме пациента А. из ОГ2 на визите 1 представлен на рис. 1.
Через 4 нед. базовой комплексной терапии отмечена статистически значимая положительная динамика всех исследуемых показателей (p<0,05). Так, среднее значение Vp в группах увеличилось на 13,1 см/с (на 49% от исходного значения) (p<0,05), а среднее значение PI уменьшилось на 0,9 см/с (на 50% от исходного значения) (p<0,05). При этом на визите 2 между результатами в ГС, ОГ1 и ОГ2 также не было выявлено статистически значимых различий (p>0,05).
К концу периода наблюдения на визите 5 было выявлено ухудшение гемодинамических показателей в ГС (p<0,05). Vp в данной группе уменьшился на 35,6%, Vd – на 43,2%, а Vm – на 30,8%, в то время как PI увеличился на 35,7%, а RI – на 25%, согласно полученным данным. В ОГ1 гемодинамические показатели ухудшились, однако были статистически значимо лучше, чем в ГС (p<0,05) (см. табл. 2). Vp в ОГ1 уменьшился на 14,2%, Vd – на 21,1%, а Vm – 12,7%, в то время как PI увеличился на 25%, а RI – на 14,3%.
В ОГ2 гемодинамические показатели статистически значимо не изменились и были достоверно лучше, чем в ГС и ОГ1 (p<0,05).
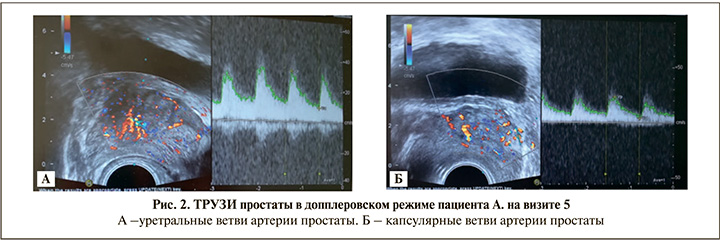
Пример ТРУЗИ простаты в допплеровском режиме пациента А. из группы ОГ2 на визите 5 представлен на рис. 2.
В течение 12 мес. терапии и наблюдения в ГС рецидивы были зарегистрированы у 21 (70%) пациента, в ОГ1 – у 7 (23%), в ОГ2 – у 3 (10%) пациентов. Таким образом, в ОГ1 и ОГ2, где пациенты получали профилактическую терапию препаратом Суперлимф®, частота рецидивов была меньше на 47 и 60% соответственно.
Обсуждение. Лечение ХАП является сложной задачей в связи с разнообразием патогенетических механизмов развития заболевания и отсутствием единых подходов к терапии [6–9]. Серьезной проблемой является не только низкая эффективность терапии, но и частые рецидивы заболевания, которые требуют поиска новых подходов к лечению и профилактике рецидивов ХАП.
Многие авторы рекомендуют начинать лечение ХАП с антибактериальной терапии продолжительностью 4–6 нед. в сочетании с α-адреноблокаторами и НПВС [12–14]. Эффективность подобной комбинированной терапии продемонстрирована в мета-анализе, проведенном А. Thakkinstian и соавт., результаты которого выявили достоверные различия между значением общего среднего балла по шкале NIH-CPSI при одновременной терапии антибиотиками и α-адреноблокаторами по сравнению с плацебо [12].
Тем не менее в исследовании, проведенном нами в 2022 г. [28], показано, что, несмотря на эффективность комбинированной терапии антибактериальными препаратами в сочетании с α-адреноблокаторами, которая позволила снизить число лейкоцитов в секрете простаты в группе сравнения на 85,4% в течение 4 нед. терапии, а также уменьшить выраженность СНМП (поллакиурию на 51,1%, ноктурию на 55,8%), снизить средний балл по шкалам IPSS на 39,1% и NIH-CPSI на 52%, значения исследуемых показателей через 4 нед. терапии не достигли референтных значений, что в целом подтверждает мнение некоторых авторов о недостаточной эффективности стандартных методов терапии ХАП [14–16].
В настоящее время продолжает активно изучаться роль иммунной системы и иммунных нарушений в развитии и рецидивировании ХП.
В исследовании 2002 г. L. J. Miller и соавт. зарегистрировали значительно более высокие уровни ИЛ-10, -2 и ИФН-γ в спермоплазме пациентов с ХП. При этом уровень ИЛ-10 достоверно коррелировал с тяжестью симптоматики ХП по данным шкалы NIH-CPSI [17].
В 2021 г. L. Chen и соавт. выявили значительное повышение ИЛ-1, -6, α-ФНО и иммуноглобулинов в секрете простаты и семенной жидкости у мужчин с ХП [18].
Сегодня цитокинотерапия широко применяется в урологии, в частности при лечении инфекционно-воспалительных заболеваний, что во многом связано со способностью модулировать иммунный ответ, а также с универсальными механизмами действия в отношении различных возбудителей, которые не позволяют микроорганизмам формировать факторы резистентности [24–29].
Результаты одного из первых отечественных исследований продемонстрировали эффективность препарата Суперлимф® в сочетании с антибактериальной терапией фторхинолонами больных ХП в 72% наблюдений [24, 25].
Полученные нами в ходе исследования 2022 г. результаты продемонстрировали эффективность Суперлимфа® в комплексной терапии пациентов с ХАП [28]. Согласно данным исследования, в группах пациентов, получавших цитокинотерапию в составе комплексного лечения, уже через 14 дней уменьшилось количество мочеиспусканий на 28,4, снизился средний балл по шкалам IPSS на 38,3%, QoL – на 45,9%, NIH-CPSI – на 37,4%, уменьшилось количество лейкоцитов в секрете простаты на 52,1%. Через 28 дней терапии показатели достигли нормальных значений. При этом наиболее быстрый и выраженный эффект был достигнут при применении препарата Суперлимф® в дозировке 10 ЕД 1 свеча 2 раза в день в течение 20 дней.
С учетом этих данных в нашем исследовании всем пациентам с ХАП была проведена базовая комплексная терапия, α1-адреноблокаторами (тамсулозин 0,4 мг 1 раз в день) в сочетании с антибиотиками из группы фторхинолонов (левофлоксацин 500 мг 1 раз в день) в течение 28 дней, а также цитокинотерапией препаратом Суперлимф® 10 ЕД по 1 суппозиторию ректально 2 раза в сутки в течение 20 дней. Полученные в ходе исследования результаты подтверждают эффективность данного режима терапии.
На визите 2 через 4 нед. после начала терапии была зарегистрирована статистически значимая положительная динамика исследуемых показателей в основных группах и ГС. Так, средний балл по шкале IPSS уменьшился на 56,4% от исходного значения, по шкале Qol – на 57,7%, по шкале NIH-CPSI – на 70,2%, количество лейкоцитов в секрете простаты уменьшилось до уровня нормы – до 7,9 в поле зрения, что на 86,2% меньше исходного значения. Среднее значение Qmax также увеличилось до нормального показателя 15,2 мл/с, что на 51,3% выше исходного значения (p<0,001).
Также был проведен сравнительный анализ эффективности двух различных режимов приема препарата Суперлимф® в отношении профилактики рецидивирования заболевания.
В ОГ1 пациентам препарат был назначен в дозе 10 ЕД 1 раз в день, в ОГ2 – по 10 ЕД 2 раза в день. Согласно полученным данным, через 3 мес. результаты статистически не различались. Однако через 6 и 12 мес. результаты в ОГ2 были статистически значимо лучше, чем в ОГ1. Кроме того, в течение 12 мес. терапии количество рецидивов в ОГ2 было меньше в 2,3 раза.
Полученные результаты, на наш взгляд, в первую очередь могут быть связаны с иммуномодулирующим, противовоспалительным и репаративным действиями препарата, описанными в ряде исследований [24–27], которые, с одной стороны, препятствуют развитию воспаления в простате, с другой – ускоряют течение воспалительного процесса, сокращая его негативное действие на ткань железы. Одним из ключевых звеньев в формировании продуктивного процесса воспаления в соединительной ткани является стимуляция функции фибробластов макрофагальными цитокинами.
Согласно результатам недавнего мета-анализа, включившего 24 клинических рандомизированных и 10 экспериментальных исследований, иммунные цитокинопосредованные реакции играют важную роль в патогенезе хронического простатита, способствуя персистенции внутрипростатического воспаления [18–20]. Соединительнотканные очаги на фоне воспалительного процесса, сопровождающегося отеком и нарушением микроциркуляции, самостоятельно способствуют усилению застойного синдрома в ПЖ, тем самым замыкая «порочный круг» и интенсифицируя течение заболевания. Следовательно, продолжительность воспалительного процесса в тканях влияет на вероятность развития склеротических изменений в ткани простаты, которые в свою очередь могут приводить к усилению воспалительного процесса и рецидивам заболевания.
Действие препарата способствует уменьшению отека предстательной железы, возникающего вследствие воспаления, что в свою очередь может оказывать положительное влияние на местный кровоток, в конечном итоге – уменьшать выраженность фиброзных изменений в простате. Это подтверждают результаты ультразвукового исследования, полученные в ходе исследования в трех группах.
Так, объем предстательной железы в ГС после значительного уменьшения на фоне проведенной базовой комплексной терапии увеличился на 24,6% с визита 2 по визит 5, тогда как в ОГ2 среднее значение данного показателя значимо не изменилось. А по данным допплерографического исследования, к концу периода наблюдения на визите 5 гемодинамические показатели в ГС были статистически значимо хуже, чем в ОГ1 и ОГ2.
Отдельно следует отметить, что в течение всего исследования в результатах микробиологического посева секрета простаты роста микроорганизмов выявлено не было.
Из-за различных факторов, таких как нарушение дренажа предстательной железы, обтурация протоков ацинусов, некоторые формы простатита симулируют ХП категории IIIb. Некоторые авторы рекомендуют назначение α-адреноблокаторов пациентам c целью более эффективного дренирования ацинусов, в некоторых случаях это приводит к выявлению бактерий в секрете простаты в процессе лечения больных ХАП. Согласно литературным данным, почти в половине случаев простатит категории IIIа может иметь инфекционное происхождение [13–15].
С одной стороны, отсутствие роста микроорганизмов в секрете простаты у пациентов может свидетельствовать об эффективности проведенной антибактериальной терапии. Однако сохранение эффекта антимикробной терапии в течение 12 мес. маловероятно. С другой стороны, полученные результаты могут быть связаны с наличием антимикробного действия у препарата Суперлимф® [21–27].
Суперлимф® содержит в своем составе АМП (цитокины) класса протегринов, считающиеся одними из наиболее мощных АМП, за счет которых препарат оказывает прямое антимикробное действие. Кроме этого препарат обладает не только прямым антибактериальным действием, но и опосредованным через активацию выхода лизосомальных ферментов (катепсина Д) из лизосом лейкоцитов.
Антимикробный эффект препарата Суперлимф® также подтвержден в исследовании профессора С. И. Гамидова, проведенном в 2023 г. [29]. В нем приняли участие 60 мужчин из бесплодных пар с верифицированной, по данным микробиологического посева эякулята, инфекцией добавочных половых желез (MAGI – «male accessory gland infection»), готовившихся к применению ВРТ. Все пациенты были разделены на две группы, в одной из которых проводилась монотерапия препаратом Суперлимф®, в другой – антибактериальная терапия доксициклином по 100 мг 2 раза в сутки 28 дней. Согласно представленным данным, эрадикация микроорганизмов, по данным бактериологического исследования, произошла у 57,1% пациентов в группе получавших монотерапию Суперлимфом® и у 88% в группе получавших антибактериальную терапию.
Заключение. Таким образом, применение препарата Суперлимф® у пациентов с ХАП в качестве профилактической терапии каждые 3 мес. способствовало более длительному сохранению терапевтического эффекта проведенной терапии и улучшению гемодинамики предстательной железы, что в свою очередь привело к увеличению продолжительности безрецидивного периода и уменьшению числа рецидивов в течение 12 мес. в 7 раз при проведении профилактических курсов препарата Суперлимф® 10 ЕД 2 раза в сутки в течение 10 дней и в 3 раза при проведении профилактических курсов препарата Суперлимф® 10 ЕД 1 раз в сутки в течение 10 дней. Наиболее эффективной схемой профилактического применения препарата у пациентов с ХАП по результатам проведенного исследования является применение препарата Суперлимф® 10 ЕД по 1 суппозиторию 2 раза в сутки в течение 10 дней каждые 3 мес.



