Введение. Мочекаменная болезнь (МКБ) – одно из самых распространенных урологических заболеваний, а доля больных уролитиазом в профильных отделениях достигает 30–40% [1]. Последние десятилетия ознаменовались бурным научно-техническим прогрессом в урологии, что привело к разработке и совершенствованию аппаратов для контактной литотрипсии, а также эндоскопического оборудования для удаления мочевых конкрементов [2, 3]. Современным общемировым трендом в оперативном лечении больных МКБ является сокращение доли дистанционной литотрипсии за счет увеличения числа эндоскопических вмешательств, обладающих высокой эффективностью при низком уровне осложнений и обеспечивающих сокращение сроков нахождения в стационаре вследствие быстрого периода восстановления больного после операции [4].
На современном этапе технологический прогресс происходит по пути совершенствования гибких эндоскопов и уменьшения калибра инструментария для чрескожной хирургии уролитиаза, что привело к созданию одноразовых фиброуретеронефроскопов и появлению микронефроскопа. Применение этих современных инструментов в лечении больных с камнями почек подразумевает использование мочеточниковых кожухов, необходимых для поддержания низкого внутрилоханочного давления и оптимальной температуры промывной жидкости, а также улучшения элиминации фрагментов и обеспечения хорошей визуализации за счет повышения прозрачности оптической среды. Помимо положительных эффектов размещение мочеточникового кожуха имеет и негативные последствия, к которым относят вероятность повреждения стенки мочеточника и риск образования в нем стриктур [5–7].
Невозможность первичной установки кожуха в интактные верхние мочевыводящие пути варьируется в диапазоне 5,9–36,7% [8–11, 18, 26]. Для повышения успеха этого пособия, а также с целью снижения количества осложнений разработаны методики, преимущественно направленные на расширение верхних мочевыводящих путей перед операцией. К ним относят предстентирование, пероральный прием альфа-адреноблокаторов, баллонную и фармакологическую дилатацию мочеточника [12–15].
В настоящее время существуют методы измерения диаметра мочеточника в его нижней трети с целью предсказания исхода лечения пузырно-уретерального рефлюкса [16, 17]. Технологии достоверного прогнозирования успешности установки кожуха в интактный мочеточник отсутствуют.
Цель исследования: улучшить результаты лечения больных МКБ, подвергшихся эндоскопическим вмешательствам с использованием мочеточникового кожуха путем разработки прогностической модели дилатации непредстентированного мочеточника.
Материалы и методы. Дизайн исследования предполагал участие 180 пациентов с камнями почек до 20 мм на базе клиники урологии Военно-медицинской академии им. С. М. Кирова и включал два этапа – предоперационную диагностику и интраоперационное исследование. Больные были разделены на две группы. В первой (I) группе (n=79) применялся мочеточниковый кожух 12/14 Ch, у пациентов второй (II) группы (n=101) использовался кожух 10/12 Ch.
В первой группе 48 (60,8%) пациентам выполнена микроперкутанная нефролитотрипсия (микро-ПНЛ) и 31 (39,2%) – трансуретральная нефролитотрипсия (ТНЛТ), в группе II 42 (41,6%) и 59 (58,4%) больных подверглись соответствующим вмешательствам.
Обе категории больных не имели статистических различий по полу, возрасту, индексу массы тела, количеству и размеру камней.
Критериями включения являлись возраст старше 18 лет, наличие камня почки до 20 мм, отсутствие предстентирования мочеточника в анамнезе или предшествующей операции, прием альфа-адреноблокаторов, а также наличие уровня скорости клубочковой фильтрации более 90 мл/мин.
Критериями невключения установлены беременность, острые инфекционно-воспалительные заболевания верхних и нижних мочевыводящих путей, отсутствие функции почки на стороне поражения, нарушение свертывающей системы крови, а также несогласие больного участвовать в исследовании.
На этапе предоперационной диагностики за 60 мин до рентгенологического исследования пациент однократно принимал внутрь 80 мг фуросемида. Далее выполнялась компьютерная томография органов брюшной полости и таза с внутривенным контрастированием по стандартной методике на аппарате «Toshiba Aquilion 128» (Япония). Оценка выделительной функции почек осуществлялась на седьмой минуте исследования. Одним из необходимых условий являлось заполнение мочевого пузыря до появления у пациента физиологического позыва в момент проведения рентгенологической диагностики. После цифрового преобразования данных компьютерной томографии и построения 3D-структуры верхних мочевыводящих путей при помощи программы обработки изображений DICOM «RadiAnt DICOM Viewer» производилась визуальная оценка мочеточника для исключения значительных девиаций и стриктур. Далее измерялся диаметр мочеточника (dм) в трех контрольных точках: в пиелоуретеральном сегменте, на уровне пересечения мочеточника с подвздошными сосудами и в юкставезикальном отделе (рис. 1). Форсирование диуреза на фоне приема фуросемида приводило к тому, что темп поступления мочи из почек превосходил эвакуаторную способность мочеточника, за счет чего достигалось его тугое наполнение, а выводимое контрастное вещество способствовало четкому изображению верхних мочевыводящих путей, что позволяло производить замеры в наиболее узких местах.
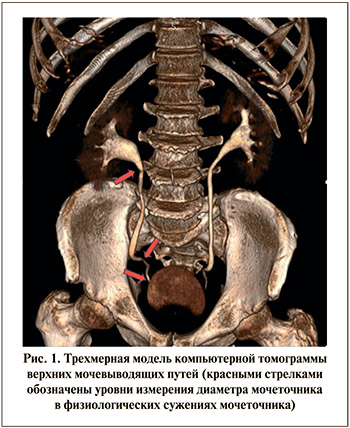
С целью стандартизации методики всем пациентам на интраоперационном этапе непосредственно перед операцией выполнялась диагностическая уретероскопия при помощи ригидного уретероскопа 9,5 Ch. В случае если эндоскопом не удавалось осмотреть весь мочеточник ввиду значительной его тракции и высокого риска травматизации, устанавливался наружный мочеточниковый катетер 6 Ch и выполнялась микро-ПНЛ. В ситуациях, когда уретероскопия проходила без технических особенностей и мочеточник был доступен осмотру на всем протяжении, осуществлялось введение кожуха и производилась ТНЛТ или микроперкутанная операция.
Оценке подвергалось число случаев успешной установки мочеточникового кожуха, под которым понимали его размещение непосредственно ниже пиелоуретерального сегмента при ТНЛТ и в лоханке при микро-ПНЛ. Невозможность проведения кожуха до этих уровней ввиду значительного натяжения и сопротивления тканей считалось безуспешной попыткой.
Всем больным после выполнения оперативного вмешательства выполнялась уретероскопия на предмет диагностики уретеральных повреждений. Оценка травматического воздействия мочеточникового кожуха определялась согласно эндоскопической классификации повреждений стенки мочеточника (табл. 1), предложенной O. Traxer и A. Thomas в 2012 г. [19].

Построение прогноза успешной установки мочеточникового кожуха в зависимости от диаметра мочеточника в физиологических сужениях проводили с помощью ROC-анализа (Receiver Operator Characteristic), который демонстрировал зависимость количества верно классифицированных положительных примеров от количества неверно классифицированных отрицательных значений. Оценка надежности выражалась в показателях чувствительности (Se) и специфичности (Sp). Прогностическая сила определялась площадью под кривыми (AUC). При этом считали, что чем ближе показатель AUC к 1,0, тем лучшей предсказательной возможностью обладает модель. В соответствии с экспертной шкалой для значений AUC принимали следующие значения: 0,9–1,0 – отличный, 0,8–0,9 – очень хороший, 0,7–0,8 – хороший, 0,6–0,7 – средний, 0,5–0,6 – неудовлетворительный прогноз. Количественные данные описывались с помощью средних арифметических величин и границ 95% доверительного интервала.
Результаты. На этапе предоперационного планирования построение трехмерной реконструкции органов мочевой системы при изучении компьютерных томограмм позволило у всех пациентов произвести измерение диаметра просвета мочеточника в контрольных точках. Установлено, что из всех физиологических сужений наибольшую ширину мочеточник имеет в пиелоуретеральном сегменте и в группе I составил 3,04±0,2 мм, в группе II – 2,9±0,03 мм. Наименьший диаметр зафиксирован в юкставезикальном отделе – 1,9±0,06 и 1,84±0,7 мм соответственно (табл. 2). При этом достоверных различий средних значений dм в исследуемых группах выявлено не было.
В группе I (n=79) успешная установка уретерального кожуха отмечена у 37 (46,8%) пациентов, в группе II (n=101) – у 84 (83,2%) больных (p<0,05). Остальным 42 (53,2%) и 17 (16,8%) пациентам соответственно размещение кожуха 12/14 Ch и 10/12 Ch было невозможно вследствие значительного сопротивления тканей и высокого риска травматического повреждения (табл. 3).

При этом наиболее частые случаи безуспешной установки при использовании мочеточниковых кожухов 12/14 Ch и 10/12 Ch отмечены на уровне юкставезикального отдела – в 23 (54,8%) и 9 (52,9%) наблюдений соответственно.
Эффективность лечения не зависела от диаметра мочеточникового кожуха. Так, полного удаления камня при микро-ПНЛ с применением кожуха 12/14 Ch удалось достигнуть у 69 (87,3%) пациентов, а в случае установки 10/12 Ch – у 81 (80,2%) (р>0,05). Показатель избавления от камней методом ТНЛТ при использовании оболочек 12/14 и 10/12 также не имел статистического различия и составил 87,1 и 88,1% соответственно.
В ходе визуального осмотра верхних мочевыводящих путей при удалении мочеточникового кожуха общее количество повреждений мочеточника составило 35 (44,3%) и 40 (39,6%) наблюдений соответственно при использовании кожухов 12/14 Ch и 10/12 Ch. При этом нежелательные явления I степени наблюдались у 24 (30,4%) больных первой группы и у 31 (30,7%) пациентов второй группы, травматические изменения II степени выявлены у 10 (12,7%) и 9 (8,9%) пациентов соответственно (р>0,05). Лишь у 1 (1,3%) пациента при установке кожуха 12/14 Ch определено повреждение стенки мочеточника, которое затронуло слизистую оболочку с гладкомышечным слоем и частичным разрывом адвентиции, что соответствовало III степени осложнений.
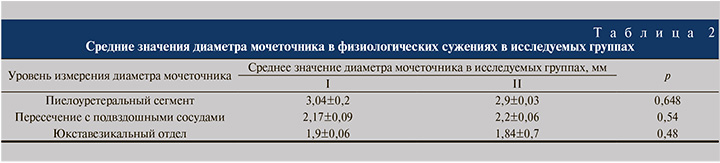
ROC-анализ является объективным графическим и математическим методом и позволил наглядно продемонстрировать распознавательную способность метода. Для определения диагностической значимости количественных признаков dм при прогнозировании возможности установки мочеточниковых кожухов 12/14 Ch и 10/12 Сh были построены ROC-кривые (рис. 2).
В первой группе площадь под ROC-кривой (AUC) составила 0,925 (95% CI: 0,871–0,98), а уровень значимости отличия положения кривой от биссектрисы не превышал 5% (p<0,001), что свидетельствовало об отличной предсказательной способности. Чувствительность и специфичность прогностической модели для установки мочеточникового кожуха 12/14 Ch показали высокие значения – Se=0,838 (95% CI: 0,689–0,923) и Sp=0,89 (95% CI: 0,77–0,93) соответственно. У пациентов второй группы площадь под ROC-кривой была 0,811 (95% CI: 0,661–0,96), а уровень значимости не превышал 5% (p<0,001). Чувствительность находилась на уровне 0,833 (95% CI: 0,739–0,898), а специфичность Sp=0,706 (95% CI: 0,496–0,867). Диагональная линия соответствовала «бесполезному» классификатору (AUC=0,5), т.е. полной неразличимости двух классов в отношении возможности и невозможности установки мочеточникового кожуха.
Таким образом, диагностическая эффективность прогностической модели при использовании кожухов 12/14 Ch и 10/12 Ch подтверждена высокими показателями AUC=0,925 (95% CI: 0,871–0,98) и 0,944 (95% CI: 0,89–0,97) соответственно.
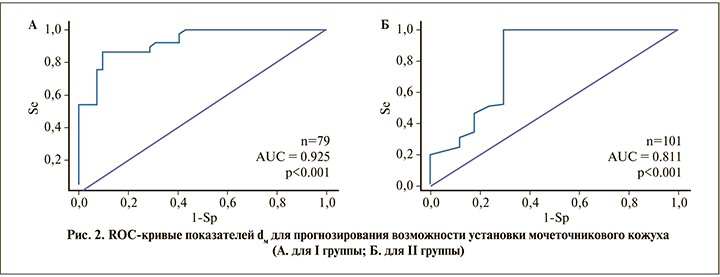
Разделяющее значение количественного признака в «точке отсечения» рассчитывалось по наивысшему значению индекса Юдена. Определение оптимального порога задавалось по критерию обеспечения минимальной чувствительности теста Se ≥0,8. В первой группе пороговое значение dм в «точке отсечения» составило 2 мм, что свидетельствовало о том, что возможность успешной установки уретерального кожуха 12/14 Ch прогнозировалась при диаметре мочеточника ≥2 мм на любом уровне измерения. Во второй группе пороговое значение показателя dм в «точке отсечения» составило 1,6 мм, а высокая вероятность установки оболочки 10/12 Ch прогнозировалась при ширине мочеточника ≥1,6 мм на каждом измеряемом уровне (рис. 3).
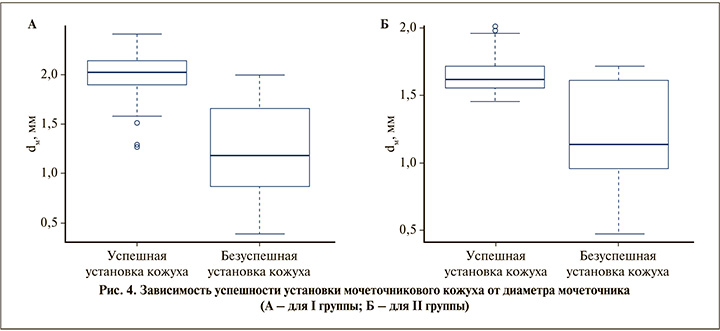
В первой группе средние значения диаметра мочеточника в физиологических сужениях при успешной установке кожуха составили 2,0±0,1 мм, при невозможности установки кожуха – 1,2±0,4 мм (р<0,05). Во второй группе аналогичные показатели отмечались при значении dм 1,6±0,1 и 1,2±0,5 мм соответственно (рис. 4).
Обсуждение. Научные публикации подтверждаю, что использование мочеточникового кожуха снижает внутрилоханочное давление, риск развития инфекционных осложнений, а также температуру ирригационной жидкости за счет улучшения оттока. Данные о влиянии последнего на интенсивность послеоперационного болевого синдрома, вероятность развития стриктур мочеточника не убедительны [19, 21, 22].
Литературные источники свидетельствуют о невозможности установки уретеральной оболочки в предстентированный мочеточник в 1,5–6,2% случаев [11, 26, 26].
В нашем исследовании позиционирование кожуха осуществлялось в интактный мочеточник после предварительного определения его проходимости при помощи уретероскопа, а также без использования подготовительных дилатирующих методик.
Предстентирование в течение как минимум 1 нед приводит к повышению эффективности установки мочеточниковых кожухов. Несмотря на многочисленные сообщения о положительном влиянии предоперационного введения альфа-адреноблокаторов, данные остаются противоречивыми. Все эти расхождения в значительной степени можно объяснить высоким риском системной ошибки при тщательном изучении всех полученных данных [12, 13, 23, 24].
Остается дискутабельным вопрос эффективности применения кожухов различного диаметра. В соответствии с немногочисленными публикациями установлено, что кожухи меньшего размера (<12/14 Ch) приводят к снижению рисков повреждения стенки мочеточника, а большего размера (≥12/14 Ch) – улучшают эффективность оперативного лечения [6, 25].
В настоящее время отсутствуют простые и доступные способы неинвазивного измерения степени дилатации мочеточника перед установкой мочеточникового кожуха.
В литературных источниках встречаются упоминания о различных методиках исследования его диаметра и разработанных на основании этого коэффициентах. Так, M. Hellström и соавт. (1986) впервые предложили использовать уровень дилатации мочеточника на основании определения диаметра в его нижней трети с целью прогнозирования результатов лечения везико-уретерального рефлюкса у детей [16]. В 2016 г. Б. М. Лолаева и соавт. усовершенствовали метод путем разработки коэффициента его расширения для оценки результатов оперативного и эндоскопического лечения обструктивного мегауретера [17]. Отличительной особенностью указанных способов являлось измерение уретерального диаметра мочеточника только на одном заданном уровне и с последующим вычислением авторских коэффициентов с привязкой к анатомическим ориентирам. Наиболее современным методом измерения ширины мочеточника с целью снижения риска его травматизации является технология, предложенная J. Fulla и соавт. (2021), которая основана на изучении данных компьютерной томографии без внутривенного контрастирования. Отсутствие анализа экскреторной фазы исследования является отрицательным моментом этой методики, поскольку не позволяет оценить важные факторы, влияющие на установку кожуха, диагностировать девиации, патологические участки сужений, а также дилатационные возможности мочеточника [18]. В отличие от представленных способов предложенная нами методика прогнозирования степени дилатации мочеточника лишена этих недостатков и имеет высокий диагностический потенциал при планировании оперативного вмешательства на верхних мочевыводящих путях.
Заключение. Измерение поперечного сечения мочеточника в физиологических сужениях по предложенной методике позволяет прогнозировать возможность свободного проведения кожуха в верхние мочевые пути на этапе предоперационного планирования. Вероятность беспрепятственной установки мочеточникового кожуха 10/12 и 12/14 Ch при диаметре мочеточника в физиологических сужениях более 1,6 и 2 мм соответственно составляет 95%. Установка мочеточникового кожуха является безопасной процедурой, а большинство осложнений относится к первой и второй степеням градации повреждения мочеточника.



