В последнее десятилетие произошли значительные изменения в определении подходов к диагностике и лечению артериальной гипертензии (АГ). Целью этих изменений является увеличение числа пациентов с АГ с достижением целевых уровней артериального давления (АД), что должно обеспечить снижение риска развития сердечно-сосудистых осложнений (ССО). Актуальность этой задачи обусловлена тем, что, по данным эпидемиологических и клинических исследований, хотя распространенность АГ во всем мире высока, контроль АГ, т.е. достижение целевого уровня АД, в разных странах недостаточный. Учитывая, что АГ является важнейшим фактором риска (ФР) развития сердечно-сосудистых заболеваний (ССЗ) и повышения сердечно-сосудистой смертности (ССС), а также то, что распространенность АГ во всех странах и в России выше, чем других ФР, задачей первостепенной важности следует признать максимально полное использование наиболее рациональных методик лечения пациентов с АГ.
Важнейшие стратегии по выбору антигипертензивных препаратов представлены в Рекомендациях Европейского общества по артериальной гипертонии (ЕОАГ) и Европейского общества кардиологов (ЕОК) по лечению АГ (2013) [1]. Современное лечение АГ основано на представлениях о необходимости эффективного снижения АД до целевого уровня для профилактики ССЗ и снижения ССС. Достижение целевого АД — основная задача лечения, сформулированная в международных и российских рекомендаций по АГ [2]. Признано, что непосредственное снижение АД, т.е. снижение АД per se, благоприятно влияет на прогноз. Целевым является уровень АД <140/90 мм рт.ст. в общей популяции и <140/80—85 мм рт.ст. у больных сахарным диабетом (СД).
Таким образом, важнейшим аспектом лечебной тактики у пациентов с АГ является решение о назначении определенного варианта медикаментозной терапии.
Прежде всего следует отметить, что, по мнению европейских и российских экспертов, больным АГ 2-й и 3-й степени с любым уровнем риска развития ССО рекомендуется быстрое начало медикаментозной терапии — через несколько недель или одновременно с началом изменения образа жизни. Медикаментозная антигипертензивная терапия также рекомендуется при наличии высокого общего риска развития ССО, обусловленного поражением органов-мишеней (ПОМ), СД, ССЗ или хронической болезнью почек (ХБП), даже при АГ 1-й степени.

Целесообразно рассмотреть назначение антигипертензивной медикаментозной терапии также у больных АГ 1-й степени с низким и средним риском, если АД остается в этом диапазоне на протяжении нескольких посещений врача или повышено по амбулаторным критериям и остается повышенным, несмотря на внедрение изменений в образ жизни на протяжении достаточного отрезка времени.
Следующим важным шагом на пути улучшения контроля АД является выбор именно комбинированной терапии на ранних этапах ведения пациентов (рис. 1).
 Важнейшим критерием, определяющим выбор комбинированной терапии, является оценка категории риска. Комбинированная терапия должна назначаться изначально большинству пациентов, так как в амбулаторной практике в основном наблюдаются пациенты из группы высокого и очень высокого риска, даже если АД у них повышено незначительно. В Рекомендациях РМОАГ и ВНОК (2010) приведен перечень состояний, которые относятся к категории высокого или очень высокого риска: наличие 3 ФР развития ССЗ и более, хотя бы один вид ПОМ, сопутствующие заболевания, СД и метаболический синдром (МС) [2].
Важнейшим критерием, определяющим выбор комбинированной терапии, является оценка категории риска. Комбинированная терапия должна назначаться изначально большинству пациентов, так как в амбулаторной практике в основном наблюдаются пациенты из группы высокого и очень высокого риска, даже если АД у них повышено незначительно. В Рекомендациях РМОАГ и ВНОК (2010) приведен перечень состояний, которые относятся к категории высокого или очень высокого риска: наличие 3 ФР развития ССЗ и более, хотя бы один вид ПОМ, сопутствующие заболевания, СД и метаболический синдром (МС) [2].
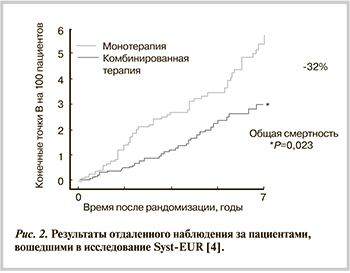
Основными преимуществами комбинированной терапии, назначаемой первично, являются большая вероятность достижения АД, более быстрый ответ на лечение, формирование лучшей приверженности к лечению, меньшее число побочных эффектов и др. Недавно получены очень важные данные о том, что раннее начало комбинированной терапии может не только уменьшить ССС, но статистически значимо значительно снизить общую смертность (рис. 2). Эти результаты получены в результате наблюдения за пациентами, участвовавшими в исследовании Syst-EUR [3, 4].
При назначении комбинированной терапии необходимо учитывать не только категорию риска развития ССО, но и уровень АД, т.е. степень АГ. Нецелесообразно всегда начинать комбинированную терапию с низких доз препарата, так как назначение такой терапии пациентам с АГ 2-й и 3-й степени неминуемо приведет к необходимости дальнейшего увеличения дозы препаратов и увеличению продолжительности периода достижения целевого АД, тем более что в европейских рекомендациях специально подчеркивается, что больным АГ 2-й и 3-й степени с любым уровнем риска развития ССЗ рекомендуется быстрое начало медикаментозной терапии. Уровень доказательности данного положения, как указано в европейских рекомендациях, соответствует I классу А [5, 6]. Это убедительно доказано и в отечественном исследовании СТРАТЕГИЯ А [7], и проведенном нами исследовании с различными дозами фиксированной комбинации (ФК) периндоприла А и индапамида [8].
В исследовании СТРАТЕГИЯ А 22,3% пациентов с неконтролируемой АГ 2-й степени потребовалось назначение высокодозовой комбинации периндоприла A и индапамида (периндоприл А 10 мг + индапамид 2,5 мг).
 В исследовании, проведенном нами в клиническом центре РНИМУ им. Н.И. Пирогова, мы показали, что в высоких дозах препарата нолипрел А Би форте (периндоприл А 10 мг + индапамид 2,5 мг) нуждались 87,6% пациентов с неконтролируемой АГ 2-й и 3-й степени. Таким образом, если врач при назначении комбинации учитывает не только категорию риска, но и степень АГ, возникает возможность еще больше увеличить вероятность достижения целевого АД без затягивания этого процесса и ухудшения приверженности к лечению.
В исследовании, проведенном нами в клиническом центре РНИМУ им. Н.И. Пирогова, мы показали, что в высоких дозах препарата нолипрел А Би форте (периндоприл А 10 мг + индапамид 2,5 мг) нуждались 87,6% пациентов с неконтролируемой АГ 2-й и 3-й степени. Таким образом, если врач при назначении комбинации учитывает не только категорию риска, но и степень АГ, возникает возможность еще больше увеличить вероятность достижения целевого АД без затягивания этого процесса и ухудшения приверженности к лечению.
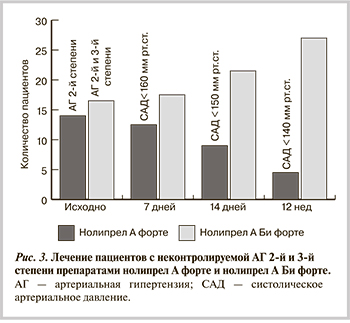
В этом исследовании мы также показали, что достижение целевого АД, безусловно, возможно при продолжении медикаментозной терапии той же комбинацией, но в большей дозе. Хотя такая возможность прописана во всех рекомендациях, на практике многие врачи вместо увеличения дозы добавляют третий, а иногда и четвертый препарат. Подобная тактика приводит к ухудшению приверженности пациентов к лечению, появлению нежелательных эффектов, а в тех случаях, когда добавление препаратов не приводит к достижению целевого АД, к необоснованному отнесению пациентов к категории с резистентной АГ. В нашем исследовании мы провели оценку возможности перевода пациентов с неконтролируемой АГ 2-й и 3-й степени с полнодозовой ФК препарата нолипрел А форте (периндоприл А 5 мг и индапамид 1,25 мг) на высокодозовую ФК нолипрела А Би форте (периндоприл А 10 мг + индапамид 2,5 мг). В исследование вошли 30 пациентов с неконтролируемой АГ 2-й и 3-й степени. Средний возраст пациентов составил 58,9±6,7 года. Все участники исследования относились к группе высокого и очень высокого риска. Пациентов разделили на 2 группы: в 1-ю вошли 16 пациентов с АГ 2-й и 3-й степени, которым вместо предшествующей терапии был назначен нолипрел А Би форте; во 2-ю — 14 пациентов с АГ 2-й степени, которым был назначен нолипрел А форте. На 7-й (при систолическом АД — САД ≥160 мм рт.ст.) и 14-й (при САД ≥150 мм рт.ст.) дни исследования, т.е. в отсутствие достижения целевых уровней АД, пациентам 2-й группы назначали нолипрел А Би форте (рис. 3).
Такая тактика позволила достичь целевые уровни АД у большинства пациентов при своевременном увеличении дозы. Фактически в нашем исследовании мы показали, что в обследованной группе больных только 12,4% пациентов с неконтролируемой АГ 2-й и 3-й степени нуждались в добавлении третьего препарата для достижения целевого АД через 12 нед лечения.
Рациональная фармакотерапия АГ подразумевает также усиленное внимание не только учету уровня АД, но и наличию ФР развития ССО, особенно выявлению бессимптомного ПОМ и клинических осложнений для оценки общего риска развития ССО, так как в последнее время обновлены данные о прогностическом значении бессимптомного ПОМ, включая сердце, кровеносные сосуды, почки, глаза и головной мозг. Показано, что при адекватном и углубленном обследовании пациентов с АГ, у которых при обычном обследовании не выявлялись ПОМ, удается обнаружить гипертрофию левого желудочка (ГЛЖ) у 21% больных и поражение почек, в виде микроальбуминурии (МАУ) и снижения скорости клубочковой фильтрации (СКФ) у 24% больных [9].
Нами также проведено обследование 72 пациентов с АГ 1-й и 2-й степени, длительностью АГ не более 10 лет в возрасте от 18 до 40 лет, не получающих регулярной лекарственной терапии, у которых при обычном обследовании не выявлялись ПОМ. Средний возраст пациентов составил 27,8±0,9 года, длительность АГ — 3,4±0,4 года. В группе было 12 (16,7%) женщин и 60 (83,3%) мужчин. Особое внимание мы уделили выявлению МАУ и определению наличия стадии ХБП по СКФ. Оказалось, что в данной группе пациентов было только 20 (28%) пациентов без ХБП с СКФ > 90 мл/мин/м2, у 45 (63%) СКФ составила 60—89 мл/мин/м2, что можно рассматривать как умеренное нарушение функции почек, соответствующее ХБП I и II стадии. Пациентов с ХБП III стадии с СКФ 30—59 мл/мин/м2, что по новым рекомендациям считается ПОМ, определяющим высокий и очень высокий риск, было 7 (9%). В исследованной нами группе не было больных с ХБП IV и V стадии.
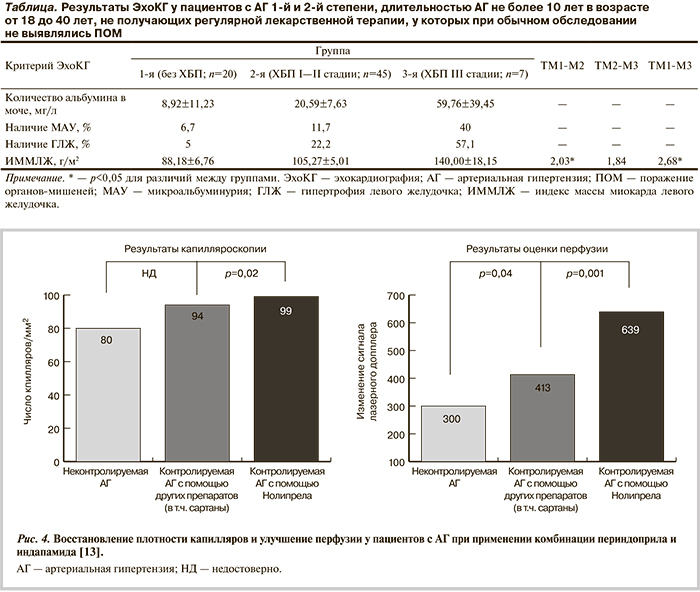
У всех больных определяли уровень альбумина в моче. Примененная нами методика оценки МАУ представляла собой точный количественный анализ уровня альбумина в моче, поэтому нам удалось в целом по группе выявить разную степень альбуминурии у пациентов с АГ 1—2-й степени. Оказалось, что количество альбумина в моче у пациентов без ХБП составляло 8,92±11,23 мг/л, с ХБП I—II стадии — 20,59±7,63 мг/л, ХБП III стадии — 59,76±39,45 мг/л, однако при сравнении этих показателей достоверных различий не получено. Тем не менее по критериальному показателю МАУ (>30 г/л) наблюдалась тенденция увеличения частоты выявления МАУ по мере прогрессирования ХБП (см. таблицу).
При эхокардиографии (ЭхоКГ) индекс массы миокарда левого желудочка (ИММЛЖ) более 115 г/м2 у мужчин и 95 г/м2 у женщин, т.е. наличие ГЛЖ по новым критериям, представленным в европейских рекомендациях, выявлено у 15 (20,8%) пациентов. Внутри групп распределение было следующим: у пациентов без ХБП ГЛЖ встречалась в 5% случаев, у пациентов с ХБП I—II стадии в 22,2%, у пациентов с ХБП III стадии — в 57,1% случаев, а ИММЛЖ у пациентов с ХБП был достоверно больше, чем у больных без ХБП (см. таблицу). Таким образом, наши данные совпали с данными А. Kearney-Swartz и соавт. [9] по частоте выявления ГЛЖ. Что касается выявления поражения почек, то по критерию ХБП III стадии мы смогли выявить ПОМ в виде поражения почек только у 9% пациентов. Помимо этого выявлена достоверная и тесная связь между наличием ГЛЖ и стадией ХБП.
Частое выявление бессимптомного ПОМ в структуре наших представлений о сердечно-сосудистом континууме требует согласования методик фармакотерапии с наличием таких ПОМ. Очевидно, что оценка функции почек является одной из важнейших при установлении риска развития ССО. Последние Европейские рекомендации доказали это, так как единственным существенным изменением критериев стратификации риска стало добавление ПОМ в виде ХБП III стадии. Известно, что именно почки при возникновении АГ наряду с сердцем и головным мозгом являются главными органами-мишенями для проявления распространенной сосудистой патологии.
При АГ почки рано становятся ведущим органом-мишенью. Своевременная клиническая и лабораторная диагностика поражения почек способствует не только оценке состояния их функции, но и дает возможность определить риск у пациентов с АГ. Если снижение СКФ является непосредственным свидетельством ухудшения функционального состояния почек, то МАУ, по результатам целого ряда исследований, служит не только показателем, определяющим поражение почек, но отражает общее состояние сосудистой стенки и служит также надежным прогностическим критерием у пациентов с АГ. Поэтому снижение МАУ — важный аспект лечения пациентов с АГ. Многочисленные клинические исследования убедительно показали, что наибольшее влияние на МАУ оказывают такие антигипертензивные препараты, как блокаторы ренин-ангиотензин-альдостероновой системы: ингибиторы ангиотензинпревращающего фермента (АПФ) и блокаторы рецепторов ангиотензина.
Одним из важнейших исследований, продемонстрировавших исключительное влияние медикаментозной терапии АГ на МАУ, было ADVANCE. В этом исследовании использовали комбинацию ингибитора АПФ периндоприла и диуретика индапамида. Показано, что эта комбинированная терапия позволяет даже у пациентов с СД 2-го типа, являющихся пациентами с особой тропностью к поражению почек, снизить риск развития МАУ на 21%, темпы прогрессирования МАУ в протеинурию — на 31%, а также вызвать обратное развитие этих состояний у 52% пациентов [10]. Одновременно комбинация периндоприла и индапамида нолипрел также позволила снизить ССС на 18% и общую смертность на 14%. Во многом эти результаты лечения нолипрелом можно объяснить способностью данной комбинации улучшать микроциркуляцию и перфузию почки [11]. Создается впечатление, что способность комбинации периндоприла и индапамида улучшать микроциркуляцию и состояние сосудистой стенки реализуется не только в почках, но и в других органах. Так, в исследовании REASON показано, что снижение САД и пульсового давления на фоне применения этой комбинации сочеталось с достоверным улучшением функции крупных артерий, уменьшением их жесткости и отраженных волн [12]. Показано также, что комбинация периндоприла и индапамида увеличивает плотность капилляров и восстанавливает перфузию у пациентов с АГ (рис. 4) [13].
На примере использования комбинации периндоприла и индапамида отчетливо видно, что только тщательный анализ результатов клинических исследований и исследований влияния медикаментозных препаратов на органы-мишени позволяет осуществить правильный выбор лекарственного препарата в конкретных клинических ситуациях. Именно поэтому в Европейских рекомендациях ЕОАГ и ЕОК (2013) в обзоре рекомендаций по выбору лекарственных препаратов отмечается, что «некоторые препараты целесообразно считать предпочтительными для конкретных ситуаций, так как они использовались в данных ситуациях в клинических исследованиях или продемонстрировали более высокую эффективность при конкретных типах ПОМ», а также то, что «предпочтительными являются комбинации, эффективность которых показана в клинических исследованиях».



