Разработка клинических рекомендаций по отдельным заболеваниям началась в 2019 г. в соответствии с приказом Минздрава России № 103н от 28.02.2019 «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требованиям к их структуре, составу и научной обоснованности, включаемой в клинические рекомендации информации». Клинические рекомендации разрабатываются медицинскими профессиональными некоммерческими организациями (Российским обществом урологов) в соответствии с типовой формой и требованиями, согласно приложениям к приказу Минздрава России.
Клинические рекомендации «Цистит у женщин» кодированы по Международной статистической классификации болезней и проблем, связанных со здоровьем N30.0, N30.1, N30.2, и строго структурированы. Степень доказательности данных приводится в соответствии со шкалой оценки уровней достоверности доказательств (УДД) для методов диагностики, профилактики, лечения и реабилитации (табл. 1) и шкалой оценки уровней убедительности рекомендаций (табл. 2).


Цистит классифицируют по различным признакам.
По этиологии выделяют инфекционный (бактериальный) и неинфекционный (лекарственный, лучевой, токсический, химический, аллергический, травматический и др.).
По течению цистит делят на острый и рецидивирующий (хронический), который подразделяют на фазу обострения и фазу ремиссии.
Выделяют также первичный (неосложненный) цистит (самостоятельное заболевание, возникающее на фоне условно-нормального пассажа мочи у женщин 18–45 лет без сопутствующих заболеваний) и вторичный (осложненный) у всех остальных, т.е. возникающий на фоне уродинамических нарушений и как осложнение другого заболевания: туберкулез, камни, опухоли мочевого пузыря, когда повышен риск неэффективности эмпирически назначенной антибактериальной терапии.
По определению бактериальный цистит — это инфекционно-воспалительный процесс в стенке мочевого пузыря, локализующийся преимущественно в слизистой оболочке [1–3].
Этиологически значимым возбудителем бактериального цистита является уропатогенная Esherichia coli (УПЕК), которую выявляют у 75% пациентов. Реже встречается Klebsiella spp. – в 10%, а также Enterococcus faecalis и Staphylococcus saprophyticus – в 5% случаев. Реже выделяются другие энтеробактерии, например Proteus mirabilis [2, 4, 5].
Восходящий (уретральный) путь инфицирования нижних мочевыводящих путей обусловлен как анатомическими особенностями у женщин: короткая и широкая уретра, близкое ее расположение к естественным очагам инфекции (влагалище, анус), так и факторами вирулентности основного возбудителя – УПЕК. Транспорту инфекции в мочевой пузырь способствует и сексуальная активность у женщин с так называемой влагалищной эктопией наружного отверстия уретры или гипермобильностью дистального отдела уретры. При осложненной ИМП, при наличии инфравезикальной обструкции у женщин, как органической, так и функциональной (на фоне детрузорно-сфинктерной диссинергии, спазма наружного сфинктера уретры), мочеиспускание происходит аномально. При повышенном внутриуретральном давлении поток мочи имеет не ламинарное, а турбулентное течение с изменением гидродинамических характеристик, появлением завихрений. Бактерии мобилизуются со стенок дистальной уретры и распространяются в проксимальные отделы, а также в мочевой пузырь из-за возникающего в таких случаях уретрально-везикального рефлюкса [6].
Необходимым условием развития бактериального цистита является колонизация и адгезия значительного количества бактерий к поверхности уротелиальных клеток и последующая возможная инвазия их в зонтичные клетки поверхностного слоя слизистой оболочки мочевого пузыря с последующим повреждением тканей [7]. Уропатогенные кишечные палочки содержат белковые структуры (фимбрии, адгезины, пилины), ответственные за адгезивную способность бактерий. Полагают, что разные типы адгезинов (1, Р, S, AFA) имеют на уровне мочевого пузыря и почек свои места адгезии [8].
Факторами хозяина, предрасполагающими к адгезии микроорганизмов, считают разрушение или изменение защитного мукополисахаридного слоя эпителия мочевого пузыря, что может быть обусловлено конституциональными особенностями муцина; нарушением кровообращения в стенке мочевого пузыря; повышенной экспрессией рецепторов для бактериальной адгезии на клеточных мембранах; снижением выработки антимикробных пептидов [9].
К факторам, препятствующим развитию инфекции нижних мочевыводящих путей, относят:
- акт мочеиспускания, т.е. механический вымывающий эффект мочи;
- наличие мукополисахаридного слоя на слизистой оболочке мочевого пузыря;
- продукция антимикробных пептидов слизистой оболочкой мочевого пузыря;
- низкий рН мочи и высокая осмолярность;
- наличие IgA в моче, препятствующее бактериальной адгезии [9].
Для острого цистита характерно острое начало. При наличии двух обострений в течение полугода или трех – в течение года говорят о рецидивирующем (хроническом) цистите [2, 3, 10]. Несмотря на определенное беспокойство, причиняемое пациентам, для цистита не характерно тяжелое течение.
При диагностике острого цистита у женщин характерными симптомами являются жалобы на боли, рези во время мочеиспускания, боли над лоном, неотложные позывы к мочеиспусканию, частые позывы к мочеиспусканию днем и/или ночью, терминальная гематурия, мочеиспускание малыми порциями при общем удовлетворительном состоянии, наличие связи жалоб с половым актом (у женщин пременопаузального возраста). При этом отсутствуют патологические выделения из влагалища, гипертермия свыше 38°С, боли в поясничной области.
Критерии установления диагноза: на основании патогномоничных данных – наличие жалоб на частое болезненное мочеиспускание малыми порциями мочи, рези и боли при мочеиспускании, императивные позывы к мочеиспусканию, отсутствие обильных выделений из влагалища (для чего необходим осмотр наружных половых органов, при котором также обращается внимание на анатомические изменения и высыпания на коже и слизистых оболочках). УУР-В, УДД-1.
Для объективной оценки симптомов заболевания предложена количественная оценка по шкале симптомов острого цистита (ACSS). Шкала ACSS (рис. 1) состоит из 18 вопросов, на которые пациентка отвечает самостоятельно. Вопросы разделены на четыре категории: а) о характерных симптомах (1–5); б) для дифференциального диагноза (7–10); в) о качестве жизни (11–13); г) дополнительные вопросы об основном заболевании (14–18). Пороговое значение 6 баллов при оценке характерных симптомов имеет чувствительность 91,2% и специфичность 86,5% в отношении прогнозирования острого цистита [11–13].


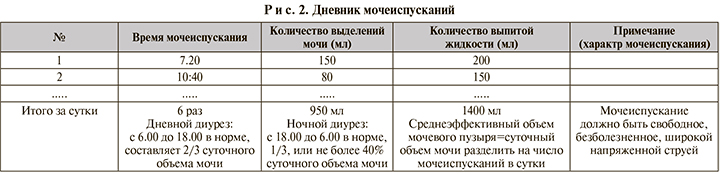
Всем пациентам с циститом рекомендуется заполнить дневник мочеиспускания в течение 2 сут. для обьективной оценки частоты и объема мочеиспускания [14, 15] (рис. 2). УУР-С, УДД-5.
При остром неосложненном цистите общий анализ мочи не обладает высокой диагностической ценностью. Диагностически значимыми показателями являются ≥10 лейкоцитов/мм3 при микроскопии осадка мочи, увеличение количества бактерий, возможна эритроцитурия. При остром неосложненном цистите и при рецидивирующем цистите анализ мочи может быть выполнен с помощью тест-полосок в качестве альтернативы общему анализу мочи – положительный тест на нитриты и лейкоцитарную эстеразу [3, 16–18]. Пациентам с острым неосложненным циститом не рекомендуется микробиологическое (культуральное) исследование мочи при первичной диагностике в связи с минимальным увеличением диагностической точности и длительностью исследования [2, 3, 10, 19]. УУР-В, УДД-2.
Рекомендуется всем пациентам при осложненном или рецидивирующем (хроническом) цистите выполнение общего (клинического) анализа мочи для выявления признаков воспаления мочевыводящих путей. [1, 3, 18, 20–24]. УУР-С, УДД-5.
Проведение микробиологического (культурального) исследования мочи должно выполняться при подозрении на пиелонефрит, при персистирующих или рецидивирующих симптомах в пределах 4 нед. после окончания антибиотикотерапии пациентов с атипичными симптомами, беременных, а также всем пациентам при осложненном или рецидивирующем (хроническом) цистите. Бактериологическое исследование мочи проводят для выявления возбудителя и его чувствительности к антибактериальным лекарственным средствам. По российским и международным исследованиям в 70–80% случаев возбудителем цистита является уропатогенная Esherichia coli (УПЕК), реже другие – грамотрицательные бактерии, чувствительные к фосфомицину и нитрофурантоину в 97–98% случаев. Эмпирическая терапия этими препаратами высокоэффективна. При неэффективности эмпирической терапии бактериологический анализ мочи с определением чувствительности уропатогена к антибактериальным препаратам существенно облегчит выбор следующего препарата. [5, 18, 19, 25–30]. УУР-В, УДД-2.
У пациентов с типичными симптомами цистита при выделении монокультуры микробное число 102–103 КОЕ/мл может быть диагностически приемлемым. Для посева мочи анализ средней порции утренней мочи необходимо исследовать немедленно, если это невозможно, то мочу необходимо хранить при температуре от +2 до +8˚С.
Очень важно различать бессимптомную бактериурию от симптоматической инфекции нижних мочевыводящих путей, т.е. цистита. Колонизация мочевыводящих путей, соответственно, наличие бактерий в моче без клинических проявлений определяются как асимптоматическая бактериурия (АСБ). АСБ диагностируется в случае выделения одного или более видов бактерий, растущих в моче в количестве ≥105 КОЕ/мл, независимо от наличия пиурии, в отсутствии признаков и симптомов присущих инфекции мочевыводящих путей (ИМП). Бессимптомная бактериурия (комменсальная колонизация) может защищать от суперинфекции вирулентными уропатогенами (16, 25).
Не рекомендуется лечение АСБ, чтобы избежать риска селекции резистентных микроорганизмов и эрадикации потенциально протективных АСБ штаммов микроорганизмов: женщинам без факторов риска развития инфекции мочевыводящих путей; пациентам с регулируемым сахарным диабетом; женщинам в постменопаузе; пожилым людям, живущим в домах престарелых; пациентам с нарушенной функцией нижних мочевыводящих путей и после реконструктивных операций на нижних мочевыводящих путях; пациентам с трансплантацией почки; пациентам до артропластики и пациентам с рецидивирующей инфекцией мочевыводящих путей (16, 25) УУР-С, УДД-5.
Рекомендуется антибактериальное лечение АСБ у беременных женщин, перед инвазивными вмешательствами на мочевыводящих путях и половых органах, при которых возможны кровотечение и повреждение слизистой оболочки, с целью профилактики невынашивания беременности, преждевременных родов и инфекционно-воспалительных осложнений (16, 25) УУР-С, УДД-5.
При рецидивирующем цистите иногда необходимо провести молекулярно-биологическое исследование влагалищного отделяемого на микроорганизмы – маркеры бактериального вагиноза и аэробного вагинита, которые могут влиять на дисбиоз влагалища и тем самым снижать их защитную функцию при восходящем пути инфицирования мочевыводящих путей.
При подозрении на острый восходящий пиелонефрит пациентам с циститом (гипертермия свыше 38°С, боли в поясничной области, боли при пальпации почек) рекомендуется ультразвуковое исследование почек и/или компьютерная томография почек [1, 2, 3, 7, 18, 31] УУР-С, УДД-4.
Женщинам старше 40 лет с рецидивирующим (хроническим) циститом и с факторами риска мочекаменной болезни, интерстициального цистита, туберкулеза или рака мочевого пузыря рекомендуется проведение УЗИ мочевого пузыря и цистоскопии [3, 26, 32]. УУР-С, УДД-5.
Рекомендуется пациентам при рецидивах заболевания, в отсутствие эффекта от проводимого лечения проведение измерения скорости потока мочи (урофлоуметрии) с определением объема остаточной мочи для уточнения диагноза и определения дальнейшей тактики ведения пациента [3, 14, 18, 19]. УУР-С, УДД-5.
Принципы лечения бактериального цистита
При остром цистите лечение направлено на достижение длительного клинического результата, в то время как целью лечения при рецидивирующем цистите являются улучшение качества жизни больного, профилактика рецидивов и профилактика и лечение осложнений.
Пациентам с острым неосложненным циститом рекомендуется назначение эмпирической антибактериальной терапии в амбулаторных условиях для элиминации возбудителя [1–3, 16, 20, 31, 33]. УУР-В, УДД-2. Продолжительность терапии острого неосложнннного цистита – 1–5–7 дней – зависит от выбранного препарата и отсутствия или наличия факторов риска [1, 3, 16, 31].
Рекомендуется назначение препарата первого выбора: фосфомицина трометамола в дозе 3 г однократно, курс лечения 1 день [16, 20, 26, 34–38]. УУР-А, УДД-1.
Препаратами выбора также являются фуразидин или нитрофурантоин в дозах, соответствующих инструкции к препарату [4, 16, 20, 25, 33, 39]. УУР-С, УДД-5.
В качестве альтернативы (при непереносимости препаратов выбора) рекомендуется назначение цефиксима в дозе 400 мг/сут. в течение 5 дней [40]. УУР-С, УДД-5.
Не рекомендованы:
- препараты группы хинолонов (фторхинолонов) не только из-за высокого уровня резистентных штаммов микроорганизмов, селекции мультирезистентных патогенов или повышенного риска развития Сlostridium difficile ассоциированного колита, но и из-за массы серьезных нежелательных побочных действий препаратов этой группы [4, 5, 16, 26, 41, 42]. УУР-С, УДД-4.
- ампициллин, амоксициллин, ко-тримоксазола из-за высокого уровня резистентных к ним уропатогенов, в частности кишечной палочки [4, 5]. УУР-С, УДД-4.
Профилактика и лечение рецидивов цистита
- рекомендуется назначение фосфомицина трометамола перорально 3 г 1 раз через 10 дней на протяжении 3 мес.или 3 г перорально однократно (при рецидиве цистита)[16, 20, 42, 38, 43]. УУР-С, УДД-4.
- женщинам в постменопаузе рекомендуется назначение вагинальной эстроген-заместительной терапии для уменьшения выраженности симптомов и улучшения качества жизни в соответствии с инструкцией к препарату [20, 26, 44–46]. УУР-В, УДД-1.
- рекомендуется прием фитотерапевтического препарата, содержащего траву золототысячника, корень любистока, листья розмарина в дозе 2 т (или по 50 кап) 3 раза в день, в течение 3 мес. приема для профилактики рецидивов цистита [20, 47–50]. УУР-С, УДД-5;
- рекомендуется назначение иммунопрофилактики лиофилизированным лизатом бактерий Escherichia coli по 1 капсуле 1 раз в день – 3 мес. [20, 51–53]. УУР-А, УДД-1.
- женщинам, когда рецидивы цистита четко связаны с половым актом, рекомендуется с целью посткоитальной антибиотикопрофилактики до или после полового акта нитрофурантоин 50 мг при неэффективности прочих не-антибактериальных методов [42, 54, 55]. УУР-В, УДД-1.
- рекомендуются внутрипузырные инстилляции протектора вязкоэластичного стерильного для слизистой мочевого пузыря, содержащего гиалуроновую кислоту, вне стадии обострения [56–58]. УУР-С, УДД-4.
Большой раздел в КР посвящен информационному материалу для пациентов, в которых кратко изложены симптомы и признаки цистита, факторы риска развития цистита, когда обращаться к врачу. Даны разъяснения по заполнению опросников и дневника мочеиспускания, правильному сбору мочи для анализов. Информация для пациентов включает рекомендации по образу жизни, питьевому режиму и домашних средств в профилактике рецидивов цистита.
После разработки проекта клинических рекомендаций они широко обсуждались на заседаниях московского и региональных обществ урологов, а также посредством размещения в информационно-телекоммуникационной сети Интернет в течение 4 мес. со дня направления в Минздрав России уведомления о начале разработки клинических рекомендаций. За время до принятия КР на научном совете в Минздраве России в 2021 г они неоднократно корректировались. В настоящее время КР приняты и размещены на сайтах Минздрава России и Российского общества урологов.



