Введение. Мочекаменная болезнь (МКБ) – заболевание обмена веществ, проявляющееся образованием камней в почках. Хроническое течение МКБ связано со способностью к рецидивированию заболевания. Всем пациентам, страдающим уролитиазом, показана специфическая метафилактика МКБ, направленная на снижение факторов риска, стимулирующих литогенез [1].
Одним из главных доказанных факторов риска развития МКБ является наличие перенасыщения камнеобразующими веществами мочи, т.е. наличие метаболических литогенных нарушений [2, 3]. К основным камнеобразующим веществам относятся кальций, оксалат, мочевая кислота [4]. Регуляция концентрации этих веществ в крови и нормализация уровня их экскреции с мочой существенно снижают риск рецидива камнеобразования при МКБ [5]. В то же время необходимо контролировать содержание ингибиторов литогенеза, цитрата и магния в моче. При снижении экскреции с мочой данных веществ необходимо корригировать возникающие нарушения назначением специфической терапии [2].
Следует подчеркнуть, что контроль за биохимическими показателями крови и суточной мочи пациентов с МКБ, коррекция метаболических литогенных нарушений должны осуществляться в течение всей жизни больного. Данный подход особенно актуален при рецидивной форме уролитиаза. Коррекция образа жизни и диетотерапия – первый шаг на пути к нормализации обмена веществ и к снижению количества рецидивов МКБ [6]. При неэффективности первичных метафилактических мероприятий или при отказе пациента от соблюдения рекомендаций возможна коррекция содержания камнеобразующих веществ в сыворотке крови и моче путем назначения лекарственных препаратов [2, 3]. С этой целью используют тиазидные диуретики, цитратные смеси, аллопуринол, метионин, магнийсодержащие препараты и др.
Тем не менее длительный регулярный прием препаратов создает психологический дискомфорт для пациентов, а иногда употребление лекарственных средств сопряжено с развитием побочных или аллергических реакций. В ряде случаев назначение растительной биологически активной добавки (БАД) как альтернативы лекарственному препарату может стать вариантом выбора: во-первых, количество побочных явлений и аллергических реакций при применении БАДа ниже, чем при приеме синтезированных препаратов, во-вторых, осторожность пациента перед их приемом может не распространяться на БАД.
БАД с успехом применяют во многих областях медицины, в том числе и в урологии. В частности, врачи активно назначают БАД пациентам, страдающим МКБ [7–11]. Однако ожидания от назначения средств данной группы зачастую бывают завышенными: как специалисты, так и пациенты надеются на литолиз мочевых конкрементов вне зависимости от их химического состава, на отхождение мелких фиксированных камней, локализованных в чашечках почки.
Одной из причин подобных заблуждений является отсутствие четко сформированных показаний к применению того или иного действующего вещества, входящего в состав БАДа. Это в свою очередь вызвано наличием небольшого количества научных работ, написанных с позиции доказательной медицины, показывающих эффективность применения препарата.
Считаем, что для улучшения качества оказания медицинской помощи пациентам с уролитиазом, для разработки четких алгоритмов назначения БАДа при МКБ необходимы исследования с целью определение четких показаний и противопоказаний к назначению биологически активных веществ с учетом метаболических литогенных нарушений у пациента. Данные исследования позволят создать научную базу для реализации принципов «4Р» медицины на примере МКБ [12].
Целью настоящего исследования стало изучение влияния БАДа «НефраДоз» на метаболизм основных камнеобразующих веществ и ингибиторов литогенеза у пациентов, страдающих уролитиазом.
Материалы и методы. В НИИ урологии и интервенционной радиологии им. Н. А. Лопаткина – филиале «НМИЦ радиологии» МЗ РФ проведено моноцентровое проспективное рандомизированное исследование БАД к пище «НефраДоз» (ООО НПО «ФармВИЛАР», Россия). Все пациенты подписали информированное согласие на участие в исследовании.
В состав БАДа «Нефрадоз» входят экстракты корней марены красильной, листьев ортосифона тычиночного, травы эпимедиума, корней родиолы розовой, корней солодки голой, листьев гинкобилоба, ресвератрол.
В исследование включены 60 пациентов, страдавших МКБ, которые методом рандомизации были разделены на 2 группы по 30 человек. Пациенты основной группы придерживались общих рекомендаций и стандартной диетотерапии, получали БАД «НефраДоз» в течение 28–30 дней по 1 капсуле (150 мг) 2 раза в сутки во время еды. В контрольной группе пациенты получали только общие рекомендации и соблюдали стандартную диетотерапию в течение 28–30 дней.
Стандартная диетотерапия включала:
- обильное потребление жидкости – до 2000–2500 мл в сутки;
- ограничение потребления пищевой соли до 3 г в сутки;
- ограничение потребления животных белков до 1 г на 1 кг массы тела. При модификации диеты пациентам рекомендовали отдать предпочтение курице, индейке, кролику, белой рыбе, воздержаться от регулярного употребления свинины, говядины, баранины, красной рыбы.
Обследование включило сбор анамнеза, заполнение анкеты стереотипа питания (www.nethealth.ru/food-quiz), биохимический анализ крови на содержание общего кальция, калия, натрия, магния, неорганического фосфора, хлора, мочевины, креатинина, мочевой кислоты; биохимический анализ суточной мочи на содержание общего кальция, калия, натрия, магния, неорганического фосфора, хлора, мочевины, креатинина, мочевой кислоты, оксалатов, цитратов; клинический анализ мочи.
Биохимические исследования осуществлены с помощью автоматического анализатора ADVIA-1200 («Bayer-Siemens»). Клинический анализ мочи выполняли ежедневно на портативном анализаторе мочи «ЭТТА АМП-01» (Россия) [13]. Определяли плотность мочи, ее кислотно-щелочное состояние (рН) , концентрацию лейкоцитов в моче, наличие микро- или макрогематурии и др.
Сбор анамнестических данных, заполнение анкеты стереотипа питания, биохимический анализ крови и суточной мочи выполняли дважды: до лечения и через 30 дней после начала терапии.
Химический состав мочевых камней и характер течения МКБ в настоящей работе не анализировали.
Статистический анализ проводили с помощью критерия Вилкоксона, критерия Манна–Уитни и t-критерия Стъюдента. Использовали компьютерную программу Statistica 10.0 («StatSoft», США). Результаты считали статистически значимыми при уровне значимости р≤0,05.
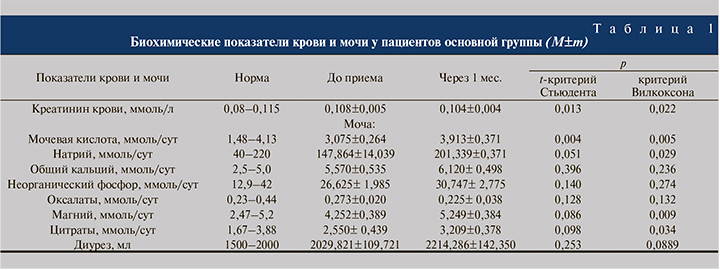
Результаты и обсуждение. У пациентов, принимавших БАД «НефраДоз», придерживавшихся общей диетотерапии и стандартных рекомендаций (основная группа), статистически значимо снижалась концентрация креатинина в сыворотке крови (табл. 1). В биохимическом анализе их суточной мочи констатировали повышение уровня экскреции основных ингибиторов камнеобразования – магния и цитратов (табл. 1).
Известно, что цитрат препятствует образованию не только мочекислых, но кальций-оксалатных и кальций-фосфатных конкрементов [14, 15]. Цитрат проявляет ингибиторную активность, связываясь с кальцием и образуя с ними комплексы [14]. Предполагают, что данное действие цитратов связано с тем, что они уменьшают резорбцию кальция из костной ткани. Лечение цитратами приводит к улучшению здоровья костей, снижению частоты переломов, а также препятствует росту кристаллов кальций фосфата в моче [16]. Полагают, что, тормозя процессы физиологической резорбции костной ткани, цитрат уменьшает концентрацию кальция в крови, что ведет к снижению уровня экскреции кальция с мочой. Опубликованы работы, в которых утверждается, что цитрат способен увеличивать реабсорбцию кальций в почечных канальцах [17]. Также установлено, что нормальный уровень цитрата в моче может повышать ингибирующую активность гликопротеида Tamm–Horsafall [18].
Магний, как и цитрат, способен ингибировать процессы камнеобразования, образуя комплексы с кальцием [19]. Низкий уровень магния связан со снижением ингибиторной активности мочи [20] и приводит к снижению экскреции цитратов с мочой, чего следует избегать пациентам с МКБ [18].
Увеличение экскреции магния и цитратов с мочой может быть связано с действием ресвератрола, который входит в состав НефраДоза. Ресвераторол обладает антиоксидантной активностью, противовоспалительным, антиапоптотическим действиями, способен уменьшать количество циркулирующих в крови свободных радикалов [21, 22].
У пациентов основной группы на фоне лечения отмечено увеличение экскреции камнеобразующей мочевой кислоты, однако значения оставались в пределах нормы, а также увеличение содержания натрия в суточной моче (табл. 1). Необходимо подчеркнуть, что увеличение показателей экскреции мочевой кислоты и натрия происходило в пределах референсных значений.
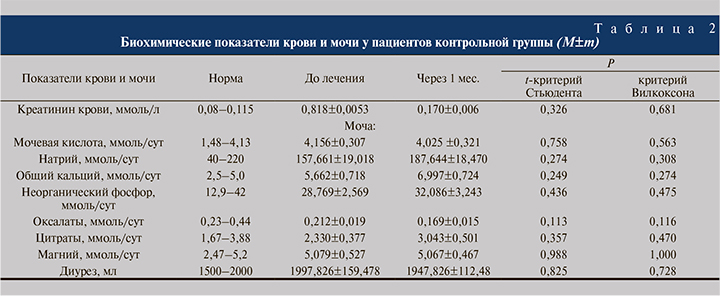
У пациентов контрольной группы статистически значимых изменений биохимических показателей крови и суточной мочи не выявлено. Отсутствие положительного эффекта от проведенной диетотерапии может быть связано с тем, что пациенты соблюдали диетические рекомендации и до включения в исследование.
Таким образом, на фоне приема препарата «НефраДоз» у пациентов отмечается статистически значимое снижение концентрации креатинина крови, увеличение уровня экскреции магния, цитратов, мочевой кислоты и натрия. Возможно повышение уровня мочевой кислоты в моче связано с тем, что препарат потенцирует выделительную функцию почек. При подтверждении данного предположения дополнительными исследованиями показания к назначению препарата могут быть расширены. Тем не менее в настоящий момент в связи с относительным повышением концентрации мочевой кислоты в суточной моче пациентов (в пределах нормальных значений), входивших в основную группу, рекомендуем с осторожностью назначать БАД «НефраДоз» пациентам с подтвержденной гиперурикурией.
Проведение оценки данных клинического анализа мочи пациентов обеих групп показало, что в основной группе показатели относительной плотности мочи оказались ниже, показатели рН мочи – выше, чем при анализе данных пациентов контрольной группы (табл. 3).
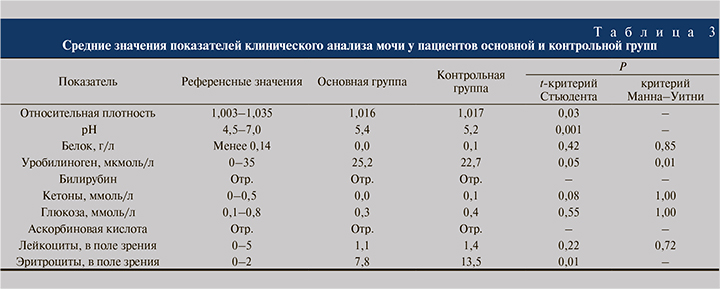
Число эритроцитов в моче на фоне применения БАДа «НефраДоз» оказалось в 2 раза ниже, чем у пациентов контрольной группы. У пациентов основной группу было зафиксировано увеличение содержания уробилиногена, что не выходило за референсные значения (табл. 3).
Концентрация общего белка, общего билирубина, кетонов, глюкозы, аскорбиновой кислоты и лейкоцитов в моче на фоне приема препарата «НефраДоз» не изменялась. Указанные показатели в обеих группах не выходили за пределы нормальных значений. Полученные данные свидетельствуют об отсутствии токсического действия НефраДоза.
Побочных эффектов при приеме препарата «Нефрадоз» не зафиксировано.
Заключение. С учетом статистически подтвержденной способности БАДа «Нефрадоз» увеличивать концентрацию основных ингибиторов камнеобразования (магния и цитратов) в моче и статистически достоверного снижения уровня креатинина крови, достигнутого в течение одного месяца, препарат может быть рекомендован к применению пациенами с МКБ, особенно при сопутствующих гипомагниурии и гипоцитратурии.



