Ведущей причиной материнской смертности по-прежнему остается послеродовое кровотечение (ПРК), частота которого возросла во всем мире [1]. Большинство причин массивной кровопотери и геморрагического шока в акушерстве носят предотвратимый характер. Для снижения частоты ПРК необходим тщательный подход к выявлению пациенток высокого риска развития ПРК, стандартизации подходов наблюдения таких женщин во время беременности и в послеродовом периоде [2, 3]. Оперативное родоразрешение должно проводиться строго по показаниям, поскольку увеличивает риск развития осложнений, в том числе массивного кровотечения [4]. Чрезвычайно важно следовать протоколу оказания неотложной помощи, поскольку время для проведения всех диагностических и лечебных мероприятий при кровотечении крайне ограничено. Своевременное купирование кровотечения позволяет избежать массивных трансфузий [5, 6]. Интегральные методы (тромбоэластометрия (ТЭM), тромбоэластография (TЭГ)) позволяют быстро выявить причину коагулопатического кровотечения или исключить его [5, 7]. Профилактические трансфузии компонентов крови, не снижая риск развития кровотечения, увеличивают число осложнений (острое повреждение легких (TRALI), перегрузка кровообращения (TACO), трансфузионно-обусловленная иммуномодуляция (TRIM)) и материнскую смертность [8, 9]. Поэтому трансфузиологическая тактика должна быть обоснована. Целенаправленная терапия кровотечения под контролем TЭM является неотъемлемой частью менеджмента крови пациента (МКП). Однако внедрение интегральных методов в акушерскую практику происходит медленнее, чем в других областях медицины.
Особенности состояния системы гемостаза во время беременности и родов
Изменение гормонального статуса во время беременности приводит к повышенному синтезу факторов свертывания и развитию физиологической гиперкоагуляции. Концентрация фибриногена к концу III триместра беременности достигает 5–7 г/л. Одновременно с повышением концентрации прокоагулянтов происходит снижение концентрации естественных антикоагулянтов (антитромбина, протеина С, протеина S) и фибринолитической активности (увеличение времени растворения фибринового тромба) [10]. Физиологическая гиперкоагуляция, поэтапно развивающаяся во время беременности, к моменту родов достигает максимума, что следует учитывать при введении факторов свертывания, в частности концентрата протромбинового комплекса (КПК), у рожениц с высоким риском венозных тромбоэмболических осложнений (ВТЭО) [11]. В послеродовом периоде нормализация прокоагуляционного статуса продолжается до 12 недель, поэтому в этот период высок риск развития ВТЭО [10]. Параметры ТЭМ у женщин в III триместре беременности и в раннем послеродовом периоде существенно отличаются от показателей вне беременности [12]. Отмечается уменьшение времени свертывания крови (СТ) с высокой прочностью фибринового сгустка (MCF) и снижением фибринолитической активности (ML) в результате эндотелиальной секреции ингибитора активатора плазминогена (PAI-1 и PAI-2) [11, 13]. Роненсоном А.М. и соавт. был проведен метаанализ, что позволило обозначить референсные интервалы показателей ТЭМ во время беременности у 1328 беременных и 121 роженицы [14]. Lee J. et al. установили статистически значимое повышение средних показателей параметров ТЭМ у рожениц по отношению к беременным: A5FIBTEM 21,05 и 19,7 мм соответственно (p=0,008); A5EXTEM 54,8 и 53,2 мм соответственно (p=0,025); CTEXTEM 52,2 и 53,7 с соответственно (p=0,049) [15].
Диагностика нарушений гемостаза при массивном кровотечении
На текущий момент нет консенсуса по вопросу о классификации степени кровотечения ввиду использования разных подходов для определения объема кровопотери: визуальная оценка, гравиметрический метод и использование расчетных формул. Визуальная оценка объема кровопотери при массивных кровотечениях имеет большую погрешность. Применение градуированных емкостей для сбора крови снижает погрешность при визуальной оценке, но данный подход неэффективен при кровопотере более 2500 мл [16]. Гравиметрическая оценка кровопотери более точная по сравнению с визуальной, но также имеет недостатки. Применение расчетных методов по изменению уровня гемоглобина или гематокрита для оценки объема кровопотери обладает низкой точностью, особенно при переливании значительного объема инфузионных сред [1]. Для определения степени тяжести кровопотери и выбора тактики терапии необходимо проводить комплексную оценку, которая учитывает клинические симптомы гиповолемии.
Наиболее частыми причинами ПРК являются нарушения сокращения матки (гипотония или атония); поэтому с целью снижения объема кровопотери используется активное ведение 3-го периода родов, которое включает введение утеротоников сразу после рождения ребенка, активные тракции за пуповину и массаж матки. Однако только введение окситоцина обладает доказанным эффектом профилактики ПРК: в 3-м периоде родов окситоцин снижает риск кровопотери свыше 500 мл на 50% и свыше 1000 мл на 40% [17, 18]. Наряду с введением окситоцина, с целью профилактики кровотечения, целесообразно использовать прогемостатические препараты [19].
Для лабораторной диагностики нарушений системы гемостаза и терапии компонентами крови рекомендуется использовать стандартные (клоттинговые) тесты (фибриноген, протромбиновое время (ПВ), активированное частичное тромбопластиновое время (АЧТВ) и подсчет количества тромбоцитов) или интегральные методы, такие как TЭГ и TЭM [5]. В отличие от коагулологических методов, ТЭГ и TЭM оценивают все этапы образования сгустка и его стабильность (активность системы фибринолиза), учитывая вклад форменных элементов крови, поскольку в качестве образца используется цельная кровь [7]. Стандартные методы оценки коагуляции имеют ряд ограничений: длительное время исследования (минимум 40 минут), отсутствие информации о стабильности сгустка и активности фибринолиза; использование в качестве биоматериала плазмы крови не позволяет оценить вклад клеток в образование сгустка; условия тестирования существенно отличаются от условий in vivo [20, 21]. Интегральные методы позволяют осуществлять диагностику нарушений гемостаза у пациентов в критическом состоянии, поскольку первые данные (время свертывания) о состоянии системы гемостаза можно получить через 1–3 минуты от начала исследования.
Результаты TЭГ и ТЭM представляются в графическом и цифровом виде. Параметры описывают четыре этапа образования сгустка: инициирование (R, CT), усиление (k, CFT), распространение (угол α) и фибринолиз (LI 30, ML) (рис. 1). Технологии, реагенты ТЭГ и ТЭМ в некоторой степени схожи, однако полученные результаты нельзя сравнивать [22].
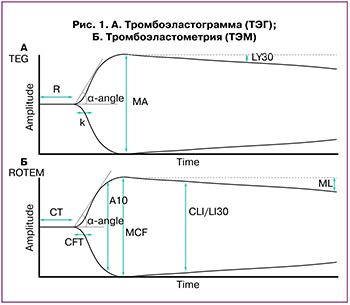
Время реакции (R, с) и время свертывания (CT, с) характеризуют концентрацию факторов свертывания (внешнего или внутреннего пути в зависимости от активатора коагуляции); кинетика образования сгустка (k, с) и время образования сгустка (CFT, с) определяют скорость полимеризации фибрина, а также функциональную активность тромбоцитов; α-угол в обоих случаях (ТЭГ и ТЭМ) характеризует скорость роста фибриновой сети. Структурные параметры отражают вклад фибриногена и тромбоцитов в образование сгустка: плотность сгустка (Ах, мм) – это амплитуда через х (5, 10, 20) минут определяется только в ТЭМ; максимальная амплитуда (MA, мм) и максимальная плотность сгустка (MCF, мм). Параметры для оценки фибринолиза в ТЭГ и ТЭМ также отличаются: лизис через 30 минут (LY30, %) показывает процентное уменьшение амплитуды через 30 минут после достижения МА, индекс лизиса сгустка через 30 минут (CLI30, %) – это сгусток, оставшийся через 30 минут после СТ, измеряемый в процентах от MCF. Максимальный лизис (ML, %) в ТЭМ характеризует активность системы фибринолиза и оценивается по разнице MCF и плотности через 60 минут [23].
При массивной кровопотере в акушерской практике многие показатели коагулограммы являются недостаточно информативными, так, параметры ПВ и АЧТВ чаще всего остаются в пределах нормы, если объем кровопотери не превышает 4000–5000 мл [24]. Karlsson O. et al. продемонстрировали, что параметры коагулограммы и ТЭГ изменяются, когда кровопотеря превышала 2000 мл. С помощью ТЭГ и ТЭМ при кровотечении можно выявить увеличение времени свертывания крови, что свидетельствует о дефиците факторов свертывания, снижение прочности сгустка за счет дефицита фибриногена и/или тромбоцитов и гиперфибринолиз [11]. Интегральные методы используются для оценки необходимости назначения препаратов протромбинового комплекса [25]. Для оценки функциональной активности тромбоцитов используются такие параметры, как PLTEM (MCFEXTEM – MCFFIBTEM = PLTEM), площадь под кривой (AUCEXTEM) и максимальная эластичность (MCE). PLTEM A5 с высокой вероятностью (100–70%) прогнозирует уровень тромбоцитопении, что обеспечивает быстрое принятие решения о необходимости трансфузии тромбоцитов [26]. Параметры PLTEM, CFTEXTEM, MaxVelEXTEM характеризуют функциональную активность и позволяют оценить гемостатический эффект после трансфузии тромбоцитов у пациентов с кровотечением [27]. Показана клиническая значимость параметра PLTEM при терапии ПРК для мониторинга уровня и функциональной активности тромбоцитов [28]. Параметр А5FIBTEM показал высокую корреляцию с концентрацией фибриногена по Клауссу [29]. Для выявления гиперфибринолиза, наиболее частой причины кровотечения, необходимо сравнить параметры EXTEM с APTEM (тест с ингибитором фибринолиза). Лучшее формирование сгустка в APTEM (CTAPTEM<CTEXTEM на 10%, CFTAPTEM<CFTEXTEM на 20%, MCFAPTEM>MCFEXTEM) указывает на гиперфибринолиз [30].
Коррекция нарушений гемостаза при послеродовых кровотечениях
Гиперактивация системы фибринолиза
Гиперфибринолиз является наиболее частой причиной развития коагулопатии в послеродовом периоде, поэтому ингибитор фибринолиза является препаратом первой линии при ПРК [18, 31]. Транексамовая кислота представляет собой наиболее изученный антифибринолитик, используемый для профилактики и лечения ПРК. Рекомендуемой дозой транексамовой кислоты для коррекции нарушений гемостаза является 15–20 мг/кг [31]. Более высокий терапевтический эффект, без повышения процента осложнений, достигается при использовании максимальных доз транексамовой кислоты 50–100 мг/кг [32]. Повторное введение препарата допустимо по истечении 30 минут после введения первой дозы. Максимальная концентрация транексамовой кислоты в плазме крови регистрируется через 3 ч, а выведение более 95% происходит в течение первых 12 ч. Гломерулярная фильтрация – основной путь элиминации препарата, поэтому он противопоказан при нарушении функции почек [31]. Антифибринолитическая концентрация в различных тканях сохраняется в течение 17 ч, а в плазме – до 7–8 ч.
Гипофибриногенемия
Концентрация фибриногена является основным маркером массивного кровотечения [33]. За счет потери крови в первую очередь снижается концентрация фибриногена, которая у беременных женщин в 2 раза повышается к III триместру. Гемодилюция физиологическими растворами при инфузионной терапии ПРК также ведет к разбавлению фибриногена и снижению его концентрации. Концентрация фибриногена в плазме крови менее 2 г/л ассоциирована с развитием тяжелого ПРК со специфичностью 99,3% [34]. Поэтому при продолжающемся ПРК необходимо поддерживать концентрацию фибриногена более 2 г/л [35]. Следовательно, трансфузия свежезамороженной плазмы (СЗП), где содержание фибриногена не более 2 г/л, с целью коррекции гипофибриногенемии не может использоваться. Целенаправленной терапией дефицита фибриногена является трансфузия криопреципитата из расчета 1 доза на 10 кг массы тела [36], что позволяет снизить на треть объем кровопотери, оптимизировать клинический эффект и избежать посттрансфузионных осложнений, обусловленных значительными объемами трансфузионных сред [37].
Снижение активности факторов свертывания
Рутинно для коррекции факторов свертывания используется СЗП. Эффективность использования в акушерской практике тактики трансфузии компонентов крови (1:1:1) в последнее время подвергается сомнению [25]. Было показано, что трансфузия СЗП не рекомендуется роженицам с массивным ПРК без лабораторного подтверждения дефицита факторов свертывания (МНО>1,5, АЧТВ ratio>1,5) [38]. Недавний обзор показал, что СЗП нельзя расценивать как альтернативу криопреципитату или концентрату фибриногена при послеродовых кровотечениях [25]. Концентрат протромбинового комплекса является гемостатическим препаратом, содержащим комплекс витамин К-зависимых факторов свертывания (II, VII, IX, X). Восполнение факторов свертывания крови в отсутствие оптимальной концентрации фибриногена и тромбоцитов не будет способствовать функционированию системы гемостаза [36]. Эксперты предполагают, что для лечения кровотечений следует применять низкие дозы (10–15 МЕ/кг) концентрата протромбинового комплекса с целью минимизации риска тромбоэмболических осложнений [39]. На сегодняшний день рутинное применение концентрата протромбинового комплекса для терапии ПРК не рекомендуется [36].
Тромбоцитопения
Безусловно, высокий риск ПРК обусловлен сочетанием тромбоцитопении <100×109/л с низким уровнем фибриногена <2,9 г/л на момент родов [40]. Во многих исследованиях показано, что при кровопотере менее 5000 мл в большинстве случаев содержание тромбоцитов сохраняется в диапазоне референсных значений [25]. Однако функциональная активность тромбоцитов не всегда соответствует их количеству [28]. Стандартная единица тромбоцитарного концентрата, приготовленная из одной дозы консервированной крови объемом 450 мл, содержит не менее 55×109/л тромбоцитов. Переливание одной дозы ориентировочно увеличивает уровень тромбоцитов у реципиента с площадью поверхности тела 1,8 м2 на 5–10×109/л при отсутствии кровотечения. Терапевтической дозой тромбоцитарного концентрата является переливание не менее 50–70×109/л тромбоцитов на каждые 10 кг массы тела или 200–250×109/л на 1 м2 поверхности тела. Следовательно, для взрослых реципиентов необходимое терапевтическое количество тромбоцитов должно составлять 300–500×109/л [41].
Стандартизованные алгоритмы для целенаправленной терапии
Мониторинг системы гемостаза при кровотечении с помощью ТЭМ стал неотъемлемой частью МКП, что является важной составляющей повышения уровня безопасности оказания медицинской помощи. Необходимо не только использовать ТЭМ с целью выявления коагулопатии, но и проводить коррекцию нарушений гемостаза с помощью научно обоснованных алгоритмов, адаптированных к конкретной популяции пациентов и доступности гемостатических средств [42]. Лидер в области лечения кровотечений, Görlinger K., представил алгоритм, c помощью которого можно исключить основные причины коагулопатического ПРК. Алгоритм учитывает особенности системы гемостаза (повышение уровня фибриногена) у родильниц и смещение референтных диапазонов (рис. 2).
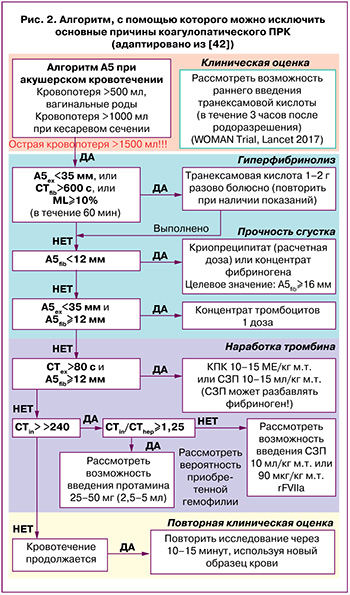
Для эффективного использования алгоритма необходима объективная оценка наличия клинически значимого (массивного) кровотечения и потенциальной необходимости переливания крови. Во-первых, исключается гиперфибринолиз, как наиболее частая причина кровотечения. При параметрах А5EXTEM<35 мм, и/или СTFIBTEM>600 с, и/или ML≥10% гиперфибринолиз подтверждается. В исследовании WOMAN trial (применение транексамовой кислоты при ПРК) параметр MLEXTEM>15% признан критерием гиперфибринолиза [21, 43]. Другие авторы предлагают использовать комбинацию MLEXTEM, MLFIBTEM и параметров APTEM [12, 44]. Но для получения результата ML должно пройти не менее 60 минут, что не допустимо при массивном ПРК.
Во-вторых, необходимо исключить дефект плотности образующегося сгустка, которая зависит от функциональной активности фибриногена и тромбоцитов. В исследовании Vries J. et al. была показана сильная (r=0,96) корреляция структурных параметров (А5, А10, MCF) теста FIBTEM и фибриногена по Клауссу [29]. Концентрация фибриногена А5<12 мм является нижней границей для принятия решения о введении концентрата фибриногена или трансфузии криопреципитата [25], но целевое значение – ≥16 мм [42]. Дефицит фибриногена увеличивает CTEXTEM и CTINTEM; следовательно, при условии, что А5FIBTEM в норме, можно объективно интерпретировать CTEXTEM и CTINTEM. Основным преимуществом FIBTEM является быстрое (в течение нескольких минут) получение информации об уровне фибриногена, в отличие от коагулометрического анализа по Клауссу, когда требуется 30–60 минут [29]. Если исключен дефицит фибриногена (А5FIBTEM>12 мм), но А5EXTEM<35 мм, причиной коагулопатии является дисфункция тромбоцитов, и пациенту необходима трансфузия тромбоконцентрата. В-третьих, исключается снижение образования тромбина, которое наблюдается только при тяжелом кровотечении (за исключением кровотечений, вызванных антикоагулянтами или гемофилией); причем сначала снижается уровень фибриногена, а затем тромбина. Следует учитывать, что повышение образования тромбина за счет использования гемостатических средств (КПК, СЗП или фактора VII) связано с более высоким риском тромбоэмболических осложнений по сравнению с восполнением субстратов (фибриногена, тромбоцитов). Поэтому сначала проводится коррекция уровня фибриногена и тромбоцитов (А5FIBTEM и А5EXTEM), а затем оценивается необходимость увеличения образования тромбина при увеличении CTEXTEM и CTINTEM [42].
Преимущества целенаправленной терапии
Многочисленные данные подтверждают высокую клиническую значимость для POINT OF CARE (POC – по месту оказания помощи) при посттравматической коагулопатии [20]. Экспресс-оценка состояния системы гемостаза, осуществляемая с помощью ТЭГ и ТЭМ, позволяет выбрать правильную тактику коррекции терапии, обосновать введение СЗП, криопреципитата или тромбоцитного концентрата либо, наоборот, доказать необоснованность переливания того или иного компонента крови [25]. Показано, что использование интегральных методов коагуляции (ТЭГ, ТЭМ) в лечении пациентов с кровотечением снижает частоту трансфузий компонентов крови и смертность [45–47]. В другом обзоре было показано, что трансфузионная терапия под контролем ТЭГ, ТЭМ снижает общую смертность (7,4% против 3,9%), использование объемов СЗП, тромбоцитов и уменьшает количество пациентов, у которых развивается почечная недостаточность. В крупном проспективном обсервационном исследовании показано, что параметры ТЭГ обладают прогностической значимостью относительно прогрессирующего акушерского кровотечения более 2500 мл [13].
Snegovskikh D. et al. показали значительное снижение предполагаемой кровопотери, частоты использования эритроцитарных компонентов и СЗП (Р<0,001), а также частоты гистерэктомий (25,0% против 53,5%, P=0,013) и госпитализаций в отделения интенсивной терапии (3,6% против 43,1%, P<0,001) при использовании интегральных методов для определения необходимости коррекции системы гемостаза [48]. Трансфузия криопреципитата для уменьшения потребности в СЗП у пациенток с ПРК была показана Wikkelso A. et al. Использование стандартизованного алгоритма, основанного на параметрах ТЭМ, показало преимущество применения концентрата фибриногена, которое привело к уменьшению потребления компонентов крови [47]. Значение A5FIBTEM и концентрация фибриногена по Клауссу в крови перед родоразрешением не имеют прогностической значимости относительно риска ПРК, но интраоперационное значение A5FIBTEM при ПРК может определить риск развития массивного кровотечения и потребность в трансфузионной и гемостатической терапии [48, 49].
Целенаправленная терапия снижает частоту и объем трансфузий компонентов крови, а также развитие ассоциированных осложнений. Поэтому использование в клинической практике TЭГ и TЭM для выявления коагулопатии при ПРК включено в клинические рекомендации «Послеродовое кровотечение» (уровень убедительности рекомендаций А-1) [50].
Заключение
Использование ТЭГ и ТЭМ позволяет получить информацию о состоянии системы гемостаза в кратчайшие сроки для раннего выявления коагулопатии и предотвращения прогрессирования ПРК. Мониторинг состояния системы гемостаза при ПРК под контролем ТЭМ стал неотъемлемой частью концепции МКП, которая повышает безопасность пациентов. Гемостатическая терапия должна проводиться согласно научно обоснованным алгоритмам, адаптированным к конкретной популяции пациентов и доступности гемостатических препаратов в учреждении. Соответственно, данный подход реализует концепцию персонализированной или прецизионной медицины при ПРК. Целенаправленная терапия эффективно снижает объем кровопотери, потребность в переливании крови, частоту осложнений и затраты на лечение пациента.



