Введение. Профилактика повторного камнеобразования (метафилактика) играет важную роль в снижении рецидивов уролитиаза. В большинстве различных национальных клинических рекомендаций по мочекаменной болезни (МКБ) приведены схемы противорецидивного лечения, где ключевая роль отводится применению цитратных смесей [1]. Действие данных препаратов базируется на фармакологических свойствах двух основных компонентов: солей щелочных металлов и лимонной кислоты, являющейся слабой кислотой [2]. В результате основной фармакологический эффект выражается в повышении уровня pH мочи [3], снижении выведения кальция с мочой, подавлении образования кристаллов мочевой кислоты и кальция оксалата [4, 5], что крайне важно для профилактики рецидивирования мочекислой и кальций-оксалатной форм МКБ [6].
Для улучшения состояния пациентов с камнями мочевыделительной системы исторически применялись растительные средства, различные вещества, основной целью которых было подщелачивание внутренней среды организма. По данным Национальной медицинской библиотеки Центра биотехнологичной информации (PubMed. gov), на сегодняшний день насчитывается более 2000 работ, посвященных изучению цитратных смесей. Первой публикацией является работа доктора T. Trotter, датированная 1800 г., в которой приводятся факты использования цитратов как ключевого компонента профилактики цинги [7]. В более поздних работах действие цитратов показано при консервировании крови, стабилизации антибактериальных растворов, интоксикации организма и других клинических ситуациях. Первое же описание применения цитратных смесей при МКБ у людей представлено в работе W. Staehler [8]. Уникальность данной публикации заключается в том, что в ней впервые описаны вопросы применения цитратных смесей для растворения мочевых камней в отношении людей путем введения лимонной кислоты через мочеточниковый катетер. Более поздние работы по применению цитратных смесей при МКБ посвящены описанию их как препаратов первой линии при проведении литолитической терапии. В 1986 г. J. S. Rodman et al. проанализировали принципы применения цитратной терапии и представили рекомендации по ее клиническому применению [9]. Данные рекомендации в 2007 г. были дополнены G. Becker et al. [10].
Вопрос применения цитратных смесей для коррекции метаболических нарушений тоже изучен и отражен в последних клинических рекомендациях Европейского и Американского обществ урологов [6, 11, 12]. Однако в большинстве работ показано действие исключительно калий-цитратных препаратов, тогда как известно, что группа цитратных смесей, или щелочных цитратов, применяемых при уролитиазе, включает разные цитрат-содержащие соли: калий-цитратные, натрий-цитратные, магнийцитратные, калий-натрий-цитратные [13]. Необходимо отметить, что для Российской Федерации этот факт имеет очень важное значение, поскольку в нашей стране зарегистрированы калий-натриевые и натрий-цитратные смеси.
В связи с вышесказанным целью настоящего исследования стало определение влияния натрий-цитратной смеси Блемарен® (далее Препарат) на состояние обмена литогенных веществ у пациентов с мочекаменной болезнью.
Материалы и методы. В исследование включены 46 пациентов (26 мужчин и 20 женщин) в возрасте от 18 до 65 лет. Подбор дозы осуществлялся последовательно. Первоначально в течение 3 сут. в одно и то же время измерялся уровень pH мочи без внесения каких-либо изменений в диете. Далее на протяжении 3 дней пациенты исключали из своего рациона пищу, богатую пуринами, повышали потребление воды на 30% и вновь измеряли уровень pH мочи 3 раза в сутки. Получив эти данные, определялся инициальный уровень pH мочи и подбирали начальную дозу препарата. Каждые 3 сут. доза увеличивалась до достижения стабильного уровня pH мочи 6,2–6,8, сохранявшегося в течение суток.
На протяжении всего исследования участники 3 раза в сутки измеряли уровень pH мочи при помощи тест-полосок, входивших в комплект препарата, и вносили результаты в дневник. Препарат принимали после еды по 1 табл. (3 г) 3 раза в день.
Дважды (в начале исследования и через 14 дней после начала приема Препарата) выполняли биохимический анализ крови и суточной мочи:
- биохимический анализ крови (общий кальций, натрий, магний, фосфор, хлор, мочевина, креатинин, мочевая кислота) выполняли на автоматическом анализаторе AU 480 (Beckman CULTER, USA);
- биохимический анализ суточной мочи (общий кальций, натрий, магний, фосфор, хлор, мочевина, креатинин, мочевая кислота, оксалаты, цитраты) определяли автоматическим анализатором ADVIA-1200 (Bayer-Siemens) по стандартным методикам с помощью диагностических наборов реагентов фирмы Siemens.
По результатам работы сформировано две группы пациентов подгруппы:
- Группа 1 – пациенты с pH мочи ниже 6,2 до приема Препарата (n=34);
- Группа 2 – пациенты с pH мочи, равным или выше 6,2, но меньше 6,8 до приема Препарата (n=12).
Статистический анализ полученных данных осуществляли с помощью критериев Стьюдента и Вилкоксона посредством компьютерной программы Statistica 12.0 (StatSoft USA).
Результаты. Средний возраст всех участников исследования составил 45,8±2,3 года. Статистической разницы в среднем возрасте мужчин (45,5±2,8) и женщин (51,2±2,6), участвовавших в исследовании, выявлено не было (p>0,05). Возрастная структура участников исследования представлена в табл. 1.
Сравнительный анализ биохимических показателей сыворотки крови до начала приема и в последний день приема препарата у пациентов, вошедших в группу 1, показал достоверное снижение только показателей натрия и хлора (p<0,05). Уровень креатинина, мочевины, мочевой кислоты, калия, фосфора, магния и общего кальция статистически не различался (табл. 2).

Сравнительный анализ биохимических показателей сыворотки крови пациентов 2-й группы до начала и в последний день приема Препарата не выявил достоверных различий в уровнях всех исследуемых веществ в сыворотке крови (табл. 3).
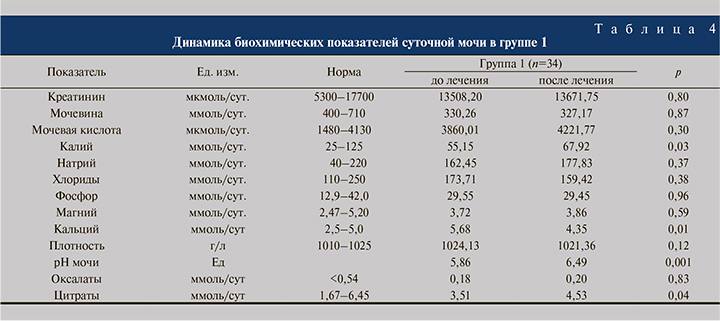
Анализ полученных данных показал, что на фоне приема Препарата в группе 1 отмечались статистически значимые изменения: снижение уровня экскреции общего кальция с 5,68 до 4,35 ммоль/сут. (p<0,05), увеличение уровня экскреции калия с 55,1 до 67,92 ммоль/сут. и увеличение уровня экскреции уровня цитратов с 3,51 до 4,5 ммоль/сут., а также увеличение среднесуточного показателя уровня pH мочи с 5,86 до 6,49 (p<0,05) (табл. 4).
При статистическом анализе данных биохимического исследования крови пациентов группы 2 выявлено, что на фоне проводимой терапии Препаратом изменения среднесуточного уровня pH мочи не отмечалось (p>0,05), однако при этом уровни почечной суточной экскреции цитратов и натрия достоверно увеличились с 4,52 до 5,65 ммоль/сут. и со 121,62 до 148,17 ммоль/сут. соответственно (p<0,05) (табл. 5) Этот факт подтверждает, что пациенты выполняли данные им рекомендации по приему препарата и что препарат оказывает свое положительное действие.
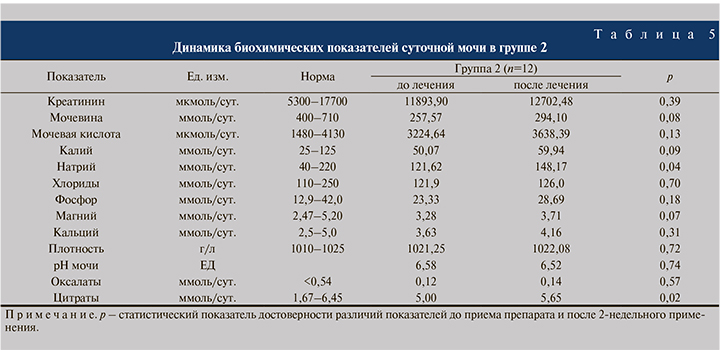
Кроме этого в группе 2 выявлены тенденции к изменению уровней экскреции мочевины с 257,57 до 294,10 ммоль/сут. (p=0,08), магния с 3,28 до 3,71 ммоль/сут. (p=0,07) и калия с 50,07 до 59,94 ммоль/сут. (p=0,09) (табл. 5).
Обсуждение. Применение цитратных смесей играет важную роль в предотвращении и лечении кристаллурии, в образовании мочевых камней. При кальций-оксалатном и мочекислом уролитиазе ингибирующее свойство цитратов основано на защелачивании мочи [14]. В ранее проведенной нами работе показано, что наибольшие изменения почечной суточной экскреции литогенных веществ отмечаются при кислой утренней моче в интервале pH мочи 5,6–5,9, характерном для мочекислой и кальций-оксалатной форм МКБ [16]. Подщелачивающим эффектом обладают не только цитратные смеси, но и бикарбонат натрия, эффективность которого хоть и сравнима, но, как показано, в работе X. Xue et al., уступает цитратной смеси по снижению частоты появления скрытой крови в моче и частоты приступов подагры [17].
Отмечающееся при приеме цитратных смесей смещение pH мочи в щелочную сторону происходит за счет не только действия самого цитрата, но и деятельности ионов бикарбоната, образующихся в печени при его метаболизме [18].
Несмотря на наличие общего компонента (цитратной соли), действие различных цитратных препаратов различается. В работе K. Sakhaee et al. показано, что на фоне приема калий-цитратных смесей отмечается значительное снижение уровня экскреции с мочой кальция, что проявляется снижением насыщенности мочи кальций-оксалатом. Тогда как на фоне применения натрий-цитратных смесей происходит увеличение насыщенности мочи кальций-фосфатом и мононатрий-уратом [19, 20].
При приеме препаратов, содержащих только калийцитрат или натрий-цитрат, существует опасность возникновения гиперкалиемиии и гипернатриемии, в связи с чем основным противопоказанием к их применению служат хроническая почечная недостаточность и риск развития гиперкальциурии на фоне гипернатриурии. Однако МКБ часто сопровождается наличием у пациента хронической почечной недостаточности. Прием же калий-натриевых цитратных смесей, где вещества сбалансированны, снижает данный риск. В проведенном нами исследовании мы не выявили статистически значимого повышения калия и натрия в крови на фоне приема поддерживающей дозы препарата, в моче же уровень экскреции не превышал референсных значений, что еще раз подчеркивает безопасность калий-натриевых смесей и позволяет его применять пациентам с легкой степенью почечной недостаточности.
В нашей работе для поддержания уровня pH мочи 6,2–6,8 [21] у пациентов с уролитиазом мы использовали препарат, относящийся к цитратным смесям. В результате работы нами выявлено, что, несмотря на изменения в концентрации натрия и хлоридов в сыворотке крови на 14-й день приема препарата, их концентрация оказалась в пределах референсных значений. Подобные результаты отмечены в работе J. Shen et al., по данным которой у детей на фоне приема в течение 5 дней калий-цитратных смесей выявлено значительное снижение концентрации в сыворотке крови натрия и повышение уровня pH мочи [22].
Проведенный анализ биохимических показателей суточной мочи на 14-й день приема препарата показал значительное снижение уровня экскреции с мочой кальция, а также повышение уровней экскреции с мочой калия, цитратов и увеличение pH мочи. Подобные результаты показаны в работе N.S. Krieger et al., проведенной на самцах крыс. В работе авторы показали, что через 18 нед. приема калий-цитратных смесей у животных зафиксировано снижение уровня экскреции с мочой кальция и повышение уровня экскреции с мочой цитратов. Кроме того, отмечено повышение уровня экскреции с мочой фосфора, оксалатов и нитратов [23]. В более раннем рандомизированном плацебо-контролируемом исследовании S. Allie-Hamdulay et al. продемонстрированы схожие результаты: на 7-й день приема натрий-цитратной смеси у исследуемой группы пациентов отмечено значительное снижение кислотности мочи, уменьшение уровня экскреции с мочой оксалата кальция и мочевой кислоты [24]. В работе R. Unno et al. продемонстрировано, что прием натрий-цитратных смесей в дозировке 3 г/сут. в течение 12 мес. не только значительно повышает уровень экскреции цитратов с мочой и ее pH, но и уменьшает количество микролитов почки по данным МСКТ [13]. Объяснением выводам этой работы может быть предшествовавшая ей работа С. Duan et al., показавшая, что на фоне применения цитратных смесей отмечается значительное сокращение количества, вида и процента агрегированных нанокристаллов мочи [25].
Применение цитратных смесей при мочекислом и кальций-оксалатном уролитиазе не вызывает вопросов [26, 27]. Однако использование цитратных смесей пациентами с кальций-фосфатной формой МКБ до сих пор остается дискутабельным. С одной стороны, увеличение уровня pH мочи на фоне приема цитратных смесей вызывает перенасыщение мочи кальций-фосфатом, что ведет к прогрессированию камнеобразования, с другой – увеличение цитрата должно повышать растворимость солей кальция в моче, что в свою очередь сопровождается снижением перенасыщения кальций-фосфатом [19]. При этом, как показано в работе A. Hess et al., в некоторых случаях рост брушита при повышении уровня pH мочи замедляется [28].
Таким образом, можно утверждать, что применение цитратных смесей является проверенным и обоснованным методом лечения мочекислого и кальций-оксалатного уролитиаза, а также в ряде случаев и пациентов с кальций-фосфатными камнями. Проведение цитратной терапии может применяться в рамках современной концепции медицины 4П [29], реализуемой как на индивидуальном уровне с при менением персонализированных медицинских устройств [30], так и в рамках программных профилактических мероприятий [31, 32].
Заключение. Применение препарата Блемарен® больными мочекаменной болезнью с pH мочи <6,2 до начала лечения достоверно снижает концентрацию в сыворотке крови натрия и хлоридов в пределах референсных значений, почечную суточную экскрецию общего кальция и повышает уровни почечной суточной экскреции калия, цитратов и pH мочи. У пациентов, у которых pH мочи больше или равен 6,2, но меньше 6,8 до начала лечения без мочевой уреазопродуцирующей микрофлоры, препарат Блемарен® повышает уровень почечной суточной экскреции натрия и цитратов.



