Аргументы необходимости применения комбинированной антигипертензивной терапии
Согласно международным и российским рекомендациям по диагностике и лечению артериальной гипертензии (АГ), для достижения целевого уровня артериального давления (АД) большинству больных требуется комбинация 2 антигипертензивных препаратов (АГП) и более; монотерапия может быть эффективной лишь в 20—30% случаев [1—6].
C 2003 г. в Американских рекомендациях и с 2007 г. в рекомендациях Европейского общества по АГ (ESH) инициация двухкомпонентной комбинированной антигипертензивной терапии (АГТ) рекомендована при увеличении систолического АД (САД) более 20 мм рт.ст., диастолического АД (ДАД) более 10 мм рт.ст. выше целевых значений, а также для больных из группы высокого риска развития сердечно-сосудистых осложнений (ССО). В дополнение к этому ESH в 2009 г. применение фиксированных комбинаций АГП представило как предпочтительное направление комбинированной терапии в лечение больных АГ [2, 3].
Используемая ранее концепция увеличения дозы АГП для снижения АД была пересмотрена после того, как были получены результаты мета-анализа 354 рандомизированных исследований, выполненного M.R. Law и соавт., в котором были показаны преимущества инициации низкодозовой комбинированной терапии над монотерапией [7]. В дальнейшем в мета-анализе D.S. Wald и соавт. было найдено, что исходное назначение комбинации АГП в 5 раз эффективнее, чем тактика удвоения дозы одного лекарственного средства [8]. Более того, используемая в начале лечения комбинированная терапия препаратами в малых дозах снижала частоту побочных эффектов у больных АГ, в отличие от тактики увеличения дозы одного препарата, и, соответственно, частота прерывания лечения была ниже, а пациенты были более к нему привержены [9]. Аналогичные данные продемонстрированы и в ряде других исследований, в которых, например, показано, что ингибиторы ангиотензинпревращающего фермента (АПФ) подавляют ангионевротический отек, обусловленный приемом антагонистов кальция, когда препараты применяются в комбинации [10, 11]. В одном из ретроспективных исследований продемонстрировано, что используемая в начале лечения комбинация АГП через 12 мес терапии обеспечивает достижение целевого уровня АД лучше, чем монотерапия [12].
Одним из важных аргументов необходимости применения комбинированной терапии с начала лечения у больных из группы высокого риска развития ССО стали результаты вторичного анализа данных, полученных в крупном многоцентровом рандомизированном клиническом исследовании (РКИ) VALUE (Valsartan Antihypertensive Long-Term Use Evaluation). В нем было определено, что в группе больных, которые контролировали АД через 6 мес терапии на целевом уровне, частота развития ССО была ниже, чем у пациентов, у которых сохранялась неконтролируемая АГ [13]. Кроме того, в той группе больных, в которой целевой уровень АД был достигнут в течение 1 мес, снижение риска неблагоприятных клинических исходов было более выражено, чем в группе пациентов, у которых снижение АД было более медленным. Как продемонстрировано в ретроспективном анализе S.A. Nasser и соавт., для достижения целевого уровня АД требуются бóльшие усилия, и оно происходит более медленными темпами у больных с исходно высоким риском развития ССО, у которых выявляются сахарный диабет (СД) 2-го типа, ожирение, микроальбуминурия, низкая скорость клубочковой фильтрации и т.п. [14]. Плохой контроль АД зависел не только от факторов, связанных с сопутствующей патологией, но и от инертности врачей, как в плане мониторинга АД на фоне назначенной терапии, так и применения начальной комбинированной АГТ, обеспечивающий более быструю динамику АД и лучший прогноз. Аргументами более быстрой динамики АД на фоне комбинированной терапии могут быть результаты другого РКИ, в котором у больных АГ с метаболическим синдромом показано, что начальная комбинированная терапия блокатором ренин-ангиотензин-альдостероновой системы (РААС) и амлодипином позволяла достигать целевого уровня АД быстрее, чем тактика, основанная на начале лечения с высокой дозы блокатора РААС в виде монотерапии [15]. A.H. Gradman и соавт. представили результаты профилактического влияния комбинированной АГТ на клинические исходы: относительный риск развития ССО был ниже на 34% по сравнению с монотерапией и зависел от скорости достижения целевого уровня АД [16].

В европейских и американских рекомендациях по АГ с 2003 г. указывается, что комбинированную терапию следует назначать не только при увеличении САД на 20 мм рт.ст. и/или ДАД на 10 мм рт.ст. или высоком риске развития ССО, но и при субклиническом поражении органов-мишеней [2, 3]. У больных неосложненной АГ с 1-й степенью повышения АД может быть более эффективной стратегия монотерапии с увеличением дозы одного препарата при необходимости. Однако в мета-анализе, в который было включено 9 РКИ, при использовании фиксированной комбинации блокатора РААС и гидрохлоротиазида 92% больных с повышением АД 1-й степени через 8 нед достигли целевого уровня АД, при использовании высокой дозы блокатора РААС — лишь в 74,7% случаев [17]. В нашем исследовании мы показали, что у больных АГ трудоспособного возраста назначение комбинированной терапии с начала лечения независимо от исходного уровня АД обеспечивает и более выраженный регресс показателей, отражающих поражение органов-мишеней [18]. В Рекомендациях Американского общества по АГ предлагается применять комбинированную терапию с начала лечения также у больных с неосложненной АГ и повышением АД 1-й степени, особенно в тех случаях, когда один препарат может улучшать профиль побочных эффектов другого лекарственного средства в комбинации [19].
В последние годы доказано еще одно преимущество использования комбинированной АГТ над монотерапией, которое заключается в оптимизации вариабельности АД. Сначала в экспериментальных исследованиях было показано, что комбинированная АГТ эффективнее снижает высокую вариабельность АД, чем монотерапия, даже в высоких дозах [20, 21]. Далее анализ когортных исследований показал, что у больных АГ, перенесших транзиторную ишемическую атаку, не только максимальное САД, но и его высокая вариабельность от визита к визиту увеличивали риск инсульта и коронарных событий [22].
Стратегия применения комбинированной антигипертензивной терапии
В Рекомендациях ESH 2013 г. в стратегии применения АГТ произошли некоторые изменения [6]. Как показано на рис. 1, при выборе АГТ учитываются не только группа риска развития ССО и степень повышения АД, но и дозировка используемых препаратов, в том числе в комбинации. Если у больного определены 1-я степень повышения АД и/или низкий/умеренный риск развития ССО, то лечение может быть начато с монотерапии. В отсутствие достижения целевого уровня АД рекомендуется либо увеличить дозу используемого ранее препарата, либо оценить эффект лекарственного средства из другого класса с возможностью дальнейшей титрации его дозы, в отсутствие достижения целевого уровня АД перейти на комбинированную терапию. У больного с высоким и очень высоким риском развития ССО и/или 2-й или 3-й степенью повышения АД рекомендуется лечение начинать с комбинированной терапии, а при недостаточном контроле АД на фоне предшествующей комбинированной терапии — либо увеличить дозы препаратов, входящих в ее состав, либо добавить третий препарат. Затем в отсутствие достижения контроля за АД — перейти на другую двухкомпонентную комбинацию или назначить 3 препарата в максимальной дозе.
Роль фиксированных комбинаций антигипертензивных препаратов
В 2009 г. в пересмотре Рекомендаций ESH отмечено, что для комбинированной терапии больных АГ предпочтительной стратегией является применение фиксированных комбинаций [5].
В целом, как при использовании фиксированных, так и свободных комбинаций АГП, достигается эквивалентный эффект снижения АД, как было показано в ряде исследований [23—25].
Тем не менее фиксированные комбинации имеют некоторые преимущества. В одном из последних мета-анализов выявлено, что применение фиксированных комбинаций АГП значительно улучшает приверженность больных к лечению в сравнении со свободными комбинациями аналогичных лекарственных средств [26]. Соответственно динамика снижения АД и частота достижения целевого уровня АД были лучше при использовании фиксированных комбинаций в сравнении со свободными. В ретроспективном исследовании также показано, что приверженность к лечению при использовании фиксированной комбинации, содержащей эналаприл и гидрохлоротиазид, в течение 12 мес была выше, чем при свободном приеме этих препаратов [27]. Более того, в ряде исследований было определено, что с увеличением приема числа таблеток в течение суток, начиная с 2 и более, не только снижается приверженность к лечению, но и увеличивается риск неблагоприятных клинических исходов [28—31]. По результатам РКИ также известно, что для увеличения частоты достижения целевого уровня АД с 24 до 32% требуется прием 3 препаратов и более [32, 33].
Использование фиксированных комбинаций АГП позволяет упростить задачу достижения целевого уровня АД за счет применения в одной таблетке 2 препаратов из различных классов и более с возможностью гибкой титрации их дозировок [34]. В настоящее время появляются фиксированные комбинации 3 АГП, что также является дополнительным преимуществом в предупреждении и устранении полипрагмазии, особенно у больных из группы высокого риска развития ССО [35].
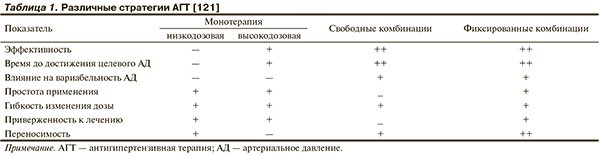
Преимущества и недостатки различных стратегий АГТ у больных АГ представлены в табл. 1.
Предпочтительные комбинации АГП
Согласно международным рекомендациям, в лечении АГ в настоящее время рассматриваются 8 классов АГП: диуретики, β-адреноблокаторы, блокаторы кальциевых каналов, ингибиторы АПФ, антагонисты рецепторов ангиотензина II (АРА), прямой ингибитор ренина, α-адреноблокаторы и препараты центрального действия [6]. Соответственно возможности комбинаций достаточно широки, но не каждая комбинация может быть эффективной, а некоторые — даже опасны. В частности, комбинация β-адреноблокаторов с препаратами центрального действия, такими, как клонидин, α-метилдопа, может приводить к развитию тяжелой брадикардии или блокадам, а их отмена — к гипертоническому кризу [16, 36]. В исследовании ONTARGET (the ONgoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial) комбинация ингибитора АПФ и АРА увеличивала частоту побочных эффектов в отсутствие влияния на прогноз [37]. В исследовании ALTITUDE (Aliskiren Trial In Type 2 Diabetes Using Cardio-Renal Disease Endpoints), которое было прекращено досрочно из-за увеличения частоты остановок сердца в группе комбинированной терапии, добавление прямого ингибитора ренина алискирена к АРА продемонстрировало увеличение частоты развития гипотензии, дисфункции почек, гиперкалиемии [38]. Хорошо известный факт указывает на то, что сочетанное использование β-адреноблокаторов с недигидропиридиновыми антагонистами кальция (например, верапамилом) может приводить к значительному усилению негативных инотропных и хронотропных эффектов комбинируемых препаратов [39]. Некоторые классы АГП не следует комбинировать из-за их антагонистических эффектов, например, доксазозин — α1-адреноблокатор (антагонист) с клонидином — агонистом α-рецепторов [39].
Следовательно, для одобрения использования в клинической практике комбинации АГП необходимо, чтобы она соответствовала определенным требованиям. Во-первых, как считает ряд авторов, следует комбинировать препараты с различными механизмами антигипертензивного действия, при этом один из препаратов должен оказывать дополнительный эффект, обеспечивающий блокаду контррегуляторного пути другого лекарственного средства, запускающего каскад гипертензивных реакций [10]. Например, диуретики и антагонисты кальция наряду с собственными механизмами снижения АД активируют РААС, комбинация их с ингибиторами АПФ или АРА обеспечит ее подавление и потенцирование антигипертензивного эффекта [40, 41].
При комбинации β-адреноблокаторов с диуретиками наблюдается аддитивный эффект снижения АД, при этом последние активируют РААС, а β-адреноблокаторы ее подавляют [42]. Другой пример, иллюстрирующий комплементарность действия, это комбинация β-адреноблокаторов и антагонистов кальция. С одной стороны, дигидропиридиновые антагонисты кальция активируют симпатическую часть вегетативной нервной системы, что может ослаблять эффект β-адреноблокаторов, с другой стороны, индуцированная β-адреноблокаторами вазоконстрикция может быть нивелирована за счет вазодилатирующего эффекта антагонистов кальция [43, 44]. В противовес этому, из-за того, что ингибиторы АПФ и β-адреноблокаторы оказывают однонаправленное действие — блокаду РААС, их сочетанное применение дает лишь умеренный дополнительный антигипертензивный эффект и, соответственно, такая комбинация не рекомендуется для лечения больных АГ [45]. Однако для больных АГ после инфаркта миокарда или с признаками хронической сердечной недостаточности (ХСН) β-адреноблокаторы и ингибиторы АПФ при непереносимости последних АРА становятся препаратами первого ряда, которые не только оказывают клинические эффекты, но и у данной категории больных снижают риск развития смертельных исходов и частоты госпитализаций [46—51].
Во-вторых, требованием оптимальной комбинации АГП является способность каждого ее компонента подавлять побочные эффекты другого составляющего ее препарата для обеспечения лучшей переносимости и безопасности. Так, ангионевротический отек, вызванный антагонистами кальция за счет вазодилатации артерий, может быть устранен ингибиторами АПФ, обеспечивающими посткапиллярную венозную дилатацию [11, 19, 52]. Блокаторы РААС или антагонисты минералокортикоидных рецепторов обеспечивают профилактику гипокалиемии, вызванной тиазидными диуретиками [40, 53].
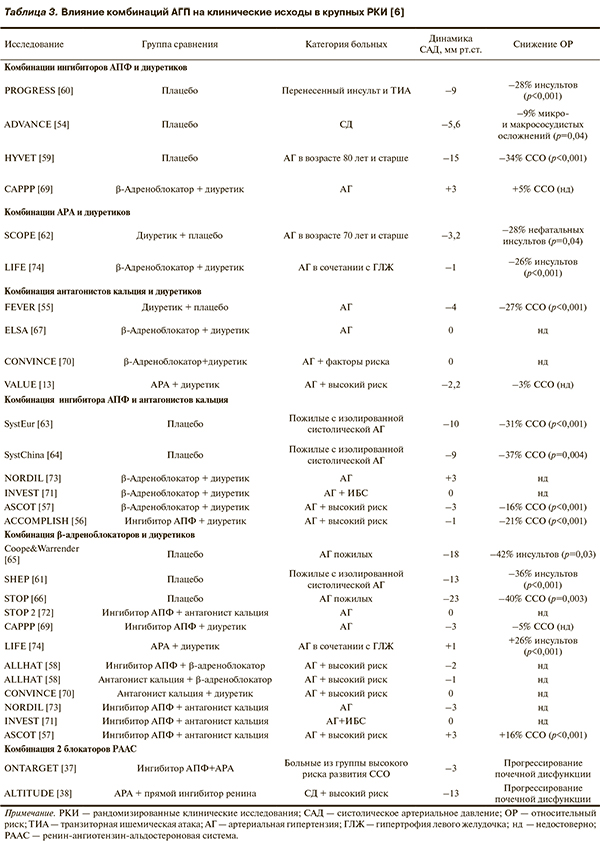
В-третьих, выбор компонентов для комбинированной АГТ должен быть осуществлен не только на основании механизмов действия каждого ее компонента, выраженности антигипертензивного эффекта и возможности подавлять побочные эффекты, но с учетом конкретной клинической ситуации и результатов клинических исследований в плане влияния лечения на клинические исходы (табл. 2, 3).
В целом имеются только косвенные результаты РКИ, которые дают информацию о влиянии комбинированной АГТ на снижение риска развития ССО. Среди крупных РКИ только в 3, по крайней мере, одной из целей была оценка влияния на клинические исходы комбинированной АГТ, назначенной в начале лечения. Это исследование ADVANCE (Action in Diabetes and Vascular Disease — PreterAx and DiamicroN MR Controlled Evaluation), в котором сравнивалась комбинация ингибитора АПФ и тиазидоподобного диуретика с плацебо (но при условии продолжения фоновой АГТ), FEVER (Felodipine Event Reduction Study), в котором дана сравнительная оценка эффекта антагониста кальция плюс диуретика с диуретиком плюс плацебо в китайской популяции, а также исследование ACCOMPLISH (Avoiding Cardiovascular events through Combination therapy in Patients Living with Systolic Hypertension), в котором проводилось сравнение комбинаций ингибитора АПФ с антагонистом кальция и с диуретиком [54—56].
Во всех других исследованиях АГТ начиналась с монотерапии и затем добавлялся другой препарат или даже несколько лекарственных средств, например, в исследовании ASCOT-BPLA (Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm) [57]. В некоторых РКИ второй АГП выбирался исследователем среди тех лекарственных средств, которые не использовались в других группах, как, например, это было ограничено протоколом исследования ALLHAT (Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack) [58].
С учетом особенностей дизайна исследований в табл. 3 представлено, что, за исключением комбинации АРА с антагонистами кальция, которая не изучалась ни в одном из исследований, определяющих влияние сочетанного приема препаратов на клинические исходы, все комбинации оценивались, по крайней мере, по сравнению с плацебо и продемонстрировали значительное преимущество [54, 55, 59—66].
В исследованиях, в которых сравнивались различные лекарственные режимы, применяемые в разной пропорции больных в группах, не было получено преимуществ той или иной комбинации АГП по влиянию на клинические исходы, за исключением двух [13, 58, 67—73]. Это исследования ASCOT и LIFE (Losartan Intervention For Endpoint reduction in hypertension study), в которых сравнивались комбинации ингибитор АПФ + антагонист кальция и АРА + диуретик с атенололом и тиазидным диуретиком [57, 74].
Данные комбинации были более предпочтительны по сравнению с β-адреноблокатором и тиазидным диуретиком в плане снижения риска развития ССО. Хотя в ряде других исследований комбинация β-адреноблокатора с тиазидным диуретиком была так же эффективна, как и другие комбинации [58, 69, 72, 73]. В 3 РКИ аналогичная комбинация была более эффективна, чем плацебо [61, 65, 66]. Одним из негативных факторов комбинации β-адреноблокатора и диуретика по сравнению с другими является увеличение частоты развития СД 2-го типа при ее использовании [75].
Только в одном исследовании ACCOMPLISH, в котором сравниваемые фиксированные комбинации ингибитора АПФ с антагониста кальция или тиазидного диуретика применялись у всех больных в группах, было найдено, что сочетанное использование ингибитора АПФ и дигидропиридинового антагониста кальция было более предпочтительно в плане снижения риска развития ССО по сравнению с комбинацией ингибитора АПФ и диуретика, несмотря на отсутствие различий между группами по динамике АД [56]. Преимущество комбинации ингибитора АПФ и антагониста кальция, вероятно, реализуется за счет способности обоих ее компонентов благоприятно влиять на центральное АД [76—78].
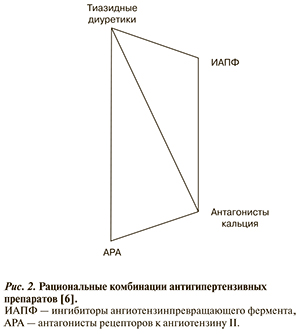
Схема рациональных комбинаций в соответствии с Рекомендациями ESH (2013) представлена на рис. 2.
Новые комбинации ингибиторов АПФ и антагонистов кальция
В последние годы появляются новые комбинации ингибиторов АПФ и антагонистов кальция, которые обладают дополнительными позитивными фармакологическими и патогенетическими свойствами в плане снижения АД и органопротекции за счет применения, например, современных антагонистов кальция. Перспективной в этом отношении является фиксированная комбинация эналаприла с лерканидипином (корипрен, RECORDATI IRELAND, Ltd).
 Эналаприл — один из самых известных и часто назначаемых в европейских странах и России АГП [79—81].
Эналаприл — один из самых известных и часто назначаемых в европейских странах и России АГП [79—81].
Хорошо известно, что в крупных РКИ эналаприл зарекомендовал себя не только как эффективный и безопасный АГП, но и как лекарственное средство, применение которого снижает риск развития ССО, обеспечивает профилактику прогрессирования почечной дисфункции и развития поражения других органов-мишеней [82—87]. Доказательная база эналаприла широка и в лечении больных с ХСН и сниженной фракцией выброса [88—91].
Препарат лерканидипин — дигидропиридиновый блокатор кальциевых каналов третьего поколения. Отличительными свойствами его являются высокая липофильность, медленное начало и большая продолжительность действия в сравнении с другими препаратами этой группы [92]. Коэффициент распределения лерканидипина между различными липидными образованиями в буферной среде с рН 7 выше, чем у амлодипина, почти в 15 раз. Соответственно в силу своей высокой липофильности, в отличие от классических антагонистов кальция, которые блокируют кальциевые каналы на внешней стороне мембраны гладкомышечных клеток сосудов и длительность их действия зависит от их концентрации в плазме, лерканидипин проникает в липидный слой клеточной мембраны, продолжительность его действия зависит от концентрации в клеточной мембране, а не в плазме, что значительно увеличивает время действия.
Данный препарат демонстрирует также высокую вазоселективность. В экспериментальных исследованиях на животных выявлено избирательное накопление препарата в кальциевых каналах клеток сосудов и незначительное — в тканях сердца [93]. Это означает, что лерканидипин в большей степени накапливается в гладкомышечных клетках сосудистой стенки, не проявляя негативной инотропной активности за счет активации симпатической нервной системы, способствующей развитию рефлекторной тахикардии, которая может привести к формированию и прогрессированию дисфункции сердца [94].
Соответственно в силу большой продолжительности и высокой вазоселективности лерканидипин хорошо переносится, частота его побочных эффектов ниже, чем у других антагонистов кальция дигидропиридинового ряда [95, 96].
Лерканидипин в одинаковой степени выводится почками и через печень, что является важным его преимуществом при лечении больных пожилого возраста, с печеночной и почечной дисфункцией, не требующим уменьшения дозы [94].
Антигипертензивная эффективность лерканидипина изучена в ряде исследований, в сравнении как с другими антагонистами кальция, так и с препаратами из других классов, характеризующаяся сходным профилем снижения АД [97—102].
По данным ряда исследований, лерканидипин дает антиатерогенный эффект, одним из механизмов которого явилась оптимизация коллагенолиза межклеточного матрикса артериальной стенки [103—105].
В ряде исследований лерканидипин проявил также нефропротективные свойства [106—108]. В сравнении с рамиприлом у больных СД 2-го типа и микроальбуминурией лерканидипин в большей степени тормозил скорость экскреции альбумина с мочой [109].
Кроме того, у больных АГ и СД лерканидипин снижал уровень гликированного гемоглобина, проявлял нейтральный метаболический эффект в отношении липидного обмена [110, 111].
Есть данные о том, что лерканидипин оказывает антиишемический эффект [112].
При использовании комбинации эналаприла и лерканидипина (корипрена) в многочисленных исследованиях показаны ее лучшая антигипертензивная эффективность и переносимость, чем монотерапии каждым препаратом в отдельности [113, 114].
Так, в двойном слепом рандомизированном плацебоконтролируемом исследовании монотерапия лерканидипином или эналаприлом в сравнении с комбинацией этих препаратов продемонстрировала значительно меньший эффект снижения АД [115]. Число больных, которые достигли целевого уровня АД, было значительно выше в группе комбинированного лечения эналаприлом и лерканидипином, чем при использовании мототерапии каждым из препаратов. Кроме того, найдено, что добавление лерканидипина к терапии эналаприлом, когда его эффект недостаточен, не уступает антигипертензивному действию гидрохлоротиазида в сочетании с ингибитором АПФ у больных СД 2-го типа [116].
Частота побочных эффектов на фоне фиксированной комбинации эналаприла с лерканидипином была низкой во всех опубликованных исследованиях и не превышала показателя, полученного при оценке монотерапии [116, 117]. Ангионевротический отек при использовании комбинации эналаприла с лерканидипином не был зарегистрирован, частота сердечных сокращений в покое, в том числе при проведении суточного мониторирования, не различалась между группами сравнения. Отсутствовал негативный эффект влияния комбинации эналаприла с лерканидипином на углеводный и липидный обмен [118].
В наблюдательном исследовании, в которое были включены более 8000 больных АГ, антигипертензивную эффективность, переносимость и приверженность к комбинированной терапии эналаприлом с лерканидипином врачи, участвующие в исследовании, оценили как «хорошую» и «очень хорошую» в 94 и 97% случаев соответственно [119]. Аналогичные данные получены в другом наблюдательном исследовании при оценке динамики не только офисного АД, но и при домашнем измерении и суточном мониторировании [120].
Таким образом, стратегия начала лечения с применения комбинированной АГТ требуется большинству больных АГ. В целях улучшения приверженности к лечению и удержания больных на терапии предпочтительнее использовать фиксированные комбинации АГП. Выбор комбинации АГП зависит не только от аддитивности эффектов препаратов, их механизмов действия на АД, но, прежде всего, от конкретной клинической ситуации, а также от наличия доказательной базы по способности комбинированной терапии обеспечивать коррекцию пораженных органов-мишеней и улучшать прогноз заболевания. В этом отношении есть данные о том, что комбинация блокатора РААС с антагонистом кальция или гидрохлоротиазидом предпочтительнее комбинации атенолола с тиазидным диуретиком, а комбинация ингибитора АПФ с дигидропиридиновым антагонистом кальция оказывает достоверно более выраженное влияние на снижение риска развития ССО, чем с гидрохлоротиазидом. Трехкомпонентная комбинация АГП может быть эффективна в случаях с неконтролируемой или резистентной АГ.