Введение. Целью послеоперационного обследования, лечения и наблюдения пациентов с мочекаменной болезнью (МКБ) стало предотвращение рецидива камнеобразования. К настоящему времени разработаны практические рекомендации по выявлению факторов риска первичного образования камней и рецидива МКБ, а также клинические рекомендации по профилактике повторного камнеобразования [1, 2].
Остеопороз – это заболевание, для которого характерны снижение прочности кости и повышение риска переломов. Снижение минеральной плотности костной ткани (МПКТ) связано с потерей кальция. У больных остеопорозом отмечено повышение частоты образования камней в почках [3]. Применение средств, препятствующих патологическому обмену костной ткани, повышение физической нагрузки позволяют предотвращать отрицательный баланс кальция и снижать вероятность образования камней в почках [4, 5].
Наличие и выраженность остеопороза могут быть фактором, вызывающим образование мочевых камней [6].
У больных нефролитиазом регистрируют снижение МПКТ и увеличение гиперкальциурии [7].
Кальций выводится почками однонаправленно с изменением выделения натрия, поэтому транспорт в почках осуществляется посредством единого механизма. Однако установлено, что на фоне приема тиазидных диуретиков выделение кальция с мочой в первые дни лечения не меняется, а к концу 1-й недели прием уменьшается и этот эффект продолжается в течение всего времени лечения [8]. При прекращении приема тиазидных диуретиков отмечается преходящий «рикошетный» эффект с подъемом уровня кальция в моче.
Увеличение выделения кальция с мочой обусловлено прямым и непрямым действием тиазидных диуретиков на почки, а также их внепочечным эффектом. В проксимальном отделе нефрона они оказывают слабое и однонаправленное действие, снижая реабсорбцию натрия и кальция. Однако в дистальном отделе нефрона тиазидные диуретики действуют разнонаправленно: реабсорбция натрия снижается, кальция повышается или не меняется. Выраженность гипокальциурического эффекта тиазидных диуретиков зависит от количества потребляемой поваренной соли и объема внеклеточной жидкости: при ограничении поступления натрия и уменьшении объема внутриклеточной жидкости реабсорбция кальция в проксимальных канальцах повышается и выделение уменьшается, а при увеличении введения натрия выделение кальция повышается. Внепочечный эффект тиазидных диуретиков, в частности, связан с прямым и опосредованным через паратгормон действием на костную ткань. Данные препараты стимулируют высвобождение и повышение активности паратгормона, что может иметь серьезное клиническое значение при наличии гиперпаратиреоидизма.
Уровень кальция в крови определяется и всасываемостью в кишечнике: тиазидные диуретики не меняют или, по данным ряда исследований, снижают всасывание, что может компенсировать задержку кальция почками. Возможно, последнее объясняет отсутствие осложнений (например, отложения кальция в тканях), обусловленное влиянием тиазидных диуретиков на выделение кальция почками [9, 10].
Таким образом, тиазидные диуретики уменьшают экскрецию кальция почки посредством следующих механизмов: 1) за счет прямого действия – повышения реабсорбции кальция в дистальных отделах нефрона; 2) опосредованно уменьшая объем внутриклеточной жидкости и повышая в проксимальных канальцах реабсорбцию не только натрия и воды, но и связанную с этим пассивную реабсорбцию кальция; 3) посредством экстраренальных механизмов: усиления секреции паратгормона, повышения всасывания из кишечника и мобилизации из костных депо.
Свойство тиазидных диуретиков влиять на обмен кальция используется при лечении больных гиперпаратиреоидизмом, гиперкальциурией и кальциевыми камнями в почках. Благоприятный эффект тиазидных диуретиков при камнях почек обусловлен и повышением выделения с мочой магния, цинка пирофосфата, а также тенденцией к снижению выделения оксалатов и цитратов [10].
Наш выбор лекарственной терапии был обусловлен результатами послеоперационного обследования.
Целью назначения тиазидных диуретиков было снижение вероятности развития рецидива МКБ после оперативного лечения путем уменьшения суточной экскреции кальция. Назначение тиазидных диуретиков оправданно не только для профилактики камнеобразования, но и для предотвращения снижения МПКТ. Применение тиазидных диуретиков снижает вероятность перелома шейки бедра у мужчин и у женщин в постменопаузальном и предклимактерическом периодах. Тиазидные диуретики не только обладают эффектом уменьшения кальциурии, но и стимулируют остеобласты, ингибируют экспрессию остеокальцина и создают условия для формирования кости и ее минерализации [8].
Аллопуринол представляет собой ингибитор ксантиноксидазы, который назначают при наличии связи образования камней, состоящих из оксалата кальция, с гиперурикозурией [11]. Эффекты аллопуринола реализуются за счет уменьшения вероятности кристаллизации мочевой кислоты и уратов, способствующих выпадению в осадок оксалата кальция, образованию комплекса между коллоидным уратом и макромолекулярными ингибиторами, а также за счет снижения экскреции оксалатов [2].
Цель исследования: уточнить влияние остеопороза и факторов его возникновения на экскрецию кальция, мочевой кислоты и рецидив камнеобразования.
Материалы и методы. С 2016 по 2018 г. обследованы 84 пациента с МКБ, которым было проведено оперативное лечение. Их средний возраст составил 48,0±14,2 года. Пациентов мужского пола было 47 (54,7%), женского – 39 (45,3%).
Всем пациентам было выполнено оперативное лечение: чрескожная нефролитотрипсия – 42 (48,8%), дистанционная ударно-волновая литотрипсия – 22 (25,6%), контактная уретеролитотрипсия – 21 (24,4%) и лапароскопическая пиелолитотомия – 1 (1,2%).
С целью выявления факторов риска остеопороза пациенты самостоятельно заполняли специальную анкету, предложенную международным обществом по остеопорозу (рис. 1) [12, 13].

Факторы риска остеопороза выявлены у 44 (51,2%) обследованных пациентов с МКБ.
Для оценки состояния костной ткани применяли двухлучевую рентгеновскую абсорбциометрию (dual-energy X-ray absorbtiometry) (DEXA) [14] как наиболее широко используемый метод определения плотности кости. С ее помощью получают изображение костей в области сканирования и вычисляемые показатели костной плотности, выраженные в граммах на 1 см² площади исследованного участка кости. Проводят сканирование поясничного отдела позвоночника, шейки бедра, предплечья или всего тела целиком. Минеральную плотность костной ткани определяют путем измерения степени проницаемости кости для рентгеновских лучей. Чем больше гасится излучение при прохождении через кость, тем выше ее плотность. При этом используют два пучка фотонов – высокой и низкой энергии, что позволяет исключать влияние структуры мягких тканей на результаты измерения костной массы и плотности. На основании многочисленных методов оценки костной плотности показано, что распространенность переломов коррелирует с МПКТ поясничного отдела позвоночника и проксимальных отделов бедренных костей (уровень доказательности А) [14].
Индивидуальный показатель МПКТ сравнивают с референсной базой данных. Ввиду использования различных методик измерения и аппаратуры оценку МПКТ проводят на основании Т- и Z-критериев.
Определение остеопороза разработано ВОЗ для женщин европеоидной расы и основано на результатах определения МПКТ в любой точке по Т-критерию. Нормальными значениями МПКТ считают показатели Т-критерия до -1 стандартного отклонения (standart deviation – SD) от пиковой костной массы. При остеопении показатели Т-критерия составляют от -1 до -2,5 SD, при остеопорозе – -2,5 SD и ниже, при тяжелом остеопорозе – -2,5 SD с наличием в анамнезе 1 и более переломов. Мужчинам в возрасте 65 лет и старше необходимо использовать Т-критерий: диагноз остеопороза устанавливают при Т-критерии, равном -2,5 SD и ниже. В возрасте 50–65 лет для диагностики остеопороза необходимо сочетание определенного Т-критерия (-2,5 SD и ниже) и других факторов риска. Мужчинам любого возраста со вторичными причинами низкой МПКТ (лечение глюкокортикоидами, гипогонадизм, гиперпаратиреоз) диагноз ставят на основании клинических данных и подтверждают низкой МПКТ.
У 17 (48,6%) пациентов с МКБ выявлено снижение МПКТ, у 18 (51,4%) плотность костной ткани была в пределах нормальных значений.
 Рентгенофазовый анализ мочевых камней и их фрагментов показал (см. таблицу), что с наибольшей частотой удаленные камни состояли из гидроксилапатита-ведделлита (44,8%), вевеллита (17,2%) и мочевой кислоты (10,3%).
Рентгенофазовый анализ мочевых камней и их фрагментов показал (см. таблицу), что с наибольшей частотой удаленные камни состояли из гидроксилапатита-ведделлита (44,8%), вевеллита (17,2%) и мочевой кислоты (10,3%).
Через 1 мес. после выписки из стационара и при нормализации показателей общего анализа мочи, при отрицательных результатах бактериологического посева мочи определяли суточную экскрецию кальция и мочевой кислоты.
Никто из пациентов не принимал диуретических препаратов, все пациенты получали письменные инструкции относительно сбора суточной мочи. Уровень кальция определяли О-крезолфталеиновым методом. Нормой считали показатели экскреции кальция на уровне 2,5–7,5 ммоль/сут.
Показатели суточной экскреции мочевой кислоты определяли энзиматически (уриказным) методом. Референсные значения составили 1,48–4,43 ммоль/сут.
Выбор метода лечения, направленного на предотвращение рецидива камнеобразования, основан на результатах исследования состава камня, суточной экскреции кальция и мочевой кислоты. Семи (8,1%) пациентам с повышенным уровнем экскреции мочевой кислоты назначен аллопуринол в дозе 100 мг в сутки 3 раза в день, 10 (11,6%) прооперированным, имевшим повышенные показатели экскреции кальция, – тиазидные диуретики в дозе 25 мг в сутки. У 69 (80,2%) пациентов изменений суточной экскреции мочевой кислоты и кальция не выявлено, и они оставались под наблюдением.
Контрольное клиническое обследование, определение суточной экскреции кальция и мочевой кислоты выполняли через 3 мес.
Результаты обработаны с применением статистической программы MedCalc [15]. Данные представлены в виде среднего и стандартного отклонений. Сравнение данных выполнены с применением критерия Краскелла–Уоллиса, критерия χ2 и регрессионного анализа, а уровень значимости p был принят равным 0,05.
Результаты. Возраст пациентов в группах статистически значимо не различался (р=0,136). У пациентов, находившихся под наблюдением, преобладали кальций-оксалатные камни (р=0,0254). Факторы риска остеопороза во всех группах пациентов выявлялись с сопоставимой частотой (р=0,2156). Частота снижения МПКТ в группах не имела значимых различий (р=0,64).
Ни в одной из групп наблюдения значимых изменений диуреза при контрольном исследовании выявлено не было (р=0,487; рис. 2).
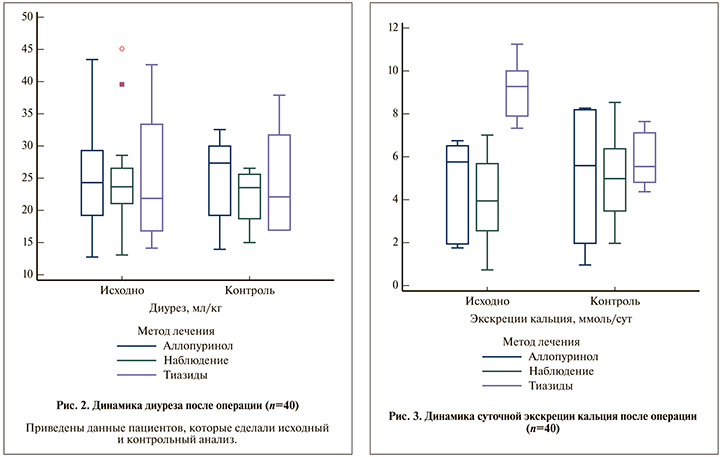
У пациентов, принимавших тиазидные диуретики, отмечено статистически значимое снижение суточной экскреции кальция (р=0,0054; рис. 3).
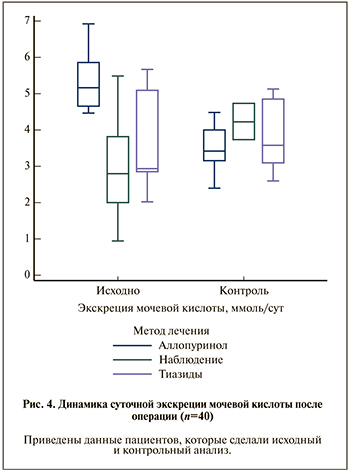 Лечение аллопуринолом сопровождалось статистически значимым снижением экскреции мочевой кислоты (р=0,021; рис. 4). Остальные показатели были без динамики.
Лечение аллопуринолом сопровождалось статистически значимым снижением экскреции мочевой кислоты (р=0,021; рис. 4). Остальные показатели были без динамики.
У пациентов, которым не проводилось лечение ввиду отсутствия объективных показаний, значимых изменений диуреза, экскреции кальция и мочевой кислоты выявлено не было.
Результаты наблюдения за пациентами с МКБ после оперативного лечения и результаты исследования МПКТ представлены на рис. 5, 6.
Рецидив МКБ на фоне лечения выявлен у 4 пациентов со снижением МПКТ.
В контрольной группе наблюдения рецидив выявлен у 5 пациентов со снижением МПКТ и у 1 – с нормальной МПКТ.
В целом рецидив камнеобразования на фоне лечения выявлен у 4 пациентов при среднем сроке наблюдения 381±61 день, в контрольной группе – у 6 пациентов при сроке наблюдения 836±64 дня.
Обсуждение. Высокая распространенность факторов риска остеопороза среди пациентов с МКБ, а также снижение МПКТ могут быть одним из условий возникновения, прогрессирования и рецидивирования камнеобразования. Показанием к назначению лечения, направленного на предотвращение рецидива МКБ, служат выявленные нарушения экскреции кальция и мочевой кислоты. Современные методы коррекции суточной экскреции кальция и мочевой кислоты позволяют контролировать эти показатели. Однако даже на фоне профилактического лечения рецидив камнеобразования выявлен у 5,8% пациентов.
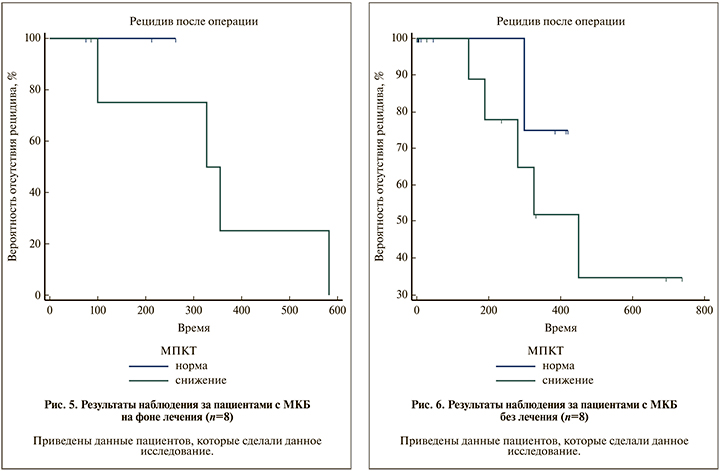
В ходе данной работы установлено, что у пациентов со снижением МПКТ повторное образование камней после оперативного лечения происходит быстрее. Это характерно как для пациентов, получающих лечение, направленное на коррекцию метаболических нарушений, так и для пациентов, у которых показаний к назначению лекарственной терапии не было. Данный факт может указывать на связь снижения МПКТ и камнеобразования за счет повышения экскреции кальция, причем воздействие этого фактора происходит неравномерно во времени и не отражается на показателях суточной экскреции кальция. Констатировать процесс снижения МПКТ можно только по результатам денситометрии.
Заключение. Лечение, направленное на предотвращение рецидива камнеобразования, основано на результатах послеоперационного обследования. Таким образом, остеопороз и его факторы создают условия для повышения экскреции кальция почками и повышают вероятность рецидива камнеобразования, уменьшения срока рецидива МКБ.
При повышении экскреции кальция были назначены тиазидные диуретики, а при повышении экскреции мочевой кислоты – аллопуринол. Эти виды лечения позволили контролировать измененные параметры. Тиазиды способствуют уменьшению экскреции кальция, аллопуринол – экскреции мочевой кислоты. Однако на частоту и скорость рецидива у больных МКБ может оказывать снижение МПКТ за счет увеличения экскреции кальция. У 51,2% обследованных пациентов были выявлены факторы риска остеопороза, у 48,6% – снижение МПКТ. При нормальной МПКТ рецидив выявлен у 1 пациента, при снижении МПКТ – у 9. Считаем, диагностика остеопороза и его факторов позволяет учитывать это на течении МКБ, эффективности метафилактики, а также на вероятности рецидива.



