В настоящее время одной из нерешенных задач в области аритмологии остается проблема адекватной коррекции диссинхронии миокарда с помощью ресинхронизирующей терапии (РТ) [1]. Выделяют электрическую и механическую диссинхронии [2]. Основная роль в формировании электрической диссинхронии отводится полной блокаде левой ножки пучка Гиса (ПБЛНПГ). Именно эта внутрижелудочковая блокада является независимым предиктором смерти у пациентов с хронической сердечной недостаточностью (ХСН) [3, 4]. У больных ПБЛНПГ может иметь различную зону поздней активации и определение ее только по электрокардиограмме (ЭКГ), снятой в 12 стандартных отведениях, невозможно [5—8]. После имплантации устройства для РТ можно подобрать оптимальный режим бивентрикулярной стимуляции (БиС) с наименьшей диссинхронией желудочков, основываясь на ширине и морфологии комплекса QRS [9, 10]. Однако по 12-канальной ЭКГ невозможно оценить характер активации миокарда желудочков сердца при БиС. Другим способом, активно применяемым на практике для оценки диссинхронии, является метод тканевой допплер-эхокардиографии (ТД-ЭхоКГ). Полученные при помощи данной методики показатели наглядно отражают механическую диссинхронию сердца до и после операции [11, 12]. Однако, как известно, метод РТ основан на электрическом влиянии стимуляции на сердце. В связи с этим физиологические параметры электрической диссинхронии важно знать в первую очередь.
Одним из современных направлений в оценке электрической диссинхронии до и после имплантации устройства для РТ является методика неинвазивного электрофизиологического картирования (НЭФК) [7, 13, 14]. В России методика реализована и постоянно совершенствуется в виде электрофизиологической системы Amycard 01C EP LAB. Отличительной особенностью данной системы является неинвазивный характер. В сравнении с наиболее известным зарубежным аналогом — системой ECVUE, система Amycard 01C EP LAB позволяет проводить оценку электрофизиологических параметров не только с эпикардиальной поверхности, но и на эндокарде [8, 14, 15].
Целью данной работы являлось изучение возможностей НЭФК при БиС и сопоставление полученных результатов с данными 12-канальной ЭКГ и ТД-ЭхоКГ.
Материал и методы
 Обследованы 25 пациентов с ПБЛНПГ, которым были имплантированы системы РТ. Правопредсердный электрод позиционировался в ушко правого предсердия, правожелудочковый электрод — в верхушку правого желудочка (ПЖ). Левожелудочковый электрод имплантировался в одну из ветвей коронарного синуса. У всех больных доля БиС составляла 95% и более по данным статистики устройств для РТ.
Обследованы 25 пациентов с ПБЛНПГ, которым были имплантированы системы РТ. Правопредсердный электрод позиционировался в ушко правого предсердия, правожелудочковый электрод — в верхушку правого желудочка (ПЖ). Левожелудочковый электрод имплантировался в одну из ветвей коронарного синуса. У всех больных доля БиС составляла 95% и более по данным статистики устройств для РТ.
Пациенты, включенные в исследование, различались по степени ответа на РТ. У 22 больных наблюдался ответ на РТ, у 3 отчетливого эффекта не отмечалось. Критериями ответа считали снижение функционального класса (ФК) ХСН не менее чем на 1, уменьшение конечного систолического объема (КСО) левого желудочка (ЛЖ) на 15% и более [16]. Исследование проводили в сроки от 6 до 30 мес после имплантации устройства для РТ. В период обследования пациенты были компенсированы и получали оптимальную медикаментозную терапию ХСН. Клинико-диагностические исходные данные представлены в табл. 1.
Всем пациентам выполнено НЭФК с использованием системы Amycard 01C EP LAB. На первом этапе проводили регистрацию ЭКГ в 240 униполярных и 12 стандартных отведениях. Исходно записывали собственный ритм c ПБЛНПГ при временном ингибировании стимуляции. После этого осуществляли запись БиС по схеме последовательного опережения правого, а затем ЛЖ (40, 30, 20, 15, 10, 5 и 0 мс). Задержки 5 и 15 мс были записаны у 11 из 25 больных, так как не все модели устройств для РТ позволяли это сделать. Время записи каждого режима стимуляции составляло 30 с. Исходный режим БиС был ПЖ—ЛЖ 0 мс у 24 пациентов, у одного — ЛЖ—ПЖ 5 мс.
На втором этапе проводили мультиспиральную компьютерную томографию — МСКТ с внутривенным контрастированием (ультравист-370). Сканирование проводилось в две серии: торса и сердца с ЭКГ-синхронизацией (на установленном исходно режиме БиС). Для торса толщина срезов составляла 3 мм, для сердца — 0,75 мм. Объем вводимого контрастного вещества определяли из расчета 1 мл на 1 кг массы тела, но не более 100 мл. Средняя экспозиционная доза DLP составила 689 (472; 992) мГр·см. Полученные ЭКГ и данные МСКТ импортировали в программное обеспечение системы Amycard 01C EP LAB.
На третьем этапе осуществляли объемную реконструкцию данных МСКТ, построение эпи/эндокардиальных моделей желудочков сердца и разделение ЛЖ маркерами на условные сегменты [8]. Стимулирующие полюса ПЖ и ЛЖ электродов обозначались специальными маркерами. Для оценки электрофизиологических параметров методом НЭФК использовались реконструированные на основе биполярных электрограмм (метод ADM) активационные статические и динамические (врежиме движения фронта возбуждения) изохронные карты [17]. Качественную и количественную оценку внутрижелудочковой диссинхронии (ВЖД) в виде расчета времени стандартного отклонения активации для 12 сегментов (SD12) ЛЖ осуществляли по статическим изохронным картам ADM (рис. 1, см. цв. вклейку). Область поздней электрической активации на данных картах окрашивалась холодными цветами (голубой, синий, фиолетовый), а область наиболее ранней активации — красным цветом. Измеренный с использованием методики НЭФК показатель SD12 сравнивали c помощью корреляционного анализа с шириной QRS комплекса при различных режимах БиС.
 Для оценки межжелудочковой диссинхронии (МЖД) методом НЭФК использовали активационные карты ADM в режиме движения фронта возбуждения. МЖД оценивали как разницу во времени между началом активации ПЖ и началом активации ЛЖ на эндокардиальной модели желудочков.
Для оценки межжелудочковой диссинхронии (МЖД) методом НЭФК использовали активационные карты ADM в режиме движения фронта возбуждения. МЖД оценивали как разницу во времени между началом активации ПЖ и началом активации ЛЖ на эндокардиальной модели желудочков.
МЖД методом ТД-ЭхоКГ оценивали по разнице во времени между началом систолических потоков в аорту и легочный ствол, измеряемых методом импульсно-волновой допплерографии.
ВЖД (по показателю SD12) методом ТД-ЭхоКГ оценивали на основании пиковых значений систолических скоростей 12 сегментов ЛЖ.
Затем методики НЭФК и ТД-ЭхоКГ сравнивали по двум показателям (SD12, МЖД) при ПБЛНПГ и при установленном режиме БиС.
Все расчеты проводили на основании одного типичного комплекса QRS каждого пациента. Ширину стимулированного комплекса QRS определяли как интервал от начала спайка желудочкового стимула с формированием желудочкового ответа и до перехода в изолинию в том стандартном отведении, где это было зафиксировано позже всего.
Кроме того, пациентам была выполнена стандартная эхокардиография для оценки размеров, объемов ЛЖ, фракции выброса (ФВ) ЛЖ. Все измерения, включая методику ТД-ЭхоКГ, проводили на аппарате Vivid 7 с датчиком 2,5 МГц.
Статистическую обработку данных осуществляли при помощи пакета статистических программ Statistica v.10. Для непрерывных переменных были рассчитаны медиана и квартили (LQ; UQ). Описание взаимосвязи между количественными показателями проводили с помощью коэффициента корреляции Спирмена. Качественные переменные представлены в виде абсолютного числа наблюдений. Согласно принципу Бонферрони при множественных сравнениях статистически значимыми принимали р<0,01.
Исследование было одобрено Этическим комитетом при ФГБУ «СЗФМИЦ им. В.А. Алмазова» МЗ РФ и выполнено в соответствии с принципами Хельсинкской декларации.
Результаты
При БиС в разных режимах, по данным статических изохронных карт ADM, на эндокардиальных моделях желудочков в режиме прозрачного эпикарда качественно и количественно была оценена ВЖД ЛЖ. Качественный визуальный анализ данных карт показал, что характер распределения и площадь зон, закрашиваемых оттенками желтого и зеленого цветов на миокарде ЛЖ, отражают степень равномерности его активации. Чем больше площадь этих зон и чем более равномерно они располагаются на поверхности миокарда ЛЖ, тем однороднее происходит его активация (охват возбуждением), что может соответствовать оптимальному режиму БиС. При наличии широких зон, закрашиваемых оттенками красного, голубого и синего цветов, охват возбуждения ЛЖ происходит неравномерно, что, вероятно, соответствует неоптимальному режиму БиС (рис. 2А, Б, см. цв. вклейку).
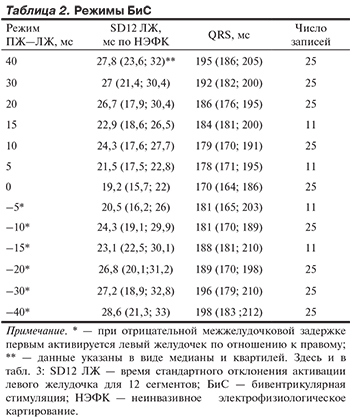
Для количественной оценки ВЖД у пациентов рассчитано SD12 ЛЖ по данным НЭФК и измерена ширина комплекса QRS на различных режимах БиС, указанных в табл. 2.
У 24 пациентов минимальные значения SD12 и QRS зарегистрированы на режиме ПЖ—ЛЖ 0 мс, у одного — на задержке ЛЖ—ПЖ 5 мс. Меньшему измеренному значению QRS у всех больных соответствовало меньшее расчетное значение времени SD12, измеренного методом НЭФК. Это подтверждается статистически значимой положительной связью показателя SD12 и ширины бивентрикулярного QRS (r=0,88; p<0,0001).
У 22 пациентов (с эффектом от РТ) на запрограммированном режиме БиС не отмечалось ВЖД на заднебоковой стенке ЛЖ по данным изохронных карт НЭФК (рис. 3, см. цв. вклейку).
У 3 пациентов (без отчетливого эффекта от РТ) отмечалась ВЖД при БиС на боковой стенке ЛЖ по данным изохронных карт НЭФК (рис. 4, см. цв. вклейку). При этом стимулирующий полюс ЛЖ электрода визуализировался не оптимально по отношению к поздней зоне при ПБЛНПГ (см. рис. 4 на цв. вклейке).
Для более полного понимания оценки диссинхронии нами был проведен сравнительный анализ метода НЭФК с методом ТД-ЭхоКГ у пациентов с ответом на РТ (табл. 3). Кроме того, у них были сопоставлены дооперационные и послеоперационные значения МЖД и ВЖД (SD12). У 3 больных (без отчетливого эффекта от РТ) подобные сравнения не проводились в связи с малой выборкой.

При сравнительном анализе методик НЭФК и ТД-ЭхоКГ по показателю МЖД при ПБЛНПГ выявлена статистически значимая положительная связь (r=0,58; p=0,005), при БиС — обнаружена положительная слабо значимая связь (r=0,46; p=0,03). При сравнительном анализе по показателю SD12 при ПБЛНПГ и БиС констатирована положительная, но слабо статистически значимая связь (r=0,43; p=0,04 и r=0,44; p=0,04 соответственно; см. табл. 3).
В результате анализа динамики показателей МЖД, измеренных методом НЭФК, выявлено, что значения при установленном режиме БиС по сравнению со значениями при ПБЛНПГ были статистически значимо меньше — 37 (28; 49) мс и 81 (60; 90) мс соответственно (p<0,001). Показатель SD12 при БиС по сравнению с ПБЛНПГ методом НЭФК также статистически значимо был меньше — 17,7 (15,5; 21,9) мс и 22,8 (20,6; 32) мс соответственно (p=0,001; см. табл. 3).
При анализе динамики показателя МЖД, измеренного методом ТД-ЭхоКГ, значения на фоне БиС по сравнению с ПБЛНПГ были статистически значимо меньше — 34 (24; 51) мс и 60 (54; 73) мс соответственно (p<0,001). Показатель SD12 при БиС по сравнению с ПБЛНПГ методом ТД-ЭхоКГ также был статистически значимо меньше — 21 (17; 34,4) мс и 38,7 (24,9; 45) мс соответственно (p=0,001; см. табл. 3). Таким образом, методики НЭФК и ТД-ЭхоКГ являются сопоставимыми при анализе электрофизиологических данных у пациентов с СРТ.
Обсуждение
Визуальная оценка изохронных карт ADM по цветовому кодированию позволила качественно оценить равномерность охвата возбуждением эндокарда желудочков сердца и синхронность их активации при БиС. Наиболее гомогенный цвет активации желудочков соответствует оптимальному режиму БиС. Данный факт описывался ранее в литературе, но только для эпикардиальных моделей желудочков [7].
В ряде научных работ показано, что узкий бивентрикулярный комплекс QRS ассоциируется с большим процентом пациентов, ответивших на РТ [18, 19]. Кроме того, известно о существовании прямой взаимосвязи электрического и механического ремоделирования миокарда, что свидетельствует о возможности оптимизации режима БиС по 12-канальной ЭКГ на основе ширины и морфологии комплекса QRS [20]. В нашем исследовании количественный параметр ВЖД (SD12 ЛЖ) при БиС, рассчитанный по методике НЭФК, и ширина комплекса QRS имели статистически значимую положительную связь у всех обследованных (r=0,88; p<0,0001). Это свидетельствует о том, что наиболее узкий бивентрикулярный комплекс QRS сопровождался самым малым значением SD. Однако, несмотря на минимальные значения как QRS, так и SD, не у всех больных отмечался эффект от РТ. У 3 пациентов сохранилась ВЖД по данным изохронных карт НЭФК. Причиной отсутствия эффекта у этих лиц, вероятно, является неоптимальная позиция левожелудочкового электрода, которая не совпадала с зоной поздней активации при ПБЛНПГ по данным изохронным картам НЭФК.
Полученные с помощью методик НЭФК и ТД-ЭхоКГ показатели ВЖД (SD12 ЛЖ) и МЖД у пациентов с ответом на РТ продемонстрировали статистически значимую положительную динамику при БиС в сравнении с исходными данными при ПБЛНПГ. Это подтверждает эффективность использования в клинической практике ресинхронизирующих устройств. Сравнительный анализ показал статистически значимую положительную связь описанных методов по показателю МЖД при ПБЛНПГ (r=0,58; p=0,005). Три остальных изученных связи (МЖД при БиС, SD при ПБЛНПГ, SD при БиС) оказались также положительными, одного порядка, но слабо значимыми (0,05>p>0,01). Полученный результат позволяет утверждать, что методики сопоставимы; однако для более детального анализа их соответствия требуются дальнейшие исследования с большей выборкой пациентов.
Ограничения данного исследования
Общая группа, включенная в работу, была небольшой и составляла 25 пациентов. Больные с правожелудочковым электродом в межжелудочковой перегородке не включались в исследование в связи с недостаточной точностью НЭФК в данной анатомической области [8]. Все расчеты выполнялись для одного типичного комплекса QRS на фоне исходного ритма с ПБЛНПГ и на различных режимах БиС, т.е. не учитывалось влияние дыхания, что могло повлиять на точность картирования. Сравнение методик НЭФК и ТД-ЭхоКГ проводилось только при установленном изначально режиме БиС в связи с высокой трудоемкостью.
Выводы
Качественная оценка изохронных карт неинвазивного электрофизиологического картирования наглядно демонстрирует внутрижелудочковую диссинхронию, что может помочь в выборе оптимального режима бивентрикулярной электрокардиостимуляции. Меньшая величина SD12 при самом узком бивентрикулярном комплексе QRS не у всех пациентов сопровождается эффектом от ресинхронизирующей терапии, что, вероятно, связано с позицией левожелудочкового электрода. Методики неинвазивного электрофизиологического картирования и тканевой допплер-эхокардиографии имеют статистически значимую положительную связь по показателю межжелудочковой диссинхронии при полной блокаде левой ножки пучка Гиса.



