Введение. Исследования последних лет показали, что при развитии обструктивной уропатии (ОУ) большое значение отводится оценке уровня цитокинов в сыворотке крови больных [1]. Возникновение ОУ приводит к структурно-функциональным изменениям паренхимы, касающимся преимущественно тубулоинтерстиция почки и возникающим в результате воспалительного процесса на фоне нарушения пассажа мочи [2]. Даже в отсутствие выраженной клинической картины и воспалительных изменений в общем анализе крови и мочи в пораженной почке происходит каскад цитокиновых изменений, сопровождающийся повреждением канальцевого аппарата почки и способный привести к снижению почечной функции в последующем [3]. Установлено, что у 86% больных мочекаменной болезнью (МКБ) при наличии даже частичной обструкции верхних мочевыводящих путей наблюдаются атаки острого калькулезного пиелонефрита, приводящие к развитию жизнеугрожающих cептических осложнений, что определяет необходимость продолжительной декомпрессии полостной системы почки с целью купирования воспалительных изменений и обеспечения условий для выполнения одного из вариантов литотрипсии [4]. Оценка динамики содержания биомаркеров, количественное определение которых позволит мониторировать выраженность структурно-функциональных нарушений, представляет значительный интерес. Выбранные нами маркеры – интерлейкин 8 (IL-8), фактор роста эндотелия сосудов (VEGF), моноцитарный хемоаттрактантный пептид 1 (MCP-1), гранулоцитарный колонистимулирующий фактор (G-CSF) и гранулоцитарно-макрофагальный колонистимулирующий фактор роста (GM-CSF) – патогенетически в достаточной мере характеризуют изменения, происходящие в почке во время обструкции и в ближайшие сроки после ее разрешения.
Повреждение почечной паренхимы при ОУ инициирует каскад молекулярных взаимодействий с последующими морфологическими изменениями. Это дает основание продолжать поиски защитных агентов, предотвращающих или хотя бы ограничивающих масштабы повреждений.
В современной литературе достаточно большое внимание уделяется поиску маркеров, характеризующих степень восстановления почечной функции.
Цель исследования: оценить нефропротекторное действие лерканидипина, влияние его на динамику клиренса креатинина и уровня цитокинов в крови больных нефролитиазом с обструктивной уропатией в процессе дренирования почки.
Материалы и методы. В исследование вошли 66 пациентов с МКБ, проходивших лечение в отделении урологии клинической больницы им. С. Р. Миротворцева ФГБОУ ВО «Саратовский ГМУ им. В. И. Разумовского» Минздрава России в 2015–2018 гг. Перед включением в исследование все пациенты подписали информированное согласие. Согласие этического комитета на проводимое исследование получено. В комплекс обследования пациентов входили изучение жалоб и сбор анамнеза, физикальное обследование, общий и биохимический анализы крови, общий анализ мочи, обзорная рентгенография почек и мочевых путей, экскреторная урография, УЗИ, мультиспиральная компьютерная томография с реконструкцией изображения, нефросцинтиграфия.
В зависимости от проводимого лечения пациенты были разделены на 2 группы по 33 человека. В 1-ю группу были включены пациенты с конкрементами лоханочно-мочеточникового сегмента, размеры которых составили от 1 до 2 см.
Средний возраст обследуемых лиц составил 45,8±4,6 года (от 25 до 60 лет). Пациенты имели признаки обструкции верхних мочевыводящих путей по данным инструментальных методов обследования: размеры чашечек почек варьировались от 8 до 10 мм, лоханки – от 1,8 до 3,5 см. Имело место замедление выделительной функции почки на стороне поражения по данным экскреторной урографии до 40–60 мин, а также снижение скорости клубочковой фильтрации (СКФ) от 30 до 60 мл/мин по формуле CKD-EPI. В общеклинических анализах на момент госпитализации сохранялись умеренный лейкоцитоз и лейкоцитурия. По данным нефросцинтиграфии имело место снижение раздельной СКФ на стороне поражения на 40–70%. На момент включения в исследование приступ почечной колики был купирован. Длительность обструкции (время с момента первичного приступа почечной колики) составила 1,5–4 нед. С целью предотвращения развития тяжелых инфекционных осложнений и восстановления функции почки первым этапом перед выполнением литотрипсии пациентам с МКБ и обструктивным синдромом осуществляли дренирование почки путем чрескожно-пункционной нефростомии в условиях операционной по принятой методике. Выбор метода дренирования был обусловлен выраженностью ретенции и планируемым способом литотрипсии. Всем больным проводилась стандартная антибактериальная и противовоспалительная терапия. Согласно рекомендациям Российского общества урологов (2017), оперативное лечение по удалению конкремента проводилось не ранее, чем через 2 недели, после нормализации показателей крови и мочи. Во 2-ю группу вошли пациенты с аналогичной клинической картиной, сопоставимые по возрасту, полу и результатам обследования. С целью нефропротекции данная группа пациентов в дополнение к стандартной антибактериальной и противовоспалительной терапии получала лерканидипин в дозе 10 мг 1 раз в сутки в течение 1 мес. В последующем пациентам обеих групп выполнялась ПНЛТ. Осложнений в послеоперационном периоде отмечено не было.
Группу сравнения составили 30 пациентов с чашечными конкрементами размером от 1 до 1,5 см, не вызывающими обструкцию. Пациенты данной группы были сопоставимыми по возрасту и полу с больными 1-й и 2-й групп.
Всем пациентам осуществляли забор крови и мочи для анализа до установки нефростомического дренажа, а также на 7-е, 14, 21 и 28-е сутки после разрешения обструкции.
В сыворотке крови определяли уровень креатинина с последующим расчетом СКФ для оценки функциональной способности почек по уравнению CKD-EPI для представителей европейской расы, а также концентрации интерлейкина 8 (IL-8), фактора роста эндотелия сосудов (VEGF), моноцитарного хемоаттрактантного пептида 1 (MCP-1), гранулоцитарного колонистимулирующего фактора (G-CSF) и гранулоцитарно-макрофагального колонистимулирующего фактора роста (GM-CSF) методом твердофазного иммуноферментного анализа, с использованием соответствующих наборов реагентов АО «Вектор-Бест» (Новосибирск).
Статистическую обработку полученных результатов проводили с помощью программ Statistika 10.0, SPSS 13.0. Распределение значений в выборках отличалось от нормального, в связи с чем в процессе статистической обработки применяли методы непараметрической статистики, которые включали вычисление медианы, квартили вариационного ряда максимальных и минимальных значений. Для определения статистической значимости различий между двумя независимыми группами использовали непараметрический критерий (U) Манна–Уитни. Во всех процедурах статистического анализа был принят уровень значимости р<0,05. Корреляционный анализ выполнялся с использованием непараметрического метода Спирмена.
Результаты. В сыворотке крови пациентов 1-й и 2-й групп выявлено статистически значимое повышение концентрации медиаторов VEGF в 6 раз, MCP-1 в 1,2, IL-8 в 1,6, GM-CSF в 4 и G-CSF в 1,03 раза по сравнению со значениями группы сравнения (табл. 1).

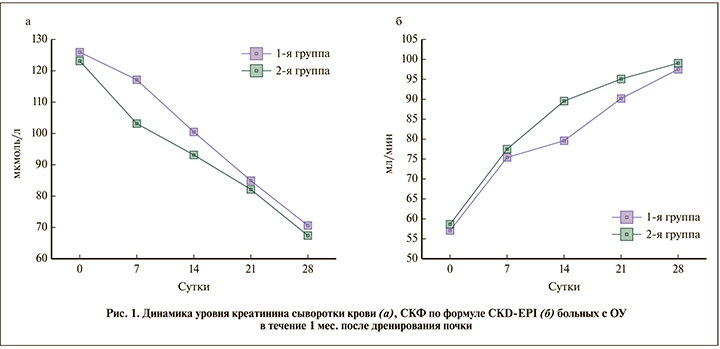
В процессе дренирования почки наблюдалось постепенное снижение уровня сывороточного креатинина и повышение скорости клубочковой фильтрации, причем во второй группе отмечено более быстрое восстановление почечной функции (рис. 1).
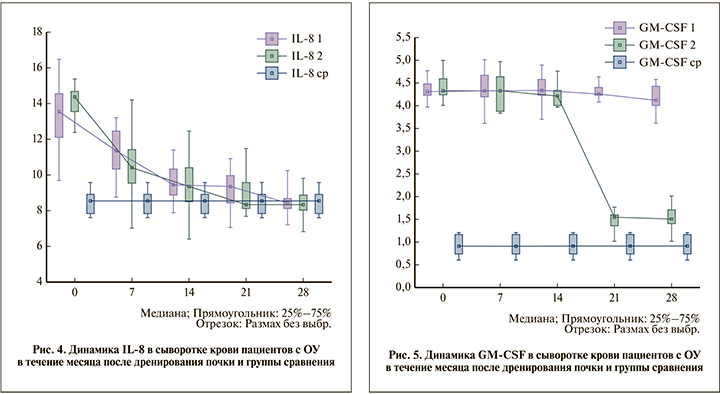
В процессе разрешения обструкции наблюдалось статистически значимое снижение уровней VEGF, MCP-1, IL-8, GM-CSF в сыворотке крови. Динамика маркеров представлена на рис. 2–5.
При оценке динамики изучаемых маркеров отмечено, что значения группы сравнения у пациентов 1-й группы достигались к 28-м суткам, при назначении лерканидипина – уже к 21-м суткам. В отношении G-CSF достоверной динамики выявлено не было.
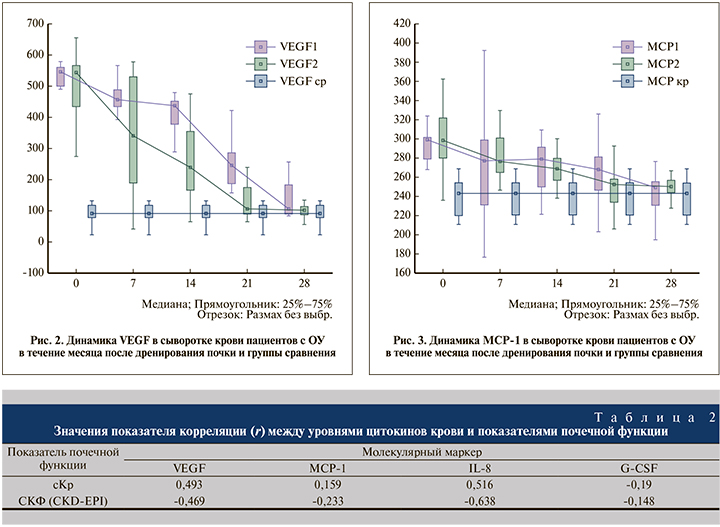
Корреляционные связи между уровнями изучаемых маркеров, содержанием сывороточного креатинина и СКФ представлены в табл. 2.
Корреляция средней силы уровней маркеров с уровнем сывороточного креатинина и СКФ, установленная для VEGF и IL-8, определяет их значимость в оценке функционального состояние почки.
Обсуждение. В практике уролога часто встречаются больные с обструкцией лоханочно-мочеточникового сегмента или мочеточника конкрементом, для которых необходимо решить вопрос о возможности удаления конкремента или необходимости восстановления оттока мочи. Обострение калькулезного пиелонефрита и развитие почечной недостаточности служат показанием к предварительному дренированию почки [5]. Однако сроки данного отведения мочи четко не обозначены. Особую сложность представляют ситуации, при которых клинически отсутствуют признаки острого воспалительного процесса в мочевыводящих путях и имеется невыраженное снижение почечной функции.
В проведенных нами ранее исследованиях показано, что даже при такой клинической картине имеет место выраженный цитокиновый выброс в сыворотке крови, что свидетельствует о необходимости установки данной категории пациентов нефростомического дренажа [6, 7].
Немаловажная роль в лечении таких пациентов отводится и более быстрому восстановлению почечной функции. Основу нефропротективной терапии составляют ингибиторы АПФ (иАПФ) и блокаторы АТ-I-рецепторов (БРА) [8]. Однако в последние годы появляется все больше публикаций о нефропротективном эффекте новой генерации блокаторов кальциевых каналов. Препарат лерканидипин приводит к снижению внутриклубочкового давления с устойчивой вазодилатацией не только афферентных (как у «классических» антагонистов кальция), но и эфферентных (как у иАПФ и БРА) артериол клубочков почек [9].
Нарушение уродинамики и локальное воспаление интерстиция сопровождается повышенной продукцией провоспалительных цитокинов крови. Так, МСР-1 обладает хемотаксической активностью, способствующей привлечению в зону почечного повреждения моноциты, макрофаги и дендритные клетки, что в дальнейшем приводит к. развитию тубулоинтерстициального фиброза – мощного фактора риска терминальной почечной недостаточности [10, 11]. Повышение внутриуретерального и внутрилоханочного давления приводит к активации клеток канальцев и эндотелия сосудов, способствует продукции ими медиаторов воспаления и ангиогенеза – VEGF, IL-8, G-CSF и GM-CSF [12–14].
Представляет интерес назначение нефропротектора, способного приводить к более быстрому снижению концентрации изучаемых маркеров в сыворотке крови, коррелирующих со скоростью восстановления почечной функции.
Заключение. У пациентов с МКБ и обструктивным синдромом выявлена корреляция ряда цитокинов со снижением уровня сывороточного креатинина и увеличением расчетной СКФ. Восстановление функции почки после дренирования на фоне лечения лерканидипином происходит быстрее, на что указывает достоверно более быстрое снижение уровня маркеров воспаления и ангиогенеза, нефрофиброза и колониестимулирующих факторов в сыворотке крови. По результатам выполненного исследования блокатор кальциевых каналов лерканидипин может быть рекомендован данной категории больных в качестве нефропротектора. При включении лерканидипина в комплексное лечение в дозе 10 мг в сутки возможно обоснованно сократить сроки до проведения одного из видов литотрипсии, что позволит сократить сроки лечения пациентов и оптимизировать работу урологического стационара.



