Введение. Нарушение мужской репродуктивной функции вследствие воздействия физических и химических факторов, генетических нарушений, перенесенных ранее заболеваний часто сопровождается изменениями структуры сперматозоидов и/или их количества, а также протеома и метаболома семенной плазмы [1–4]. Частым фактором, отрицательно влияющим на свойства эякулята, является воспаление в органах репродуктивной системы у мужчин [5].
Важную роль в формировании воспалительного иммунного ответа играют цитокины [6]. Провоспалительные цитокины (интерферон-γ, интерлейкины-1, -2, -6, -8) отвечают за формирование воспалительного ответа, индукцию лихорадки, активацию мононуклеарных фагоцитов, стимуляцию синтеза белков острой фазы – это обеспечивает уничтожение и элиминацию патогена. Противовоспалительные цитокины (интерлейкины-4, -10) регулируют активность воспалительного процесса.
К провоспалительным цитокинам относится также фактор некроза опухоли-α (ФНО-α, англ. TNFα) [6–8], который вырабатывается различными клетками – активированными макрофагами, В-лимфоцитами, Т-лимфоцитами, NK-клетками, полиморфно-ядерными лейкоцитами, тучными клетками, базофилами, фибробластами, клетками эндотелия сосудов и др. ФНО-α экспрессируется как трансмембранный белок с молекулярной массой 26 кДа, включающий остатки 233 аминокислот. Под действием специфического TNF-конвертирующего фермента ADAM17 (A Disintegrin And Metalloprotease 17, CD156b) фрагмент, связанный с мембраной, отщепляется и формируется растворимый ФНО-α (17 кДа, 157 аминокислотных остатков) [6–10].
Физиологическая функция ФНО-α разнообразна и включает регуляцию пролиферации, дифференцировки, апоптоза, формирования структуры органов и тканей, участие в ремиелинизации нейронов, ремоделировании миокарда, регенерации хрящевой ткани, десенсибилизации макрофагов, подавлении онкогенеза [7–13]. ФНО-α определяется как в сыворотке крови, так и в других биологических жидкостях организма – в моче, слюне [14], ликворе [15], синовиальной жидкости [16]. Установлено присутствие данного белка в органах мужской репродуктивной системы – яичках и их придатках [17], а также в содержимом кист придатка яичка [18].
В доступной литературе обнаружено небольшое количество публикаций, посвященных изучению ФНО-α в сперме [5,19–21, 24–26]. В связи с этим представляется актуальным сравнительный анализ концентрации данного протеина в крови и в эякуляте, изучение возможных изменений его концентрации в сперме у больных с нарушением фертильности.
Цель исследования: определить содержание ФНО-α в сыворотке крови и в семенной плазме здоровых мужчин и у пациентов со сниженной фертильностью.
Материалы и методы. В исследование включены 70 мужчин репродуктивного возраста (средний возраст – 38,38±9,86 года), проходивших обследование с целью уточнения причины бесплодного брака. У всех обследованных отсутствовали изменения в общем и биохимическом анализах крови, общем анализе мочи. Исследование выполнено с соблюдением этических принципов проведения медицинских исследований с участием людей в качестве субъектов, изложенных в Хельсинкской декларации ВОЗ.
В работе использовали остаточные образцы биологических материалов (сыворотки крови и спермы) мужчин, проходивших обследование с целью оценки фертильности. Образцы эякулята собирали после 2–4 дней полового воздержания и оценивали в соответствии с рекомендациями ВОЗ [22]. Кровь брали методом венепункции кубитальной вены перед сбором эякулята. После выполнения всех назначений остатки проб обезличивали. Сыворотку крови и семенную плазму отделяли путем центрифугирования при 2000 g в течение 20 мин на центрифуге СМ-6М (ELMI, Латвия). Аликвоты супернатантов биологического материала в пробирках типа Эппендорф хранили до исследования при температуре -40°С. Для подсчета концентрации и общего количества сперматозоидов, а также оценки их подвижности использовали анализатор спермы SQA-V (MES, Израиль) [23].
Концентрацию ФНО-α определяли методом твердофазного иммуноферментного анализа (ИФА) с использованием тест-системы «альфа-ФНО-ИФА-БЕСТ» (A-8756) («Вектор-Бест», Россия). Оптическую плотность проб регистрировали на вертикальном фотометре StatFax 3200 (Awareness Technology, США).
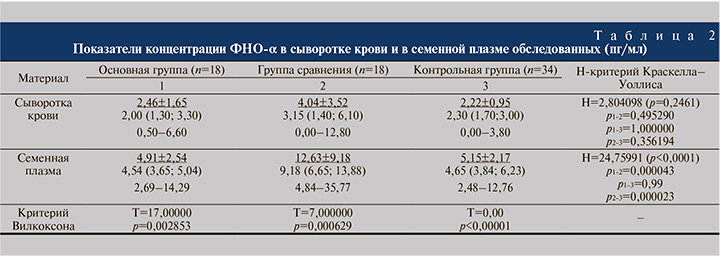
В зависимости от результатов лабораторного анализа спермы обследованные были разделены на три группы. Основную группу составили 18 пациентов с отсутствием сперматозоидов в эякуляте (азооспермия). Группа сравнения включила 18 пациентов с олигоастенозооспермией, критерием включения являлась концентрация сперматозоидов ниже 15 млн/мл или общее содержание сперматозоидов в эякуляте ниже 40 млн. Контрольная группа была представлена образцами спермы 34 здоровых мужчин, характеризовавшимися нормальными параметрами спермы и сыворотки крови [22]. Группы были сопоставимыми по возрасту. Характеристика групп обследованных и проб эякулята представлена в табл. 1.

Статистическую обработку полученных результатов проводили с помощью пакета программ STATISTICA v.7 (StatSoft Inc., США). Для каждого массива данных рассчитывали параметры описательной статистики: среднюю арифметическую (М), стандартное отклонение (SD), медиану (Me) и нижний и верхний квартили (Q1; Q3), а также минимальное (min) и максимальное (max) значения. Полученные результаты оценивали с использованием критерия Шапиро–Уилка. Эти данные позволили отвергнуть нулевую гипотезу о нормальном характере распределения данных и послужили основанием для использования непараметрических критериев при выполнении дальнейшего статистического анализа.
Для сравнения двух зависимых выборок использовали Т-критерий Вилкоксона, для сравнения нескольких независимых выборок – H-критерий Краскела–Уоллиса. Количественную оценку линейной связи между двумя случайными величинами определяли с использованием коэффициента ранговой корреляции (R) Спирмена. За максимально приемлемую вероятность ошибки первого рода (р) принимали величину уровня статистической значимости, равную или меньшую 0,05.
Результаты исследования. Фактор некроза опухоли-α был обнаружен во всех исследованных пробах эякулята (табл. 2), что совпадает с данными других исследователей [5, 19–21, 24–26]. Средняя концентрация ФНО-α в семенной плазме составила 7,01±5,98 пг/мл, медиана и интерквартильный диапазон – 4,93 (4,08; 7,11) пг/мл (рис. 1). Отмечен значительный разброс данных (коэффициент вариации [CV] – 85,31%); минимальное и максимальное значения составили 2,48 и 35,77 пг/мл и различались в 14,42 раза.
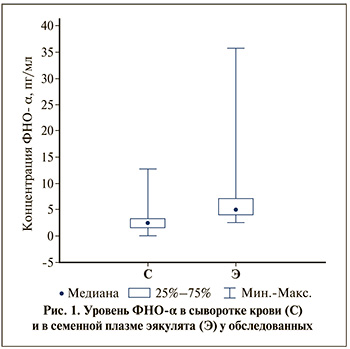
Фактор некроза опухоли-α был также выявлен во всех образцах сыворотки крови: его содержание составило 2,75±2,18 пг/мл, медиана и интерквартильный размах – 2,35 (1,50; 3,30) пг/мл. Как и в семенной плазме, наблюдался большой разброс концентрации аналита (CV=126,15%) – от неопределяемого значения до 12,80 пг/мл (см. рис. 1). Среднее значение концентрации ФНО-α в сыворотке крови было статистически значимо ниже аналогичного показателя в семенной плазме в 2,55 раза, медиана – в 1,79 раза (критерий Вилкоксона Т=117,00; р<0,00001). Выявленная закономерность имела место во всех исследованных группах (табл. 2).
При сравнении значений ФНО-α в семенной плазме у пациентов с азооспермией, олигозооспермией и у здоровых лиц были установлены статистически значимые различия (р<0,0001) (см. табл. 2). При попарном сравнении выявлена статистически значимая разница между группой сравнения и контрольной группой, а также между основной группой и группой сравнения (см. табл. 2). При попарном сравнении концентрации ФНО-α в семенной плазме обследованных основной и контрольной групп статистически значимых различий не обнаружено. Сравнение результатов исследования ФНО-α в сыворотке крови и попарное сравнение уровня аналита в сыворотке крови в разных исследуемых группах статически значимой разницы не выявило) (см. табл. 2).
Анализ корреляционных взаимосвязей между концентрацией ФНО-α в сыворотке крови и в семенной плазме также не выявил достоверных различий. Коэффициент корреляции Спирмена для суммарных массивов данных во всех группах (R) составил 0,295374; в основной группе (R1) – 0,007235; в группе сравнения (R2) – 0,222739; в контрольной группе (R3) – 0,393601.
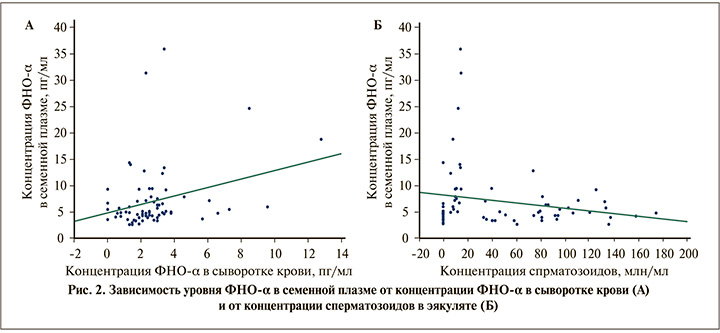
Зависимость уровня ФНО-α в семенной плазме от его концентрации в сыворотке крови описывается уравнением линейной регрессии (рис. 2 А):
концентрация ФНО-α в спермоплазме (пг/мл)=4,8054+0,802×x,
где x – концентрация ФНО-α в сыворотке крови (пг/мл).
Не выявлено статистических значимых закономерностей при анализе корреляционных взаимосвязей между концентрацией ФНО-α в семенной плазме и показателями фертильности эякулята – концентрацией и общим количеством сперматозоидов. Коэффициент корреляции между уровнем ФНО-α и количеством сперматозоидов в эякуляте составил R=-0,027945 (R2=0,345896; R3=0,130119 соответственно); между концентрацией ФНО-α и концентрацией сперматозоидов в эякуляте R=-0,042902 (R2=0,513430; R3=0,130119).
Зависимость концентрации ФНО-α в семенной плазме от концентрации сперматозоидов в эякуляте может быть выражена уравнением линейной регрессии (рис. 2 Б):
концентрация ФНО-α в спермоплазме (пг/мл)=8,1536–0,0253×x,
где х – концентрация сперматозоидов в эякуляте (млн/мл).
Обсуждение. В большинстве источников приводятся результаты определения ФНО-α в сыворотке крови [11–13]. Меньшее число публикаций отражает содержание данного белка в других биологических жидкостях: моче, слюне, ликворе [14–16]. Исследованию ФНО-α в таких биологических жидкостях, как эякулят и семенная плазма, посвящено лишь небольшое число работ [5, 19–21, 24–26]. Еще реже приводятся результаты определения исследуемого цитокина в сперме и сыворотке крови у одних и тех же мужчин [27–29]. Наше исследование также было посвящено изучению концентрации ФНО-α у одних и тех же лиц в эякуляте и сыворотке крови. Полученные нами результаты позволили подтвердить наличие ФНО-α в семенной плазме и показать, что его содержание статистически значимо выше, чем в сыворотке крови (р<0,05).
В работе E.M. Eldamnhoury и соавт. [25] была обнаружена взаимосвязь между содержанием ФНО-α, общим количеством сперматозоидов (p=0,023) и их концентрацией (p=0,001). У бесплодных мужчин со сниженной фертильностью и воспалением органов репродуктивной системы, одним из признаков которого являлась лейкоцитоспермия, отмечалось статистически значимое повышение уровня ИЛ-6 (p=0,001) и ФНО-α (p=0,003) в семенной плазме по сравнению со здоровыми лицами [25]. В нашем исследовании вероятной причиной снижения концентрации сперматозоидов у пациентов группы сравнения в числе прочего может быть воспалительный процесс в органах мужской репродуктивной системы. Полученные нами результаты, как и данные E. M. Eldamnhoury и соавт. [25], подтверждают наличие достоверных различий концентрации ФНО-α в семенной плазме между пациентами с олигоастенозооспермией и здоровыми мужчинами (p=0,000023).
Нами не выявлено статистически значимой корреляционной зависимости между содержанием ФНО-α в семенной плазме и концентрацией/количеством сперматозоидов в эякуляте. Полученные результаты совпадают с данными W. Eggert-Kruse и соавт. [20], которые также не обнаружили связи между концентрацией ФНО-α в семенной плазме и качественными показателями спермы и показателями функциональной активности сперматозоидов. Однако в других работах [19] показано влияние повышенного уровня ФНО-α на подвижность сперматозиодов, как находящихся в урогенитальном тракте мужчин, так и попадающих в организм женщин. Возможно, повышение содержания ФНО-α в семенной плазме является одним из проявлений воспалительного процесса, результатом которого может быть ухудшение показателей спермограммы.
Окончательно не решен вопрос о происхождении ФНО-α в составе эякулята. С учетом более высокого уровня данного белка в семенной плазме по сравнению с сывороткой крови более вероятно, что ФНО-α секретируется в эякулят органами репродуктивной системы мужчины. В пользу данного предположения свидетельствуют результаты исследования R. Payan-Carreira и совт. [17], в котором иммуногистохимичеcкими методами показана экспрессия ФНО-α в тканях яичка, придатка яичка и в самих сперматозоидах.
В настоящее время продолжаются исследования, направленные на изучение белкового состава семенной плазмы, выявление взаимосвязи ее компонентов с показателями фертильности сперматозоидов [3–5, 26, 27]. Если рассматривать гипотезу о том, что ФНО-α продуцируется яичками и их придатками, а также попадает в эякулят с секретами других желез, то логично предположить, что уровни этого цитокина в семенной плазме пациентов со сниженной фертильностью и здоровых мужчин могут быть различными вследствие возможного патологического процесса в железах (воспаление, нарушения в микрососудистом русле и др.). В пользу этого предположения свидетельствует статистически значимая разница концентрации ФНО-α в эякуляте больных олигоастенозооспермией и здоровых лиц (р<0,05). В то же время в нашем исследовании не выявлено статистически значимых различий между содержанием ФНО-α в эякуляте у здоровых лиц и пациентов основной группы (р=0,99), у которых отсутствовали сперматозоиды и признаки воспаления (по результатам анализа эякулята).
Полученные результаты легли в основу способа прогнозирования инфертильности эякулята у мужчин (патент на изобретение № 2785487) [30]. Предложено определение содержания ФНО-α в семенной плазме как маркера прогнозируемого снижения фертильности эякулята вследствие воспалительной реакции в органах мужской репродуктивной системы. Предложенный способ позволяет выявлять снижение фертильности эякулята на доклинических стадиях, в ранние сроки ставить таких пациентов на учет и проводить им своевременную адекватную терапию с целью профилактики бесплодия в супружеской паре.
Заключение. В настоящем исследовании установлена роль увеличения концентрации ФНО-α в сперме как одного из маркеров снижения фертильности эякулята. Однако физиологическая роль ФНО-α в сперме, патогенетические механизмы участия данного протеина в патологических процессах в органах мужской репродуктивной системы окончательно не выяснены. Необходимы дальнейшие исследования концентрации ФНО-α в норме и при заболеваниях органов урогенитального тракта у мужчин, в том числе у пациентов с различными причинами олигозооастеноспермии.



