Появление чрескожного метода реваскуляризации коронарных артерий стало настоящим прорывом в кардиологии. За 30 лет существования чрескожных коронарных вмешательств (ЧКВ) произошло значительное развитие данного метода. Появление стандартных металлических стентов (СМС) в 90-х годах ХХ века позволило резко снизить число интраоперационных и госпитальных осложнений, значительно уменьшить частоту рестеноза и повторных реваскуляризаций поражений по сравнению с аналогичными показателями при чрескожной транслюминальной коронарной ангиопластике (ЧТКА) [1]. Так, если после ЧТКА частота рестеноза в зависимости от диаметра артерии, локализации и протяженности поражения, наличия сахарного диабета и других факторов риска колеблетсяот 25 до 50% [2, 3], то после ЧКВ с имплантацией СМС данный показатель снизился до 20—30% [4, 5].
Несмотря на улучшение технологий в интервенционной кардиологии, появление новых устройств для выполнения ЧКВ и современных антитромботических препаратов, которые значительно повысили эффективность чрескожных вмешательств и привели к снижению частоты развития осложнений, для проведения диагностических процедур и ЧКВ все также требуются йодсодержащие контрастные вещества (КВ) [6]. С момента появления первых КВ свойства препаратов данного класса были значительно улучшены [7] и безопасность КВ значительно увеличилась. Это позволило шире выполнять диагностические и лечебные вмешательства с использованием КВ [8, 9]. Тем не менее использование КВ по-прежнему ассоциируется с риском развития контрастиндуцированной нефропатии (КИН).
В настоящее время КИН занимает 3-е место среди причин, вызывающих госпитальную острую почечную недостаточность, а ее развитие связано с неблагоприятным результатом лечения [10]. У больных с КИН, развившейся после ЧКВ, зарегистрирована более высокая частота кардиальных и системных госпитальных осложнений по сравнению с таковой у больных без КИН [11, 12]. К тому же среди больных ишемической болезнью сердца, переносящих ЧКВ, все больше наблюдаются лица с сопутствующей хронической болезнью почек (ХБП). Только в США ХБП страдают 19 млн человек, у которых сердечно-сосудистые заболевания являются основной причиной смерти [13, 14]. Большинство больных, подвергающихся ЧКВ, находятся в группе низкого риска развития КИН, который не превышает 5% [15]. Однако у больных ХБП, особенно в сочетании с сахарным диабетом, риск развития КИН может достигать 50% [16, 17]. Так как число выполняемых ЧКВ растет из года в год [18, 19], то увеличивается и число больных в группе риска развития КИН. По этой причине профилактика и прогнозирование КИН и других осложнений, связанных с ЧКВ, у больных ишемической болезнью сердца и ХБП является чрезвычайно актуальной проблемой и нуждается в детальном изучении.
Материал и методы
В настоящее в проспективное исследование были включены 727 пациентов, последовательно перенесших в 2004 г. ЧКВ с имплантацией одного или более СМС в Медицинском центре им. Сани Конукоглы (Газиантеп, Турция). В исследование включали пациентов, госпитализированных со стабильной стенокардией напряжения (от II до IV функционального класса по Канадской классификации) или с острым коронарным синдромом — ОКС (нестабильная стенокардия с отрицательными биохимическими маркерами поражения миокарда), который был стабилизирован до выполнения ангиографии. У некоторых пациентов с ишемической болезнью сердца имелась ХБП.
Критерием включения в настоящее исследование была возможность выполнения ЧКВ со стентированием в пораженных сегментах в отсутствие строгих противопоказаний к коронарному вмешательству. В исследование не включали больных, имеющих в анамнезе любые операции реваскуляризации: ЧКВ или открытую операцию коронарного шунтирования. Таким образом, все поражения у включенных больных были нативными. Не включали также больных с поражением ствола левой коронарной артерии, в первые 7 сут после развития инфаркта миокарда (ИМ) с подъемом сегмента ST или ИМ без подъема сегмента ST, но с положительными биохимическими маркерами поражения миокарда («тропониновый» ИМ). Кроме того, в исследование не включали больных с непереносимостью аспирина или клопидогрела. Ангиографическим критерием исключения из группы стентирования были должный диаметр сосуда в месте стеноза менее 2,5 мм или более 4,5 мм, изгиб в месте стеноза более 60°. Все больные были информированы о методах лечения и давали письменное информированное согласие на каждый вид вмешательства до начала лечения. Протоколы проведения коронарографии (КГ), ЧКВ были одобрены этическим комитетом клиники.
С целью характеристики функционального состояния почек использовали Рекомендации K/DOQI (2002) [20]. Согласно данным рекомендациям критериями ХБП считали: повреждение почки ≥3 мес со снижением СКФ или СКФ <60 мл/мин/1,73 м2 ≥3 мес с повреждением почки или без него.
КИН согласно общепринятым критериям констатировали при более чем 25% относительном увеличении или более чем на 0,5 мг/дл абсолютном увеличении от начального уровня креатинина в сыворотке крови в течение 48—72 ч после введения КВ в организм [21].
Для анализа отдаленных результатов вмешательств пациентов наблюдали клинически до 36 мес после операции. Пациентов, перенесших ЧКВ без госпитальных осложнений, приглашали вернуться на клинический контроль. В случае появления возвратной стенокардии или других осложнений пациентов госпитализировали для оценки изменений и решении вопроса о повторных вмешательствах. К концу срока наблюдения (36 мес) были опрошены по телефону все больные, которые не обращались повторно после индексной госпитализации.
Статистический анализ. Полученные данные были обработаны при помощи пакетов прикладных программ BioStat, Statistica for Windows 6.0. При нормальном распределении для первичного сравнения данных между группами использовали однофакторный дисперсионный анализ (ANOVA) с применением методов множественного сравнения в случае выявления достоверных различий. Если не подтверждалась нормальность распределения, то применялись порядковые критерии Манна—Уитни или Крускала—Уоллиса. При оценке качественных признаков использовали критерий χ2 или точный критерий Фишера. Доли сравнивались Z-критерием с поправкой Йейтса или точным критерием Фишера. Связи между показателями выявляли с помощью корреляционного анализа по Пирсону и Спирмену, а также с использованием различных регрессионных моделей с определением для значимых предикторов отношения шансов или относительного риска (ОР) с 95% доверительным интервалом (ДИ). Для всех видов анализа проводили оценку репрезентативности полученных результатов. Статистически значимыми считали различия при p<0,05.
Клиническая и ангиографическая характеристика больных. Все пациенты были разделены на 3 группы по исходной степени нарушения функции почек (или отсутствию таковой). Степень нарушения функции почек оценивали по скорости клубочковой фильтрации — СКФ, определенной до ангиографии/ЧКВ. СКФ рассчитывали по формуле MDRD: в группу нормальной или незначительно сниженной СКФ (непораженные почки, а также ХБП I и II стадии) вошли 466 больных с показателем более 60 мл/мин/1,73 м2, в группе умеренно сниженной СКФ (ХБП III стадии) оказались 223 пациента с показателем от 30 до 60 мл/мин/1,73 м2, группу выраженной почечной дисфункции (ХБП IV стадии) составили 38 больных с СКФ менее 30 мл/мин/1,73 м2.
Внутри группы из 466 больных с СКФ более 60 мл/мин/1,73 м2 было 78 пациентов с ХБП I и II стадии (без снижения СКФ), т.е. больные, у которых имелось повреждение почек давностью более 3 мес, проявляющееся одним из известных признаков.
Мужчины в исследовании составили 72%. Возраст больных колебался от 33 до 79 лет, составив в среднем 59±11 лет (табл. 1.)
Таблица 1. Исходные клинические показатели обследованных больных*
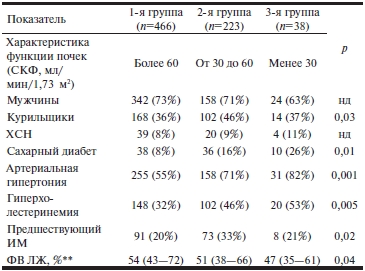
Примечание. Здесь и в табл. 2, 4—7: данные представлены * — в виде абсолютного числа больных (%), если не указано другое; ** — в виде медианы (диапазон). ИМ — инфаркт миокарда; ФВ — фракция выброса; ЛЖ — левый желудочек; здесь и в табл. 2—7: нд – недостоверно.
У 37% больных был повышен уровень холестерина (ХС) в крови (более 5,2 ммоль/л) и/или уровень ХС липопротеидов низкой плотности (более 2,6 ммоль/л). В среднем у всех больных отмечалось умеренное повышение уровня общего ХС до 6,3±0,6 ммоль/л. Сахарным диабетом страдали 12% больных, которые получали специфическую терапию внутрь или инсулин подкожно. Артериальная гипертония была диагностирована у 77% пациентов. ИМ переносили 24% пациентов. У 12% больных на момент настоящей госпитализации имелась клиническая картина ОКС. Исходные реологические показатели у обследованных пациентов находились в пределах нормы.
При мониторировании электрокардиограммы по Холтеру до инвазивных вмешательств у 84% пациентов регистрировались эпизоды глубокой депрессии сегмента ST при обычной нагрузке.
У всех больных со СКФ менее 60 мл/мин/1,73 м2 перед выполнением КГ проводили профилактику КИН. Для этого осуществляли адекватную гидратацию (не менее 100 мл/ч жидкости) за 4 ч до и в течение 24 ч после ангиографии, ограничение приема нефротоксичных лекарственных препаратов. Кроме того, дополнительно назначали N-ацетилцистеин в дозе 600 мг/сут за 48 ч до инвазивного исследования.
У всех больных со сниженной СКФ (2-я и 3-я группы) использовали только неионный изоосмолярный контрастный препарат иодиксанол, по возможности старались уменьшить его количество. Суммарное количество КВ для диагностической КГ и стентирования не превышало 350 мл при СКФ от 45 до 59 мл/мин/1,73 м2 и 250 мл — при СКФ менее 45 мл/мин/1,73 м2.
У всех больных со СКФ более 60 мл/мин/1,73 м2 (1-я группа) применяли различные низкоосмолярные неионные контрастные препараты, а суммарное количество КВ для КГ и стентирования не превышало 600 мл.
У всех больных со сниженной СКФ (менее 60 мл/мин/1,73 м2 — 2-я и 3-я группы) коронарное стентирование выполняли через 3—5 сут после КГ для профилактики КИН, а у 310 из 466 больных 1-й группы с СКФ более 60 мл/мин/1,73 м2 стентирование было выполнено в ходе единой процедуры с диагностической КГ.
Однососудистое поражение имелось у 38% больных 1-й группы с нормальной СКФ, у 61% больных 2-й группы с СКФ от 30 до 59 мл/мин/1,73 м2 и у 74% больных 3-й группы с СКФ менее 30 мл/мин/1,73 м2. Меньше всего во всех 3 группах было больных с трехсосудистым поражением — 20, 14 и 3% соответственно. Калибр пораженных артерий оказался в среднем больше всего в 1-й группе с нормальной СКФ и меньше всего — во 2-й группе с СКФ от 30 до 60 мл/мин/1,73 м2, а стеноз сосуда — наибольшим в 3-й группе с СКФ менее 30 мл/мин/1,73 м2 (табл. 2).
Таблица 2. Исходные ангиографические показатели обследованных больных
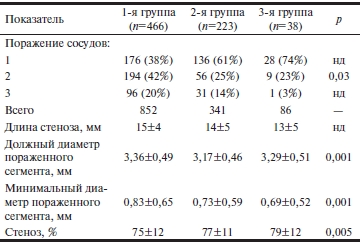
Средний должный диаметр в месте поражения был больше в 1-й группе, бифуркационные стенозы чаще отмечались во 2-й группе, трехсосудистое поражение реже всего встречалось в 3-й группе.
Результаты
Госпитальные результаты исследования. При наличии бифуркационного поражения обычно выполняли стентирование основной ветви. Непосредственные результаты ЧКВ представлены в табл. 3. Наименьший остаточный стеноз был в 1-й группе, а наибольший — в 3-й (р<0,05), но их разница составила менее 6%. Наибольшие различия по непосредственным результатам проявились в количестве введенного КВ (р<0,001), который ограничивали во 2-й группе и строго лимитировали в 3-й группе. Поэтому количество пролеченных сосудов (в пересчете на одного пациента) было значительно меньше во 2-й и 3-й группах (р<0,001). Разумеется, это было обусловлено характером поражения коронарных сосудов, и в указанных группах больных с двух- и трехсосудистым поражением оказалось меньше, чем в 1-й группе (р<0,001), поскольку при многососудистом поражении и выражено сниженной СКФ больных чаще направляли на открытую операцию коронарного шунтирования. Тем не менее индекс полноты реваскуляризации все равно был значительно выше (р<0,001) в 1-й группе (0,941), где отсутствовали существенные ограничения по количеству КВ, по сравнению с индексами во 2-й группе (0,845) и 3-й группе (0,837).
Таблица 3. Непосредственные результаты реваскуляризации
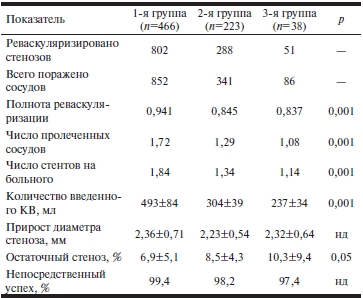
Примечание. КВ — контрастное вещество.
В ходе вмешательства в 1-й группе были имплантированы 1477 стандартных стентов, во 2-й группе — 387 стентов, в 3-й группе — 47. Имплантацию выполняли планово у всех больных. Максимальное давление в баллоне при дилатации стента составило от 12 до 20 атм, в среднем 13,2±1,6 атм. Для оптимальной имплантации каждого стента потребовалось от 2 до 4 дилатаций, в среднем 2,73±0,65 дилатации. Потребность в имплантации дополнительного стента возникала редко — соответственно в 7, 4 и 6% в 1-й, 2-й и 3-й группах. Прирост диаметра оказался сопоставимым — от 2,23 до 2,36 мм (табл. 3).
Большинство стентов было успешно имплантировано без диссекций D-F, окклюзий и феномена no reflow. Оптимального результата стентирования (остаточный стеноз менее 20% с кровотоком TIMI 3) не удалось достичь у 3 больных в 1-й группе, у 4 — во 1-й и у одного — в 3-й группе. Таким образом, непосредственный успех имплантации стентов составил по группам 99,4, 98,2 и 97,4% соответственно (различия статистически незначимы), но все пациенты были живы и переведены под наблюдение в палату.
В течение 2—3 сут после ЧКВ КИН развилась у 2 (0,4%) больных в 1-й группе, у 11 (4,9%) — во 2-й группе и у 5 (13,2%) — в 3-й группе, несмотря на проводимую профилактику во 2-й и 3-й группах (р<0,001). Кроме того, при наблюдении в течение 2 сут после ЧКВ острый тромбоз развился у 2 (0,4%) больных в 1-й группе, у 6 (2,7%) — во 2-й группе и у 2 (5,3%) — в 3-й группе (р<0,01). Это привело к развитию ОКС (ИМ с подъемом нд ST или ИМ без подъема сегмента ST/нестабильная стенокардия) по группам в 2, 6 и 2 случаях соответственно. Во всех случаях развития ОКС больного повторно доставляли в рентгенооперационную и выполняли вмешательство на тромбированном сосуде на фоне болюса и последующей инфузией блокатора IIb/IIIa гликопротеиновых рецепторов тромбоцитов тирофибана. Повторное ЧКВ было успешным в одном случае (0,2%) в 1-й группе, в 4 (1,8%) случаях во 2-й группе и в одном случае (2,6%) в 3-й группе и безуспешными с летальными исходами в одном (0,2%), в 2 (0,9%) и в одном (2,6%) случае соответственно (табл. 4).
Таблица 4. Госпитальные результаты стентирования
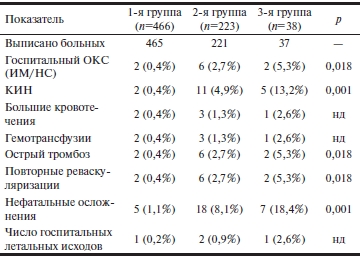
Примечание. ОКС — острый коронарный синдром; ИМ — инфаркт миокарда; НС — нестабильная стенокардия; КИН — контрастиндуцированная нефропатия.
За время пребывания больных в стационаре возникали большие кровотечения, обусловившие необходимость в гемотрансфузии, у 2 (0,4%) больных в 1-й группе, у 3 (1,3%) больных во 2-й группе и у одного (2,6%) больного в 3-й группе. Таким образом, за время последующей госпитализации произошли фатальные осложнения в 1-й группе с частотой 0,2%, во 2-й группе — 0,9% и в 3-й группе — 2,6%, а нефатальные осложнения — с частотой 1,1, 8,1 и 18,4% по группам соответственно (р<0,001).
Отдаленные результаты исследования. После выписки при наблюдении до 6 мес 51 (11%) больной из 1-й группы, 48 (22%) больных из 2-й группы и 13 (34%) больных из 3-й группы обратились в связи с появлением возвратной стенокардии (табл. 5). У них при контрольной КГ был выявлен гемодинамически значимый рестеноз или новый стеноз. Все больные с рестенозом или новым стенозом были повторно реваскуляризированы. Им были выполнены повторные ЧКВ, а в случае двух- или трехсосудистого поражения — операции коронарного шунтирования.
Таблица 5. Отдаленные результаты ЧКВ до 6 мес и 3 лет
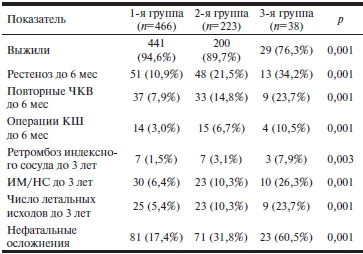
Примечание. ЧКВ — чрескожное коронарное вмешательство; КШ — коронарное шунтирование; ИМ — инфаркт миокарда; НС — нестабильная стенокардия.
При наблюдении до 3 лет в 1-й группе ретромбоз в индексном сосуде развивался в 7 (1,5%) случаях, во 2-й группе — в 7 (3,1%), а в 3-й группе — в 3 (7,9%) случаях. Он был одной из причин развития ОКС (ИМ и нестабильная стенокардия), которые отмечались у 30 (6,4%) больных 1-й группы, у 23 (10,3%) больных 2-й группы и у 10 (26,3%) больных 3-й группы. Всего до 3 лет наблюдения умерли от сердечных и несердечных причин в 1-й группе 25 (5,4%) больных, во 2-й группе — 23 (10,3%) и в 3-й группе — 9 (23,7%) (табл. 5).
При многофакторном регрессионном анализе отдаленных (до 3 лет) результатов оказалось, что значимыми независимыми предикторами смерти и нефатального ИМ стали во всех группах больных снижение фракции выброса левого желудочка (ОР 2,42 при 95% ДИ от 1,37 до 3,86; р=0,007), и больший возраст больных (ОР 1,61 при 95% ДИ от 1,22 до 2,89; р=0,009).
При рассмотрении событий до 3 лет с учетом развития КИН во время индексной госпитализации выявлены интересные закономерности. В 1-й группе КИН развивалась в 2 случаях, во 2-й группе — в 11, а в 3-й группе — в 5. Анализ показал, что в целом частота развития ИМ до 3 лет возрастала в 1,57 раза во 2-й группе по сравнению с таковой в 1-й группе и в 3,91 раза — в 3-й группе по сравнению с таковой в 1-й группе. Разделение больных на подгруппы по частоте развития КИН позволило выявить чрезвычайно высокую частоту развития ИМ после КИН во всех 3 группах с тенденцией к росту от 1-й к 3-й группе (с 50 до 80%) и значимый, но умеренный рост частоты развития ИМ от 1-й к 3-й группе (с 6,3 до 18,8%), если КИН не развивалась (табл. 6).
Таблица 6. Частота и риск развития ИМ до 3 лет с учетом КИН

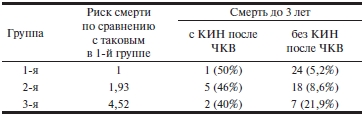
Анализ летальности показал, что в целом частота летальных исходов до 3 лет возрастала в 1,93 раза во 2-й группе по сравнению с 1-й группой и в 4,52 раза в 3-й группе по сравнению с 1-й группой. При разделении больных на подгруппы по частоте развития КИН обнаружены чрезвычайно высокая частота летальных исходов после КИН во всех 3 группах, но без роста от 1-й к 3-й группе (с 50 до 40%) и значимый, но умеренный рост частоты летальных исходов от 1-й к 3-й группе (с 5,2 до 21,9%), если КИН не развивалась (табл. 7).
Таблица 7. Частота и риск летальных исходов до 3 лет с учетом КИН
Обсуждение
У большинства больных, которым вводится КВ, не развиваются побочные эффекты или осложнения. Однако в случае развития КИН прогноз заболевания значительно ухудшается. Такие пациенты чаще переносят различного рода госпитальные осложнения, включая выраженные сердечные осложнения, инсульты, кровотечения/гематомы и т.д. Частота развития КИН сильно зависит от степени ХБП.
В ряде исследований был показан более неблагоприятный прогноз у больных с ХБП по сравнению с таковым у больных без данной патологии. В нескольких исследованиях проводилось сравнение исходов ЧКВ у больных с ХБП и больных, не подвергавшихся интервенционным методам лечения. Так, в исследовании, проведенном D.N. Reddan и соавт., было показано, что у больных с умеренной или выраженной ХБП результаты после ЧКВ лучше, чем после медикаментозной терапии, несмотря на введение КВ при ЧКВ [22].
В полученных нами результатах наибольшую ценность представляют несколько ключевых моментов. Несмотря на проводимую профилактику, КИН чаще всего развивалась у больных 2-й группы со СКФ от 30 до 60 мл/мин/1,73 м2 (4,9%) и у больных 3-й группы со СКФ менее 30 мл/мин/1,73 м2 (13,2%) по сравнению с больными с нормальной СКФ (0,4%) (р<0,001). Кроме того, у больных 2-й и 3-й групп чаще наблюдались подострые тромбозы после ЧКВ (соответственно в 2,7 и 5,3%) с развитием ОКС по сравнению с больными из 1-й группы (0,4%; р<0,01). Частота фатальных осложнений в 1-й группе составила 0,2% против 0,9% и 2,6% во 2-й и 3-й группах соответственно, а нефатальные осложнения также развивались чаще во 2-й и 3-й группах (8,1 и 18,4% против 1,1% в 1-й группе; р<0,001). Таким образом, полученные нами данные подтверждают, что у больных с умеренной или выраженной ХБП значительно чаще развивается КИН, а также увеличивается частота всех выраженных сердечных осложнений [23—26].
В последние годы некоторые исследователи обратили внимание на прогноз у больных с почечной недостаточностью после ЧКВ [27, 28]. В этих исследованиях было показано, что даже умеренная почечная недостаточность увеличивает риск смерти в 2 раза. Полученные нами данные были сопоставимы с известными прогнозами. Так, при анализе летальности в целом до 3 лет было показано увеличение частоты летальных исходов во 2-й группе в 1,93 раза по сравнению с таковой в 1-й группе и 4,52 раза — в 3-й группе по сравнению с 1-й группой. В то же время при оценке отдаленных результатов лечения (до 3 лет) было установлено, что у больных 2-й и 3-й групп частота развития ОКС была значительно выше (10,3 и 26,3%), чем у больных 1-й группы (6,4%; p<0,001). Подобные данные были получены в исследовании, проведенном Q. Zhang и соавт. с участием 3763 пациентов [29]. Ими было установлено, что у больных с тяжелой почечной недостаточностью риск смерти увеличивается в 15 раз (около 80% смертей приходится на кардиальные причины) и примерно в 9 раз увеличивается риск развития ИМ в течение 2 мес наблюдения по сравнению с таковым у больных с нормальной функцией почек.
Однако риск развития КИН у больных с ХБП не должен являться причиной отказа от проведения необходимых диагностических или лечебных вмешательств. В то же время при ХБП следует осторожно использовать КВ. На наш взгляд, можно констатировать, что ограниченное по объему использование КВ способствует более благоприятным результатам лечения больных с ХБП разной степени выраженности. Не стоит также забывать о превентивных мерах, направленных на снижение частоты развития КИН. Для этого необходимо проводить оценку факторов риска развития КИН, которые включают сахарный диабет, застойную сердечную недостаточность, гипо- и гипертензию, недавно перенесенный ИМ. Следует также помнить о своевременной отмене нефротоксичных препаратов и адекватной гидратации пациентов.
Выводы
Исходное снижение скорости клубочковой фильтрации увеличивает риск развития контрастиндуцированной нефропатии после плановых имплантаций стандартных коронарных стентов (с 0,4 до 13,2%).
Снижение скорости клубочковой фильтрации приводит к росту частоты рестеноза и повторных реваскуляризаций (с 11 до 34%) в период до 6 мес.
Снижение скорости клубочковой фильтрации после плановых имплантаций стандартных коронарных стентов увеличивает риск развития нефатального инфаркта миокарда (с 6 до 26%) и смерти (с 5 до 24%) в период наблюдения до 3 лет.
Развитие контрастиндуцированной нефропатии обусловливает чрезвычайно высокую частоту развития нефатального инфаркта миокарда в период до 3 лет (от 50% в группе с нормальной скоростью клубочковой фильтрации до 80% в группе с выражено сниженной скоростью клубочковой фильтрации) и к аналогично высокой частоте летальных исходов в период до 3 лет (от 40 до 50%).



