Адекватное лечение артериальной гипертонии (АГ) и достижение целевых уровней артериального давления (АД), несомненно, приводит к снижению смертности от сердечно-сосудистых заболеваний [1—3]. Обычно в качестве причин неэффективного лечения АГ рассматривают осложненное течение заболевания (наличие поражения органов-мишеней, сочетанные заболевания), терапевтическую инертность врачей, плохую переносимость лекарственных препаратов и низкую приверженность больных к назначенному лечению [4, 5]. Предпринимаются различные попытки улучшить приверженность пациентов к лечению. Многие вопросы удается решить за счет назначения препаратов, содержащих фиксированные комбинации антигипертензивных препаратов [6—9]. Этот подход позволяет уменьшить количество принимаемых таблеток и числа приема препаратов. Используют различные системы напоминания для уменьшения забывчивости пациентов [10]. Ведение пациентами дневников по измерению АД увеличивает их внимание и внимание врачей к проблеме [11].
 Один из новых подходов связан с увеличением удобства приема препаратов — создание, например, лекарственных форм, диспергируемых во рту. Причем эти формы используют не только у пациентов, испытывающих затруднения в глотании таблеток [12], или у детей и лиц пожилого возраста, но и у людей, не имеющих возможности запивать принимаемые лекарства, например, в дороге, на работе и т.д. Ранее разработка диспергируемых во рту форм в основном касалась противоэпилептических, психотропных, антибактериальных препаратов [13—16]. Такие формы разрабатывают также для улучшения фармакокинетических свойств препаратов, в частности для уменьшения эффекта первого прохождения через печень в процессе всасывания в желудочно-кишечном тракте [17].
Один из новых подходов связан с увеличением удобства приема препаратов — создание, например, лекарственных форм, диспергируемых во рту. Причем эти формы используют не только у пациентов, испытывающих затруднения в глотании таблеток [12], или у детей и лиц пожилого возраста, но и у людей, не имеющих возможности запивать принимаемые лекарства, например, в дороге, на работе и т.д. Ранее разработка диспергируемых во рту форм в основном касалась противоэпилептических, психотропных, антибактериальных препаратов [13—16]. Такие формы разрабатывают также для улучшения фармакокинетических свойств препаратов, в частности для уменьшения эффекта первого прохождения через печень в процессе всасывания в желудочно-кишечном тракте [17].
В настоящее время в клинической практике появилась диспергируемая форма антигипертензивного препарата из класса ингибиторов ангиотензинпревращающего фермента (АПФ) — периндоприла аргинин.
Целью настоящего исследования была оценка антигипертензивной эффективности периндоприла аргинина в виде таблеток, диспергируемых в полости рта, в широкой клинической практике.
Материал и методы
Программа ОПТИМУМ — постмаркетинговая наблюдательная открытая программа. Проведение ее утверждено на заседании межвузовского Этического комитета, протокол №09-14.
Критерии включения:
- возраст от 18 до 79 лет;
- диагноз эссенциальной АГ;
- при включении систолическое АД (САД) не менее 140 мм рт.ст. или диастолическое АД (ДАД) не менее 90 мм рт.ст.;
- при включении САД менее 180 мм рт.ст. и ДАД менее 110 мм рт.ст.;
- решение врача назначить престариум А в виде таблеток, диспергируемых в полости рта, в случае неэффективности или отсутствия предшествующей антигипертензивной терапии.
В программу не включали пациентов с симптоматической АГ, перенесших инфаркт миокарда или нарушение мозгового кровообращения в течение последнего года, при наличии нестабильной стенокардии или стабильной стенокардии III—IV функционального класса, хронической сердечной недостаточности III—IV функционального класса, сахарного диабета 1-го типа или декомпенсированного сахарного диабета 2-го типа, непереносимости или противопоказаний к ингибиторам АПФ.
Исследуемый препарат и рекомендованный режим дозирования. Периндоприла аргинин (престариум А) в виде диспергируемых таблеток рекомендовали принимать по 1 таблетке 1 раз в сутки, предпочтительно утром, перед едой. При этом таблетку следует положить на язык и, после того как она распадется на поверхности языка, проглотить ее. В случае впервые диагностированной АГ или отсутствия предшествующей терапии рекомендовали начинать лечение с дозы 5 мг, при переводе с предшествующей монотерапии ингибиторами АПФ или сартанами — 10 мг. Если исследуемый препарат в дозе 5 мг окажется недостаточно эффективным, через 1 мес терапии доза могла быть увеличена до 10 мг.
Схема исследования. В ходе программы было предусмотрено 4 визита пациента к врачу: визит включения и начала терапии, контрольный визит через 2 нед после начала терапии, через 1 и 2 мес после начала терапии.
Критерии оценки эффективности терапии:
- изменение САД в ходе терапии;
- изменение ДАД в ходе терапии;
- частота достижения целевых значений АД (%);
- оценка изменения АД по данным самоконтроля больными АД ежедневно утром и вечером в ходе терапии;
- изменение приверженности больных к терапии по суммарной оценке по опроснику Мориски—Грина;
- оценка предпочтений пациентов в отношении исследуемого препарата.
Статистическая обработка полученных данных проведена с использованием пакета SPSS 16.0. Анализ выполнен методами описательной статистики: для количественных показателей, распределенных по нормальному закону, использовали среднее значение, стандартное отклонение, минимальное и максимальное значение, медиану; для количественных показателей, не распределенных по нормальному закону, — среднее значение, стандартное отклонение, минимальное и максимальное значение, а также медиану, первый и третий квартили. Для качественных показателей или количественных показателей, принимающих только небольшое число возможных значений, — абсолютную и относительную частоту каждого из возможных значений. При сравнении параметров до начала и после терапии использованы для количественных параметров, распределенных по нормальному закону, — критерий Стьюдента для парных выборок; для количественных параметров, не распределенных по нормальному закону, — критерий Вилкоксона. Все используемые статистические критерии были двусторонними. Для всех используемых статистических критериев уровень значимости 0,05.
Результаты
Программа проведена в 48 регионах Российской Федерации. В ней приняли участие 197 врачей, которые включили в наблюдение 957 пациентов с октября 2014 г. по март 2015 г. Последний пациент завершил исследование в мае 2015 г.
Досрочно выбыли из исследования 17 пациентов, завершили наблюдение в соответствии с протоколом 940.
Клиническая характеристика пациентов, включенных в программу ОПТИМУМ, представлена в таблице. Как видно из представленных данных, женщины составляли более 2/3 включенных больных, почти 2/3 пациентов были работающими, однако 13% уже имели инвалидность. Рассматривая факторы риска развития и прогрессирования заболевания, следует отметить, что каждый третий пациент, включенный в программу ОПТИМУМ, имел ожирение, причем многие имели абдоминальный его вариант, каждый третий больной был курящим и каждый четвертый имел неблагоприятный семейный анамнез.
 Многие пациенты уже имели заболевания, связанные с атеросклеротическим поражением сосудов. Так, каждый пятый имел стенокардию, ряд больных перенесли инфаркт, либо инсульт, а также имели поражение периферических артерий, каждый четвертый имел признаки сердечной недостаточности. Обращает внимание большое число пациентов с повышенным уровнем холестерина в крови.
Многие пациенты уже имели заболевания, связанные с атеросклеротическим поражением сосудов. Так, каждый пятый имел стенокардию, ряд больных перенесли инфаркт, либо инсульт, а также имели поражение периферических артерий, каждый четвертый имел признаки сердечной недостаточности. Обращает внимание большое число пациентов с повышенным уровнем холестерина в крови.
При включении в программу каждый пятый больной имел АГ 1-й степени и 3/4 включенных — АГ 2-й степени. Средняя продолжительность заболевания составила 7,0±6,2 года (медиана 5 лет). Важно, что 16% пациентов из числа включенных в программу ранее не лечились. Из тех, кто принимали препараты, более 50% получали монотерапию различными антигипертензивными препаратами, более 1/3 — двухкомпонентную терапию и существенно меньшее число больных — трех- и более компонентную терапию.
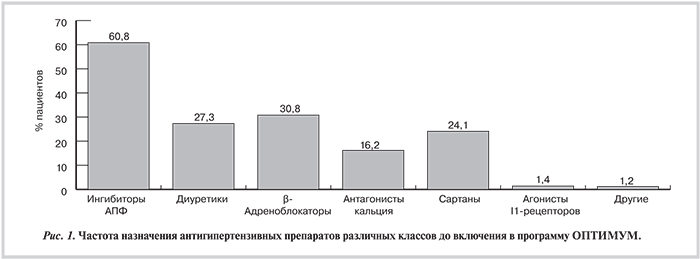
Антигипертензивная терапия, которая предшествовала включению в программу, представлена на рис. 1. Видно, что 50% больных получали ингибитор АПФ, каждый пятый — сартаны и диуретики, каждый четвертый — β-адреноблокаторы.
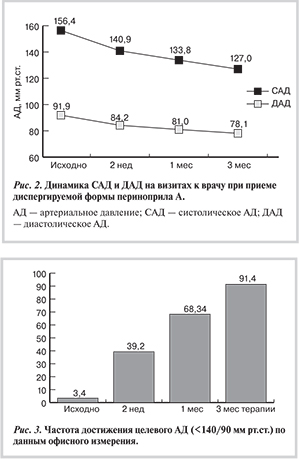
При включении больных в программу ОПТИМУМ была произведена замена принимаемых ранее ингибиторов АПФ и сартанов на диспергируемую форму периндоприла А, что привело к существенному уменьшению САД и ДАД (рис. 2). На каждом следующем визите и САД, и ДАД статистически значимо снижалось (р<0,00001) по сравнению с предыдущим визитом. К 3-му месяцу терапии 9 из 10 больных достигли целевого АД (рис. 3).
По данным дневников самоконтроля АД пациентов также отмечено статистически значимое снижение САД и ДАД, причем отчетливо в процессе лечения снижались различия между уровнями АД, измеренного утром и вечером.
Периндоприл А в начале исследования в дозе 5 мг был назначен 76% пациентов, в дозе 10 мг — 23,4%. К концу исследования дозу 5 мг получали до 48,9% пациентов, дозу 10 мг — 50%. У 9 пациентов в ходе исследования назначали дозы периндоприла А 2,5 мг, 7,5 мг, 20 мг.
Важно, что назначение диспергируемой во рту формы периндоприла А привело к значительному улучшению приверженности больных к лечению (рис. 4). Средняя суммарная оценка по опроснику Мориски—Грина статистически значимо (р<0,00001) увеличилась в среднем с 2,76±1,25 до 3,57±0,89 балла.
В конце наблюдения пациентам предлагали заполнить специальную анкету, которая состояла из 9 вопросов, на каждый из которых мог быть дан один из 4 ответов. Более 2/3—3/4 пациентов были согласны или полностью согласны с утверждениями, что форма более проста в употреблении, быстро растворяется и легко проглатывается, удобнее для приема вне дома, в целом оценили ее как более удобную в употреблении. Около 5—6% пациентов не дали ответа или были не согласны с этими утверждениями.
Оценка безопасности лечения. Досрочно завершили исследование 17 человек (1,8% из числа включенных в наблюдение). Из них отказались от наблюдения 6, утрачен контакт с 4, без указания причин — у 3 человек, в связи с отъездом у 2, в связи с материальными затруднениями у 1 и лишь в 1 случае — из-за появления сухого кашля.
Обсуждение
В рамках наблюдательной программы ОПТИМУМ нами получены данные о возможности использования диспергируемой во рту формы периндоприла А в широкой клинической практике с высокой степенью эффективности и безопасности. Так, 98,2% завершили программу согласно протоколу, причем из-за возникновения нежелательных явлений выбыл лишь 1 пациент, что составило 0,1% от общего числа наблюдавшихся.
При этом отмечено выраженное снижение офисного АД (САД в среднем на 20% и ДАД в среднем на 15%). Аналогичная степень снижения АД отмечена и по данным самоконтроля АД. Выраженность снижения АД совпадает с той, которая показана в ранее проведенных исследованиях с традиционной таблетированной формой периндоприла [18—21]. Можно полагать, что это отчасти обусловлено увеличением приверженности к лечению, в том числе за счет использования новой лекарственной формы, так как 79% пациентов ответили, что эта форма для них была более удобной, и 74,4% пациентов сказали, что эта новая форма могла бы помочь им принимать препарат регулярно. Это совпадает с данными об увеличении приверженности при использовании диспергируемых форм при других патологических состояниях [22, 23].
То, что растворимая форма периндоприла более удобна для приема и повышает приверженность к лечению, важно также в связи с тем, что периндоприл является препаратом, который имеет большую доказательную базу по возможности в моно- и комбинированной терапии снижать неблагоприятные, в том числе смертельные, исходы у очень широкого круга пациентов. Так, это показано у пациентов с АГ в исследовании ASCOT [24], у пациентов с ИБС [25], у больных, перенесших мозговой инсульт или транзиторную ишемическую атаку [26, 27], у пациентов с сахарным диабетом [28].
Объяснением этих благоприятных эффектов могут служить данные о том, что периндоприл, помимо длительного и выраженного снижения АД, уменьшает степень ремоделирования сосудов, в том числе коронарных, церебральных, уменьшает выраженность атеросклеротического повреждения сосудов, увеличивает их эластичность. Причем это действие у периндоприла может быть более выраженным, чем у других ингибиторов АПФ и сартанов [29]. Периндоприл в большей степени, чем другие ингибиторы АПФ и сартаны, снижает в плазме и сосудах уровни АПФ [30], увеличивает уровень брадикинина и улучшает соотношение брадикинин/ангиотензин II, в большей степени снижает апоптоз прогениторных эндотелиальных клеток. Это происходит не только за счет увеличения уровня брадикинина (периндоприл среди других ингибиторов АПФ имеет наибольшее сродство с участками АПФ, связывающими брадикинин), но и за счет увеличения уровня ангиотензина-(1—7), оказывающего эффекты, противоположные действию ангиотензина II [31]. Под влиянием периндоприла возрастают экспрессия eNOS и уровень вазодилататора NO в эндотелии и гладких мышечных клетках сосудов. В прямых сравнительных исследованиях с сартанами показано, что периндоприл значительно улучшает функцию эндотелия [32], например, по снижению фактора Виллебранда, оказывает антитромбоцитарный эффект, снижая растворимый селектин Р или гликопротеин V, усиливая фибринолитическую активность, снижая уровень ингибитора тканевого активатора плазминогена 1-го типа [33].
Таким образом, можно ожидать, что расширение возможности использования периндоприла А, в том числе за счет назначения новой формы для приема, может привести к улучшению контроля АД и уменьшению частоты развития неблагоприятных исходов у больных с АГ.
Заключение
В результате проведения постмаркетинговой наблюдательной открытой программы ОПТИМУМ установлено, что при использовании пероральной рассасывающейся формы периндоприла А у большинства пациентов с артериальной гипертонией, ранее не леченных или находящихся на монотерапии, можно достичь целевых уровней артериального давления. У пациентов с ранее неэффективной комбинированной терапией замена терапии ингибиторами ангиотензинпревращающего фермента или сартанами на диспергируемую форму периндоприла А приводит к дополнительному выраженному снижению артериального давления и достижению целевых уровней офисного артериального давления. Использование этой формы приводит к статистически значимому увеличению приверженности пациентов к лечению и хорошо переносится.



