Широкий спектр поражений нервной системы, включающий цереброваскулярные заболевания, демиелинизирующие заболевания, дегенеративные и опухолевые процессы, а также травмы центральной и периферической нервной системы, может сопровождаться различными видами нарушений функций нижних мочевыделительных путей. При этом развитие различных нейрогенных расстройств мочеиспускания, таких как гипо- или гиперактивность детрузора или сфинктера, может в перспективе приводить к хронической задержке мочи, пузырно-мочеточниковому рефлюксу и хронической болезни почек [1]. Чистая интермиттирующая катетеризация на сегодняшний день является наиболее безопасным и физиологичным методом отведения мочи. Но одним из самых частых осложнений, с которым сталкиваются пациенты, являются бактериурия и хроническая рецидивирующая инфекция мочевыводящих путей [2]. В то же время растущая антибиотикорезистентность принимает глобальный характер, что затрудняет лечение рецидивирующих инфекций нижних мочевыводящих путей (РИНМП) у больных нейрогенной дисфункцией нижних мочевыводящих путей (НДНМП). В связи этим поиск новых возможностей профилактики рецидива клинически значимых инфекций нижних мочевыводящих путей в настоящее время представляет собой чрезвычайно актуальную задачу. Одной из таких возможностей является разработка препаратов на основе бактериофагов.
Бактериофаги (вирусы бактерий) – естественные природные агенты, способные избирательно и эффективно поражать бактерии. Впервые они были описаны русским микробиологом Н. Ф. Гамалеей в 1889 г. Свое название бактериофаги получили благодаря Феликсу Д‘Эреллю (F. d’Hérelles, 1873–1949), канадскому сотруднику Института Пастера в Париже.
В настоящее время в связи с замедлением темпа создания новых антибиотиков и ростом резистентности микроорганизмов к уже имеющимся антибиотикам очевидна необходимость поиска альтернативных методов лечения и профилактики инфекционных заболеваний. И фаготерапия может рассматриваться в качестве одного из перспективных новых методов.
Информация о пациентах
В данной статье рассмотрен опыт применения препарата на основе бактериофагов у трех пациенток с нарушениями мочеиспускания, обусловленными НДНМП, осложненной РИНМП.
Пациентка Е. 54 лет. Основной диагноз: нейрогенная дисфункция нижних мочевыводящих путей, хроническая задержка мочи, хроническая РИНМП. В качестве фоновых заболеваний были диагностированы миелопатия проксимальных отделов седалищного нерва, радикулопатия, протрузия дисков пояснично-крестцового отдела позвоночника, гемангиома на уровне поясничного утолщения, полное удвоение правой почки, хроническая ишемия головного мозга, гипертоническая болезнь 1-й степени 1-й стадии. Из анамнеза известно, что первые симптомы нарушения мочеиспускания, которые проявлялись в виде ослабления струи мочи, необходимости «натуживания» при мочеиспускании и ощущения неполного опорожнения мочевого пузыря, стала отмечать с января 2013 г. после перенесенной острой стрессовой ситуации. При дообследовании в июле 2013 г., по данным комплексного уродинамического исследования (КУДИ), у пациентки был диагностирован гипосенсорный арефлекторный мочевой пузырь (рис. 1). По данным МРТ пояснично-крестцового отдела позвоночника: остеохондроз, спондилез, спондилоартроз с нарушением статики, диффузное выбухание и протрузия межпозвонкового диска L4‒L5. По данным ультразвуковой диагностики (УЗИ) и мультиспиральной компьютерной томографии (МСКТ) мочевой системы, выявлено полное удвоение правой почки. Азотемические показатели крови были в пределах референсных значений. С 2014 г. самостоятельное мочеиспускание отсутствует, в связи с чем была начата аутокатетеризация до 5 раз в день. С 2014 г. страдает хронической РИНМП, которую купирует короткими курсами антибактериальной терапии (фосфомицин, нитрофураны, цефалоспорины). С 2015 г. диагностирован пролапс тазовых органов, цисторектоцеле POP‒Q3, в связи с чем в 2016 г. пациентке выполнена передняя кольпорафия, леваторопластика. С 2017 г. отмечает рецидивы хронической инфекции нижних мочевыводящих путей не менее 4‒5 раз в год, что затрудняет аутокатетеризацию в период обострения.
Пациентка К. 57 лет. Основной диагноз: нейрогенная дисфункция нижних мочевыводящих путей, хроническая РИНМП, двусторонний гидронефроз, хроническая болезнь почек, стадия ‒ С4 (СКФ ‒ 28 мл/мин/1,73 м3). Фоновые заболевания: гипертоническая болезнь 2-й степени 2-й стадии, сахарный диабет 2-го типа, лейомиома матки. Анамнез больной отягощен, так как в младенческом возрасте перенесла сфинктеропластику по поводу прямокишечно-промежностного свища, что могло стать причиной НДНМП. Нарушение качества мочеиспускания отмечает с 2020 г., когда впервые стала отмечать затрудненное мочеиспускание. В 2020 г. отмечен эпизод острого необструктивного пиелонефрита на фоне хронической задержки мочи, потребовавший стационарного лечения. При дообследовании в 2021 г. по данным КУДИ диагностирован гипосенсорный аконтрактильный мочевой пузырь, обращает на себя внимание, что максимальная цистометрическая емкость составила 330 мл, кашлевая проба отрицательная, гиперактивности детрузора не выявлено, при попытке мочеиспускания сократимость детрузора отсутствует. С 2021 г. пациентка самостоятельно не мочится, выполняет аутокатетеризацию 4‒5 раз в сутки. С 2022 г. отмечает рецидивы хронической инфекции нижних мочевыводящих путей не менее 4 раз в год.
Пациентка Ко. 25 лет. Основной диагноз: нейрогенная дисфункция нижних мочевыводящих путей, РИНМП.
В анамнезе: 05.07.2017, бытовая травма в результате ДТП. Закрытая черепно-мозговая травма. Переломы костей верхних и нижних конечностей. Множественные оскольчатые переломы крестца и переломы поперечных отростков L4 слева, L5 с обеих сторон. В результате полученных травм отмечено отсутствие мочеиспускания. С августа 2017 г. пациентка находится на интермиттирующей катетеризации лубрицированными катетерами (6‒8 раз в сутки в зависимости от питьевого режима, не реже 1 раза в 4 ч).
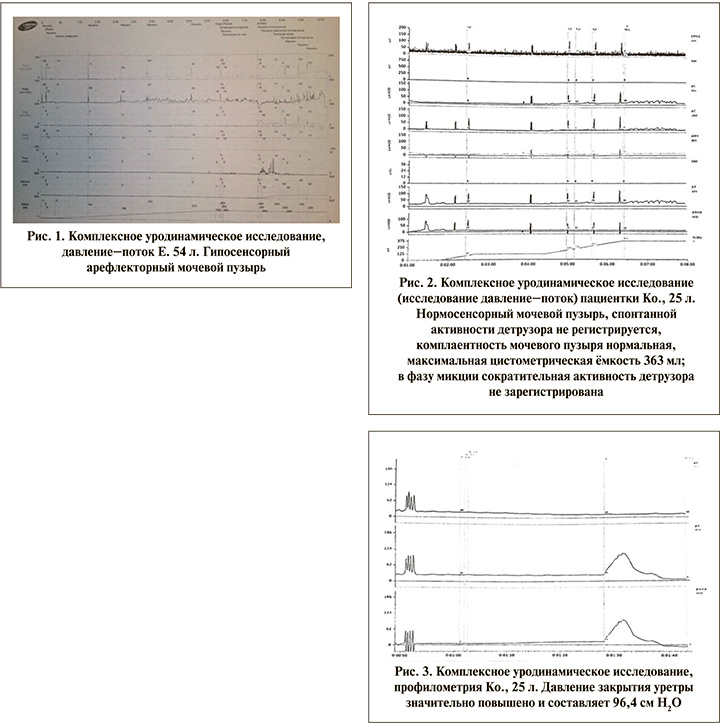
В 2021 г. дообследована, по данным КУДИ нормосенсорный мочевой пузырь, спонтанной активности детрузора не регистрируется, комплаентность мочевого пузыря нормальная, максимальная цистометрическая емкость ‒ 363 мл; в фазу микции сократительная активность детрузора не зарегистрирована, мочеиспускание отсутствует; на фоне абдоминального напряжения отмечается одномоментное повышение внутрипузырного давления (рис. 2). По данным профилометрии уретры, давление закрытия уретры значительно повышено и составляет 96,4 см H2O. Таким образом, у пациентки аконтрактильный мочевой пузырь, спазм сфинктера уретры. С 2020 г. РИНМП. В 2022 г. дообследована в НМИЦ нейрохирургии им. академика Н. Н. Бурденко. Данные КУДИ: нейрогенная дисфункция нижних мочевыводящих путей, гиперсенсорный, гипоконтрактильный мочевой пузырь, признаки функциональной инфравезикальной обструкции, цистометрическая емкость 200 мл. Таким образом, по сравнению с предыдущими исследованиями отмечено снижение цистометрической емкости, снижение комплаентности. По данным УЗИ верхних мочевыводящих путей, патологии не выявлено. Лабораторные азотемические показатели крови в пределах референсных значений. В 2022 г. в НМИЦ нейрохирургии им. академика Н. Н. Бурденко выполнена операция по имплантации системы для стимуляции S3 Precision Montage (Boston Scientific). С 2022 г. отметила усугубление симптоматики РИНМП: частые позывы к мочеиспусканию (10–12 раз в день), дискомфорт и боль внизу живота после опорожнения мочевого пузыря, изменение цвета и запаха мочи; а также обострения хронической мочевой инфекции до 6 раз в год, что требовало регулярного приема антибактериальных препаратов и уросептиков.
В 2023 г. все пациентки были консультированы урологом, рекомендовано обследование и лечение на кафедре урологии МГМСУ им. А. И. Евдокимова.
Описание клинических наблюдений
Основной целью данного исследования явилась оценка терапевтической эффективности внутрипузырного применения препарата на основе бактериофагов в лечения РИНМП у пациентов с НДНМП.
В рамках трех клинических наблюдений мы оценили эффективность внутрипузырного применения препарата на основе бактериофагов в лечения РИНМП у пациентов с НДНМП. Все пациенты подписали информированное согласие на участие в исследовании.
Применяемый препарат на основе бактериофагов «Урофаг» прошел доклинические испытания в экспериментах, подтвердивших его безопасность. Этот препарат на основе расширенного спектра бактериофагов был разработан в 2021 г.
в рамках гранта РНФ «Разработка антибактериальных и обезболивающих средств для профилактики мочевой инфекции при проведении лечебных и диагностических манипуляций в урологии», соглашение № 19-15-00379, проведено клиническое исследование в параллельных группах по изучению эффективности и безопасности препарата для внутрипузырного введения на основе бактериофагов производства ООО НПЦ «МикроМир» (Россия) в терапии пациентов с хроническим рецидивирующим циститом, на проведение данного исследования было получено одобрение Межвузовского комитета по этике (выписка из протокола № 03 заседания от 18.03.2021).
«Урофаг» – уникальное по своему составу антибактериальное средство в терапии пациентов с хроническим рецидивирующим циститом в форме раствора для инстилляций. Состав данного средства включает более 70 видов вирулентных фагов (т.е. фагов с доказанной высокой активностью в отношении условно-патогенных бактерий; титры по Appelman 10*9–10*10 БОЕ/см3), лизирующие уропатогены Staphylococcus aureus, Streptococcus agalactiae, Streptococcus pyogenes, Escherichia coli, Enterococcus faecalis, Proteus vulgaris, Klebsiella pneumoniae, Staphylococcus warneri, Staphylococcus haemolyticus, Staphylococcus capitis, Staphylococcus caprae, Staphylococcus succinus, Pseudomonas aeruginosa, Klebsiella ozaenae, Proteus mirabilis, Enterococcus faecalis, Enterobacter kobei, Enterobacter cloacae, Acinetobacter baumannii, Stenotrophomonas maltophilia, Citrobacter freundii и Propionibacterium acnes.
Преимущества разрабатываемого средства перед другими антибактериальными препаратами с бактериофагами:
- ✓ содержит строго вирулентные бактериальные вирусы с широким литическим спектром по отношению к штаммам конкретного патогена;
- ✓ содержит широкий набор фагов, подавляющих рост наиболее часто встречающихся патогенных бактерий) для снижения вероятности смены возбудителя;
- ✓ бактериофаги, входящие в состав средства, не снижают литической активности после хранения в течение 6 мес. при температуре +4С–+8С: показатели микробиологической чистоты и рН стабильные.
Пациенткам проводилось лечение препаратом «Урофаг» путем внутрипузырного введения. Трехмесячный курс терапии подразумевал инстилляции препарата «Урофаг» в виде раствора по 50 мл 2 раза в неделю в течение 12 нед. На 1-й, 30-й, 90-й и 180-й дни наблюдения проводилась оценка состояния пациенток, эффективности терапии и оценка лабораторных показателей.
Пациентка Е. 54 лет в 2023 г. дообследована на кафедре урологии МГМСУ им. А. И. Евдокимова МЗ РФ, по результатам бактериологического исследования мочи выявлен рост Escherichia coli 107 КОЕ/мл, обнаружена устойчивость к цефалоспоринам, фторхинолонам, пенициллинам; к бактерио-фагам чувствительность оказалась сохраненной. На момент обследования пациентка выполняет самостоятельную катетеризацию мочевого пузыря 6 раз в сутки с объемом выводимой мочи до 400 мл, средний суточный диурез составляет около 1500 мл. С марта 2023 г. назначен трехмесячный курс терапии препаратом «Урофаг». Спустя 3 мес. терапии рецидивов РИНМП не зафиксировано, спустя 6 мес. зафиксирован единичный эпизод обострения инфекции нижних мочевыводящих путей. По результатам контрольных посевов мочи выявлен рост Escherichia coli, но в меньших титрах (на 90-й день 102 КОЕ/мл, на 180-й день 103 КОЕ/мл), устойчивость к противомикробным препаратам прежняя. На фоне лечения отмечает улучшение состояния в виде уменьшения частоты рецидивов инфекции мочевыводящих путей в течение 6 мес. Также пациентка не отметила побочных и нежелательных эффектов на фоне профилактики с использованием внутрипузырных инстилляций препарата на основе бактериофагов.
Пациентка К. в 2023 г. обследована на кафедре урологии МГМСУ им. А. И. Евдокимова МЗ РФ. Результаты КУДИ не изменились с 2021 г. По данным цистоуретроскопии, патологических изменений выявлено не было. По данным ультразвукового исследования, имеет место двусторонняя гидронефротическая трансформация (лоханка слева – 32 мм, справа – 28 мм; чашечки слева – 14 мм, справа – 12 мм). Имеет место азотемия (уровень креатинина в диапазоне – 150–170 мкмоль/л). По результатам бактериологического исследования мочи выявлен рост Escherichia coli 107 КОЕ/мл, обнаружена устойчивость к широкому спектру антибиотиков (цефалоспоринам, фторхинолонам, пенициллинам, нитрофуранам), к бактериофагам чувствительность сохранена. С марта 2023 г. назначен трехмесячный курс терапии препаратом «Урофаг». Спустя 3 и 6 мес. терапии рецидивов РИНМП не было. По результатам конт-рольных посевов мочи выявлен рост Escherichia coli, но в меньших титрах (на 90-й день 105 КОЕ/мл, на 180-й день 104 КОЕ/мл), устойчивость к противомикробным препаратам прежняя. На фоне лечения отмечает улучшение состояния в виде отсутствия рецидивов инфекции мочевыводящих путей в течении 6 мес.
Пациентка Ко. в 2023 г. также обследована на кафедре урологии МГМСУ им. А. И. Евдокимова. По результатам бактериологического исследования мочи выявлен рост Escherichia coli 107 КОЕ/мл, чувствительность к широкому спектру антибиотиков и бактериофагам сохранена. С июня 2023 г. назначен трехмесячный курс терапии препаратом «Урофаг». Спустя 3 мес. терапии отмечен один рецидив РИНМП, при последующем наблюдении до 6 мес. дальнейших рецидивов не зарегистрировано. По результатам контрольных посевов мочи выявлен рост Escherichia coli, в меньших титрах (на 90-й и 180-й дни 104 КОЕ/мл). На фоне лечения отмечает улучшение состояния в виде уменьшения количества рецидивов инфекции мочевыводящих путей в течении 6 мес.
Таким образом, у всех пациенток имеет место поражение поясничного и крестцового отделов позвоночника, что могло явиться причиной нейрогенных нарушений мочеиспускания.
Инфекции мочевыводящих путей являются показанием к назначению антибактериальной терапии. Имеющиеся исследования свидетельствуют о нерациональном применении антибиотиков как в госпитальной, так и в амбулаторной практике, что ведет к росту резистентности микроорганизмов к антибактериальным препаратам [2]. В настоящее время в связи с замедлением темпов создания новых антимикробных препаратов и ростом резистентности микроорганизмов к антибиотикам очевидна необходимость в поиске альтернативных методов профилактики и лечения.
Впервые действие бактериофагов было описано в 1896 г. английским микробиологом Е. Hankin, описавшим литическое действие фильтрата воды из реки Ганг на возбудителя холеры Vibrio cholera. Десятилетием позже F. Twort предположил вирусную гипотезу данного явления. А в 1917 г. микробиолог F. d’Hérelles предложил термин «бактериофаг» и провел успешное клиническое испытание противодизентерийного фага.
Бактериофаги не влияют на ферментативные системы организма, действуют избирательно и эффективно по отношению к бактериям, к которым тропны. Стоит также особо отметить способность бактериофагов предотвращать образование и бороться с уже появившейся биопленкой [3, 4].
В нашей стране препараты бактериофагов успешно использовали при лечении бактериальных осложнений у больных с послеоперационными и ожоговыми ранами [5]. Получены положительные результаты наблюдений клинической и микробиологической эффективности использования препаратов бактериофагов в урологической практике [6, 7].
На данный момент публикаций, посвященных применению бактериофагов при лечении РИНМП у больных нейрогенной дисфункцией нижних мочевыводящих путей, практически не представлено, имеющиеся носят описательный характер, что требует проведения качественных исследований с достаточным количеством пациентов в будущем, на что мы и акцентируем внимание в том числе и в наших работах [8–10].
Отсутствие плацебо-контролируемых рандомизированных клинических исследований, подтверждающих клиническую эффективность и преимущества бактериофагов в отношении инфекций, вызванных устойчивыми к антибиотикам бактериями, предполагает дальнейшее накопление клинических и статистических данных, на что и была направлена данная работа.
Безусловно, применение препарата на основе бактериофагов у больных НДНМП, осложненной РИНМП, позволит уменьшить использование антибактериальных препаратов и в значительной степени способно сократить рост развития резистентности к ним.



