Метаболический синдром (МС) — актуальная проблема современной медицины за счет его достаточно
высокой распространенности, негативного влияния на риск развития сердечно-сосудистых заболеваний, а также многообразия поражения внутренних органов [1—3]. Так, согласно результатам последних исследований, одним из проявлений МС может рассматриваться поражение почек. Инсулинорезистентность, являясь неотъемлемым компонентом МС, взаимосвязана с почечной дисфункцией [4]. По данным американских исследователей, МС увеличивает вероятность развития
хронической болезни почек (ХБП) у пациентов старше 20 лет в 2,6 раза, причем эта вероятность увеличивается по мере увеличения числа компонентов МС [5]. Важность проблемы коморбидности МС и ХБП обусловлена и их большой распространенностью, и повышенным риском не только сердечно-сосудистых, но и неблагоприятных и почечных исходов. Так, по данным регистра NHANES III предполагается, что только в США к 2030 г. число лиц, нуждающихся в диализе и трансплантации почек, может составить более 2 млн [6].
Важная задача врача состоит в выявлении самых ранних, начальных проявлений нарушения функции почек, оптимальный выбор фармакотерапии для их коррекции и, тем самым, улучшение прогноза.
В силу частого наличия у больных с МС и артериальной гипертонией (АГ), они, как правило, принимают антигипертензивные лекарственные средства. В связи с этим актуальной является оценка осо-
бенностей фармакологического действия антигипертензивных лекарственных средств у больных с МС
при наличии начальных, доклинических признаков нарушения функции почек.
Известно, что негативное влияние на состояние сердечно-сосудистой системы и на функциональные
показатели почек оказывает активация ренин-ангиотензин-альдестероновой системы [7]. Увеличение образования ангиотензина II вызывает сужение выносящей артериолы клубочков почек, увеличение реабсорбции натрия, экскреции калия, нарастание протеинурии, окислительного стресса и увеличение диаметра пор клубочковой мембраны [8, 9].
Одним из классов антигипертензивных препаратов, влияющих на ренин-ангиотензин-альдестероновую систему, являются блокаторы рецепторов к ангиотензину II (БРА). По данным ряда крупных многоцентровых рандомизированных клинических исследований, таких как RENAAL, TRANSCEND,
MARVAL, IDNT и др., БРА способствуют замедлению прогрессирования ХБП, оказывая корригирующее
влияние на скорость клубочковой фильтрации (СКФ) и антипротеин урическое действие [10—13]. Однако в большинстве исследований изучалось нефропротективное действие БРА у пациентов с клинически значимой патологией почек, в то время как исследований по оценке эффективности и безопасности применения БРА у пациентов с начальными, доклиническими признаками поражения почек (ХБП I—II стадии) практически нет, что делает актуальной проблему применения БРА у таких больных.
В связи с этим целью исследования явилась оценка эффективности и безопасности одного из БРА лозартана (презартан, Ipca Laboratories Limited, Индия) у больных МС и ХБП I—II ст.
Материал и методы
В исследовании приняли участие 20 больных МС (9 мужчин, 11 женщин) в возрасте от 32 до 79 лет (средний возраст 55,45±12,97 года). Наличие МС определяли по классификации Международной федерации диабета (International Diabetes Federation, IDF, 2005) с учетом следующих критериев: абдоминальное ожирение — окружность талии (ОТ) для мужчин ≥94 см, для женщин ≥80 см; наличие любых двух из следующих критериев:
— повышение уровня триглицеридов (ТГ) ≥1,7 ммоль/л или нормальный уровень ТГ при приеме соответствующей терапии,
— снижение уровня холестерина (ХС) липопротеидов высокой плотности (ЛВП) <1,03 ммоль/л для мужчин
и <1,29 ммоль/л для женщин или нормальный уровень ХС ЛВП при применении соответствующей терапии,
— артериальное давление (АД) ≥130/85 мм рт.ст. или нормальный уровень АД или проводимая антигипертензивная терапия по поводу ранее выявленной АГ,
— повышение уровня глюкозы плазмы крови ≥5,6 ммоль/л — гипергликемия натощак, нарушение
толерантности к глюкозе или их сочетание.
Критериями включения были также нормальный уровень креатинина сыворотки крови (менее 1,4 мг/дл), СКФ >60 мл/мин/1,73 м2, возраст старше 18 лет, информированное согласие пациента на участие в исследовании.
В исследование не включали больных с симптоматическими формами АГ; острым нарушением мозгового
кровообращения, инфарктом миокарда, нестабильной стенокардией, реваскуляризацией миокарда в течение последних 6 мес; с сердечной недостаточностью II—IV функционального класса; с нарушениями ритма сердца, требующими постоянной антиаритмической терапии; с тяжелыми нарушениями функции печени, почек; с сахарным диабетом 2-го типа; женщин детородного возраста, не использующих надежных средств контрацепции; беременных и кормящих; а также лиц, имеющих противопоказания к назначению БРА. Подробная клинико-демографическая характеристика
больных представлена в табл. 1.
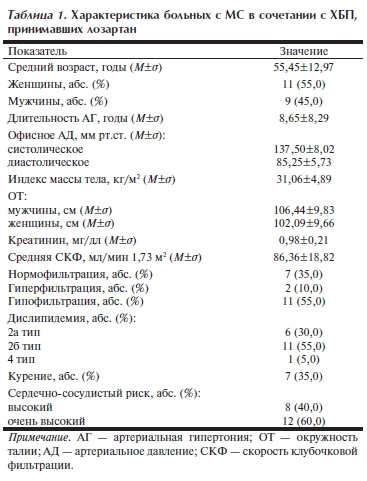
Всем больным в начале и в конце наблюдения проводили общеклиническое обследование с измерением антропометрических показателей. Кардиогемодинамические эффекты лозартана оценивали по результатам офисного измерения АД, суточного мониторирования АД (СМАД), эхокардиографии (ЭхоКГ) с расчетом индекса массы миокарда левого желудочка (ИММ ЛЖ) и оценкой диастолической функции по отношению Е/А.
Лабораторные исследования включали биохимический анализ крови с измерением уровня креатинина сыворотки крови, показателей липидного состава крови; уровня глюкозы в сыворотке крови натощак и в условиях перорального теста на толерантность к глюкозе.
СКФ рассчитывали по формуле Кокрофа—Голта с приведением на стандартную поверхность тела по формуле Дюбуа, уровень микроальбуминурии (МАУ) измеряли методом иммунотурбидиметрии.
Анализировали также показатели качества жизни больных с использованием опросников «Качество
жизни у больных гипертонической болезнью» и ВАШ—«термометр здоровья».
Безопасность терапии лозартаном оценивали по частоте и характеру побочных эффектов и по динамике лабораторных показателей.
Все пациенты получали БРА лозартан в средней суточной дозе 50,00±13,06 мг. Длительность наблюде-
ния составила 12 нед.
Результаты исследований обработаны с помощью пакета программ «SPSS 11.5 for Windows». Статистический анализ проводили с использованием непараметрических методов в связи с негауссовским распределением показателей с использованием корреляционного анализа по Спирмену, критерия Вилкоксона для парных сравнений, медианного теста (с использованием критерием χ2)
для множественных независимых групп. Данные представлены в виде средней (M), стандартной ошибки средней в 95%-доверительном интервале (σ), а также в виде медианы (Me) и диапазона верхнего и нижнего квартиля с учетом непараметрического характера распределения. Достоверными считались различия при р<0,05.
Результаты и обсуждение
На фоне терапии лозартаном у 70,0% больных были достигнуты целевые значения АД, что для группы
пациентов с МС и другими факторами риска составляло 130/80 мм рт.ст. При анализе данных СМАД отмечено достоверное снижение систолического АД (САД) и диастолического АД (ДАД) во все временные промежутки, а также достоверное уменьшение нагрузки повышенным САД и ДАД в дневные часы и тенденция к уменьшению нагрузки повышенным АД в ночные часы. Лозартан также способствовал снижению вариабельности АД и нормализации суточного профиля АД в виде увеличения количества пациентов с нормальным суточным профилем dipper (табл. 2).
Таблица 2. Показатели СМАД на фоне терапии лозартаном у больных метаболическим синдромом и хронической болезнью почек, M±σ или Me (25, 75 процентиль).
При оценке морфофункциональных параметров сердца по данным ЭхоКГ на фоне 12 нед терапии лозартаном отмечена тенденция к уменьшению выраженности гипертрофии миокарда ЛЖ (снижение ИММЛЖ) и диастолической дисфункции ЛЖ (увеличение отношения Е/А) (табл. 3).
Таблица 3. Влияние лозартана на показатели ЭхоКГ у больных метаболическим синдромом и субклиническим поражением почек.
Таблица 4. Степень МАУ у больных МС в зависимости от СКФ.
Таблица 5. Влияние лозартана на показатели углеводного и липидного обменов у больных МС и субклиническим поражением почек.
При оценке состояния функции почек у больных МС было выявлено, что исходно нормальная СКФ
была у 35% больных, а у 65% были скрытые нарушения функции почек в виде гиперфильтрации у 10% и в виде гипофильтрации — у 55%.
При оценке уровня МАУ, определяемого в разовой моче методом иммунотурбидиметрии, была выявлена
следующая закономерность — по мере ухудшения функции почек (прохождения ряда последовательных стадий — гиперфильтрации, нормофильтрации и гипофильтрации с развитием хронической почечной недостаточности) уровень МАУ нарастает, что согласуется с данными литературы о последовательности процессов прогрессирования нарушения почечной функции (табл. 4) [14].
Клинически значимым считается уровень МАУ более 30 мг/дл, однако уже имеется достаточно свидетельств того, что даже при МАУ ниже 30 мг/дл, происходит существенное ухудшение прогноза как за счет увеличения частоты почечных, так и за счет увеличения риска развития сердечно-осудистых осложнений [15]. В связи с этим в нашем исследовании были не только пациенты с диагностически значимым уровнем МАУ (МАУ = 30—300 мг/дл), но и с МАУ <30 мг/дл, возникающей уже на начальных стадиях поражения почек.
Терапия лозартаном привела к незначительным и недостоверным изменениям соотношения больных
с нарушением СКФ — количество больных с нормофильтрацией уменьшилось на 5%, с гипофильтрацией увеличилось на 5%, с гиперфильтрацией осталось неизменным (10%). Детальный индивидуальный анализ показал, что увеличение СКФ сохранилось только у больных, не достигших целевых значений АД. Выявлена также тенденция к снижению МАУ у больных с 5,60 (3,50; 9,20) до 3,25 (0,40; 7,82) мг/дл.
Динамика биохимических показателей на фоне терапии лозартаном у больных МС свидетельствует о благоприятном метаболическом профиле препарата. Ни у одного больного не было отмечено негативного влияния на показатели углеводного и липидного обменов, более того, через 12 нед лечения лозартаном отмечено достоверное снижение уровня ТГ и уменьшение нарушения углеводного обмена в виде тенденции к снижению уровня глюкозы плазмы крови натощак и статистически значимому ее снижению через 2 ч после приема 75 г глюкозы (табл. 5).
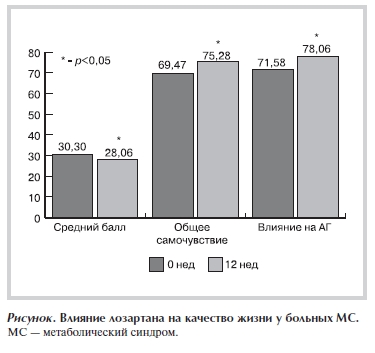
Кроме того, на фоне терапии лозартаном отмечено улучшение показателей, характеризующих качество жизни, а именно уменьшение суммарного балла по опроснику «Качество жизни у больных гипертонической болезнью» и улучшение общего самочувствия и самочувствия, связанного с АГ, по ВАШ—«термометр здоровья» (см. рисунок).
Заключение
Таким образом, лозартан (презартан) у больных метаболическим синдромом и начальными проявлениями нарушения функции почек, помимо выраженного антигипертензивного действия, оказывает благоприятное влияние на параметры суточного профиля артериального давления, обладает хорошим профилем безопасности и дает благоприятные метаболические эффекты (снижает
уровень триглицеридов и глюкозы в плазме крови в условиях теста на толерантность к глюкозе), снижает уровень микроальбуминурии. Кроме того, применение лозартана приводит к достоверному улучшению показателей качества жизни у больных с метаболическим синдромом и хронической болезнью почек I—II стадии.



