Артериальная гипертензия является самым распространенным модифицируемым независимым фактором риска развития фибрилляции предсердий (ФП) и ее осложнений [1, 2]. Контроль артериального давления (АД) может стать стратегией профилактики фибрилляции предсердий (ФП). У больных с гипертрофией левого желудочка (ЛЖ) повышается риск развития ФП. Препараты, модулирующие активность ренин-ангиотензин-альдостероновой системы, уменьшают структурные изменения сердца [3, 4].
 Среди многообразия патологических процессов, которые могут осложниться пароксизмальной фибрилляцией предсердий (ПФП), можно выделить ряд основных: ишемия миокарда, нарушение электролитного обмена, адренергический дисбаланс, изменение геометрии сердца — ремоделирование [5—7]. При артериальной гипертензии (АГ), как правило, имеется сочетание этих факторов [5], и, вероятно, каждый из них способен играть существенную роль в инициации или поддержании пароксизма аритмии. Кроме того, установлено, что АГ и увеличение левых отделов сердца также являются факторами риска развития ПФП [1, 8, 9].
Среди многообразия патологических процессов, которые могут осложниться пароксизмальной фибрилляцией предсердий (ПФП), можно выделить ряд основных: ишемия миокарда, нарушение электролитного обмена, адренергический дисбаланс, изменение геометрии сердца — ремоделирование [5—7]. При артериальной гипертензии (АГ), как правило, имеется сочетание этих факторов [5], и, вероятно, каждый из них способен играть существенную роль в инициации или поддержании пароксизма аритмии. Кроме того, установлено, что АГ и увеличение левых отделов сердца также являются факторами риска развития ПФП [1, 8, 9].
Повышение активности ангиотензина II (ATII) усиливает пролиферацию фибробластов, продукцию коллагена. Нарастанию жесткости ЛЖ и уменьшению его способности к расслаблению способствуют возникающие гипертрофия кардиомиоцитов и увеличение мышечной массы. При АГ высока вероятность дистрофических изменений в миокарде, способствующих снижению «податливости» миокарда ЛЖ вследствие прогрессирования интерстициального фиброза. Известно, что ингибирование ангиотензинпревращающего фермента (АПФ), кроме снижения АД может приводить к уменьшению ремоделирования и гипертрофии миокарда [10], нормализации электролитного баланса, оказывает косвенное антиишемическое действие [8, 11].
Указанные свойства ингибиторов АПФ связывают с их положительным влиянием на течение и прогноз АГ, сердечной недостаточности, снижением риска фатальных аритмий [9, 12]. Результаты крупнейших международных клинических исследований (PROGRESS, EUROPA, ADVANCE) свидетельствуют о сердечно-сосудистых эффектах ингибиторования АПФ с помощью периндоприла и его благоприятном влиянии на прогноз [11, 13, 14].
Цель исследования — оценить частоту возникновения пароксизмов ФП, выраженность ремоделирования и гипертрофии миокарда ЛЖ при применении престариума A у больных этой категории.
Материал и методы
В исследование включены 32 больных АГ, имеющих приступы ПФП. Из них 19 мужчин, 13 женщин, средний возраст пациентов, включенных в исследование, составлял 54,3±3,4 года. Критерии включения: рецидивирующая ПФП, успешная кардиоверсия, АГ 1—2-й степени, II стадии. Диагноз АГ устанавливали в соответствии с «Рекомендациями по диагностике и лечению артериальной гипертензии» (Всероссийское научное общество кардиологов, 2010). Критерии исключения: хроническая сердечная недостаточность III—IV функционального класса по классификации NYHA, пороки сердца, тяжелые заболевания печени и почек, длительность пароксизмов более 48 ч, редкое возникновение ПФП (менее 1 раза в 2 мес). В качестве антиаритмического средства применялся амиодарон. После рандомизации пациентам в качестве антигипертензивного препарата был назначен периндоприла аргенин (престариум А «Лаборатория Сервье», Франция) в дозе 10 мг/сут.
Критерием эффективности терапии по АД считали достижение целевых уровней АД: систолического АД (САД) <140 мм рт.ст., диастолического АД (ДАД) <90 мм рт.ст. По показаниям проводили лечение сочетанной патологии (ацетилсалициловая кислота, нитраты и т.п.). Длительность контролируемого исследования составила 16 нед. Оценку эффективности проводили по частоте рецидивов ПФП за последние 4 нед, по достижению целевого уровня АД и динамике показателей суточного мониторирования АД, изменению показателей эхокардиографии (ЭхоКГ).
Кроме общеклинического обследования проводили ЭхоКГ на эхосканере Vivid-3 (GE) с использованием датчика с частотой 2,5—3,5 МГц в стандартных позициях в положении больного лежа на левом боку по общепринятой методике. Скорость и характер внутрисердечного кровотока оценивали методом допплер-ЭхоКГ в импульсном режиме на уровне приносящего тракта ЛЖ сразу над местом смыкания створок митрального клапана и на уровне впадения легочных вен в левое предсердие с расчетом общепринятых показателей — максимальной скорости кровотока раннего диастолического наполнения (Е), максимальной скорости кровотока во время систолы предсердия (А), соотношения Е/А, максимальной скорости кровотока в легочных венах во время систолы и диастолы. Определяли показатели систолической функции сердца (фракция выброса — ФВ, %) [15]. Массу миокарда (ММ) ЛЖ определяли по формуле R.B. Devereux: ММЛЖ=1,04×([ТМЖПД+ТЗСЛЖД+КДР]3-КДР3)-13,6 [16].
При ЭхоКГ также рассчитывали относительную толщину стенок (ОТС) ЛЖ, индекс массы миокарда (ИММ) ЛЖ.
Этот индекс рассчитывали делением массы миокарда ЛЖ на площадь поверхности тела. На основе показателей ОТСЛЖ и ИММЛЖ оценивали геометрическую модель ЛЖ и выделяли типы ремоделирования ЛЖ по классификации, предложенной A. Ganau и соавт. (1992): 1) нормальная геометрия ЛЖ — при нормальном значении ИММЛЖ и ОТСЛЖ<0,45; 2) эксцентрическая гипертрофия ЛЖ — при ИММЛЖ больше нормы и ОТСЛЖ<0,45; 3) концентрическая гипертрофия ЛЖ — при ИММЛЖ больше нормы и ОТСЛЖ>0,45; 4) концентрическое ремоделирование ЛЖ — при нормальном значении ИММЛЖ и ОТСЛЖ>0,45.
Суточное мониторирование электрокардиограммы по Холтеру, оценка вариабельности ритма сердца на системе Кардиотехника 4-08 (СМАД) проводили с помощью системы автоматического носимого монитора ВРLab.
Статистическая обработка материала выполнена с применением пакетов прикладных программ Statistica 6.0 с использованием параметрических и непараметрических методов статистики, корреляционного анализа, t-критерия достоверности Стьюдента с последующим определением уровня достоверности различий (р) с заданным уровнем надежности 95%.
 Частота возникновения приступов аритмии была стратифицирована следующим образом: 1 приступ и более в неделю, 1—3 пароксизма в месяц, реже чем 1 пароксизм в месяц.
Частота возникновения приступов аритмии была стратифицирована следующим образом: 1 приступ и более в неделю, 1—3 пароксизма в месяц, реже чем 1 пароксизм в месяц.
Результаты и обсуждение
За трехмесячный период из исследования выбыли 5 больных по причинам, не связанным с лечением. Побочных эффектов лечения не отмечено. Это свидетельствовало о хорошей переносимости периндоприла аргенина. Уменьшение частоты приступов ПФП у больных, получавших престариум А, произошло в 17 (60,7%) случаях. Распределение больных в зависимости от частоты ПФП представлено в табл. 1.
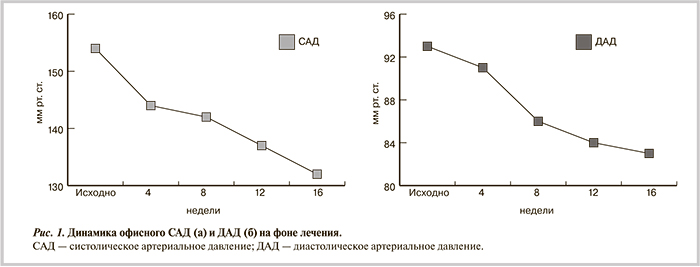
На фоне лечения, по данным клинических измерений АД, у пациентов во время контрольных визитов отмечено достоверное снижение офисного САД и ДАД, причем целевой уровень АД достигнут по САД у 80,1% больных, по ДАД — у 76,3% (р<0,05) (рис. 1).
В табл. 2 представлена динамика показателей СМАД до лечения и через 16 нед лечения.
При анализе исходных данных СМАД отмечено повышение среднесуточных САД (154,4±8,8 мм рт.ст.) и ДАД (92,4±5,8 мм рт.ст.) при выраженном индексе времени гипертензии: 68,3±6,2 и 58,6±5,3% соответственно. Снижение среднесуточного САД и ДАД составило 13,9 и 9,4% соответственно. Получено статистически значимое снижение показателей нагрузки давлением. Индекс времени гипертензии за сутки, отражающий процент времени, в течение которого величины АД превышали нормальный уровень, уменьшился: САД на 30% и ДАД на 25,7%.
С максимальным риском развития сердечно-сосудистых осложнений при АГ сопряжен патологический профиль АД. При оценке суточного ритма АД патологический профиль выявлен у 75% больных, из них к категории нон-дипперов отнесены 16 (50%), т.е. у пациентов отсутствовало физиологическое снижение уровня АД в ночное время. Случаи извращенного суточного ритма АД с преимущественно ночной гипертензией отмечены в 6 (19%) наблюдениях. При применении периндоприла аргенина достоверно снизилось САД (днем на 14,8%, ночью на 6,9%) и ДАД (днем на 9,5%, ночью на 7,5%). Нами не зафиксировано статистически значимого изменения показателей утреннего подъема АД, что, возможно, связано с высоким разбросом показателей, однако имеется тенденция к снижению этого показателя на фоне терапии. Отмечалось достоверное уменьшение среднесуточной вариабельности АД (САД на 19,8%, ДАД на 36,8%), уменьшилось число больных с патологическим суточным ритмом АД на 42%. Статистически значимой динамики частоты сердечных сокращений у больных на фоне лечения не наблюдалось.
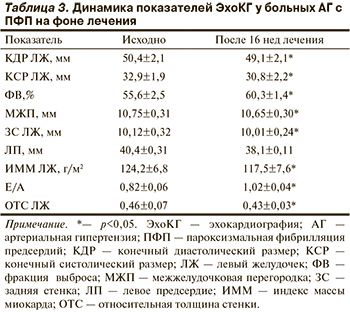
 По данным ЭхоКГ (табл. 3), сократительная способность ЛЖ была сохранена у всех обследуемых пациентов: ФВ ЛЖ составила 55,6±2,5%, фракция систолического укорочения переднезаднего размера ЛЖ — 31,7±0,9%. На фоне лечения отмечалась положительная динамика размерных показателей, характеризующих процесс ремоделирования ЛЖ: уменьшение конечного диастолического размера (КДР) и конечного систолического размера (КСР) ЛЖ на 2,6 и 6,4% соответственно, увеличение ФВ на 8,5% (р<0,05). О снижении гемодинамической нагрузки и улучшении диастолической функции свидетельствует уменьшение размеров левого предсердия с 40,4±0,31 до 38,1±0,11 мм, что положительно коррелировало (r=0,61) с уменьшением количества ПФП. Анализ индивидуальных данных ОТСЛЖ и ИММЛЖ позволил определить наличие эксцентрического ремоделирования ЛЖ у 6 (19%) больных, концентрического ремоделирования ЛЖ у 8 (25%), концентрической гипертрофии ЛЖ — у 16 (50%); нормальная геометрия ЛЖ отмечена лишь в 2 (6%) случаях. При корреляционном анализе выявлена зависимость ОТС ЛЖ и ИММ ЛЖ с недостаточной степенью ночного снижения АД (r=0,59; г=0,60; р<0,05 соответственно) и частотой развития ПФП (г=0,57; р<0,05). Наше исследование подтверждает данные J. Mayet и соавт. о взаимосвязи регрессии гипертрофии ЛЖ и антиаритмического эффекта антигипертензивной терапии [13].
По данным ЭхоКГ (табл. 3), сократительная способность ЛЖ была сохранена у всех обследуемых пациентов: ФВ ЛЖ составила 55,6±2,5%, фракция систолического укорочения переднезаднего размера ЛЖ — 31,7±0,9%. На фоне лечения отмечалась положительная динамика размерных показателей, характеризующих процесс ремоделирования ЛЖ: уменьшение конечного диастолического размера (КДР) и конечного систолического размера (КСР) ЛЖ на 2,6 и 6,4% соответственно, увеличение ФВ на 8,5% (р<0,05). О снижении гемодинамической нагрузки и улучшении диастолической функции свидетельствует уменьшение размеров левого предсердия с 40,4±0,31 до 38,1±0,11 мм, что положительно коррелировало (r=0,61) с уменьшением количества ПФП. Анализ индивидуальных данных ОТСЛЖ и ИММЛЖ позволил определить наличие эксцентрического ремоделирования ЛЖ у 6 (19%) больных, концентрического ремоделирования ЛЖ у 8 (25%), концентрической гипертрофии ЛЖ — у 16 (50%); нормальная геометрия ЛЖ отмечена лишь в 2 (6%) случаях. При корреляционном анализе выявлена зависимость ОТС ЛЖ и ИММ ЛЖ с недостаточной степенью ночного снижения АД (r=0,59; г=0,60; р<0,05 соответственно) и частотой развития ПФП (г=0,57; р<0,05). Наше исследование подтверждает данные J. Mayet и соавт. о взаимосвязи регрессии гипертрофии ЛЖ и антиаритмического эффекта антигипертензивной терапии [13].
Таким образом, необходимо учитывать суточный профиль АД, так как он может влиять на формирование гипертрофии ЛЖ и провоцировать ПФП у больных АГ.
Диастолическая дисфункция ЛЖ представляет собой неспособность ЛЖ к расслаблению и полноценному кровенаполнению в период диастолы. Полученные данные указывают на повышение ригидности миокарда у больных АГ с ПФП. При оценке трансмитрального потока выявлена диастолическая дисфункция ЛЖ по 1-му типу (аномальная релаксация) у 22 (68,8%) из 32 больных.
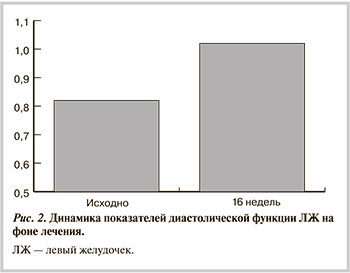
При лечении периндоприлом аргенином отмечалось достоверное уменьшение толщины стенок ЛЖ, ИММЛЖ. Улучшение морфометрических показателей ЛЖ ассоциировалось с улучшением диастолической функции сердца (рис. 2).
По характеристикам вариабельности синусового ритма статистически значимых различий до и после лечения не замечено. Это не позволяет утверждать, что имеется какая-либо специфика в отношении влияния периндоприла аргенина на регуляцию синусового ритма у больных данной категории.
Выводы
- Лечение периндоприлом аргенином (престариумом А) пациентов с сочетанием артериальной гипертензии и пароксизмальной фибрилляции предсердий сопровождается уменьшением частоты пароксизмов аритмии.
- Периндоприла аргенин обладает существенной эффективностью и хорошей переносимостью при лечении артериальной гипертензии у больных с пароксизмальной фибрилляцией предсердий.
- Вероятным механизмом положительного влияния периндоприла аргенина на течение пароксизмальной фибрилляции предсердий у больных артериальной гипертензией является высокий гипотензивный эффект и уменьшение массы миокарда левого желудочка.



