Анализ крупных регистров, выполненных по всему миру за последнее десятилетие [1—8], убедительно показал, что летальность, годичная смертность и частота повторных госпитализаций после выписки у больных с синдромом острой декомпенсации кровообращения остаются высокими. У больных с декомпенсацией кровообращения смертность и потребность в повторных госпитализациях составляют соответственно 15 и 30%. Почти 18% повторных госпитализаций происходит в первые 30 дней после выписки, причем за последние 22 года этот показатель значительно не изменился. Именно госпитализации по поводу хронической сердечной недостаточности (ХСН) доминируют в стационарах большинства стран [9]. Исследование, выполненное в 2013 г. в 12 странах Европы в 136 центрах (5118 пациентов), показало, что годичная смертность у пациентов с декомпенсацией кровообращения составляет 17,4%, а это в 2,4 раза выше, чем тот же показатель у больных без эпизодов декомпенсации в течение года [10]. Это же исследование выявило значительные различия основных показателей в странах разных географических регионов. Так, сердечно-сосудистая смертность у больных с декомпенсацией кровообращения составила в странах западной Европы 45%, а в восточной Европе — 71,3%. Разброс данных делает практически невозможным автоматический перенос результатов анализа регистров, выполненных в западных странах, на российскую популяцию. С учетом того, что в Российской Федерации не проводилось крупных исследований по анализу популяции больных с декомпенсацией кровообращения, создание собственного российского полномасштабного регистра стало актуальной задачей.
Цель исследования — оценить летальность, годичную смертность и частоту повторных госпитализаций на 30-й, 90, 180, 360-й дни наблюдения; оценить распространенность сопутствующих заболеваний (в том числе инфекционных) и их влияние на прогноз пациентов; оценить демографические, анамнестические и клинические характеристики пациентов, госпитализированных с декомпенсацией кровообращения; изучить назначаемые в стационаре препараты и приверженность пациентов рекомендациям.
Материал и методы
Регистр формировался на основе добровольности — личная инициатива врачей стационаров, подтвержденная коммуникацией в интернете; материальной независимости участников регистра; отсутствия отбора стационаров (в регистр включался любой стационар Российской Федерации, осуществляющий лечение пациентов с декомпенсацией кровообращения). Эти принципы позволяют считать регистр независимым. Исследование было одобрено этическим комитетом Российского национального исследовательского медицинского университета им. Н.И. Пирогова.

В регистре использовалась электронная индивидуальная регистрационная карта в формате excel либо бумажная версия. По результатам заполнения все типы индивидуальных карт добавлялись в единую базу, созданную на базе MS Access 2010. Окончательная версия индивидуальной регистрационной карты была доступна для скачивания с 02.09.2010 на сайте www.ingorts.ru (официальный электронный адрес исследования oracul@ingorts.ru).
Для статистической обработки полученных данных использовали программное обеспечение Statistica 10. Нормальность распределения определяли с помощью критерия Шапиро—Уилка. При изложении результатов пользовались методами непараметрической и параметрической статистики. Количественные показатели представлены в виде среднего (M)±стандартное отклонение (S) или медианы (25-й процентиль; 75-й процентиль). Проводили многофакторный анализ с помощью модели пропорциональных рисков Кокса. Анализ выживаемости оценивали с помощью метода Каплана—Мейера. Для построения прогностической шкалы применяли нейросетевое моделирование. Статистически значимыми признавали значения при р<0,05.
Дизайн исследования и критерии включения. Регистр формировался в 41 центре в 20 городах РФ. Спрогнозированная мощность исследования составила 2450 пациентов. Сроки выполнения: начало 02.09.2010, окончание набора по достижению необходимого числа пациентов 01.06.2011. Были набраны 2498 пациентов. Окончание периода наблюдения 01.06.2013. Наблюдение за пациентами осуществляли в течение одного года. После выписки из стационара осуществлялся визит или телефонный контакт на 30-й, 90, 180 и 360-й дни. После выписки учитывали частоту повторных госпитализаций и смертность, а также причины этих нежелательных исходов.

В регистр включали мужчин и женщин старше 18 лет:
- с симптомами застойной ХСН любой этиологии в период декомпенсации кровообращения, при которой требуется госпитализация;
- имеющих клинические признаки перегрузки объемом, что подтверждалось, по крайней мере, двумя из следующих признаков:
- а) одышка или положение ортопноэ;
- б) влажные хрипы в легких;
- в) периферические отеки;
- г) увеличение пульсации яремных вен;
- д) признаки застоя в малом круге кровообращения на рентгенограмме органов грудной клетки;
- е) содержание в плазме мозгового натрийуретического пептида (BNP) >150 пг/мл или его N-концевого предшественника (NT-proBNP) ≥450 пг/мл.
- желающих участвовать в регистре и подписавшие информированное согласие.
Результаты
 В исследование были включены 2498 пациентов. Окончательному анализу были доступны данные 2404 пациентов. Связь с 94 пациентами на постгоспитальном этапе была утеряна, что составило 3,76% от общего числа пациентов.
В исследование были включены 2498 пациентов. Окончательному анализу были доступны данные 2404 пациентов. Связь с 94 пациентами на постгоспитальном этапе была утеряна, что составило 3,76% от общего числа пациентов.
Данные, приведенные в табл. 1, свидетельствуют, что в популяции пациентов преобладали женщины (53%), а средний возраст пациентов указывал на превалирование пациентов старших возрастных групп. Следует отметить, что 49,7% пациентов были старше 70 лет. У 8 из 10 пациентов этиологической основой развития ХСН была артериальная гипертония и ишемическая болезнь сердца (ИБС). Каждый 6-й пациент имел дефицит тощей массы тела, более 10% от должной массы, дефицит тощей массы определялся при ИМТ<16 кг/м2, у каждого 8-го пациента уровень систолического артериального давления (САД) был ниже 110 мм рт.ст., а у каждого 5-го пациента уровень гемоглобина был ниже 110 г/л. Абсолютное большинство пациентов имели выраженную одышку и отеки нижних конечностей. Только у 39,6% фракция выброса (ФВ) была менее 30%. Выраженную тахикардию (более 100 уд/мин) имели 3/4 пациентов, у 23% пациентов отмечена хроническая болезнь почек (ХБП), выявленная по результатам расчета скорости клубочковой фильтрации (СКФ). Обращает на себя внимание высокий уровень сопутствующей инфекции — в день госпитализации в 17% случаев был поставлен диагноз пневмонии, суммарно за период пребывания в стационаре диагноз пневмонии был зафиксирован в 31% случаев. Преимущественно диагностировалась правосторонняя нижнедолевая пневмония, что соответствует наиболее частой зоне локализации гидроторакса, либо двусторонняя нижнедолевая пневмония, установленная по данным рентгенографии или клинической картины. У 2% пациентов с пневмонией потребовалось проведение искусственной вентиляции легких. У каждого третьего пациента имелось 3 заболевания и более. Таким образом, выраженная коморбидность стала доминирующей клинической характеристикой в популяции пациентов, госпитализированных по поводу декомпенсации кровообращения. В рамках одного из центров регистра ОРАКУЛ-РФ (ГКБ № 4, Москва) проводилась дополнительная оценка данных всех пациентов на соответствие критериям шкалы оценки тяжести декомпенсированных пациентов (модифицированная шкала Forrester [11]). Всего проанализировано состояние 195 пациентов, что соответствует примерно 8,79% от общей популяции регистра. Общепринятым критерием оценки общего состояния пациента является критерий «мокрый-холодный» и «теплый-сухой». Под терминами «мокрый», «сухой» подразумеваются явления застоя в легких или их отсутствие, под терминами «теплый», «холодный» — наличие или отсутствие признаков гипоперфузии на периферии. Комбинация «мокрый-холодный» соответствует неблагоприятному прогнозу. Этот признак отмечен у 31,8% пациентов в субпопуляции, т.е. у группы пациентов с фенотипом «мокрый-холодный» . Таким образом, в целом популяция пациентов характеризуется тяжелым течением заболевания и выраженной коморбидностью.
Данные, представленные в табл. 2, показывают, что только 3/4 всей популяции пациентов в момент госпитализации получали ингибиторы ангиотензинпревращающего фермента (АПФ) и β-адреноблокаторы. Важно отметить, что только у 1/3 пациентов, получавших лечение этими препаратами, врач осуществлял титрование дозы, так как 35—38% пациентов получали дозу препарата ≥50% от терапевтической. Суммарно ингибиторы АПФ и антагонисты рецептора ангиотензина II (АРА) получали 88,9%. Средняя доза спиронолактонов составила 83,5±65,0 мг; это позволяет предполагать, что в реальной клинической практике назначаются дозы, превышающие рекомендованные. Почти 80% пациентов получали петлевые диуретики (в их числе торасемид 9,2%), 12% — гидрохлоротиазид, доза которого составила 28,5±9,8 мг. В целом лечение соответствовало рекомендациям, однако индивидуальный подбор доз требует существенной коррекции.
 Повторные госпитализации. В течение 30 дней после выписки из стационара повторно (проанализированы данные 2196 пациентов) госпитализированы 686 (31%) пациентов. В течение 90 дней после выписки из стационара повторно госпитализирован 251 (11%) пациент. К 180-му дню число повторных госпитализаций составляло 246 (11%), к 360-му дню — 210 (9,5%).
Повторные госпитализации. В течение 30 дней после выписки из стационара повторно (проанализированы данные 2196 пациентов) госпитализированы 686 (31%) пациентов. В течение 90 дней после выписки из стационара повторно госпитализирован 251 (11%) пациент. К 180-му дню число повторных госпитализаций составляло 246 (11%), к 360-му дню — 210 (9,5%).
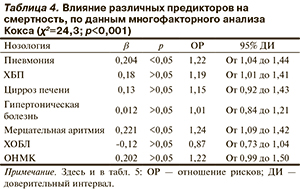
Общая смертность. Данные, представленные на рис. 1, свидетельствуют, что госпитальная смертность составила 9%. Самая высокая смертность наблюдалась в течение первых 30 дней после выписки. К 30-му дню наблюдения общая смертность составила 13%. Вероятность летального исхода была несколько выше у женщин в возрастной группе старше 60 лет, хотя и превышала этот показатель у мужчин — 19,4% против 16% (р>0,05). В течение 180 дней наблюдения умер каждый третий пациент, а в течение года общая смертность составила 43%. Наиболее выраженное негативное влияние на прогноз оказывали пневмония, дефицит тощей массы тела, стойкая гипотония и признаки застоя в обоих кругах кровообращения (табл. 3). Важно отметить, что эти параметры, анализируемые изолированно друг от друга, не оказывали достоверного влияния на смертность. Однако смертность при их наличии достигает 51%.
Среди проанализированных 16 параметров, отражающих коморбидный статус пациентов, наиболее значительное влияние на смертность оказывали параметры, приведенные в табл. 4. Наиболее выраженное влияние на риск смерти оказали пневмония и цирроз печени; летальность при пневмонии достигала 49,5%, при циррозе печени — 45,7%, что свидетельствует о большой роли данных заболеваний в структуре летальности у пациентов с декомпенсированной ХСН.
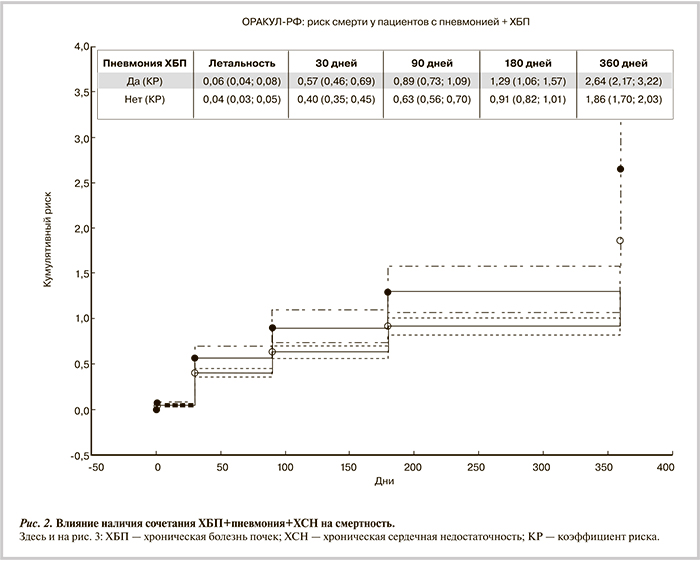
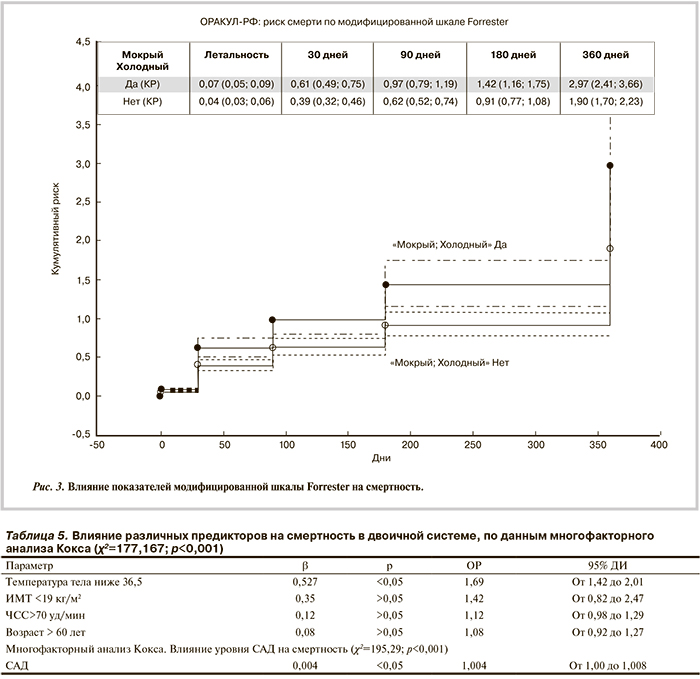
На третьем месте в структуре смертности оказалось ХБП (47,2%). На основании модели Кокса, в которую были включены клинически наиболее значимые факторы и состояния, оказавшие достоверное влияние на смертность пациентов с декомпенсацией кровообращения, были сформированы комбинации факторов, так называемые клинические фенотипы. Наиболее клинически значимыми оказались следующие фенотипы: цирроз печени+пневмония+декомпенсация кровообращения и ХБП+пневмония+декомпенсация кровообращения (рис. 2), повышающие риск смерти (отношение рисков — ОР 2,9 95% ДИ и ОР 2,64 [2,17; 3,22] соответственно). Клинический фенотип, соответствующий критериям «мокрый-холодный», также статистически значимо повышал риск смерти (ОР 2,9 95% ДИ [2,4; 3,6]). Самым неблагоприятным был клинический фенотип цирроз печени+пневмония+ХБП+декомпенсация кровообращения. Роль этого фенотипа представлена на рис. 3.
На основании проведенного статистического анализа была построена прогностическая шкала. В табл. 5 представлены клинически наиболее значимые факторы, оказавшие максимальное влияние на смертность. Клинически наиболее значимыми были снижение температуры тела ниже 36,5 °С, снижение САД менее 110 мм рт.ст. Менее выраженное, но клинически значимое влияние оказывали возраст старше 60 лет, частота сердечных сокращений (ЧСС) более 70 уд/мин и дефицит массы тела (индекс массы тела — ИМТ≤19 кг/м2).
Для определения прогностической ценности параметров было применено нейросетевое моделирование. В модель обучения были введены параметры, клиническая значимость которых была выявлена в ранее проведенном многофакторном анализе Кокса (см. табл. 5). Обучение проводилось на 75% выборки, 15% выборки составили контроль, а 15% — тренировочную выборку. После построения сетей была выбрана сеть с наилучшими результатами, по которой проводилось дальнейшее прогнозирование. По результатам нейронального анализа прогностическая ценность факторов выстроилась в следующем порядке убывания: возраст, ИМТ<19 кг/м2, снижение САД ниже 100 мм рт.ст., ЧСС>70 уд/мин, снижение температуры тела ниже 36,5 °С. Каждому предиктору был присвоен 1 балл, при оценке 5 баллов риск смерти приближался к 100%, шаг в 1 балл составляет 20% увеличения риска смерти.
Обсуждение
Результаты изучения выполненных в начале ХХI века крупных регистров, посвященных анализу проблемы декомпенсации кровообращения [1—10], внесли существенные коррективы в усредненный клинический «портрет» пациента с декомпенсацией кровообращения. Так, вопреки представлениям, сформированным 15—20 лет назад, в современной клинике значительно, до 50%, увеличилось число пациентов с сохраненной ФВ левого желудочка, превалируют женщины в возрасте 65 лет и старше. Важнейшей чертой современного клинического «портрета» пациента с декомпенсацией кровообращения является выраженная коморбидность, включающая помимо широко обсуждаемых артериальной гипертонии, сахарного диабета, ИБС, также хроническую обструктивную болезнь легких (ХОБЛ), ХБП, анемию, дефицит тощей массы тела, хронические и острые заболевания, обусловленные бактериальной инфекцией. Отмеченные тенденции имеют большое значение для реальной клинической практики, так как в контролируемые исследования включаются более молодые пациенты, преимущественно мужчины, и, как правило, с минимальным числом сопутствующих заболеваний. Регистр ОРАКУЛ-РФ в целом выявил те же тенденции в российской популяции: 53% пациентов — женщины, средний возраст составил 67±13 лет, а мода возраста — 72 года, средняя ФВ — 48±13% и только у 39,6% ФВ достигала 30% и менее. Однако в российской популяции выявлен ряд следующих клинически значимых отличий.
В большем, чем в цитируемых выше регистрах, числе случаев встречалась пневмония (17%). Для сравнения в Cardiovascular Health Study анализ данных 5880 пациентов старше 65 лет, находившихся под наблюдением более 10 лет, показал, что пневмония развилась у 10% пациентов с сердечно-сосудистой патологией, а сочетание ХСН и пневмонии, обусловившей необходимость госпитализации, повышало риск смерти в 4,9 раза [11,12]. В исследовании V. Kaplan [13] проанализированы данные 67 162 пациентов, госпитализированных по поводу декомпенсации ХСН, а группа сравнения была сформирована из пациентов без признаков ХСН (n=671 620). Сравнение групп показало, что наличие ХСН увеличивает риск развития пневмонии в 1,82 раза. Самый высокий риск отмечался у пациентов, получающих петлевые диуретики. Наблюдение за 5474 пациентами старше 55 лет в течение 12 лет (исследование NHANES I Epidemiologic Follow up Study) показало, что пневмония развивалась чаще всего у пациентов с недостаточностью кровообращения — 16%, онкологическими заболеваниями, сахарным диабетом и дефицитом мышечной массы. Таким образом, пневмония встречается у каждого 6-го пациента с декомпенсацией ХСН и у каждого 16-го со стабильным течением ХСН, а в российской популяции — примерно у каждого 3-го.
В регистре ОРАКУЛ-РФ риск смерти у пациентов с пневмонией возрастал статистически значимо больше (отношение шансов — ОШ 1,5 при 95% ДИ от 1,3 до 1,7), чем в регистре OPTIMIZE-HF, в котором наличие пневмонии приводило к увеличению риска смерти всего на 10,6% [5], или в мета-анализе V.F. Corrales-Medina (4215 пациентов), в котором увеличение риска смерти составило 23,9% (95% ДИ 16,9—32,6) [14].
Такой результат может быть объяснен только большей исходной коморбидностью и большей исходной тяжестью состояния российских пациентов.
Существенно чаще, чем в цитируемых регистрах, встречались пациенты с СКФ≤44 мл/мин. Число пациентов с СКФ≤60 мл/мин в цитируемых регистрах составляет 30—40% популяции [5, 15, 16] и только в одном исследовании [17] (4102 пациента с декомпенсацией кровообращения) поражение почек отмечено у 2145 (57%). В регистре ОРАКУЛ-РФ у 23% пациентов имелась СКФ≤60 мл/мин, из них у 37% — СКФ≤44 мл/мин. У 1906 пациентов, страдающих декомпенсацией кровообращения, в исследовании Second Prospective Randomized Study of Ibopamine on Mortality and Efficacy [18] была изучена частота летальных исходов в зависимости от СКФ. Анализ показал, что при СКФ≤60 мл/мин риск смерти возрастает, но только при низкой СКФ (≤44 мл/мин) отмечен статистически значимый рост риска смерти. В регистре ОРАКУЛ-РФ наличие ХБП значительно увеличивало риск смерти (ОШ 3,82 при 95% ДИ от 3,37 до 4,33). Таким образом, в популяции российских пациентов у 8% больных с декомпенсацией кровообращения имелась исходно низкая (≤44 мл/мин) СКФ, что кроме прогностического значения указывает на сложности в индивидуальном подборе мочегонной терапии.
У 16% (347 пациента), включенных в регистр, зафиксирована ХОБЛ, тогда как в регистре OPTIMIZE-HF — у 28%, в регистре ADHERE — у 31%. Эти данные свидетельствуют о гиподиагностике ХОБЛ врачами первичного звена здравоохранения. Наличие ХОБЛ в регистре ОРАКУЛ-РФ резко увеличивало риск смерти (ОШ 1,62 при 95% ДИ от 1,43 до 1,84), в регистре OPTIMIZE-HF ОР равнялся 1,19 при 95% ДИ от 1,04 до 1,35. Следует отметить, что 31% пациентов в этой группе не получали β-адреноблокаторов.
Впервые в рамках регистра проанализированы данные группы пациентов (n=61), получавших комбинированную ингаляционную терапию, включающую глюкокортикостероид и β2-агонист. В этой группе 57% пациентов не получали β-адреноблокаторов. Анализ 2 подгрупп — ХОБЛ с терапией β-адреноблокаторами и ХОБЛ без терапии β-адреноблокаторами — показал, что смертность составила соответственно 39 и 56% (p<0,05), а риск смерти был 38%. Общий риск смерти составлял 38%.
Цирроз печени зафиксирован у 8% пациентов. Следует отметить, что асцит и выраженный синдром задержки жидкости имелся только у 159 (44%) пациентов. Это позволяет предполагать значительную роль других этиологических факторов в развитии цирроза печени у пациентов с декомпенсацией кровообращения. Наличие цирроза печени статистически значимо повышало риск смерти (ОШ 1,9 95% ДИ 1,6–2,1); для сравнения в регистре OPTIMIZE-HF ОР составляло 2,33 95%ДИ [1,43—3,80].
Исходная ЧСС в среднем составила 87±21 уд/мин. При синусовом ритме пульса более 70 уд/мин увеличивался риск смерти, однако в диапазонах 90—100 уд/мин и 100—110 уд/мин смертность не различалась. Самый значительный прирост риска смерти отмечен в диапазоне 80—90 уд/мин. Для сравнения в исследовании ADHERE ЧСС≥78 уд/мин статистически значимо увеличивала риск смерти (ОШ 1,34 95% ДИ 1,20—1,49), причем этот эффект сохранялся независимо от величины ФВ. В регистре OPTIMIZE-HF повышение ЧСС на 10 уд/мин приводило к увеличению риска смерти (ОШ 1,09 при 95% ДИ от 1,062 до 1,127). Самый высокий риск смерти —39% — отмечен при ЧСС≥80 уд/мин у пациентов, подпадающих под характеристику «мокрый-холодный». У пациентов с IV функциональным классом с ЧСС больше 100 уд/мин риск смерти составлял 49% (ОШ 1,1 при 95% ДИ от 1,1 до 2,0).
Постоянная форма фибрилляции предсердий зафиксирована у 37% пациентов, что существенно больше, чем в других регистрах (до 31% в регистрах ADHERE и OPTIMIZE-HF). Наличие фибрилляции предсердий в регистре ОРАКУЛ-РФ статистически значимо влияло на смертность в течение года (ОШ 2,829 при 95% ДИ от 2,60 до 3,07).
Повторные госпитализации. С учетом того что на частоту повторных госпитализаций оказывает прямое влияние ряд факторов (индивидуальная приверженность лечению, качество медицинской помощи, семейное положение, уровень образования), исследовательская группа регистра сочла более корректным проанализировать этот параметр в первые 30 дней после выписки, когда влияние этих факторов минимально. В течение 30 дней после выписки из стационара (2196 пациентов) повторно были госпитализированы 686 (31%). Этот факт должен рассматриваться как самостоятельная проблема и требует отдельного углубленного анализа для ответа на вопрос, с чем связана повторная госпитализация каждого 5-го пациента.
Коморбидность. Анализ числа пациентов с декомпенсацией кровообращения на фоне еще 1, 2, 3 и более самостоятельных (не приведших к развитию декомпенсации кровообращения) заболеваний показал, что 3 заболевания и более имели 66% пациентов. Таким образом, у абсолютного большинства пациентов имелась выраженная коморбидность, что стало важнейшей отличительной чертой российской популяции. По сути, следует говорить о выраженной гетерогенности группы пациентов, объединенных понятием «декомпенсация кровообращения».
Традиционно анализ регистров построен по принципу связи одного или нескольких, как правило, лабораторных параметров с ростом риска смерти у пациентов с декомпенсацией кровообращения. Так, было установлено [20], что ишемический генез декомпенсации кровообращения в момент госпитализации приводил к росту летальности (3,7% против 2,9% у больных без ИБС) и смертности после выписки из стационара (10,6% против 6,9% у пациентов без ИБС). Анализ в рамках того же регистра OPTIMIZE-HF не выявил самостоятельного влияния величины ФВ (сохраненная ФВ и ФВ <40%) на частоту развития летальных исходов, т.е. величина ФВ не обладала самостоятельным прогностическим значением [20]. В рамках этого же регистра было проанализировано влияние на прогноз уровня натрия <135 ммоль/л на [21]. Было установлено, что гипонатриемия ухудшает прогноз болезни, повышая риск развития летального исхода. Так, риск смерти в стационаре и смерти после выписки из стационара возрастал соответственно на 19 и 10%, а риск развития комбинированного показателя смерть+повторная госпитализация — на 8% при снижении уровня натрия на каждые 3 ммоль/л ниже уровня 140 ммоль/л.
В рамках исследования EVEREST [22] была определена прогностическая роль продолжительности комплекса QRS на электрокардиограмме. Из 2962 пациентов, включенных в исследование, у 1321 длительность QRS была более 120 мс. Смертность в когорте больных с длительностью QRS менее 120 мс и более 120 мс составила 18,7 и 28,1% соответственно. Эта тенденция сохранялась до 9-го месяца после выписки пациента из стационара. Анализ клинической симптоматики у пациентов, включенных в исследование EVEREST [23], показал, что увеличение массы тела, наличие внешних признаков застоя и тахикардия являются неблагоприятными маркерами, увеличивающими вероятность смерти и повторной госпитализации. Так, из 635 повторных госпитализаций за 60 дней в исследовании EVEREST 184 случая зафиксированы у пациентов с прибавкой массы тела менее 2 кг, и 401 — у пациентов с прибавкой массы тела более 2 кг. В регистре ОРАКУЛ-РФ было проанализировано влияние на риск развития летального исхода следующих параметров, определяемых лабораторно или при физикальном обследовании: уровень гемоглобина ниже 110 г/л; дефицит тощей массы тела >10%; наличие асцита или анасарки; динамика уровня креатинина <0,3 мг/дл; уровень САД<100 мм рт.ст.; ИМТ>30 кг/м2; наличие признаков, характеризуемых термином «мокрый-холодный». Определено, что каждый из этих параметров, оказывая самостоятельное влияние, приобретает клинически значимое влияние только в конкретной клинической ситуации. Так, низкий уровень гемоглобина достоверно повышал риск смерти у пациентов с пневмонией и ФВ <30% (ОШ 1,69 при ДИ от 1,27 до 2,25); дефицит тощей массы тела — только у пациентов с выраженным застоем в малом круге кровообращения 9,2% к выраженному застою в малом круге (ОШ 1,45 при 95% ДИ от 1,28 до 1,64); рост уровня креатинина более 0,3 мг/дл только у пациентов с СКФ<44 мл/мин повышал риск смерти на 4,4%; наличие ИМТ>30 кг/м2 снижало риск смерти во всех клинических группах (ОШ 0,84 95% ДИ 0,76–0,92).
Эти данные еще раз подчеркивают гетерогенность группы пациентов с декомпенсацией кровообращения. Именно гетерогенность группы делает малоперспективной попытку прогнозирования исходов по отдельным параметрам. Клинически значимым нам видится другой подход, основанный не на комбинациях отдельных параметров, а на клинических фенотипах. Клинический смысл этого термина несколько отличается от общепринятого биологического — «фенотип формируется на основе генотипа, опосредованного рядом внешнесредовых факторов» — и предполагает, что это характерная комбинация таких признаков, которые описывают различия между пациентами с декомпенсацией кровообращения, связанные с клинически значимыми исходами (симптомы, обострения, ответ на терапию, скорость прогрессирования заболевания, смерть). Фенотипирование дает возможность формировать группы пациентов со сходными прогностическими, клиническими и иными характеристиками, что в повседневной практике врача позволяет быстро выбрать оптимальную тактику лечения. Количество сформированных фенотипов может быть огромным, но отличить фенотип, представляющий реальную значимость для повседневной практики от малозначимого, позволит анализ регистров. В рамках регистра ОРАКУЛ-РФ было изучено 16 клинических комбинаций. Комбинации включали в различных вариантах цирроз печени, ХБП, пневмонию, ХОБЛ, анемию, фибрилляцию предсердий, онкологические заболевания, дефицит тощей массы тела, ИМТ>30 кг/м2, другие бактериальные инфекции и ряд других параметров. Самыми неблагоприятными фенотипами оказались цирроз печени+пневмония+декомпенсация кровообращения и ХБП+пневмония+декомпенсация кровообращения. Риск смерти при этих фенотипах равен 61 и 73% соответственно.
Выводы
Больные, госпитализируемые в стационар в Российской Федерации по поводу декомпенсации ХСН, имеют существенно более тяжелое течение болезни: фракция выброса <40% в исследовании ОРАКУЛ-РФ встречалась в 1,89 раза чаще, чем в регистре Euro HS; существенно большее число больных соответствуют критерию «мокрый-холодный». Пациенты в Российской Федерации имеют меньшую фракцию выброса, меньшую скорость клубочковой фильтрации, бóльшую частоту сердечных сокращений и меньшую приверженность научно-обоснованному лечению.
Другой важной особенностью российской популяции является высокая частота встречаемости пневмоний в момент госпитализации пациента с декомпенсацией ХСН. Спектр бактериальной микрофлоры у этих пациентов не всегда соответствует классическому спектру внебольничной пневмонии — значительный процент в спектре микрофлоры занимает микрофлора, более типичная для больничной пневмонии. Вероятно, пневмония выступала в качестве пускового механизма декомпенсации и вносила значительный вклад в прогноз у этих пациентов относительно уровня летальности.
Ограничения исследования. В рамках исследования не проводился мониторинг исследовательских центров. Подлинность первичной информации подтверждалась врачом-исследователем. Исследование выполнялось в терапевтических и кардиологических отделениях и не затрагивало реанимационные отделения.
Благодарность. Исследовательская группа приносит искреннюю благодарность профессору С.А. Шальновой и профессору А.Д. Дееву за консультативную помощь в организации и проведении исследования.
Наблюдательный комитет. Академик РАН проф. А.И. Мартынов, академик РАН проф. Г.И. Сторожаков, академик РАН проф. В.С. Моисеев, проф. Н.А. Козиолова, проф. А.А. Спасский, проф. В.П. Терентьев, проф. А.И. Чесникова.
Исполнительный комитет. А.Г. Арутюнов, Д.Д. Пашкевич, Д.О. Драгунов, А. В. Соколова.
Исследовательские центры
Владивосток: Кулаков Ю.В. Приморская краевая клиническая больница №1.; Кулакова Н.В. КГБУЗ ПККБ №1; Волгоград: Деревянченко М.В., Инина Л.И., Соловьева О.Е., Стаценко М.Е. ГУЗ ГКБ №3; Волгоград: Лопатин Ю.М. ВОККЦ; Екатеринбург: Архипов М.В. Быков А.Н. ГБУЗ СО «СОКБ №1»; Иваново: Громова М.А., Мясоедова С.Е., Торкашова Е.В.; ГБОУ ОБУЗ ГКБ №4; Кемерово: Барбараш О.Л., Завырылина И.Н., Зверева Т.Н. ФГБУ НИИ комплексных проблем сердечно-сосудистых заболеваний СО РАМН; Краснодар: Павлищук С.А., Петрик Г.Г. ГБУЗ Краевая КБ №1;
Красноярск: Вырва П.В., Петрова М.М., Штегман О.А. Городская поликлиника №14; Красноярск: ККБ КГБУЗ Краевая больница; Курск: Безуглова Е.И., Крюкова С.В., Поветкин А.С., Поветкин С.В., Филиппенко Н.Г. ОБУЗ «Курская ГБ №1» им. Н.С. Короткова; Михин В.П., Прокопова Т.А., Сокаленко Н.П., Ченятина Н.А., Шевякина Т.В. МУЗ ГБ СМП.; Махачкала: Маммаев С.Н., Омарова Д.А., Магомедова П.М. Республиканская КБ; Москва: Арутюнов А.Г., Арутюнов Г.П., Былова Н.А., Витер К.В., Звонова Е.В., Пашкевич Д.Д. ГБУЗ ГКБ №4; Гордеев И.Г., Кокорин В.А., Орлова О.С. Суворова Н.А. ГКБ №15 им. О.М. Филатова; Хоткина Т.В. ГП №45.; Журавлева Н.В. ГБОУ ВПО РНИМУ «НКЦ Геронтологии»; Омск: Васильева Ю.С., Кореннова О.Ю., Петренко А.В. Клинический кардиологический диспансер; Евсеенко Е.К., Темникова Е.А. БУЗ ОО «Госпиталь для ветеранов войн»; Зайцева И.Г. МСЧ №4; Коринева О.Ю., Нечаева Г.И. ФГБУЗ ЗСМЦ ФМБА России; Петренко А.В. ГКБ №11; Ражева Н.Г. МСЧ №7.; Пермь. Козиолова Н.А. ГКБ №1; Пермь. Козлова Е.ВМСЧ 9 им. М.А. Тверье; Пермь: Лучникова Е.А., Щекотов В.В. ГБУЗ «Клиническая медико-санитарная часть № 1»; Ростов-на-Дону: Волкова Н.И. ГКБ №7, Б №4.; Джериева И.С. ГБ №4; Терентьев В.П., Хайло Н.В., Чесникова А.И. ГБУЗ Ростовской области «Областная клиническая больница №2»; Хайло Н.В. ОКБ №1; Рязань: Борисова М.В., Якушин С.С. Рязанский областной кардиологический диспансер; Саратов: Бородкин А.В., Ребров А.П., Яковлева Е.В. ГУЗ «Областная клиническая больница»; Майскова Е.А., Шварц Ю.Г. КБ им. С.Р. Миротворцева.; Ульяновск: Феофанова С.Г. ГУЗ УОКБ; Макеева Е.Р., Мензоров М.В., Страхов А.А. МБУЗ «ЦГКБ»; Уфа: Закирова А.Н., Шепель Р.Н. Кафедра клинической кардиологии ИПО БГМУ; Челябинск: Богданов Д.В., Кириллов А.М., Лебедев Е.В., Шапошников И.И. Челябинская городская клиническая больница №1; Шахты: Паневкина И.В. Муниципальное бюджетное учреждение здравоохранения «Городская больница скорой медицинской помощи им. В.И. Ленина»; Ярославль: ДКБ на станции Ярославль ОАО РЖД.; КБ №9.; Рыбачкова Ю.В., Хохлов А.Л. КБ №2.



