Введение. За последние два десятилетия робот-ассистированная радикальная простатэктомия (РАРПЭ) приобрела широкую популярность в мире в лечении локализованного рака простаты [1]. Благодаря ее малоинвазивности хирурги предпочитают РАРПЭ для улучшения качества жизни пациентов за счет снижения послеоперационного болевого синдрома без ущерба для онкологической безопасности. По сравнению с радикальной позадилонной простатэктомией (РППЭ) РАРПЭ показывает сходные онкологические результаты в отношении положительного хирургического края и биохимического рецидива [2]. Хотя хирургический опыт, а не непосредственно техника анастомоза может оказывать существенное влияние на частоту возникновения послеоперационных осложнений и восстановления эректильной и мочевыделительной функции [2–7], РАРПЭ связана с меньшей кровопотерей, длительностью катетеризации мочевого пузыря (МП) и меньшим сроком госпитализации [2, 8].
Помимо опыта хирурга предложены различные факторы, определяющие сохранение удержания мочи после РАРПЭ, такие как предоперационные характеристики пациентов и различия в хирургических методах. Среди них в последнее время в центре внимания находится задняя реконструкция (ЗР) уретровезикального анастомоза (УВА) [4, 7, 9–21]. Обоснование ЗР состоит в том, чтобы восстановить длину уретрального сфинктерного комплекса (УСК), предотвратить его каудальную ретракцию, избежать чрезмерного натяжения пузырно-уретрального анастомоза и обеспечить заднюю поддержку для УСК, чтобы облегчить его эффективное сокращение [3, 21]. В то время как некоторые исследования продемонстрировали клинические преимущества ЗР в восстановлении удержания мочи, другие оспорили данное предположение, поскольку не наблюдали улучшения функциональных результатов [2, 4].
Еще один параметр, который может влиять на качество формирования герметичного анастомоза без натяжения, – это использование оптимального шовного материала. Однонаправленные нитки с насечками, в отличие от обычных монофиламентных нитей, недавно показали, что могут сокращать время операции и длительность формирования анастомоза и задней реконструкции [22–25].
Таким образом, цель настоящего исследования – оценить функциональные результаты раннего удаления уретрального катетера (через 3 дня) после РАРПЭ с использованием модифицированной хирургической техники задней реконструкции УВА по сравнению со стандартным сроком удаления катетера (через 7 дней после операции).
Материалы и методы. Дизайн исследования. В исследование были включены 30 мужчин, которым была проведена РАРПЭ на базе Института урологии и репродуктивного здоровья человека Сеченовского Университета. Критерием включения был локализованный рак простаты (сТ1с–Т2с). Критериями невключения – стриктуры уретры, предшествовавшие операции на простате, нейрогенные нарушения мочевого пузыря, лучевая терапия на область малого таза и длительная катетеризация мочевого пузыря до операции. Пациенты случайным образом были разделены на две группы по 15 человек: группа раннего удаления уретрального катетера (через 3 дня после РАРПЭ, основная группа) и группа стандартного удаления уретрального катетера (через 7 дней после РАРПЭ, контрольная группа). Пациентам основной группы была выполнена ретроградная цистограмма через 3 дня после РАРПЭ. Если экстравазации контрастного вещества не было обнаружено, уретральный катетер удаляли, после чего пациенты наблюдались в больнице в течение суток. Если на цистограмме обнаруживалась экстравазация контрастного препарата, катетеризацию мочевого пузыря пролонгировали и цистограмма повторялась через 7 дней после операции. В группе контроля пациентам проведена цистограмма через 7 дней после РАРПЭ.
Хирургическая техника. Все операции выполнены одним хирургом на системе Da Vinci Si в конфигурации с четырьмя руками и с трансперитонеальным доступом [26]. С помощью 23-сантиметровой нити с насечками V-Loc 3-0 на игле 5/8 первый слой УВА создан путем соединения пересеченной мышечно-фасциальной пластинки (рабдосфинктера) позади уретры с рассеченным краем фасции Денонвилье. Второй слой УВА формировался путем прошивания мышечного слоя мочеиспускательного канала и детрузора на расстоянии около 1–1,5 см кзади от шейки мочевого пузыря без вовлечения слизистой оболочки [28]. В результате достигалось меньшее натяжение тканей при сопоставлении слизистых и формировании анастомоза между шейкой мочевого пузыря и уретрой. Далее формировался непосредственно уретровезикальный анастомоз. Мочевой пузырь был дренирован катетером Фоли № 20 Ch, баллон которого заполнялся 15 мл изотонического раствора хлорида натрия. Герметичность анастомоза проверяли путем введения по катетеру 150 мл изотонического раствора хлорида натрия.
Сбор информации. Данные были собраны проспективно, включая следующие характеристики пациентов: возраст, уровень простатспецифического антигена (ПСА) в крови, объем простаты, балл по ISUP (International Society of Uropatologists – гистологическая прогностическая классификация РПЖ Международной ассоциации уропатологов), группа риска D’Amico, используемая для оценки вероятности прогрессирования заболевания после проведенного радикального лечения. Собранные периоперационные данные включали время операции, предполагаемую кровопотерю, интра- и послеоперационные осложнения, сохранение сосудисто-нервных пучков (СНП), время катетеризации мочевого пузыря и пребывание в стационаре. Осложнения оценивались по классификации Clavien–Dindo. Влияние недержания мочи на качество жизни после операции определяли с помощью опросника ICIQ UI-SF через 1, 3, 6 и 12 мес. после операции. Уровень недержания мочи оценивали по количеству используемых урологических прокладок через 1, 3, 6 и 12 мес. после оперативного вмешательства.
Статистический анализ. Непрерывные переменные были представлены как медиана и межквартильный диапазон. Сравнение дооперационных и послеоперационных исходов оценивали с помощью критерия согласия Пирсона, U-критерия Манна–Уитни, t-критерий Уэлча, t-критерий Стьюдента, p<0,05 считался статистически достоверным. Все статистические тесты проводились с помощью программного обеспечения StatTech v. 2.4.1.
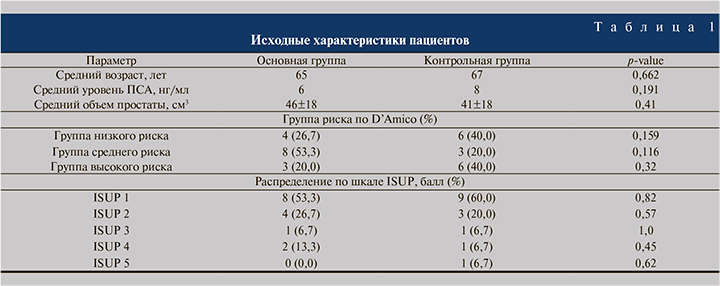
Результаты. В табл. 1 представлены исходные характеристики пациентов. Между двумя группами статистически значимых различий выявлено не было.
Продолжительность операции в основной группе составила 144±27 мин по сравнению с 128±23 в контрольной группе (р=0,101). Объем кровопотери в основной и контрольной группах составил 141,4±62,2 и 160,9±75,1 (р=0,151). Не было выявлено статистически значимой разницы в частоте сохранения СНП (р=0,964) и выполнения регионарной лимфаденэктомии (р=0,85).
Следует отметить, что при сравнении между группами продолжительности катетеризации мочевого пузыря и продолжительности госпитализации пациентов выявлены существенные различия в пользу основной группы (через 3 дня по сравнению с удалением катетера через 7 дней; p<0,001).
Периоперационные параметры, такие как длительность оперативного вмешательства, частота лимфодиссекции, сохранения СНП и кровопотеря, не различались между группами. В табл. 2 показано среднее количество используемых пациентами урологических прокладок в течение суток после РАРПЭ через 1, 3, 6 и 12 мес. Статистических различий между группами выявлено не было. Результаты анкетирования пациентов с помощью опросника ICIQ UI-SF через 1, 3, 6 и 12 мес. описаны в табл. 3. Также следует отметить, что ни у кого из пациентов не было острой задержки мочи после удаления уретрального катетера.

При анализе осложнений по классификации Clavien– Dindo I степени в зависимости от группы не было выявлено статистически значимых различий. У одного пациента из каждой группы отмечена лихорадка выше 380С, у пациента основной группы выявлено лимфоцеле и еще у одного пациента из контрольной группы отмечена динамическая кишечная непроходимость. Осложнений Clavien–Dindo II степени не отмечено ни в одной группе.
Обсуждение. В данной статье сообщается о проспективном рандомизированном исследовании, оценивающем результаты после раннего удаления катетера после РАРПЭ с использованием модифицированной техники ЗР УВА пациентами с локализованным раком простаты. Продемонстрированы хорошие краткосрочные функциональные результаты после удаления катетера через 3 дня после операции, аналогичные результатам после удаления катетера через 7 дней. В частности, отсутствовало увеличения частоты затека мочи, негативное воздействие на удержание мочи в раннем послеоперационном периоде, также не наблюдалось повышения частоты задержки мочи. С учетом значительного дискомфорта, связанного с длительностью катетеризации мочевого пузыря, его удаление уже через 3 дня после операции может иметь значительные клинические преимущества с точки зрения послеоперационного качества жизни.
За последние десятилетия функциональные результаты радикальной простатэктомии значительно улучшились вследствие расширения знаний об анатомии предстательной железы, сфинктера мочевого пузыря, рабдосфинктера, пубопростатических связок, дорсального венозного комплекса и внутритазовой фасции [3]. С учетом трехмерноего изображения, увеличения и большой степени свободы движения инструментов теоретически робот-ассистированный подход может способствовать дальнейшему улучшению функциональных результатов оперативного лечения рака простаты. Однако недавние результаты исследований продемонстрировали противоречивые данные и поставили под сомнение предположение, согласно которому роботассистированная хирургия приводит к лучшим функциональным результатам. В систематическом обзоре Ficarra et al. [3] показали, что удержание мочи после РАРПЭ зависит от различных факторов, таких как характеристики пациента до операции (особенно возраст), опыт хирурга, хирургическая техника и методы, используемые для сбора и представления данных. Показано небольшое, но значительное преимущество РАРПЭ по сравнению с РППЭ и лапароскопической радикальной простатэктомией в сохранении удержания мочи. Однако совсем недавно бельгийская группа ученых обнаружила значительные преимущества РАРПЭ по сравнению с РППЭ. Среднее время восстановления полного удержания мочи составило 16 и 46 дней в группах РАРПЭ и РППЭ соответственно. Также пациенты в группе РАРПЭ имели значительно лучшие показатели по шкале IPSS (International Prostate Symptom Score – Международная шкала симптомов простаты) через 1 (р=0,013) и 3 (р=0,038) мес. Через 12 мес. после операции 96 и 97% мужчин полностью удерживали мочу после РППЭ и РАРПЭ соответственно [27].
Независимо от различий между открытыми и минимально инвазивными подходами растет объем знаний об интраоперационных факторах, способствующих после-операционному удержанию мочи. Сохранение важных анатомических структур, таких как шейка мочевого пузыря, СНП, пубопростатическая связка и длинная культя уретры, по-видимому, имеет первостепенное значение и связано с улучшением удержания мочи после РАРПЭ [4]. Кроме того, реконструкция рабдосфинктера может быть ключевым фактором улучшения удержания мочи. Мышечно-фасциальная пластинка и фасция Денонвилье, по всей видимости, действуют как сложная система, которая помогает поддерживать простатическо-мембранозный отдел уретры. Восстановление этих анатомических структур после удаления простаты представляется логичным, чтобы сохранять максимальную длину культи уретры и избегать ненужного натяжения уретровезикального анастомоза. Данная концепция была первоначально предложена Rocco et al. в 2006 г. [12]. Однако в недавнем систематическом обзоре показано, что ЗР УВА улучшает восстановление недержания мочи первые 30 дней после РПЭ, но не через 90 дней [13]. В настоящее время продолжаются рандомизированные исследования, цель которых оценить значимость данной хирургической техники ЗР.
В данном исследовании использована модифицированная методика ЗР, которая подразумевает выполнение уретроцистоанастомоза с использованием швов с насечками [28]. Несостоятельность анастомоза не наблюдалась ни у одного из пациентов. В то время как только у 33,3% пациентов было восстановлено полное удержание мочи сразу после удаления катетера, при среднем периоде наблюдения в 6 мес. восстановление удержания мочи составило 86,7 и 80% в основной и контрольной группах соответственно, а стриктура анастомоза, потребовавшая оперативного вмешательства, не возникла ни у одного из пациентов. Разница в количестве используемых урологических прокладок через 1, 3, 6 и 12 мес. после операции не была статистически значимой между группами. В данном исследовании нашей целью было оценить состоятельность УВА и восстановление удержания мочи при раннем удалении уретрального катетера (через 3 дня после РАРПЭ) и сравнить результаты со стандартным удалением катетера (через 7 дней после РАРПЭ). Обе группы продемонстрировали хорошие показатели удержания мочи. Тот факт, что не было случаев задержки мочи и несостоятельности уретроцистоанастомоза, подтверждает предположение, согласно которому удаление катетера через 3 дня после РАРПЭ после операции является безопасной манипуляцией. При оценке влияния недержания мочи на качество жизни с помощью опросника ICIQ UI-SF не было выявлено статистически значимой разницы между группами. Предполагается, что раннее удаление уретрального катетера не окажет негативного влияния на качество жизни пациента.
Хотя РАРПЭ, по-видимому, приводит к аналогичным функциональным результатам по сравнению с РППЭ через 6 мес. и более после оперативного вмешательства, удаление катетера в раннем послеоперационном периоде (через 3 дня после РАРПЭ) может приводить к значительному улучшению качества жизни пациентов. Поскольку статистически значимой разницы по частоте сохранения СНП в обеих группах выявлено не было, маловероятно, что выполнение нервосбережения оказало значительное влияние на результат.
Заключение. Представленные данные подтверждают, что ЗР УВА, включая пузырно-уретральный анастомоз во время РАРПЭ, является безопасным и эффективным хирургическим приемом при выполнении РАРПЭ в лечении пациентов с локализованным раком простаты. Данные показывают хорошие результаты при удалении катетера через 3 дня после РАРПЭ без увеличения частоты затека мочи, отрицательного воздействия на удержание мочи и повышения частоты задержки мочи по сравнению со стандартным удалением катетера через 7 дней после операции. Необходимы дальнейшие более крупные рандомизированные исследования для подтверждения представленных результатов с более длительным периодом наблюдения.



