Введение. На сегодняшний день доброкачественная гиперплазия предстательной железы (ДГПЖ) является урологическим заболеванием, при котором хирургическое вмешательство – наиболее эффективный метод лечения. По поводу ДГПЖ предложена масса методов оперативных вмешательств. С учетом современных минимально инвазивных радикальных операций и паллиативных процедур их число превышает 20 [1].
В историческом аспекте на протяжении длительного времени единственным эффективным методом лечения ДГПЖ выступала открытая аденомэктомия простаты (ОАЭП). Надлобковая, или трансвезикальная (чреспузырная), открытая аденомэктомия была впервые выполнена в 1894 г. Юджином Фуллером и получила широкое распространение после публикации трудов Питера Фрейера (1900) [2]. По рекомендациям Европейской ассоциации урологов (ЕАУ), открытая аденомэктомия представляет собой наиболее инвазивный и в то же время наиболее эффективный метод лечения ДГПЖ с длительным сохранением эффекта [3]
После внедрения эндоскопической трансуретральной резекции простаты (ТУРП) данная методика последние 40 лет остается «золотым» стандартом хирургического лечения ДГПЖ. Она приводит к значимому улучшению качества мочеиспускания и жизни пациента [4]. Тем не менее и ТУРП может сопровождаться различными осложнениями, самыми грозными среди которых являются кровотечение и ТУР-синдром. Число и тяжесть этих осложнений находятся в прямой зависимости от объема железы.
Постоянно существующая необходимость в совершенствовании хирургии ДГПЖ служит отправной точкой прогресса новых технологий и, соответственно, появления новых методов оперативного лечения. Стремление к совмещению радикальности ОАЭП с малоинвазивностью эндоурологических вешательств открыли широкую дорогу для различных вариантов эндоскопической энуклеации простаты (ЭЭП). В 1998 г. появилась принципиально новая методика HoLEP (Holmium Laser Enucleation of the Prostate) – гольмиевая лазерная энуклеация простаты.
Важной вехой в становлении процедуры HoLEP стало создание и использование морцеллятора в 1996 г. Именно благодаря морцелляции – удалению крупных фрагментов ткани посредством их предварительного измельчения в мочевом пузыре – через канал небольшого диаметра стало возможным создание той полноценной гольмиевой лазерной энуклеации [5], которую некоторые авторы называют новым «золотым» стандартом хирургического лечения ДГПЖ [6].
Тем не менее в ряде стран в тех центрах, где отсутствует необходимое оборудование либо эндоурологические методики находятся на стадии освоения, открытая аденомэктомия остается востребованной и необходимой опцией оперативного лечения ДГПЖ. В соответствии с Рекомендациями ЕАУ от 2021 г. [3] ОАЭП необходимо предлагать пациентам с объемом простаты >80 см3 и СНМП умеренной или тяжелой степени в том случае, если отсутствует возможность выполнения биполярной трансуретральной энуклеации простаты или гольмиевой лазерной энуклеации простаты.
Кроме того, открытая операция может оказаться необходимой в любых урологических центрах при сочетании ДГПЖ с другими урологическими патологиями заболеваний нижних мочевыводящих путей, например при камнях или дивертикуле мочевого пузыря [7,8].
После любого оперативного вмешательства возможно развитие осложнений той или иной степени тяжести. До сих пор среди врачебного сообщества, в том числе и среди урологов, нет единого мнения, как правильно определять осложнения и оценивать их тяжесть по единой системе. Это затрудняет надежные и воспроизводимые сравнения различных методов лечения в одном центре, внутри центра в динамике с течением времени, а также идентичных методов лечения между центрами, использующими аналогичные или разные подходы. Следовательно, необходима стандартизированная классификация осложнений, предлагающая общую платформу для взаимодействия урологов.
В Узбекистане за последние годы в разных государственных медицинских центрах и частных клиниках наравне с выполнением традиционной ОАЭП активно внедряются и высокотехнологичные малоинвазивные эндоскопические методы хирургического лечения ДГПЖ. Одновременное существование и использование на практике различных методов хирургического лечения одного и того же заболевания как в нашей республике, так и во многих других странах говорит о сложности и до сих пор нерешенности оптимального хирургического метода лечения данного заболевания. Это зависит в свою очередь от различных причин, одна из которых – отсутствие объективной оценки качества хирургических методов.
Классификация Clavien-Dindo для систематизации послеоперационных осложнений применима ко всем видам хирургических вмешательств, так как она по своей логике универсальна [9, 10]. Однако данная классификации применима к различным методам хирургического лечения ДГПЖ только после ее адаптации с учетом специфики метода.
При выполнении как открытых, так и малоинвазивных вмешательств по поводу ДГПЖ даже опытными хирургами нередко наблюдаются осложнения как легкой, так и тяжелой степеней тяжести. Тяжелые осложнения могут оказаться угрожающими жизни, а легкие, изматывающие пациента, нарушают качество его жизни длительное время даже после избавления от инфравезикальной обструкции (ИВО). Все это необходимо регистрировать и проводить мониторинг осложнений. Следовательно, важно внедрение единой системы оценки качества вмешательств, которая должна быть принята урологическим сообществом.
Целью данного исследования стала адаптация классификации Clavien-Dindo к оценкам послеоперационных осложнений хирургического лечения ДГПЖ, оценка эффективности и безопасности различных хирургических методов лечения ДГПЖ путем систематизации послеоперационных осложнений.
Материалы и методы. В соответствии с поставленной задачей нами ретрои проспективно были изучены результаты вмешательств в отношении 150 пациентов, оперированных по поводу ДГПЖ.
Пациенты были распределены на три группы в зависимости от метода хирургического лечения гиперплазии простаты. Первую группу составили 40 (26,7%) больных, которым была выполнена HoLEP (период освоения нового метода). Вторую группу – 50 (33,3%) пациентов, которым выполнена трансуретральная моно(26 пациентов) и биполярная (24 пациента) электрорезекция предстательной железы. Третью группу составили 60 (40%) больных, которым была выполнена открытая чреспузырная аденомэктомия простаты (ОАЭП), при этом гемостаз осуществлялся путем тампонирования ложа аденомы.
Пациенты первой группы были прооперированы в Республиканском специализированном научно-практическом медицинском центре урологии Ташкента (РСНПМЦУ), второй и третьей групп – в Самаркандском филиале Республиканского научного центра экстренной медицинской помощи (СФ РНЦЭМП). Все операции были выполнены опытными хирургами с многолетним стажем работы в данной области.
Для адаптации классификации к оценке послеоперационных осложнений хирургического лечения ДГПЖ и в последующем для систематизации осложнений мы использовали усовершенствованную классификацию хирургических осложнений Clavien-Dindo [11].
Эффективность проведенного хирургического лечения оценивалась на основе показателей шкалы IPSS и качества жизни (QoL), максимальной скорости потока мочи (Qmax), объема простаты (Vпр) и объема остаточной мочи (ООМ). Все перечисленные параметры определялись до операции, а также в сроки через 1, 3 и 6 мес. после операции.
Для корректной оценки предоперационного физического статуса пациента использовали классификацию Американского общества анестезиологов (ASA – American Society of Anesthesiologists physical status classification system) [12].
Результаты, полученные в ходе исследования, были подвергнуты статистической обработке. Математический анализ полученных данных проведен на персональном компьютере с использованием программы Microsoft Excel, 2019. Применялись критерии Стьюдента, Фишера. Статистически значимыми считали различия при p<0,05.
Результаты. Первым шагом для унификации данной классификации мы сочли необходимым создать единый стандарт послеоперационного течения хирургического лечения ДГПЖ. По нашему мнению, созданный единый стандарт (нормальное течение) послеоперационного периода как для ОАЭП, так и для малоинвазивных методов хирургического лечения ДГПЖ, позволит объективно оценить качество хирургического вмешательства по поводу ДГПЖ и выявить недостатки того или иного метода лечения.
Исходя из многолетнего опыта наших клиник в лечении ДГПЖ и послеоперационного ведения пациентов, мы унифицировали критерии неосложненного послеоперационного течения:
- незначительное (неинтенсивное) окрашивание мочи кровью по уретральному катетеру и/или цистостоме;
- отсутствие сгустков крови, нарушающих функцию дренажей, требующих дополнительной инфузионной (более 1 л), диуретической терапии и назначения гемостатиков;
- постоянное капельное промывание мочевого пузыря до 36 ч после оперативного вмешательства;
- повышение температуры тела пациента до 37,9°С без озноба в течение не более 48 ч, не требующее жаропонижающей инфузионной терапии (более 1 л);
- нахождение интраоперационно установленного гемостатического уретрального катетера от 12 до 72 ч (по решению хирурга) без развития инфекционно-воспалительного процесса в мочевыводящих путях (МВП) и потребности в дополнительных вмешательствах;
- нахождение цистостомического дренажа до 5 сут. после оперативного вмешательства;
- преходящее недержание мочи сроком до 1 мес. в отсутствие инфекции МВП.
Учтя созданные нами критерии стандартного течения послеоперационного периода хирургического лечения ДГПЖ, мы определились с той границей, где нормальное неосложненное течение послеоперационного периода может перейти в осложненное течение и, исходя из созданной нами картины, определились с критериями осложненного послеоперационного течения хирургического лечения ДГПЖ. При этом мы учитывали степень их тяжести, а также дополнительные консервативные и инвазивные вмешательства, потребовавшиеся для их ликвидации, приводя в соответствие со смыслом каждой из 5 степеней классификации Clavien-Dindo, табл. 1.

На наш взгляд, особенно сложна оценка легких – I и II степеней – осложнений и проведение между ними границы, исходя из нарастания их тяжести. По этой причине создание стандарта (нормы) послеоперационного периода играет важную роль в проведении границы между относительно легкими осложнениями, которые на практике устраняются консервативно.
Анализ послеоперационного периода первой группы пациентов, которым выполнена была HoLEP, отклонение от нормального послеоперационного периода наблюдали в 28 (70%) наблюдениях, которые сочли как осложненное течение.
Наличие осложнений I степени мы расценили в 8 (28,6%) наблюдениях из 28 и включили:
- 2 наблюдения острой задержки мочи после удаления уретрального катетера;
- 6 наблюдений однодневной лихорадки выше 38°C или фебрильной лихорадки (37-38°C) более 2 сут., потребовавших назначения жаропонижающих препаратов.
Наличие осложнений II степени мы расценили в 16 (57,1%) наблюдениях из 28 и включили:
- 3 наблюдения интенсивного окрашивания кровью мочи, поступающей по уретральному катетеру и/или цистостоме, гиповолемии вследствие кровотечения, потребовавших назначения гемостатиков и/или дополнительной инфузионной терапии;
- 1 наблюдение кровотечения, потребовавшее выполнения гемотрансфузии;
- 2 наблюдения затрудненного мочеиспускания, потребовавших дополнительной консервативной терапии альфаадреноблокаторами и противовоспалительными препаратами;
- 2 наблюдения потребности в анальгетиках более 72 ч после операции;
- 8 наблюдений обострения инфекционно-воспалительного процесса в мочевых путях (1 – острый простатит, 7 – острый уретрит).
Наличие осложнений IIIа-степени мы расценили в 3 (10,7%) наблюдениях из 28:
- 2 наблюдения, потребовавших проведения лечебно-диагностической уретроцистоскопии;
- 1 наблюдение гастродуоденального кровотечения, потребовавшее выполнения эндоскопического гемостаза.
Наличие осложнений IIIb-степени отмечено в 1 (3,6%) наблюдении:
- 1 наблюдение тампонады мочевого пузыря, потребовавшее выполнения цистоскопии и с отмыванием сгустков крови из мочевого пузыря, которая была выполнена под спинномозговой анестезией.
Осложнений IVа-степени выявлено не было. V степень – летальных исходов не отмечено.
Таким образом, всего наблюдали 28 (70%) осложнений у 20 (50%) пациентов. Из всех осложнений 24 (85,7%) оказались относительно легкими, они были ликвидированы консервативно. Для ликвидации 4 (14,3%) осложнений потребовались инвазивные вмешательства, одно из них под общей анестезией.
Эффективность данного оперативного вмешательства представлена в табл. 2.

Анализ результатов лечения второй группы пациентов показал, что частота осложнений между монополярной ТУРП (мТУРП) и биполярной ТУРП (бТУРП) статистически не различалась, по этой причине мы их рассматриваем вместе. Среди 50 пациентов всего наблюдали 41 (82,0%) осложнение (табл. 3).
Наличие осложнений I степени имело место в 16 (39%) наблюдениях из 41 и включали:
- 2 наблюдения острой задержки мочи после удаления уретрального катетера;
- 1 наблюдение выделения мочи по надлобковому свищу после удаления цистостомического дренажа;
- 1 наблюдение нахождения цистостомического дренажа длительностью более 5 сут.;
- 11 наблюдений нахождения уретрального катетера длительностью более 72 ч;
- 1 наблюдение пареза кишечника, потребовавшее дополнительных лекарственных средств.
Наличие осложнений II степени имело иесто в 17 (41,5%) наблюдениях:
- 10 наблюдений, потребовавших назначения гемостатиков и/или дополнительной инфузионной терапии, и/или кровезаменителей;
- 2 наблюдения кровотечения, потребовавших выполнения гемотрансфузии;
- 1 наблюдение потребности в анальгетиках в течение более 72 ч после операции;
- 4 наблюдения обострения инфекционно-воспалительного процесса в мочевыводящих путях (уретрит).
Наличие осложнений IIIа-степени выявлено в 1 (2,4%) наблюдении:
- 1 наблюдение обильного выделения мочи из надлобкового свища после удаления цистостомы, потребовавшее установки уретрального катетера;
Наличие осложнений IIIb-степени выявлено в 7 (17,1%) наблюдениях:
- 3 наблюдения тампонады мочевого пузыря (3-цистоскопия с отмыванием сгустков крови из мочевого пузыря);
- 2 наблюдения стриктуры задней части уретры (поздние осложнения);
- 2 наблюдения склероза шейки мочевого пузыря (поздние осложнения).
Осложнений IVa, IV b и V степеней отмечено не было.
Таким образом, после ТУРП из всех осложнений 33 (80,5%) оказались относительно легкими, которые были ликвидированы консервативно. Для ликвидации 8 (19,5%) осложнений потребовались инвазивные вмешательства, (17,1%) из них под общей анестезией.
Анализ результатов лечения третьей группы пациентов, оперированных методом ОАЭП, показал наибольшее число осложнений (154; 256,6%) при систематизации послеоперационных осложнений у 60 пациентов (табл. 4).
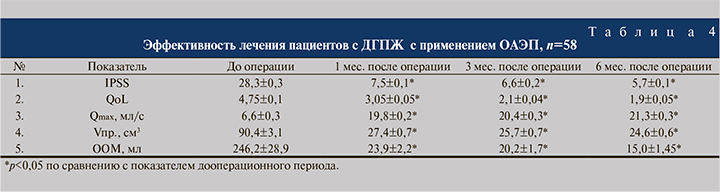
Наличие осложнений I степени имело место в 89 (57,8%) наблюдениях из 154 и включало:
- 3 наблюдения острой задержки мочи после удаления уретрального катетера;
- 1 наблюдение однодневной лихорадки выше 38°C или фебрильной лихорадки (37-38°C) в течение более 2 сут., потребовавшее назначения жаропонижающих препаратов;
- 5 наблюдений пареза кишечника, потребовавших назначения дополнительных медикаментозных средств;
- 9 наблюдений выделения мочи мимо цистостомического дренажа длительностью до 2 сут.;
- 2 наблюдения преходящего повышения уровня креатинина;
- 1 наблюдение тошноты, однократной рвоты;
- 2 наблюдения необходимости лечения раневой инфекции;
- 6 наблюдений нахождения цистостомического дренажа в течение более 5 сут.;
- 60 наблюдений нахождения уретрального катетера в течение более 72 ч;
Наличие сложнений II степени имело место в 48 (31,2%) наблюдениях:
- 15 наблюдений кровотечения (интенсивного окрашивания кровью мочи, поступающей по уретральному катетеру и/или цистостоме, гиповолемии вследствие кровотечения), потребовавшего назначения гемостатиков и/или дополнительной инфузионной терапии, и/или кровезаменителей;
- 4 наблюдения кровотечения, потребовавшего выполнения гемотрансфузии;
- 12 наблюдений потребности в анальгетиках в течение более 72 ч после операции;
- 1 наблюдение назначения наркотических анальгетиков в связи с перенесенным вмешательством;
- 6 наблюдений обострения инфекционно-воспалительного процесса в мочевыводящих путях (2 – острый пиелонефрит, 2 – цистит, 2 – орхоэпидидимит);
- 3 наблюдения выделения мочи мимо цистостомического дренажа в течение более 2 сут.;
- 1 наблюдение мочевого затека в мошонку;
- 6 наблюдений обострения хронических сопутствующих заболеваний или развившихся после перенесенного наркоза (1 – бактериальный конъюнктивит, 3 – обострение хронического бронхита, 2 – гипоксическая энцефалопатия с развитием психоза).
IIIа-степень осложнений выявлена в 9 (5,8%) наблюдениях:
- 1 наблюдение подтекания мочи после удаления цистостомы, потребовавшего рекатетеризации уретральным катетером;
- 2 наблюдения инфравезикальной обструкции из-за сгустков крови, потребовавшей промывания мочевого пузыря и дренажных трубок;
- 1 наблюдение нефункционирующей цистостомы, потребовавшей промывания мочевого пузыря и дренажных трубок;
- 1 наблюдение частичной непроходимости уретральных дренажей, потребовавшей рецистостомии (без анестезии, по старому ходу);
- 2 наблюдения тампонады мочевого пузыря (1 – выполнение цистоскопии; 1 – промывание мочевого пузыря под местной анестезией);
- 1 наблюдение эрозивного гастрита, по поводу которого была выполнена эзофагогастродуоденоскопия;
- 1 наблюдение стойкого пареза кишечника, потребовавшего установки газоотводной трубки.
Осложнения IIIb степени отмечены в 3 (1,95%) наблюдениях:
- 2 стриктуры задней части уретры+камни мочевого пузыря (позднее осложнение);
- 1 наблюдение склероза шейки мочевого пузыря (позднее осложнение).
IVа-степень осложнений выявлена в 3 (1,95%) наблюдениях:
- 2 наблюдения сердечно-сосудистой недостаточности;
- 1 наблюдение ишемического инсульта.
V степень – умерли 2 (1,3%) пациента: в 1 случае смерть наступила в результате острой сердечно-сосудистой недостаточности (ССН), в 1 – вследствие ишемического инсульта (острого нарушения мозгового кровоснабжения – ОНМК).
Таким образом, из всех осложнений 137 (89%) оказались относительно легкими, которые были ликвидированы консервативно. Для ликвидации 12 (7,8%) осложнений потребовались дополнительные инвазивные вмешательства, 5 пациентам потребовалось нахождение в отделении интенсивной терапии, из них 2 (1,3%) пациента умерли из-за ССН и ОНМК.
Сравнительная оценка частоты и тяжести осложнений после трех различных методов хирургического лечения ДГПЖ приведена в табл. 5.

Послеоперационное кровотечение наблюдалось всего у 37 (24,7%) пациентов. Проведение гемотрансфузии потребовалось 7 пациентам, показатель после применения методики HoLEP составил 1 (2,5%), после ТУРП – 2 (4,0%), после ОАЭП – 4 (6,7%).
Средний послеоперационный койко-день составил при применении методики HoLEP – 3,8±0,2, ТУРП – 3,3±0,2; ОАЭП – 8,6±0,3 (p<0,05 между первой и второй группами; <0,01 между первой и третьей, второй и третьей группами). Детальный анализ осложнений показал, что было выявлено 7 поздних осложнений, 2 (4,0%) – стриктуры задней части уретры и 2 (4,0%) – стриктуры шейки мочевого пузыря развились после ТУРП; 2 (3,3%) – стриктуры уретры и 1 (1,7%) – склероз шейки мочевого пузыря после ОАЭП.
Таким образом, после применения методики HoLEP в отдаленном послеоперационном периоде фиброзно-склеротических процессов уретры и шейки мочевого пузыря не наблюдали и дополнительных оперативных вмешательств по поводу поздних осложнений не проводилось.
Обсуждение. После публикации работы по систематизации осложнений [11], классификацию Clavien-Dindo стали применять также в урологии для оценки послеоперационных осложнений и за последние годы она стала популярной в силу универсальности. Причина в том, что систематизация осложнений объективно показывает преимущества одного метода и недостатки другого, позволяет сравнивать качество вмешательств различных хирургов, результаты и эффективность лечения в различных центрах.
Есть данные по использованию системы классификации для оценки послеоперационных осложнений радикальных позадилонных, лапароскопических и робот-ассистированных простатэктомий [13–15], радикальных цистэктомий [16, 17], почечной хирургии [18, 19]. В 2019 г. E. Sagen et al. [20], а в 2020 г. T. Mbaeri et al. [21] применили систему классификации для оценки осложнений трансуретральной резекции простаты (ТУРП). В 2020 г. S. Yalçın et al. опубликовали данные по использованию системы Clavien для оценки осложнений HoLEP [22].
Но обратной стороной медали является то, что оценка того или иного послеоперационного осложнения различается у разных врачей, в разных отделениях и центрах из-за некоторой субъективности в оценке осложнений, особенно если она сделана непосредственно хирургом, выполнившим операцию.
Для того чтобы оценить характер осложнений, а также распределить их по степени тяжести согласно логике, предложенной авторами классификации, мы должны четко разграничить нормальное и осложненное течение послеоперационного периода. В доступной нам литературе касательно хирургического лечения ДГПЖ мы не нашли анализа данной проблемы, где были бы четко указаны критерии нормального и осложненного течения послеоперационного периода в лечении ДГПЖ. Ранее критерии стандартного течения послеоперационного периода в отношении эндоскопического лечения нефролитиаза были определены коллективом нашего Центра урологии [23, 24]. Ряд авторов, которые использовали в своей работе классификацию Clavien-Dindo для оценки послеоперационных осложнений при лечении ДГПЖ, не акцентировали на этом своего внимания [19–22, 25]. В результате из-за отсутствия критериев стандартного послеоперационного течения при хирургическом лечении ДГПЖ авторы по-своему систематизировали осложнения в разных центрах. Одни исследователи некоторые легкие осложнения считали осложнением согласно логике классификации, другие подобные же изменения в послеоперационном периоде расценивали как нормальное послеоперационное течение. Следовательно, сравнение результатов лечения в одном центре оказывается корректным, но между центрами некорректным.
Для устранения подобных ограничений в отношении оперативных вмешательств, выполняемых при ДГПЖ, в частности, при таких операциях, как ОАЭП, ТУРП и HoLEP, мы предприняли попытку адаптации системы классификации Clavien-Dindo к вышеуказанным вмешательствам, предварительно определив, какое послеоперационое явление считать нормой и где начинается осложнение.
У некоторых ученых может появиться мнение, согласно которому стандарт послеоперационного течения для ОАЭП должен отличаться от такового для современных эндоскопических методов лечения в силу ее травматичности и особенностей послеоперационного ведения. Однако это ошибочное мнение, ведущее к заблуждению специалистов в данном вопросе. Оперативное лечение ДГПЖ вне зависимости от того, каким методом оно будет осуществлено, преследует единую конечную цель – избавление пациента от ИВО путем устранения ДГПЖ.
Следовательно, результаты лечения должны быть оценены единой системой оценки качества вмешательств вне зависимости от того, каким методом или объемом вмешательства была достигнута цель.
Сравнение осложнений, полученных после систематизации с данными литературы, где даны осложнения без систематизации, не всегда оказывается корректным, так как при систематизации выявляемость осложнений всегда больше. По данным J. Rassweiler et al. [26] по мере улучшения технологического и инструментального обеспечения трансуретральной резекции необходимость в гемотрансфузии снизилась до 0,4% против прежних 7,1% (у нас показатель составил 4%), частота ТУР-синдрома практически равна 0 (ранее 1,1%, у нас – 0), обструкция сгустками крови составляет 2% (ранее 5%, у нас – 6%), инфекция мочевого тракта – 1,7% (8,2%, у нас – 8%), задержка мочи – 3% против прежних 9% (у нас 4%). К поздним осложнениям относятся стриктуры уретры (2,2–9,8%, у нас – 4%), склероз шейки мочевого пузыря (0,3–9,2%, у нас – 4%). Смертность после ТУРП составляет 0,0–0,025% (у нас – 0).
При сравнении техник ТУРП и HoLEP в мета-анализе S. A. Ahyai et al. [27] были обнаружены следующие особенности: ни в одном из случаев при выполнении HoLEP не потребовалось гемотрансфузии, в то время как после ТУРП частота переливания крови составила 2,2% (у нас показатели 4 и 2,5% соответственно); время катетеризации после HoLEP варьировалось от 17,7 до 31 ч, после ТУРП – от 43,4 до 57,8 ч (у нас также менее 3 сут. после обоих методов). Длительность госпитализации после лазерной энуклеации в среднем составила 2–3, после ТУРП – 3–6 дней [28], данный показатель среди наших пациентов составил 3,8±0,2 и 3,3±0,2 соответственно.
В ретроспективном исследовании, посвященном сравнению методик ОАЭП и ThuFLEP (Thulium fiber laser enucleation of the prostate), установлено, что ОАЭП характеризуется массой осложнений, длительным сроком госпитализации и поздним возвращением к повседневной активности [7], что и мы также подтвердили в нашем исследовании.
В проспективном мультицентровом исследовании G. Bozzini et al. [29], в котором сравнивались методики с применением тулиевого и гольмиевого лазера (ThuLEP и HoLEP) с 12-месячным периодом наблюдения, значимых различий в эффективности лечения отмечено не было.
ОАЭП характеризуется массой послеоперационных осложнений, а также высокой летальностью. Уровень смертности для европейских стран составляет порядка 0,25%. Общий процент осложнений в конце 1990-х гт. колебался в пределах 12,5–23,02%, ко второй декаде XXI в. составил 17,3% [5, 30–33].
Интересным фактом является то, что проведенный нами анализ эффективности лечения при всех трех методах хирургии на основе показателей IPSS, QoL, Qmax, Vпр и ООМ (табл. 2–4) продемонстрировал, что все показатели достоверно различались по сравнению с исходными параметрами и все методы оперативного лечения можно расценивать как эффективными с относительным различием в сроках наступления улучшения по баллам IPSS и качества жизни пациентов, что наступало позже на 1–2 мес. после ТУРП. Но только после проведения систематизации послеоперационных осложнений оказалось возможным выявить реальную картину особенности послеоперационного периода каждого метода лечения.
Выводы
1. Адаптировать классификацию хирургических осложнений Clavien-Dind применительно к хирургическому удалению ДГПЖ возможно через разработку критериев неосложненного послеоперационного течения хирургического лечения ДГПЖ.
2. ТУРП и HoLEP оказались малотравматичными, после которых частота и тяжесть осложнений, согласно систематизации, были достоверно ниже (82,0 и 70,0% соответственно) по сравнению с ОАЭП (256,6%), р<0,01. После ТУРП и HoLEP реабилитация пациентов наступала раньше за счет достоверно раннего удаления мочевых катетеров (2,9±0,1 и 2,2±0,1 сут. соответственно по сравнению с ОАМП 8,4±0,3 (р<0,01), статистически достоверно сокращалось пребывание пациентов в стационаре: 3,3±0,2 и 3,8±0,2 сут. соответственно по сравнению с ОАЭП 8,6±0,3 сут. (р<0,05).



