В 2005 г. R. Berglund и соавт. впервые опубликовали результаты успешной лапароскопической радикальной цистопростатэктомии и билатеральной нефроуретерэктомии у двух мужчин с терминальной почечной недостаточностью (ТХПН) и раком мочевого пузыря [3]. Позже C. Li и соавт. [4], C. Ou и W. Yang [5], V. Lin и соавт. [6] сообщили о высокой эффективности лапароскопической и ретроперитонеоскопической билатеральной нефруретерэктомии с цистпростатэктомией или гистерэктомией у диализных пациентов. I. H. Chen и соавт. [7] представили данные о 14 женщинах, находившихся на гемодиализе, которым выполнена билатеральная нефруретерэктомия, цистэктомия, гистерэктомия с двусторонней сальпингоовариэктомией из мини-доступа. Во всех случаях использован срединный разрез ниже пупка на протяжении 10 см, при этом нефрэктомия осуществлена из забрюшинного доступа. С целью мобилизации брюшинного мешка выполнено рассечение круглых связок матки с обеих сторон, применены ретракторы Bookwalter.
Таким образом, несмотря на то что пациенты с ТХПН, находившиеся на программном гемодиализе, относятся к группе высокого анестезиолого-хирургического риска, выполнение им больших по объему оперативных вмешательств видится вполне осуществимым [1, 2]. Безусловно, использование минимально инвазивных технологий данной категорией пациентов наиболее безопасно. Однако у ряда больных могут быть противопоказания к проведению малоинвазивного лечения, такие как сепсис, гнойный пиелонефрит, нестабильность гемодинамики и др. В подобных ситуациях возникает необходимость в выполнении открытого вмешательства.
 Приводим клиническое наблюдение.
Приводим клиническое наблюдение.
Б о л ь н о й К. 53 лет, столяр, поступил в приемное отделение ГБУЗ ГКБ № 52 ДЗ г. Москвы 20.05.14 по наряду скорой медицинской помощи с направительным диагнозом «отек Квинке».
Жалобы на шелушение кожи, зуд, отечность голеней, щек, уменьшение количества мочи. Из анамнеза известно, что резкое ухудшение состояния отмечает в течение недели. Около 1 мес получал амбулаторное лечение у дерматолога по месту жительства. Год назад впервые отметил макрогематурию, однако за медицинской помощью не обращался. При диспансеризации в октябре 2013 г. зафиксировано повышение АД до 140/90 мм рт.ст. Страдает варикозной болезнью вен нижних конечностей. Витилиго с 18 лет. Операции, травмы отрицает.
Объективно: состояние средней тяжести. Сознание ясное. Кожные покровы бледные, сухие. По всему телу отмечается мелкопластинчатое шелушение. Отеки голеней, стоп, пастозность лица. Температура тела 36,6°С. Аускультативно над легкими дыхание везикулярное, хрипов нет. ЧДД 18 в 1 мин. Тоны сердца приглушены, ритм правильный. АД 160/80 мм рт.ст., ЧСС 107 в 1 мин. Живот равномерно участвует в акте дыхания, мягкий, не вздут, безболезненный при пальпации. Перитонеальных симптом нет. Печень не увеличена; селезенка, почки не пальпируются. Мочевой пузырь определяется на уровне +3 см над лоном. Наружные половые органы не изменены. Ректально: простата не увеличена, с четкими, ровными контурами, плотно-эластической консистенции, безболезненная, срединная бороздка выражена, слизистая прямой кишки смещаема.
Данные дообследования при поступлении в стационар. УЗИ: расширение чашечно-лоханочной системы (ЧЛС) с обеих сторон (лоханки до 40 мм, чашечки до 20 мм), толщина паренхимы 16–20 мм, объем мочевого пузыря 650 мл, по задней стенке определяется объемное образование размером 70×82×52 мм.
Общий анализ крови: Hb 69 г/л, э. 2,3×1012/л, л. 9,5×109/л. Биохимический анализ крови: мочевина 56,3 ммоль/л, креатинин 1501 мкмоль/л, калий 6,2 ммоль/л. Общий анализ мочи: цвет соломенно-желтый, плотность 1005, белок 0,3 г/л, лейкоциты 0 кл/мкл, реакция на кровь положительная (+++). Рентгенография органов грудной клетки – легочные поля без отчетливых очаговых и инфильтративных изменений.
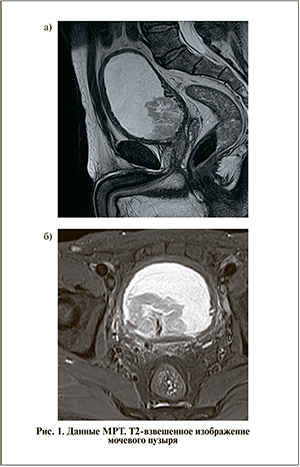
Пациент госпитализирован в отделение реанимации для нефрологических больных. Установлен уретральный катетер Фолея, получена светлая моча в объеме 1000 мл, начата заместительная почечная терапия по витальным показаниям. Диурез составлял до 5000 мл в сутки, отмечена достаточно интенсивная макрогематурия, проведены гемотрансфузии, гемостатическая антибактериальная терапия. При контрольном УЗИ почек сохранялось расширение ЧЛС с обеих сторон, в связи с чем 24.05.14 выполнена билатеральная чрескожная пункционная нефростомия (ЧПНС). С 01.06.14 у пациента отмечена гипертермия до 37,2–38,7°С с непродолжительными периодами нормализации температуры тела. С учетом сохраняющейся макрогематурии и неэффективности гемостатической терапии 10.06.14 произведена трансуретральная электрокоагуляция образования мочевого пузыря, биопсия. При цистоскопии визуализировалась мелковорсинчатая опухоль, занимающая практически всю полость мочевого пузыря, исходящая из задней стенки, на широком основании; подслизистые сосуды с выраженным варикозным расширением, детализировать устья мочеточников не представлялось возможным. Гистологическое заключение: уротелиальная карцинома умеренной степени злокачественности. По данным МРТ по задней, нижней, правой латеральной стенкам мочевого пузыря имеется экзофитное образование размером 74х60х46 мм, затрагивающее простатический отдел уретры и устья мочеточников. Отмечается экстравезикальный рост с прорастанием мышечной оболочки, пенетрацией в правый семенной пузырек на 18 мм. Образование имеет неоднородный слабоинтенсивный сигнал в режиме Т2-взвешенного изображения и изоинтенсивный сигнал – Т1-взвешенного. Подвздошные сосуды не изменены. Параректальная клетчатка не инфильтрирована. Выявлено увеличение паховых лимфатических узлов до 25 мм (рис. 1).
Общий диурез по нефростомам составил 2000–3000 мл, однако азотемия не регрессировала, что потребовало регулярного проведения гемодиализа, в связи с чем 16.06.14 сформирована артериовенозная фистула.
На фоне адекватно дренированных почек нефростомами (отсутствовало расширение ЧЛС по данным УЗИ) у больного сохранялась гипертермия до 37,5–38°С, что было расценено как активное течение пиелонефрита, так как других источников септического состояния выявлено не было. Проведена антибактериальная терапия (фторхинолоны, цефалоспорины III поколения) без существенного эффекта, постепенно нарастал лейкоцитоз до 27,9×109/л. При динамическом УЗ-контроле признаков гнойного пиелонефрита не обнаружено. По данным компьютерной томографии от 29.06.14 почки несколько уменьшены в размерах, паренхима однородная. После контрастного усиления равномерно накапливают и выделяют контрастное вещество. ЧЛС и мочеточники не расширены, в полости лоханок обеих почек проксимальные концы нефростомических дренажей. Посев мочи из нефростом (от 20.06.14) выявил рост Enterococcus faecalis 107 КОЕ/мл и Alcaligenes faecalis 107 КОЕ/мл.
 С учетом активного течения пиелонефрита, неэффективности антибактериальной терапии, терминальной почечной недостаточности, сохраняющейся макрогематурии было решено выполнить билатеральную нефруретерэктомию, цистпростатэктомию, лимфаденэктомию. Данные предоперационного обследования. Общий анализ крови: Hb 101 г/л, э. 3,5×1012/л, л. 23,5×109/л, тромбоциты 134×109/л. Биохимический анализ крови: мочевина 20 ммоль/л, креатинин 170 мкмоль/л (после диализа), С-реактивный белок 113,72 мг/л, общий белок 59,2 г/л, альбумин 33,1 г/л. Коагулограмма: протромбиновое время 22,8 с, протромбиновый индекс 69,3%, МНО 1,54, АЧТВ 111,2 с.
С учетом активного течения пиелонефрита, неэффективности антибактериальной терапии, терминальной почечной недостаточности, сохраняющейся макрогематурии было решено выполнить билатеральную нефруретерэктомию, цистпростатэктомию, лимфаденэктомию. Данные предоперационного обследования. Общий анализ крови: Hb 101 г/л, э. 3,5×1012/л, л. 23,5×109/л, тромбоциты 134×109/л. Биохимический анализ крови: мочевина 20 ммоль/л, креатинин 170 мкмоль/л (после диализа), С-реактивный белок 113,72 мг/л, общий белок 59,2 г/л, альбумин 33,1 г/л. Коагулограмма: протромбиновое время 22,8 с, протромбиновый индекс 69,3%, МНО 1,54, АЧТВ 111,2 с.
Принимая во внимание ожидаемую длительность оперативного пособия, возможные негативные последствия от карбоксиперитонеума, от лапароскопического варианта оперативного вмешательства решено воздержаться. 07.07.14 пациент подан в операционную с диагнозом «основной: рак мочевого пузыря Т4аNxM0. Осложнения: макрогематурия. Билатеральная уретерогидронефротическая трансформация. Нефростомы с обеих сторон. Хронический пиелонефрит активного течения. Терминальная стадия хронической почечной недостаточности. Лечение гемодиализом. Анемия, средней степени тяжести».
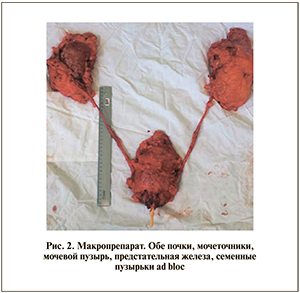
Выполнена срединная лапаротомия от мечевидного отростка до лонного сочленения. Первым этапом произведена билатеральная нефруретерэктомия. Доступ в забрюшинное пространство осуществлен через париетальную брюшину путем ее рассечения по линиям Тольда с обеих сторон. Ревизия почек выявила апостематозную форму гнойного пиелонефрита. При посеве гноя получен рост Proteus mirabilis 108 КОЕ/мл. Далее выполнена цистпростатвезикулэктомия. На данном этапе операции использовали биполярную электрохирургическую установку «LigaSure»; это позволило сократить время на выделение органокомплекса и осуществить надежный гемостаз, что чрезвычайно актуально для пациентов, находящихся на гемодиализе. При ревизии лимфоузлов малого таза (запирательные, по ходу наружных и внутренних подвздошных сосудов, общих подвздошных, пресакральных) увеличения и уплотнения последних не выявлено. С целью определения стадии заболевания выполнена лимфодиссекция по ходу наружных подвздошных сосудов с обеих сторон (рис. 2).
По данным гистологического заключения в почках выявлены воспалительные изменения и участки гнойного расплавления, в мочевом пузыре – уротелиальная карцинома умеренной степени дифференцировки с прорастанием мышечной оболочки; предстательная железа с очаговой воспалительной инфильтрацией; уретра, семенные пузырьки обычного строения; в лимфатических узлах метастатического поражения не выявлено. Таким образом, послеоперационный диагноз сформулирован следующим образом: «рак мочевого пузыря Т2bN0M0 (G2 по классификации ВОЗ от 1973 г.). Гнойная форма острого пиелонефрита с обеих сторон. Терминальная стадия хронической почечной недостаточности».
Продолжительность операции составила 215 мин, кровопотеря – 1300 мл. Интраоперационно перелито 2100 мл свежезамороженной одногруппной плазмы. Переведен в отделение реанимации. В раннем послеоперационном периоде общий анализ крови: Hb 69 г/л (до вмешательства – 101 г/л), эритроциты 2,38×1012/л, лейкоциты 10,9×109/л.; биохимический анализ крови: креатинин 960 мкмоль/л, мочевина 25,7 ммоль/л, общий белок 57,2 г/л, альбумин 32,4 г/л. Через 12 ч пациент экстубирован, продолжены сеансы заместительной почечной терапии. По дренажам не более 250 мл серозно-геморрагического отделяемого в сутки, спустя 3 сут отделяемое уменьшилось до 100 мл. 11.07.14 у больного отмечен многократный жидкий стул. Диагностирован псевдомембранозный колит, проведена терапия ванкомицином per os с эффектом. 15.07.14 страховые дренажи удалены, больной переведен в отделение нефрологии.
В течение 1 мес после операции сохранялась гипертермия с максимальными подъемами температуры тела до 38,2°С. Заживление раны первичным натяжением в верхней и нижней трети, в средней трети на протяжении 2 см развилось гнойное воспаление подкожно-жировой клетчатки с формированием свища над апоневрозом на глубину до 4 см. Посев из раны – Proteus mirabilis 108 КОЕ/тамп. Проведена антибактериальная терапия в соответствии с результатами определения антибиотикочувствительности, местная терапия антисептиками, ежедневные перевязки с эффектом. Помимо этого пациент получал гастропротективную, гипотензивную терапию, препараты, стимулирующие гемопоэз, препараты железа, даптомицин. По данным компьютерной томографии от 05.08.14 в ложах удаленных почек имеются отграниченные жидкостные скопления объемом до 50 мм, в малом тазу – отграниченное жидкостное образование размером 44х58 мм. С 16.08.14 у больного дважды констатировали клиническую картину динамической кишечной непроходимости, проведена консервативная терапия с эффектом.
В удовлетворительном состоянии пациент выписан из стационара 20.08.14. Произошло окончательное заживление послеоперационной раны, температура тела нормализовалась. Живот безболезненный, стул оформленный 1–2 раза в день. При выписке в общем анализе крови Hb 78 г/л, эритроциты 2,98×1012/л, лейкоциты 10,3×109/л. В настоящее время больной получает программный гемодиализ.
Данное клиническое наблюдение показывает, что ТХПН, проведение гемодиализа, септическое состояние, рак мочевого пузыря не являются абсолютными противопоказаниями к обширным открытым хирургическим вмешательствам, которые являются единственной надеждой на спасение жизни больного. В то же время нельзя забывать, что у пациентов на гемодиализе высок риск кровотечения. Поэтому такие больные должны проходить тщательную предоперационную подготовку, необходима коррекция анемии, гипопротеинемии, гипоальбуминемии, гемодиализ накануне операции целесообразно проводить без гепаринизации. Использование биполярного электрохирургического инструментария позволяет добиваться лучшего гемостаза.



