Введение. К наиболее частым заболеваниям почек и верхних мочевых путей (ВМП) относят нефролитиаз, стриктуры мочеточника и кисты почек. Мочекаменной болезнью в среднем страдают от 30 до 40% урологических больных [1, 2], при этом до 50% приходится на камни почки, в том числе крупный, множественный и коралловидный нефролитиаз [3]. Кистозные образования почек встречаются среди 50% взрослых [4]. Не уменьшается и число больных различными стенозами ВМП [5]. Подавляющая часть больных данными заболеваниями подвергаются оперативному лечению.
 Широкое внедрение достижений научно-технического прогресса в урологию, появление высокотехнологического оборудования и инструментов в оперативной урологии в значительной степени изменили традиционный подход к диагностике и лечению ряда заболеваний почек и ВМП [6]. Все больше хирургов отдают предпочтение малоинвазивным, в том числе и эндоскопическим, методам оперативного вмешательства в отношении больных с заболеваниями почки и ВМП [7, 8].
Широкое внедрение достижений научно-технического прогресса в урологию, появление высокотехнологического оборудования и инструментов в оперативной урологии в значительной степени изменили традиционный подход к диагностике и лечению ряда заболеваний почек и ВМП [6]. Все больше хирургов отдают предпочтение малоинвазивным, в том числе и эндоскопическим, методам оперативного вмешательства в отношении больных с заболеваниями почки и ВМП [7, 8].
Однако до сих пор результаты оперативного лечения пациентов с нефролитиазом, кистами почки и стриктурами мочеточника не всегда удовлетворяют урологов [9, 10], решены далеко не все проблемы, связанные с профилактикой и купированием различных осложнений, в том числе и наиболее грозным – кровотечением [11, 12].
Так, при перкутанном доступе к почке наиболее частым и опасным осложнением остается кровотечение из раневого канала [13, 14], которое встречается в 5–7,5% наблюдений. Кровотечение при любом оперативном вмешательстве угрожает жизни больного осложнением, но, если при открытых операциях ликвидация этого, обычно видимого на глаз, осложнения не вызывает больших трудностей (электрокоагуляция, лигирование или прошивание сосудов и тканей), то в эндоскопической хирургии, когда руки хирурга выведены из оперируемой зоны, что резко сужает спектр диагностических и лечебных возможностей [15], а раневой доступ не визуализируется, гемостаз при перкутанных операциях проблематичен.
Уровень осложнений перкутанной хирургии является основным фактором, побуждающим к поиску новых методов лечения [2]. Для решения самых разнообразных проблем в медицине врачи разных специальностей все большее внимание обращают на применение биосовместимых материалов и методы лечения на основе длительно функционирующих материалов и имплантатов, близких по поведению к тканям организма, обладающих новой совокупностью свойств: гистерезисное поведение материала; отсутствие химической реакции на введение материала в ткани организма; изменение формы при изменении напряжения и температуры; демпфирующее соответствие свойств материала характеристикам тканей; пористо-проницаемые свойства материала, соответствующие свойствам тканей организма; соответствие капиллярности и смачиваемости структур материала характеристикам тканей; способность материала инкубировать клеточные культуры и создавать условия для их роста в проницаемой структуре имплантата, а после имплантации поддерживать функцию органа; надежность материала функционировать в организме в условиях знакопеременного воздействия; отсутствие проблем стерилизации материала и имплантатов [16].
 В доступной литературе мы не нашли публикаций об использовании данных материалов в малоинвазивной хирургии почки и ВМП. В связи с этим использование биосовместимых, сверхэластичных материалов из никелида титана в малоинвазивной хирургии некоторой патологии почки представляет несомненный интерес.
В доступной литературе мы не нашли публикаций об использовании данных материалов в малоинвазивной хирургии почки и ВМП. В связи с этим использование биосовместимых, сверхэластичных материалов из никелида титана в малоинвазивной хирургии некоторой патологии почки представляет несомненный интерес.
Цель исследования: внедрить технологии на основе никелид-титановых сплавов в перкутанную хирургию почки и оценить их эффективность.
Материалы и методы. Основу для создания новых поколений медицинских материалов и технологий составили никелид титана и его монолитные и пористые сплавы, в которых был обнаружен эффект памяти формы.
Свойства никелид-титановых сплавов позволили нам совместно с НИИ медицинских материалов и имплантатов с памятью формы Сибирского физико-технического института при Томском государственном университете разработать и внедрить в практическую деятельность конструкции и технологии на основе никелид-титановых сплавов: криогемостаз перкутанного канала для профилактики и купирования кровотечения (патент на изобретение «Устройство для гемостаза при эндоскопических операциях на почках» № 2318457); подвесную перкутанную нефропексию с никелид-титановыми мелкодисперсными гранулами при сочетании нефролитиаза и нефроптоза (патент на изобретение «Способ хирургического лечения нефроптоза» № 2285456); использование никелид-титановых конструкций: постоянного стента «корона» и временного стента из никелид-титановой фольги при внутренней эндотомии стриктур мочеточника; перкутанная хирургия кист почек с использованием никелид-титановых гранул (патент на изобретение «Способ хирургического лечения поликистоза почек» № 2264177).
Нами были проанализированы результаты 402 рентгенэндоскопических операций, выполненных пациентам с нефролитиазом, стриктурами мочеточника и кистами почки.
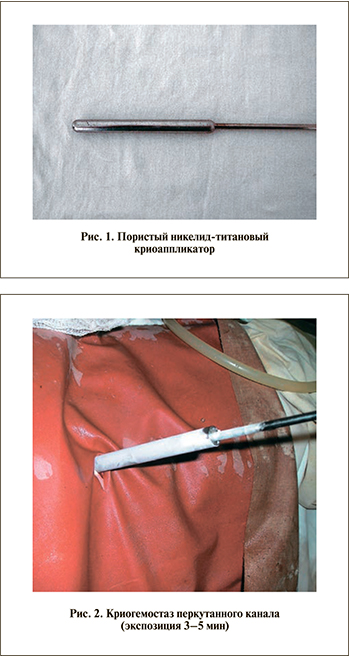
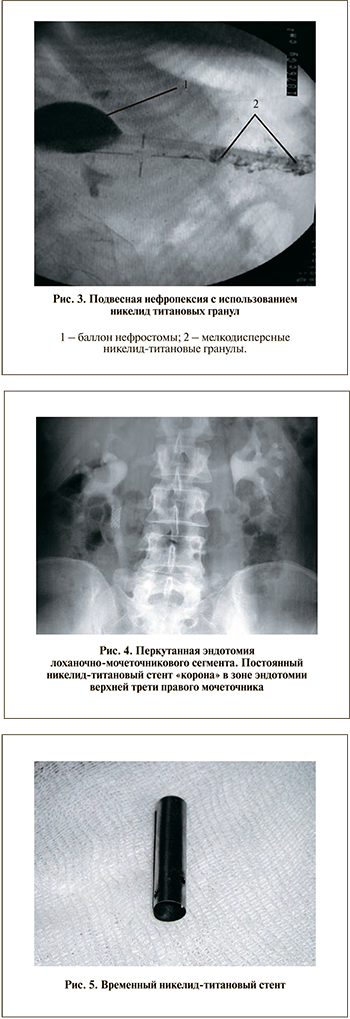
Технология криогемостаза перкутанного канала для профилактики и купирования кровотечения заключается в следующем. После введения амплац-трубки, удаления сгустков крови, аспирации ирригационной жидкости из полостной системы и тампонирования дистального просвета амплац-трубки марлевым шариком (внутренние стенки должны быть сухими) в ее просвет вводится криоаппликатор, предварительно охлажденный в жидком азоте до -196°С (рис. 1, 2), экспозиция до 3–5 мин, выполняется основной этап операции; при необходимости криоаппликация выполняется в конце вмешательства.
Для оценки эффективности предложенного метода гемостаза было проведено несколько исследований. В первом из них при проведении перкутанных операций исследовался уровень эритроцитов и гемоглобина в промывной жидкости. После введения амплац-трубки и нефроскопа с подключенной ирригацией жидкости в пробирку в течение 3 с набирали истекающую из амплац-трубки жидкость (пробирка № 1). Выполняли криогемостаз раневого канала никелид-титановым криоаппликатором по предложенной методике. Сразу после этого при повторной нефроскопии также в течение 3 с набирали промывную жидкость в пробирку № 2. Уровень эритроцитов и гемоглобина определяли по стандартной методике выполнения общего анализа крови.
Из 63 пациентов, которым проведено данное исследование, было выделено две группы: первая, состоящая из 8 (12,7%) человек, у которых кровотечение из раневого канала отмечалось визуально (интенсивное окрашивание вытекающей промывной жидкости, у трех больных отмечено образование сгустков), и вторая, в которую вошли 55 (87,3%) пациентов без явных признаков кровотечения (слабое окрашивание промывной жидкости).
В другом исследовании при выполнении перкутанной нефролитолапаксии (ПНЛЛ) по поводу коралловидного нефролитиаза (в анализ были включены больные с камнями К3 и К4 по классификации Э. К. Яненко) оценивали показатели красной крови (эритроциты, гемоглобин и гематокрит) до и после операции в двух группах пациентов. В первой группе (n=48) криогемостаз выполнен в начале или конце, а также и в начале и конце операции, во второй, контрольной, группе (n=67) криогемостаз не проведен.
 Технология использования мелкодисперсных никелид-титановых гранул размером 50–1000 мкм при перкутанной нефропексии при сочетании нефролитиаза и нефроптоза заключается в следующем. После установки нефростомы и подтягивания за нее почки в нормальное физиологическое положение вдоль нефростомы имплантировали мелкодисперсные никелид-титановые гранулы (рис. 3).
Технология использования мелкодисперсных никелид-титановых гранул размером 50–1000 мкм при перкутанной нефропексии при сочетании нефролитиаза и нефроптоза заключается в следующем. После установки нефростомы и подтягивания за нее почки в нормальное физиологическое положение вдоль нефростомы имплантировали мелкодисперсные никелид-титановые гранулы (рис. 3).
В проспективное исследование были включены 28 пациентов, у которых нефролитиаз сочетался с нефроптозом. Правосторонняя патология была у 24 пациентов, левосторонняя – у 4. Опущение почки 1-й степени выявлено у 7 пациентов, 2-й – у 19, 3-й – у 2; камни размером до 2 см имели место у 15 пациентов, до 3 см – у 10, коралловидные камни – у 3. Для анализа эффективности новой методики пациенты были разделены на две группы: первую (n=17), где подвесная нефропексия проведена по общепринятой методике, и вторую (n=11) – с использованием никелид-титановой крошки.
Для оценки эффективности результатов рентген-эндоскопической хирургии стриктур ВМП анализу подвергнуты 126 историй болезни пациентов, пролеченных по поводу стриктур и облитераций ВМП, которым было выполнено 119 (94,44%) перкутанных вмешательств и 7 (5,56%) – трансуретральных.
С первичными стриктурами были 83 (65,87%) пациента, с рецидивными – 43 (34,13%). У 38 (30,16%) больных стриктура сочеталась с нефролитиазом. Из всех больных 19 (15,08%) было выполнено бужирование, 107 (84,92%) – эндотомия и реканализация ВМП. В зависимости от способа интубации мочеточника все пациенты были распределены на 7 групп. В 1-й группе из 23 (18,25%) пациентов использовали стент-катетер длиной 26–27 см и диаметром 5–7 Сh; во 2-й (n=43) – эндотомический стент-катетер длиной 26–27 см, диаметром 5–6 Сh с расширенной частью 9–14 Сh; в 3-й (n=31) – полихлорвиниловую трубку от разовой инфузионной системы; в 4-й (n=7) – постоянную стент-«корону» из никелида титана (рис. 4) собственной конструкции; в 5-й (n=9) – временный стент из никелид-титановой фольги (рис. 5); в 6-й (n=8) – нитиноловый стент Мемокат для ретроградной и антеградной установки длиной от 3 до 20 см, диаметром 10 Сh; в 7-й группе из 5 пациентов интубация не проведена.
Для оценки эффективности использования мелкодисперсных никелид-титановых гранул при выполнении перкутанной пункционной аспирации простых кист почки было проанализировано 70 историй болезни. У 39 пациентов пункционная аспирация выполнена со склеротерапией, у 17 – без склеротерапии и у 14 – с имплантацией никелид-титановых гранул.
Нами разработана методика имплантации в дно кисты никелид-титановой мелкодисперсной крошки, обеспечивающей «склеивание» ее стенок. На этапе после контрастирования полости кисты поисковую иглу меняют на иглу-канюлю, после удаления струны-проводника 2 г мелкодисперсного никелид-титанового порошка засыпают в просвет иглы канюли, из шприца 10 мл порошок вымывают в просвет кисты физиологическим раствором (вымывание можно повторить 2–3 раза) до полного осаждения порошка на стенки кисты, жидкость аспирируют (рис. 6).

Результаты. При исследовании уровня эритроцитов и гемоглобина в ирригационной жидкости до и после выполнения криогемостаза раневого канала установлено следующее. В первой группе средний уровень эритроцитов в пробирке № 1 составил 1,37, а гемоглобина – 32,37; во второй группе – 0,19 и 3,16 соответственно. В пробирке № 2 (после криогемостаза) в первой группе средний уровень эритроцитов составил 0,096, гемоглобина – 0,22, во второй – 0,015 и 0,0016 соответственно. В целом в первой группе больных средний уровень эритроцитов уменьшился более чем в 14 раз, гемоглобина – более чем в 147, а во второй – примерно в 13 и 197 раз соответственно.
В следующем исследовании при оценке показателей красной крови в группах пациентов с коралловидным нефролитиазом мы получили следующие результаты. В первой группе данные показатели на следующие сутки после операции были недостоверно, но ниже исходных, в то время как во второй эти показатели были достоверно ниже не только исходных, но и послеоперационных из первой группы (см. таблицу).
При оценке эффективности подвесной нефропексии выявлено, что в первой группе нефростому после тренировки удаляли в среднем через 23,45±2,21 сут, во второй – через 8,47±1,18 сут. При контрольном обследовании через год из наблюдения по разным причинам выбыли 2 пациента из первой группы и 3 – из второй. По данным УЗИ, обзорной и экскреторной урографии, в первой группе из 9 человек хорошие (нет патологической подвижности почки) и удовлетворительные (нет прогрессирования нефроптоза) результаты отмечены у 5 (55,6%), рецидив нефроптоза констатирован у 4 (44,4%) больных. Во второй группе из 14 человек хорошие и удовлетворительные результаты получены у 12 (85,71%), неудовлетворительные – у 2 (14,29%).
При обследовании пациентов, которым выполнена коррекция стриктур мочеточника через год. эффективным результатом мы считали полное восстановление проходимости ВМП, купирование или значительное уменьшение гидронефроза, что было отмечено в отношении 105 (83,33%) больных; в отношении 21 (16,67%) прооперированного признаны мало- и неэффективными. Необходимо отметить, что в этой группе подавляющее число (19 [90,48%]) пациентов были с рецидивными стриктурами.
Интересными, на наш взгляд, получились результаты оценки эффективности различных способов интубации оперированных стриктур. Так, наибольшая эффективность отмечена в группах со стентом «корона» (100%) и эндотомическим стент-катетером (97,67%), наихудшая – в безинтубационной (40%); хорошие результаты получены в группах с временным никелид-титановым стентом (88,89%) и со стентом Мемокат – (87,5%; необходимо подчеркнуть, что это единственная группа, где все больные были с рецидивными стриктурами после одной и более пластических операций), в группах с ПХВ-трубкой и обычным стент-катетером эффективность составила 70,97 и 73,91% соответственно.
При анализе 70 перкутанных аспираций кист было выявлено (длительность наблюдения – 2 года), что в группе с применением мелкодисперсного никелидтитанового порошка рецидивов не было, тогда как в группе больных, которым выполнена пункционная аспирация кисты со склеротерапией, рецидив наступил у 3 (7,69%) больных, в группе без склеротерапии – у 5 (29,41%).
Таким образом, внедрение никелид-титановых имплантатов в хирургию простых кист почек привело к значительному повышению эффективности этих операций, улучшению отдаленных результатов, повышению качества жизни пациентов с данной патологией почки.
Обсуждение. Такие заболевания почек ВМП, как мочекаменная болезнь, стриктуры мочеточника и кисты, в совокупности являются самой распространенной патологией в урологии, в большинстве случаев требующей оперативного лечения. Внедрение современных малоинвазивных и эндоскопических оперативных вмешательств позволило значительно повысить эффективность лечения урологических пациентов. Однако даже при их использовании не удается достигать 100%-ной эффективности и приходится сталкиваться с осложнениями.
Существующие в настоящее время методы купирования кровотечения из перкутанного канала не могут полностью удовлетворить урологов, занимающихся рентген-эндоскопической хирургией, а отсутствие надежных средств профилактики тормозит ее повсеместное внедрение. Разработанный нами криоаппликатор из пористого никелида титана, инновационная технология и алгоритм его применения в перкутанной хирургии почки позволили не только купировать возникшие как интраоперационные, так и послеоперационные кровотечения, но и предупредить их развитие практически в 100% случаев. Предложенный нами способ гемостаза на основе криогенных методов лечения с использованием пористо-проницаемых аппликаторов основан на принципиально отличающихся от традиционных методов преимуществах. Так, холодовое воздействие блокирует мелкие артериальные и венозные сосуды, что позволяет осуществлять разрезы в очаге деструкции даже в самых богато васкуляризованных органах, при этом гемостатический эффект замораживания предупреждает возможность вторичных кровотечений; очаг крионекроза обладает своеобразной «биологической инертностью», практически не вызывая реакции.
Полученные данные позволяют говорить о новом способе криогемостаза как об эффективном и надежном методе купирования и профилактики кровотечения при выполнении перкутанных операций.
При ПНЛЛ, выполняемой на опущенной почки, ее фиксация осуществляется за счет рубца, образующегося вдоль нефростомы, установленной чрескожным доступом. Так, И. А. Абоян и соавт. [17] 7 пациентам с нефролитиазом и нефроптозом выполнили ПНЛЛ, после чего установили баллонную нефростому № 14–16 Ch с последующей ее фиксацией на 20–25 дней. В послеоперационном периоде отмечена фиксация почки за счет соединительнотканного тяжа, сформированного в месте стояния нефростомы. Всеми больными достигнут хороший результат. По нашему мнению, единственным недостатком методики можно признать длительное (до 25 дней) нахождение пациентов с нефростомой и, соответственно, длительный период трудовой и социальной реабилитации.
Использование мелкодисперсных никелид-титановых гранул в подвесной нефропексии при выполнении перкутанной нефролитотрипсии больным нефролитиазом и нефроптозом позволило сократить продолжительность периода стояния нефростомы до 8,5 сут, что в 3 раза меньше, чем при стандартной методике, при этом частота рецидива нефроптоза снизилась в 1,5 раза, что, несомненно, повысило качество жизни пациентов.
Проблема лечения первичных и вторичных стриктур лоханочно-мочеточникового сегмента и мочеточника не теряет своей актуальности. Об этом свидетельствуют многообразие форм и методов лечения, а также высокая частота выявления рецидивных стриктур, достигающая более 15% [18]. Показания к различным способам оперативной коррекции стриктур ВМП – открытому, лапароскопическому, перкутанному или трансуретральному – уже определены. Вместе с тем дискутабельным остается вопрос о способе дренирования, материале, диаметре интубатора и длительности его стояния. По мнению некоторых авторов, это особенно актуально для внутренней эндотомии, результаты которой приближаются к традиционным открытым операциям [19].
Как показали результаты проведенного нами исследования, при выполнении рентгенэндоскопических перкутанных и трансуретральных вмешательств по поводу стриктур ВМП большое значение имеет выбор интубатора. При первичных стриктурах методом выбора являются эндотомические стент-катетеры с расширенной частью 12–14 Ch. Между тем при рецидивах, особенно неоднократных стриктур ВМП, применение стентов из материала с памятью формы обеспечивает практически полное восстановление уродинамики и функции почки. Предложенные методы интубации постоянным и временным стентом с памятью формы после перкутанной коррекции стриктуры лоханочно-мочеточникового сегмента перспективны в лечении больных данной патологией ВМП и могут стать операцией выбора. Очевидно, бездренажные пластические операции даже через год показали свою неэффективность и мы не рекомендуем их применение. В то же время существенным недостатком металлических стентов при их использовании для длительного дренирования считается выраженная солевая инкрустация.
Хорошие результаты мы получили и при использовании мелкодисперсных никелид-титановых гранул в ходе пункционной аспирации кист почек. Наиболее эффективными, не приводящими к рецидивам мы считаем малоинвазивные вмешательства с использованием никелид-титановых гранул — пункционную аспирацию. Пункционную аспирацию без склеротерапии проводить нецелесообразно.
Заключение. Использование инновационных технологий на основе никелид-титановых биосовместимых материалов в перкутанной хирургии почки и ВМП, несомненно, позволило достичь лучших результатов лечения пациентов с осложненным нефролитиазом, стриктурами мочеточника и простыми кистами почки, что, по нашему мнению, может служить толчком к дальнейшему развитию данного направления.



