Введение. Благодаря знаниям этиологии и патогенеза аденомы предстательной железы (АПЖ), полученным за последние десятилетия XX в., произошел революционный скачок в ее медикаментозной терапии. Это заболевание, или, точнее было бы назвать, состояние, является прогрессирующим, о чем регулярно свидетельствуется в ежегодно переиздаваемых клинических рекомендациях Европейской ассоциации урологов (ЕАУ) [1]. Подтверждение прогрессирующего течения АПЖ, а также выявление факторов, влияющих на прогрессирование этого заболевания, было представлено в ряде публикаций по результатам основополагающих в этом вопросе исследований Olmsted и PLESS. Основные критерии прогрессирования АПЖ: степень снижения максимальной скорости потока мочи; увеличение объема остаточной мочи; увеличение объема предстательной железы; возраст мужчины; уровень простатического специфического антигена (ПСА) [2–4]. Субъективная оценка больными ухудшения их состояния, определяемая по шкале IPPS, в настоящее время является важным признаком прогрессирования АПЖ, так как она позволяет врачу выбирать наиболее подходящий вариант лечения [5]. Имеются исследования, позволяющие не только доказать прогрессирование заболевания, но и уточнить наиболее вероятные факторы риска развития АПЖ, такие как, например, возраст, уровень ПСА, объем предстательной железы и др. [6].
Современные знания о факторах и критериях прогрессирования АПЖ позволяют врачам назначать лечение, когда симптомы заболевания еще не слишком выражены. Однако применение медикаментозной терапии с целью профилактики риска прогрессирования АПЖ на ранних стадиях в настоящее время изучено мало, а результатов длительных многолетних наблюдений, подтверждающих эффективность и безопасность медикаментозной терапии в отношении прогрессирования АПЖ, практически нет. Это связано в первую очередь с тем, что наиболее распространенные в настоящее время препараты, применяемые в лечении больных АПЖ, либо обладают только симптоматическим эффектом, вследствие чего не влияют на прогрессирование заболевания, либо в случае наличия патогенетического механизма действия не всегда безопасны, могут негативно влиять на сексуальную функцию и обусловливать развитие ряда других нежелательных эффектов. Все перечисленное выше делает обоснованным применение такой терапии только при выраженной симптоматике и достаточном объеме (не менее 50 см3) предстательной железы. Применение тактики активного наблюдения приводит к назначению лекарственных препаратов уже в тот момент, когда симптомы АПЖ начинают заметно оказывать влияние на качество жизни пациентов. В связи с этим крайне актуально изучение длительной медикаментозной терапии пациентов с минимальными субъективными проявлениями АПЖ и риском ее прогрессирования.
 В настоящей публикации мы впервые представляем результаты 10-летнего наблюдательного исследования эффективности и безопасности непрерывного применения растительного экстракта Serenoa repens пациентами с риском прогрессирования АПЖ. Обоснованием выбора растительного экстракта послужил ряд причин. Во-первых, экстракт Serenoa repens имеет высокий профиль безопасности, не влияет на артериальное давление, не ухудшает эректильную функцию, обладает отличной переносимостью, что особенно важно в случае длительного многолетнего применения [7–12]. Во-вторых, данный экстракт оказывает доказанное комплексное патогенетическое действие, которое одновременно направлено на ингибирование процесса роста АПЖ и ликвидацию симптомов хронического простатита [13]. В-третьих, препарат не снижает уровень ПСА, а потому не маскирует развитие рака простаты, что крайне важно для скрининга данного заболевания, особенно в случае многолетней терапии АПЖ [6].
В настоящей публикации мы впервые представляем результаты 10-летнего наблюдательного исследования эффективности и безопасности непрерывного применения растительного экстракта Serenoa repens пациентами с риском прогрессирования АПЖ. Обоснованием выбора растительного экстракта послужил ряд причин. Во-первых, экстракт Serenoa repens имеет высокий профиль безопасности, не влияет на артериальное давление, не ухудшает эректильную функцию, обладает отличной переносимостью, что особенно важно в случае длительного многолетнего применения [7–12]. Во-вторых, данный экстракт оказывает доказанное комплексное патогенетическое действие, которое одновременно направлено на ингибирование процесса роста АПЖ и ликвидацию симптомов хронического простатита [13]. В-третьих, препарат не снижает уровень ПСА, а потому не маскирует развитие рака простаты, что крайне важно для скрининга данного заболевания, особенно в случае многолетней терапии АПЖ [6].
Основной целью нашего наблюдательного исследования было изучение эффективности и безопасности многолетней терапии экстрактом Serenoa repens в отношении остановки прогрессирования АПЖ, которую мы оценивали как по объективным, так и по субъективным критериям. В течение 10 лет мы наблюдали пациентов, у которых была диагностирована АПЖ, а также имелись факторы риска ее прогрессирования, опубликованные в соответствующем руководстве ЕАУ [1]. Наличие риска прогрессирования АПЖ являлось обязательным параметром включения пациентов в группу наблюдения. Это объясняется тем, что наличие в группе наблюдения мужчин без критериев риска прогрессирования АПЖ затруднило бы доказательство эффективности многолетнего непрерывного применения растительного экстракта Serenoa repens в отношении прогрессирования этого заболевания. Ввиду того что исследование подразумевало длительное наблюдение, в нем отсутствует группа сравнения. Очевидно, что группой сравнения могла быть либо группа активного наблюдения (пациенты, на протяжении всего времени исследования не получавшие никакой терапии, направленной на лечение или профилактику прогрессирования АПЖ), либо группа плацебо-контроля. Однако совершенно очевидно, что за время исследования у пациентов группы плацебо или группы активного наблюдения возникло бы прогрессирование АПЖ и как исход – выраженная симптоматика, требующая лечения. В таком случае к концу исследования с большой степенью вероятности выбыли бы все пациенты контрольной группы. Наш собственный опыт аналогичного сравнительного исследования 3-летнего применения растительного экстракта Serenoa repens показал, что даже в течение этого периода из контрольной группы выбыло 22% пациентов, что косвенно доказывает правомочность несравнительного дизайна исследования в случае 10-летнего периода оценки прогрессирования АПЖ [14].
Целью исследования была оценка эффективности простамола® уно в предотвращении прогрессирования симптомов заболевания у больных АПЖ с начальными ее проявлениями при помощи анкет IPSS и QoL (BS).
Для достижения цели исследования были поставлены следующие задачи:
- оценить изменения максимальной скорости потока мочи;
- оценить изменения объема мочеиспускания;
- оценить изменения объема остаточной мочи;
- оценить изменения объема предстательной железы;
- оценить безопасность и переносимость простамола® уно.
Материалы и методы. Проведено открытое несравнительное наблюдательное исследование эффективности и безопасности непрерывного применения растительного экстракта Serenoa repens (простамола® уно) в дозировке 320 мг 1 раз в сутки в течение 10 лет 38 пациентами с риском прогрессирования АПЖ.
Критерии включения: мужчины в возрасте от 45 до 60 лет с диагнозом АПЖ; выраженность симптомов по шкале IPSS от 8 до 15 баллов и длительность симптомов – более 3 мес; объем простаты – более 30 см3; максимальная объемная скорость потока мочи (Qmax) – 10–15 мл/с; объем мочеиспускания – 125–350 мл; объем остаточной мочи – менее 50 мл; уровень ПСА в сыворотке крови – менее 4 нг/мл; отсутствие роста микрофлоры в бактериологическом анализе 3-й порции мочи/ секрета простаты; наличие письменного согласия на участие в исследовании.
Критерии исключения: проводимая терапия АПЖ или хронического простатита за последние 6 и 3 мес соответственно; злокачественный онкологический процесс в мочеполовой системе; острая задержка мочеиспускания; нейрогенные дисфункции и дивертикулы мочевого пузыря; камни мочевого пузыря; стриктура уретры, склероз шейки мочевого пузыря; наличие в анамнезе оперативных пособий на органах малого таза; инфекции мочеполовой системы в фазе активного воспаления; систематический прием средств, влияющих на функцию мочевого пузыря и мочеотделение; тяжелые сопутствующие заболевания сердечнососудистой и неврологической систем, психиатрические заболевания, клинически значимая почечная и печеночная недостаточность (увеличение показателей в два и более раз) и пр.; заведомо известная аллергия на исследуемые препараты или любой из их компонентов; любое клинически значимое состояние, из-за которого, по мнению исследователя, пациент не может принимать участие в исследовании, включая злоупотребление наркотиками или алкоголем или выраженную печеночную недостаточность; участие в любом клиническом исследовании в течение 90 дней или участие более чем в трех клинических исследованиях в течение 12 мес до предположительной даты включения в исследование.
Критерии эффективности: изменение баллов по шкалам IPSS, QoL; изменение показателя Qmax, объема мочеиспускания, объема остаточной мочи, объема предстательной железы; отсутствие задержек мочеиспускания, оперативных пособий по поводу АПЖ.
Критерии безопасности: выявление нежелательных эффектов, непосредственно связанных с проводимой терапией простамолом® уно; их частота и выраженность, показатели жизненных функций (АД, ЧСС), лабораторные показатели.
Основным показателем эффективности являлось изменение балла по шкалам IPSS и QoL (BS). Все пациенты проходили обследование 11 раз: 1-й раз – в момент включения, в дальнейшем – каждый год в течение 10 лет. Общая продолжительность наблюдения составила 10 лет.
Методы исследования эффективности: оценка симптомов заболевания в баллах по шкалам IPSS и QoL (BS), урофлоуметрия, УЗИ предстательной железы и мочевого пузыря, определение уровня ПСА в сыворотке крови.
Методы исследования безопасности: измерение АД и ЧСС, ЭКГ в 6 стандартных отведениях, общий и биохимический анализ крови (включая печеночные ферменты АсАТ и АлАТ), регистрация нежелательных эффектов и изучение их возможной связи с исследуемым препаратом.
 К настоящему моменту исследование полностью завершено и результаты всех описанных выше объективных и субъективных методов обследования обработаны. Для удобства восприятия представлены исходные параметры и результаты за каждые последующие два года наблюдения – итого 6 контрольных точек.
К настоящему моменту исследование полностью завершено и результаты всех описанных выше объективных и субъективных методов обследования обработаны. Для удобства восприятия представлены исходные параметры и результаты за каждые последующие два года наблюдения – итого 6 контрольных точек.
Поскольку число ретроспективных наблюдений было невелико, однако в них больные длительное время применяли препарат, для анализа показателей использовали тест Фридмана. Данный тест представляет собой расширение теста Уилкоксона в случае наличия более чем двух зависимых выборок. Он основывается на ранговых последовательностях, которые строятся для значений всех переменных, участвующих в тесте. Логика критерия Фридмана весьма проста. Каждый больной один раз наблюдается в фиксированные моменты времени. Результаты наблюдений у каждого больного упорядочиваются. Таким образом, получается столько упорядоченных рядов, сколько больных участвует в исследовании. Далее для каждого момента наблюдения вычисляется сумма рангов. Если разброс сумм велик – различия статистически достоверны. Ранг – номер, под которым стоят данные, если выстроить их по возрастанию.
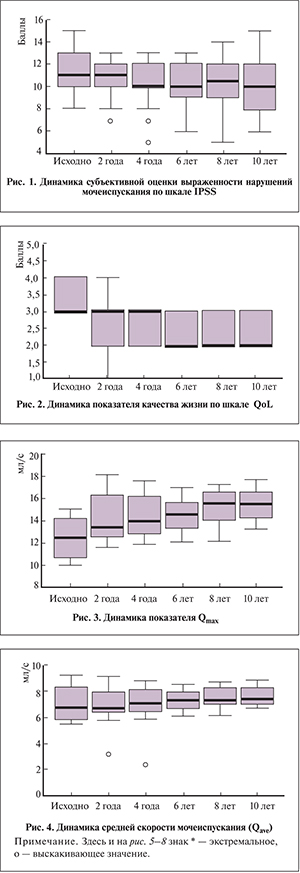
Результаты и обсуждение. Как видно на рис. 1, на протяжении всего срока наблюдения ни у кого из пациентов ухудшения субъективной оценки симптомов АПЖ не происходило. Более того, у пациентов наступало достоверное уменьшение выраженности симптоматики (p=0,012).
Качество жизни всех пациентов за время наблюдения достоверно улучшилось (p=0,001), о чем свидетельствуют результаты опроса пациентов (рис. 2).
Динамика Qmax и Qave (рис. 3, 4) свидетельствовала об улучшении обоих показателей (p=0,001 для обоих показателей), что является крайне важным объективным критерием эффективности длительной постоянной терапии растительным экстрактом Serenoa repens.
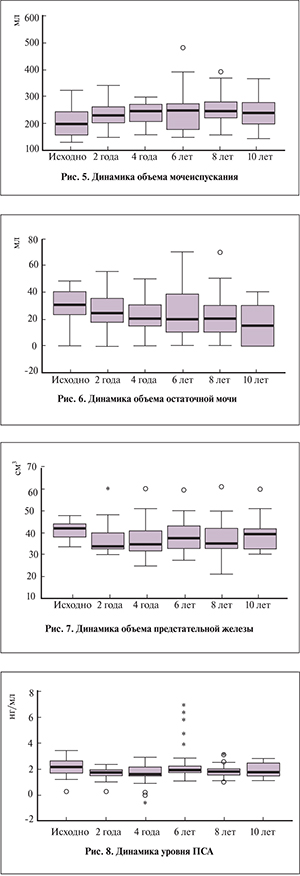
За время наблюдения у пациентов достоверно увеличился объем выделяемой мочи во время акта мочеиспускания (p=0,004), а также уменьшился объем остаточной мочи (p=0,001), что свидетельствует об объективном улучшении состояния мочевого пузыря (рис. 5, 6).
Одним из самых важных объективных критериев эффективности лечения пациентов с АПЖ является динамика размеров простаты. В ходе нашего исследования на протяжении 10 лет размеры простаты претерпевали определенные колебания в незначительных пределах, однако эти изменения были достоверными (p=0,001). Важно подчеркнуть, что по окончании наблюдения за пациентами в группе не наблюдалось достоверного роста АПЖ (рис. 7). Тем самым мы хотим подчеркнуть, что данный вид терапии позволяет остановить прогрессирование роста АПЖ и улучшить функцию мочевого пузыря, проявлявшуюся в увеличении скоростей мочеиспускания, объема выделяемой мочи и уменьшении объема остаточной мочи.
Одним из признаков отсутствия прогрессирования АПЖ являлось достоверно стабильное содержание ПСА (p=0,02) у наших пациентов (рис. 8). При этом терапия, проведенная пациентам, не влияла на истинный уровень ПСА – у ряда пациентов была выполнена биопсия простаты в связи с увеличением показателя выше 4 нг/мл.
По окончании исследования был проведен анализ нежелательных эффектов. За весь период наблюдения ни у одного пациента не было диагностировано острой задержки мочеиспускания. Ни одно из изменений общесоматического состояния, зарегистрированных в ходе исследования (респираторные болезни, обострения хронических заболеваний легких, желудочно-кишечного тракта и сердечно-сосудистых заболеваний), не было расценено как связанное с приемом исследуемого препарата. Двое пациентов перенесли травмы легкой степени тяжести, связанные с дорожно-транспортными происшествиями. Пятеро пациентов были планово прооперированы: двоим выполнена лапароскопическая холецистэктомия по поводу калькулезного холецистита, троим – стентирование коронарных сосудов в связи с ишемической болезнью сердца. Пациенты продолжали принимать исследуемый препарат до, после и частично во время госпитализаций. Пятерым пациентам была проведена биопсия предстательной железы в связи с повышением уровня ПСА более 4 нг/мл, однако ни у одного из них гистологических признаков рака предстательной железы не выявлено.
Заключение. Результаты проведенного исследования позволяют утверждать, что применение растительного экстракта Serenoa repens на постоянной основе в суточной дозе 320 мг является эффективным и безопасным способом проведения профилактики прогрессирования АПЖ. Эффективность назначения экстракта Serenoa repens выражалась как в отсутствии увеличения выраженности субъективных симптомов по шкалам IPSS, QoL (BS), так и в объективном отсутствии прогрессирования заболевания, обычно выражающегося в росте объема простаты, снижении скорости мочеиспускания, увеличении объема остаточной мочи. При этом у пациентов не возникали нежелательные эффекты, связанные с непосредственным приемом исследуемого препарата.



