Введение. Распространенность эректильной дисфункции (ЭД) среди мужчин в возрасте от 40 до 70 лет составляет 52% [1]. Однако в России этот показатель предположительно выше, чем в индустриально развитых странах, в связи с высоким травматизмом мужского населения, значительным потреблением низкокачественного алкоголя и низкосортного табака [2].
Адекватность эрекции обеспечивается сохранной нервной регуляцией, функциональной состоятельностью сосудов и здоровой кавернозной тканью. Васкулогенная ЭД, а точнее: артериогенный вид, – наиболее распространенная форма заболевания [3, 4]. Она является следствием нарушения притока крови к кавернозным телам, вследствие чего невозможно достичь необходимого для совершения полового акта уровня интракавернозного давления [5].Однако эти нарушения не всегда имеют органический характер, как предполагалось раньше с позиций атеросклеротического поражения сосудов. Доказательством отсутствия органических поражений внутренних половых и кавернозных артерий служат отсутствие сужения их и без того малого диаметра, обратимость нарушений эрекции на фоне терапии ингибиторами фосфодиэстеразы 5-го типа (ФДЭ-5) [6]. Именно изменения функционирования эндотелиальных клеток пещеристых тел полового члена по выработке оксида азота (NO) являются первоосновой нарушения артериального кровенаполнения полового члена. Потеря функциональной целостности эндотелия и последующие нарушения эндотелиальной функции играют ключевую роль в возникновении эндотелиальной дисфункции [7]. Поскольку эндотелиальная дисфункция – состояние обратимое, определение уровня ее маркеров, а значит, и диагностика степени поражения сосудов могут иметь решающее значение в диагностике и лечении нарушений эректильной функции.
Процессы эндотелиальной дисфункции, возможность их обратного развития на начальных этапах ЭД изучены на примере пациентов, страдающих артериальной гипертензией (АГ) и имеющих отклонения в половой сфере. Общим у АГ и ЭД является патогенез развития, в частности нарушение правильного функционирования клеток эндотелиального слоя сосудов. Выделяют так называемые нагрузочные гипертонически направленные профессии, к которым относятся работники подвижного состава, в связи с необходимостью сохранения высокого внимания, готовности к экстренному действию в условиях монотонно действующих факторов, скорости реагирования и др. [8, 9]. В Российских клиническиихрекомендациях впервые прозвучал термин «скрытая гипертония», одной из форм которой является «гипертония на рабочем месте». Последняя является клиническим проявлением стресс-индуцированной АГ, характеризующейся повышением АД под воздействием психоэмоциональных факторов на фоне нормального или стабильно повышенного его уровня [10].

Материалы и методы. После получения добровольного согласия и заполнения соответствующей документации в отделении урологии проведено дополнительное обследование 51 больного, получавшего лечение в отделении терапии ОКБ на ст. Барнаул по поводу первичной АГ (гипертонической болезни) I– II стадий, 1–3-й степеней повышения АД, риск 2–3. Целью данных мероприятий явилась ранняя диагностика нарушений в половой сфере у лиц с АГ с позиции связи двух этих патологических состояний через эндотелиальную дисфункцию.
Комплексное клиническое обследование включало сбор анамнеза, осмотр, клинические анализы крови и мочи, определение уровня общего тестостерона, глобулина, связывающего половые гормоны (ГСПГ), гормонов щитовидной железы, липидограммы. Кроме того, использовали специальные методы для диагностики эндотелиальной дисфункции и ЭД. Для выявления ЭД и оценки ее тяжести использовали опросник мужской копулятивной функции Лорана–Сегала (МКФ), международный индекс эректильной функции (МИЭФ). Объективным показателем нарушения половой функции можно считать оценку субстрата, непосредственно ответственного за осуществление полового акта, а именно: состояние эндотелиоцитов кавернозных тел. Микроциркуляцию сосудов полового члена оценивали с помощью метода лазерной допплеровской флоуметрии (ЛДФ).
Для полного представления об ЭД у пациентов с АГ были использованы общепринятые при оценке состояния сердечно-сосудистой системы, но нестандартные в урологической практике методы определения маркеров функции эндотелия. Данные маркеры позволяют определять тактику лечения, непосредственную эффективность применяемых схем терапии, а также оценить прогноз развития заболевания. Выраженность эндотелиальной дисфункции определяли по уровню содержания в крови эндотелина 1, асимметричного диметиларгинина (АДМА).
Методом случайной выборки больные АГ были разделены на две группы. В 1-й группе (n=25) проводилась базисная антигипертензивная терапия совместно с ингибитором ФДЭ-5 уденафилом (зидена) по 50 мг 1 раз в день ежедневно в течение 1 мес. Двадцать шесть человек 2-й группы получали только антигипертензивную терапию. Все пациенты, согласно международной классификации возраста человека, рекомендованной Европейским региональным бюро ВОЗ (Женева, 1973), относились к молодому и среднему возрасту, т.е. к возрастной группе сексуальной зрелости от 30 до 50 лет. Средний возраст составил 47,3±1,3 года.
В группу контроля вошли 32 условно здоровых работника локомотивных бригад без хронических заболеваний (средний возраст – 44,5±3,5 года), которых также обследовали по вышеописанному плану. Достоверных различий между больными и группой контроля не обнаружено. Показатели лабораторных исследований маркеров эндотелиальной дисфункции у здоровых лиц были приняты за норму, что соответствовало принятым в литературе нормальным показателям.
Результаты. До начала терапии у всех пациентов имелись проявления нарушений половой функции (табл. 1). Оценка по вопроснику МКФ для пациентов в возрасте 36–50 лет в норме составляет 36 баллов. В нашем исследовании она составила 21,4±2,6 балла. Нарушения, в частности, касались эректильной составляющей анкеты МКФ – 3,1±1,8 балла. По шкале МИЭФ для здорового пациента максимальная сумма баллов составляет 75, в нашем исследовании средний балл соответствовал 41,2±3,8. Таким образом, у 37% пациентов диагностирована легкая степень ЭД, у 67% – средняя. При этом ни один из обследуемых не обращался и не планировал в ближайшее время прибегать к специализированной медицинской помощи в связи с имеющимися нарушениями. После месячного курса лечения у пациентов 1-й группы констатировано увеличение баллов по всем составляющим опросников, достоверное увеличение общего балла по обоим опросникам, МКФ (см. табл. 1). В то же время во 2-й группе достоверно увеличилось только количество баллов в психогенном домене, что в нашем исследовании не представляет клинического интереса.
Ни у одного из пациентов отклонений в гормональном профиле не выявлено, что исключает гормональную этиологию ЭД. Андрогенный индекс, определяемый как отношение уровня общего тестостерона к ГСПГ, у всех пациентов был больше 70%, что соответствует норме.
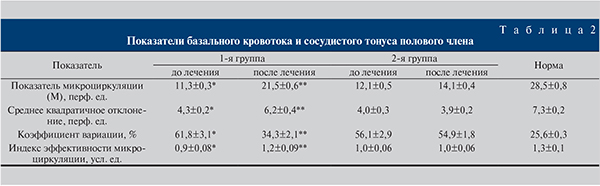
При оценке показателей микроциркуляции сосудов кавернозных тел полового члена исходно зарегистрированы изменения расчетных показателей в сторону спастического нарушения микроциркуляции (табл. 2). Об этом свидетельствует снижение показателя величины среднего потока крови М, снижение интенсивности перфузии кавернозной ткани. По результатам оценки ритмических изменений потока эритроцитов в пользу спастических нарушений свидетельствует низкая амплитуда пульсовых колебаний, пассивного механизма регуляции микроциркуляции и соответственное увеличение амплитуды медленных колебаний, а также возрастание вазомоторной активности. У пациентов, прошедших курс терапии уденафилом, отслеживалась достоверная тенденция к вазодилатации, отмечено снижение ишемизации тканей, увеличение показателя микроциркуляции, увеличение пассивного механизма регуляции кровотока; практически нормальных показателей достиг индекс эффективности микроциркуляции. Достоверного изменения показателей микроциркуляции во 2-й группе отмечено не было.
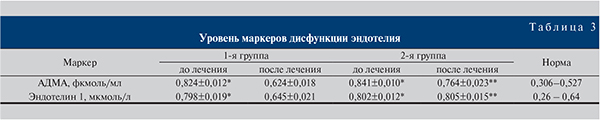
Как видно из табл. 3, перед началом лечения у всех пациентов, страдавших ЭД на фоне АГ, уровень маркеров эндотелиальной дисфункции был повышен, что вписывается в рамки представления о патогенезе обоих заболеваний. Это свидетельствует о нарушении процессов NО-зависимой вазодилатации, а также непосредственном дефиците NO. Выбранный метод коррекции ЭД курсовой схемой ежедневного приема ингибитора ФДЭ-5 уденафила является патогенетически обоснованным. Интерес представляют динамическое наблюдение за маркерами и возможность коррекции ЭД путем влияния на эндотелиальную дисфункцию. В 1-й группе отмечено уменьшение уровня обоих маркеров эндотелиальной дисфункции, а следовательно, нормально протекает NO-зависимая регуляция сосудистого тонуса. Нивелирование состояния, при котором вследствие повышенного уровня АДМА, NO-синтаза блокируется последним и нарушается NO-зависимая вазодилатация, как и множество ингибирующих эффектов NO на клеточную пролиферацию, межклеточное взаимодействие, а также на образование свободных радикалов, т.е. корректируется сама эндотелиальная дисфункция.
Обсуждение. Повышение уровня маркеров эндотелиальной дисфункции у пациентов с ЭД на фоне стресс-индуцированной АГ расширяет понимание этиологии процессов нарушения половой функции. АДМА вызывает значительное, причем зависящее от концентрации подавление синтеза NO; вмешивается в работу NO-синтазы, которая вместо молекул NO начинает накапливать О2-. При возрастании в крови уровня АДМА NO-синтаза блокируется последним, что приводит к нарушению NO-зависимой вазодилатации, реализации ингибирующих эффектов NO на клеточную пролиферацию, межклеточное взаимодействие, а также на образование свободных радикалов [11]. Указанные изменения свидетельствуют об эндотелиальной дисфункции, которая в свою очередь усугубляет течение ЭД. Второй выбранный нами маркер эндотелиальной дисфункции – эндотелин 1 – является одним из основных контрагентов NO. В физиологических концентрациях эндотелин действует на эндотелиальные рецепторы, вызывая высвобождение факторов релаксации, а в более высоких – активирует рецепторы на гладкомышечных клетках, стимулируя стойкую вазоконстрикцию. С учетом механизма действия ингибиторов ФДЭ-5 именно восстановление NO-зависимых процессов вазодилатации играет ключевую роль в коррекции эндотелиальной дисфункции у пациентов с ЭД.
Следовательно, процессы, приводящие к ЭД на фоне АГ, носят характер функциональных сосудистых патологических изменений. Уменьшение уровня маркеров эндотелиальной дисфункции на фоне терапии ингибитором ФДЭ-5 свидетельствует о восстановлении функции клеток эндотелия и нормализации процессов вазодилатации и вазоконстрикции, что подтверждается показателями микроциркуляции сосудов полового члена по данным ЛДФ.
Заключение. О функциональном характере нарушений в половой сфере больных АГ свидетельствует положительная динамика уровня маркеров дисфункции эндотелия и показателей микроциркуляции на фоне лечение ингибитором ФДЭ-5 уденафилом. Это позволяет расценивать ЭД для данной категории пациентов как стресс-индуцированную. Наличие ЭД у лиц нагрузочных «гипертонически» направленных профессий является потенциальным признаком бессимптомного заболевания сердечно-сосудистой системы.
Поскольку эндотелиальная дисфункция сосудов – состояние обратимое, определение уровня ее маркеров вносит значимый вклад не только в диагностику, но и в эффективность терапии как заболеваний сердечно-сосудистой системы, так и нарушений эректильной функции.
Это меняет раннее бытовавшее мнение об ЭД как о вторичном осложнении системных сосудистых заболеваний и позволяет сформировать принципиально новый подход к вопросам ее лечения. При этом очевидным является и то, что для возможности предупреждения и прогрессирования ЭД как сосудистого патологического процесса важно выявление эндотелиальной дисфункции на ранних стадиях до развития необратимых состояний.



