Введение. Радикальная простатэктомия (РПЭ) обеспечивает высокую безрецидивную и раковоспецифическую выживаемость [1], оставаясь одним из основных и наиболее часто используемых методов лечения клинически локализованного и местнораспространенного рака предстательной железы [2]. Вне зависимости от варианта хирургического доступа и технических особенностей оперативного вмешательства необходимость формирования уретровезикального анастомоза предполагает последующее дренирование мочевого пузыря. Несмотря на ряд исследований, указывающих на безопасность раннего (на 2–3-е сутки после операции) удаления уретрального катетера, общепринятым стандартным подходом остается дренирование мочевого пузыря в течение 6–10 дней [3–5].
В настоящее время отсутствует консенсус относительно оптимальной схемы периоперационной антибактериальной профилактики при РПЭ [6]. Так, клинические рекомендации Европейской ассоциации урологии указывают на слабую доказательную базу, не позволяющую сделать однозначный вывод о схеме и целесообразности антибактериальной профилактики при РПЭ. Ряд других международных и отечественных клинических рекомендаций, в том числе Стратегия контроля антимикробной терапии (СКАТ), относят РПЭ к условно чистым процедурам и рекомендуют однократное введение дозы антибиотика до операции (наиболее часто применяются цефалоспорины III–IV поколений). В случае отсутствия факторов очень высокого риска инфекционных осложнений или активной инфекции продолжение антибактериальной профилактики свыше 24 ч не показано, а наличие дренажей или катетеров не является обоснованным аргументом в пользу ее продолжения [7–9].
В реальной клинической практике антибиотики достаточно часто назначаются на все время катетеризации мочевого пузыря [10]. Очевидно, что это повышает риск развития резистентности, антибиотик-ассоциированной диареи и других осложнений, а формирование на катетере биопленок делает такую терапию неэффективной. В то же время наличие уретрального катетера является одним из наиболее значимых факторов риска развития осложненной инфекции мочевыводящих путей (ИМП), риск которой возрастает на 3–7% с каждым днем катетеризации [11]. Одним из возможных направлений предотвращения развития катетер-ассоциированной ИМП является антибактериальная профилактика при удалении катетера, однако имеющиеся сведения об эффективности данного подхода имеют противоречивый характер [12].
Цель исследования: оценить эффективность антибактериальной профилактики с применением фосфомицина при удалении уретрального катетера после радикальной простатэктомии в отношении развития эпизодов инфекции мочевыводящих путей, бактериурии и лейкоцитурии, а также оценить влияние антибиотикопрофилактики на степень выраженности симптомов нижних мочевыводящих путей.
Материалы и методы. Дизайн исследования. Одноцентровое открытое проспективное рандомизированное контролируемое исследование выполнено на научно-клинической базе ГБУЗ ГКБ им. С. П. Боткина ДЗМ и кафедры урологии и хирургической андрологии ФГБОУ ДПО РМАНПО Минздрава РФ. Протокол исследования был одобрен Локальным этическим комитетом. В рамках исследования фиксировались клинические и периоперационные характеристики, включая возраст, сопутствующие медицинские заболевания, индекс массы тела, простатспецифический антиген, объем предстательной железы, время операции, объем кровопотери, продолжительность госпитализации, длительность катетеризации, послеоперационные осложнения.
Пациенты включались в исследование и случайным образом распределялись в группы анализа и контроля на момент госпитализации в стационар перед оперативным лечением. Рандомизация в группу 1 (исследование) и группу 2 (контроль) проводилась с использованием онлайн-генератора случайных чисел (www.random.org). Все пациенты заполняли опросник IPSS (International Prostate Symptom Score) и сдавали клинический анализ мочи до операции. При наличии отклонений в клиническом анализе мочи выполнялось бактериологическое исследование мочи (посев мочи) с определением чувствительности к антимикробным препаратам. В исследование не включались пациенты с наличием цистостомического дренажа на момент операции, а также с ростом микрофлоры по данным предоперационного посева мочи. Во всех случаях была выполнена периоперационная антибактериальная профилактика в течение 24 ч препаратами из группы цефалоспоринов III поколения, далее пациентам была выполнена позадилонная или робот-ассистированная радикальная простатэктомия.
Все пациенты были выписаны из стационара на 4–6-е сутки после операции, удаление уретрального катетера осуществлялось амбулаторно без выполнения уретроцистографии, средняя длительность катетеризации составила 8,4 дня в группе исследования и 8,5 дней в контрольной группе (p=0,89). Пациенты группы 1 (исследование, n=40) принимали две дозы фосфомицина по 3 г перорально: вечером в день удаления катетера (первая доза) и через 48 ч после удаления катетера (вторая доза). Пациентам группы 2 (контроль, n=37) антибактериальная профилактика при удалении уретрального катетера не проводилась. Пациентам были предоставлены устные и письменные инструкции, как принимать антибиотик, а также о признаках и симптомах ИМП. Каждому пациенту выдавались опросник IPSS и памятка о необходимости сдать клинический анализ мочи и посев мочи на микрофлору через 4 нед. после удаления уретрального катетера (посев мочи выполнялся ранее в случае наличия клинической картины ИМП). Критерием исключения из исследования являлись отказ пациента от рекомендованного приема антибактериального препарата, самостоятельное использование иных антибактериальных препаратов, а также развитие после операции хирургических осложнений III–IV классов по классификации Clavien–Dindo. Со всеми пациентами через 1 мес. после удаления уретрального катетера проводилась беседа по телефону, в том числе посредством приложений для обмена сообщениями (мессенджеров), либо проводилась очная консультация.
Оцениваемые исходы. Конечными точками исследования являлись подтвержденные клинические эпизоды ИМП в течение 1 мес. после удаления уретрального катетера, результаты лабораторных исследований (лейкоцитурия и бактериурия в клиническом анализе мочи/рост микрофлоры в посеве мочи), степень выраженности СНМП по данным опросника IPSS. Симптоматическая ИМП определялась как положительный посев мочи (рост одного и более микроорганизмов в концентрации >105 КОЕ/мл) и наличие как минимум одного характерного симптома (болезненное/учащенное мочеиспускание, задержка мочи, лихорадка, боль в надлобковой области/животе, гематурия) [13]. Вторичной точкой исследования было развитие специфических осложнений при антибактериальной профилактике при удалении уретрального катетера (аллергические реакции, головная боль, головокружение, диспептические явления, боли в животе, диарея, тахикардия и др).
Статистический анализ. Для оценки непрерывных переменных использовался U-тест Манна–Уитни, при сравнительном анализе категориальных данных использовался хи-квадрат-тест (хи-квадрат Пирсона). При всех видах статистического анализа за достоверное принималось значение p<0.05. Для статистической обработки информации использовалось программное обеспечение GraphPad Prism 8 (GraphPad Software Inc, La Jolla, CA, USA).
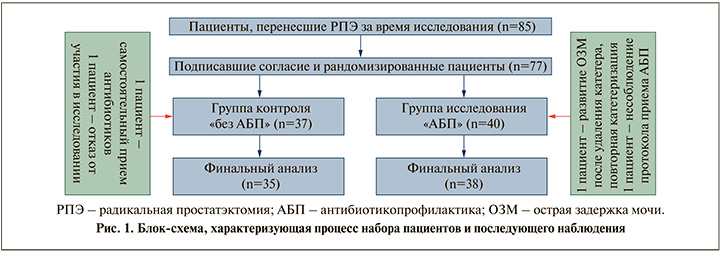
Результаты. В период с августа по октябрь 2023 г. в исследование были включены в общей сложности 77 пациентов, из которых 73 включены в окончательный анализ (1 пациент был исключен по причине несоблюдения протокола исследования; 1 – в связи с развитием осложнения, потребовавшего повторной катетеризации; 1 – в связи с самостоятельным приемом иных антибиотиков; 1 – вследствие отказа от участия в исследовании). Группу исследования составили 38 пациентов, группу контроля – 35 (рис. 1). Клинические характеристики и периоперационные исходы были схожими в обеих группах (табл. 1). Длительность катетеризации статистически значимо не различалась, составив 8,5 (±1,4) дней в контрольной группе и 8,4 (±1,2) дня в группе антибиотикопрофилактики фосфомицином (p=0,89; табл. 1).
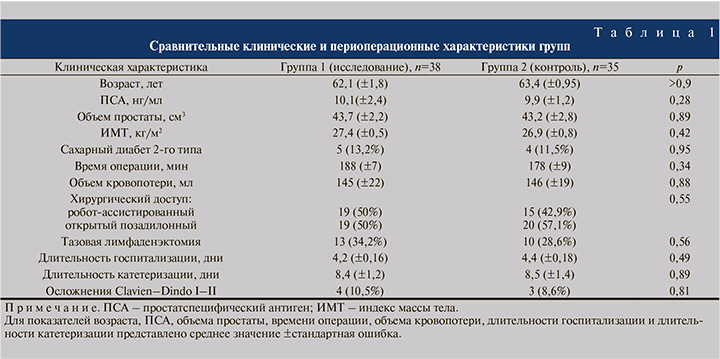
В целом у 7 (9,6%) пациентов развилась ИМП в течение 4 нед. после удаления уретрального катетера, из них в контрольной группе ИМП отмечена у 6 (17,1%) пациентов, в группе исследования – у 1 (2,6%) (p=0,032). Наблюдалась значительная вариабельность в сроках: от удаления катетера до эпизода ИМП (от 4 до 20 дней). Лейкоцитурия и бактериурия при контрольном клиническом анализе мочи существенно реже наблюдались в группе пациентов, которым была проведена антибактериальная профилактика фосфомицином при удалении уретрального катетера: 18,4 и 48,6% соответственно (p=0,006). В табл. 2 приведены результаты посева мочи на микрофлору в обеих группах в течение исследования, включая пациентов, которым культуральное исследование было выполнено в связи с развитием клинического эпизода ИМП. Рост микрофлоры, по данным посева мочи, в рамках исследования наблюдался у 7,9% в группе пациентов, которым проводилась антибактериальная профилактика, и у 25,7% в группе контроля (p=0,035).

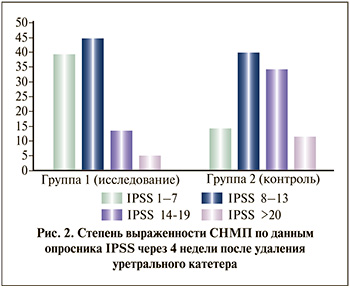
До РПЭ между группами исследования и контроля не было выявлено достоверных различий в выраженности СНМП: средний балл по шкале IPSS составил 11,3 и 11,1 соответственно (p=0,85). При этом при анкетировании в контрольной точке через 4 нед. после удаления уретрального катетера средний балл по шкале IPSS оказался существенно выше в группе, не получавшей антибактериальной профилактики фосфомицином (13,2 и 9,5; p=0,002).
У данной группы чаще наблюдались умеренные и тяжелые СНМП, по данным анкетирования (рис. 2). В рамках исследования в обеих группах не было отмечено случаев аллергической реакции, а также не было выявлено случаев псевдомембранозного колита, связанного с C. difficile.
У 2 (5,2%) пациентов из группы антибиотикопрофилактики отмечено развитие диареи (в одном наблюдении после приема первой дозы, в другом – второй дозы фосфомицина), при этом в обоих случаях диарея разрешилась в течение 48 ч на фоне терапии энтеросорбентами.
Обсуждение. Катетер-ассоциированные ИМП являются наиболее частой внутрибольничной инфекцией и причиной развития вторичной бактериемии, приводя к существенной морбидности и дополнительным финансовым затратам на лечение [11]. Уретральный катетер может обеспечивать прямой путь для периуретрального проникновения микробов в мочевой пузырь. Катетеры проходят сфинктерный аппарат мочеиспускательного канала, исключают естественную эвакуацию бактерий, связанную с самостоятельным мочеиспусканием, тем самым увеличивая риск развития ИМП. Уропатогенная Escherichia coli является наиболее распространенным возбудителем как неосложненной, так и осложненной ИМП, на долю которой приходится 75 и 65% инфекций соответственно. При осложненной катетер-ассоциированной ИМП наиболее распространенными возбудителями после E. coli являются Enterococcus spp. (11%), Klebsiella pneumoniae (8%), Candida spp. (7%), Staphylococcus aureus (3%), Proteus mirabilis (2%), Pseudomonas aeruginosa (2%) [11]. Краеугольным камнем профилактики и лечения являются антибиотики, однако поверхность катетера подвержена образованию биопленок, следовательно, часто устойчива к проникновению препаратов. На это указывают и клинические исследования: например, в работе F. Hartung и соавт. одна доза ципрофлоксацина или левофлоксацина внутривенно до РПЭ оказалась также эффективной в отношении профилактики инфекционных осложнений, как и длительная многодневная антибактериальная профилактика до удаления уретрального катетера (одна доза внутривенно с последующим пероральным приемом) [14]. Кроме того, известно, что лечение антибиотиками имеет нежелательные эффекты, способствуя формированию устойчивых штаммов бактерий и изменяя микробиоту кишечника, что в свою очередь может открыть дополнительные ниши для колонизации устойчивыми организмами [11, 15].
В качестве возможного пути профилактики инфицирования рассматривались различные модификации уретральных катетеров. Была проведена оценка катетеров с покрытием из гидрогеля, тефлона, сплава серебра c импрегнацией нитрофуразоном [16]. Разработаны модели с дополнительным количеством перфоративных отверстий, что дает возможность интенсивного орошения слизистой уретры растворами антисептиков и отведения экссудата [17]. Однако, несмотря на позитивные результаты отдельных исследований, в целом использование различных покрытий и технических модификаций не продемонстрировало значительного снижения частоты развития инфекционных осложнений, что в совокупности с экономическими аспектами не способствовало широкому внедрению таких катетеров в клиническую практику [11, 18].
Противоречивый характер имеют и научные данные относительно эффективности антибактериальной профилактики при удалении уретрального катетера. Так, в проспективном рандомизированном исследовании C. Berrondo и соавт. применение ципрофлоксацина перед удалением уретрального катетера после РПЭ не привело к снижению частоты ИМП [19]. С другой стороны, согласно мета-анализу J. Marschall и соавт., пациенты, госпитализированные в стационар и перенесшие непродолжительную (14 дней) катетеризацию мочевого пузыря, могут выиграть от антибактериальной профилактики при удалении уретрального катетера: абсолютное снижение риска составило 5,8%, а для профилактики одного случая ИМП необходимо пролечить 17 пациентов [20]. Последующий мета-анализ L. Liu и соавт. подтвердил данное наблюдение – авторы указали на наибольшие преимущества при антибактериальной профилактике у пациентов старше 60 лет, при длительной катетеризации (более 5 дней), а также при использовании триметоприма/сульфаметоксазола [12]. В рандомизированном исследовании O. Gildor и соавт. однократный пероральный прием цефуроксима 500 мг или триметоприма/сульфаметоксазола 160/800 мг (в случае известной аллергии на пенициллины) за час до удаления катетера значительно снизил выраженность дизурии и частоту повторных госпитализаций по поводу ИМП (1% по сравнению с 7,3% в контрольной группе, p=0,032) [21]. В рандомизированном исследовании B. Ehdaie и соавт., включившем суммарно 824 пациента, сравнивался одно- и трехдневный режимы профилактики с использованием ципрофлоксацина при удалении уретрального катетера. В группе однодневной профилактики не было выявлено ни одного наблюдения ИМП, в то время как в группе трехдневной профилактики частота ИМП составила 0,7% (3 наблюдения), что позволило авторам сделать вывод о целесообразности применения однодневной профилактики [22]. Обращает на себя внимания в целом очень низкая частота ИМП в рамках данного исследования с учетом того факта, что другие работы указывают на высокую встречаемость резистентных к ципрофлоксацину микроорганизмов при посеве образца мочи на момент удаления катетера после РПЭ [23].
Отсутствие единых клинических рекомендаций и неоднозначные результаты исследований диктуют необходимость поиска новых схем антибактериальной профилактики при удалении уретрального катетера. Фосфомицин является стандартом терапии неосложненных ИМП у женщин, а в последнее время появляются данные о его эффективности при терапии осложненных ИМП [24–26]. Кроме того, опубликованный под эгидой Европейской урологической ассоциации мультидисциплинарный консенсус рекомендовал пероральное применение фосфомицина в качестве возможной антибактериальной профилактики при трансректальной биопсии предстательной железы с учетом низкого уровня резистентности, высокой эффективности и хорошего профиля безопасности [27]. Данные обстоятельства стали основой для планирования нашего исследования.
Полученные результаты в очередной раз подтвердили значимость проблемы катетер-ассоциированных ИМП и продемонстрировали сравнительно высокую частоту развития эпизодов инфекции после удаления уретрального катетера после РПЭ. Пероральная антибактериальная профилактика фосфомицином 3 г при двукратном приеме представляется эффективной схемой, приводя к значимому сокращению эпизодов ИМП, бессимптомной бактериурии и лейкоцитурии, а также выраженности СНМП, не вызывая при этом значимых осложнений. Главным ограничением проведенного исследования является отсутствие «ослепления», что могло оказать влияние на результаты с позиции пациентов или врачей. Другое ограничение – невозможность достоверно дифференцировать этиологию СНМП в обеих группах, которые могут быть следствием как ИМП, так и непосредственно оперативного вмешательства и катетеризации. Тем не менее с учетом одинаковой выраженности СНМП в обеих группах до операции представляется возможным вывод о потенциальном влиянии антибактериальной профилактики на полученные результаты в отношении качества мочеиспускания. Очевидно, требуются дальнейшие исследования, изучающие эффективность и безопасность антибактериальной профилактики фосфомицином при удалении уретрального катетера не только после РПЭ, но и при длительной катетеризации по поводу других причин, проведение слепых плацебо-контролируемых исследований, а также изучение возможности использования одной пероральной дозы фосфомицина.
Выводы. Антибактериальная профилактика с использованием двух пероральных доз фосфомицина 3 г в день удаления уретрального катетера и через 48 ч после удаления уретрального катетера после РПЭ представляется эффективной схемой, снижающей частоту ИМП и тяжесть СНМП, а также характеризующейся минимальным риском нежелательных явлений. Необходимы проведение дальнейших исследований и разработка единых клинических рекомендаций по антибактериальной профилактике при урологических вмешательствах, требующих длительной (более 48–72 ч) катетеризации мочевого пузыря.



