Введение. Радикальная простатэктомия является «золотым» стандартом лечения пациентов с локализованным раком предстательной железы (РПЖ), несмотря на достижения лучевой терапии и различных экспериментальных видов лечения, таких как криоабляция и др. [1–3]. Робот-ассистированная радикальная простатэктомия (РАРПЭ) широко применяется в качестве стандартного хирургического лечения локализованного рака предстательной железы (РПЖ). Хотя показатели удержания мочи в отдаленном периоде, как показывают результаты современных исследований, улучшились после введения роботизированной хирургии, раннее послеоперационное недержание мочи по-прежнему остается одним из самых неприятных осложнений для пациентов [4, 24, 33]. Таким образом, важной целью РАРПЭ является предотвращение развития послеоперационного недержания мочи.
В литературе представлено множество методик улучшения послеоперационного восстановления мочеиспускания после радикальной простатэктомии [5–16]. Задняя реконструкция (ЗР) – один из наиболее распространенных способов улучшения мочеиспускания, имеющий несколько модификаций [17–24]. Этот метод направлен на обеспечение задней поддержки уретровезикального анастомоза путем приближения пересекающейся мышечно-фасциальной пластинки (рабдосфинктер) к краю фасции Денонвилье (стандартная техника ЗР), а также на облегчение последующего формирования пузырно-уретрального анастомоза при меньшем натяжении тканей. Мы посчитали, что дальнейшее усиление задней поддержки и меньшее напряжение на пузырно-уретральный анастомоз может быть предпосылкой к предотвращению недержания мочи после простатэктомии.
Цель исследования: оценить эффективность модифицированной методики ЗР (двухслойная ЗР уретроцистоанастомоза) в улучшении удержания мочи пациентов, перенесших РАРПЭ, по сравнению со стандартной техникой ЗР.
Материал и методы. В исследование включены 65 пациентов (средний возраст – 63 года) с локализованным РПЖ, находившихся на лечении в Институте урологии и репродуктивного здоровья человека Сеченовского Университета с июня 2016 по июнь 2019 г. Критерии включения в исследование: клинически локализованный рак предстательной железы (T1c–Т2); возраст менее 75 лет; состояние пациента по шкале ECOG (Eastern Cooperative Oncology Group) 0 или 1 балл. Критерии невключения в исследование: стриктуры уретры, нейрогенный мочевой пузырь, операция на предстательной железе в анамнезе, интерстициальный цистит или лучевая терапия на область таза. Критерием исключения было обнаружение местнораспространенного или метастатического РПЖ по результатам гистологического заключения. Пациентам была выполнена РАРПЭ одним хирургом с опытом более 100 операций РАРПЭ до начала исследования.
Пациенты были разделены на две группы в примерном соотношении 1:1. Пациентам первой группы (n=32) выполнена стандартная ЗР при формировании уретроцистоанастомоза, больным второй группы (n=35) – ЗР по модифицированной двухслойной методике.
Исследование было одобрено Локальным этическим комитетом Сеченовского Университета. Информированное согласие было получено от всех пациентов после объяснения цели и методов исследования.
Всем пациентам РАРПЭ выполнялась трансперитонеальным доступом. Задняя реконструкция выполнена до формирования пузырно-уретрального анастомоза. Для стандартной методики ЗР использована нить 3–0 с насечками (V-Loc™, Covidien, Mansfield, MA). Первый слой создавали путем соединения пересеченной мышечно-фасциальной пластинки (рабдосфинктера) позади уретры с рассеченным краем фасции Денонвилье, расположенной посередине между мочевым пузырем и уретрой. Далее формировали непосредственно анастомоз между шейкой мочевого пузыря и уретрой (рис. 1).
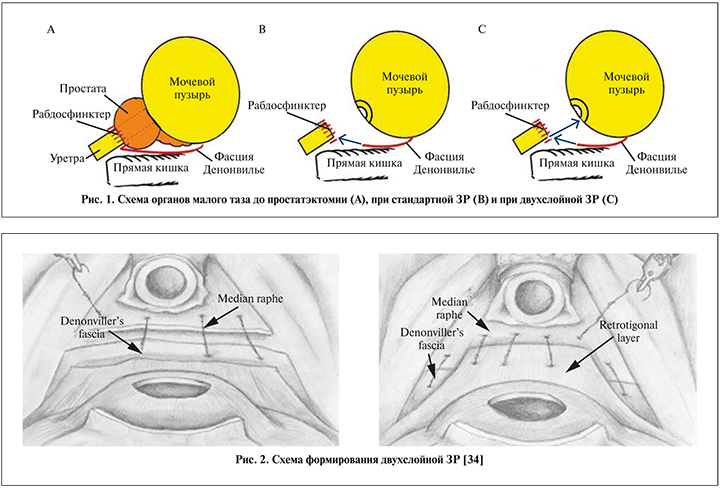
При двухслойной методике ЗР первый слой формировали так же, как и при стандартной технике, второй слой формировали путем прошивания рабдосфинктера чуть ниже мочеиспускательного канала с задней стенкой мочевого пузыря на расстоянии примерно 1–1,5 см кзади от шейки мочевого пузыря (дорсальная часть наружного слоя детрузора), в результате чего имело место меньшее натяжение тканей при формировании анастомоза между шейкой мочевого пузыря и уретрой (рис. 2).
Влияние недержания мочи на качество жизни оценивали с помощью опросника ICIQ-SF [28]. Легкая степень недержания мочи соответствовала 1–5 баллам, средняя – 6–12, тяжелая – 13–18, очень тяжелая – 19–21 баллу. Оценку проводили через 3 и 6 мес. после РАРПЭ. Первичной конечной точкой была оценка влияния недержания мочи на качество жизни после РАРПЭ в разные моменты времени.
Всем пациентам после операции выполнена уретроцистография для выявления возможного затека мочи в области уретроцистоанастомоза [29].
Статистическая обработка результатов проведена в программе IBM SPSS Statistics. 22. Непрерывные переменные представлены в виде медианы (с межквартильным диапазоном). Мы проанализировали данные, используя критерий согласия Пирсона, U-критерий Манна–Уитни, точный тест Фишера в зависимости от ситуации. Различия между показателями считали статистически значимыми при p<0,05.
Результаты. Группы были сопоставимыми по основным характеристикам: возрасту, уровню ПСА, объему простаты (см. таблицу) и клинической стадии. Никому из пациентов обеих групп не потребовалось выполнения конверсии. Ни в одном наблюдении в течение 6 мес. после РАРПЭ не зафиксировано послеоперационных осложнений, включая кишечную непроходимость и задержку мочи.

Группы достоверно не различались по среднему объему кровопотери и продолжительности операции, тогда как уретральный катетер в группе двухслойной ЗР удаляли статистически значимо раньше, чем в группе стандартной ЗР (р=0,001; см. таблицу).
В данном исследовании все пациенты были опрошены по опроснику ICIQ-SF для оценки влияния недержания мочи на качество жизни. Через 1 мес. после РАРПЭ в группе стандартной ЗР средний балл по опроснику ICIQ-SF составил 6,72, в группе двухслойной ЗР – 4,57 (p=0,04), через 3 мес. – 3,8 и 2,3 соответственно (p=0,09), через 6 мес. – 1,94 и 1,2 соответственно (p=0,23).
Обсуждение. Задняя реконструкция уретроцистоанастомоза является одной из наиболее распространенных процедур, используемых для предотвращения послеоперационного недержания мочи после простатэктомии. В 2001 г. Rocco et al. впервые сообщили об использовании этого метода при позадилонной радикальной простатэктомии [30]. При ЗР достигается анатомическое состояние, близкое к предоперационному, с восстановлением эффективной компрессионной системы уретры для предотвращения послеоперационного недержания мочи [17–24, 26]. Кроме того, ЗР уменьшает натяжение пузырно-уретрального анастомоза и снижает риск его несостоятельности [17–24]. Предложено несколько модификаций ЗР [17–23], которые можно разделить на одно- и двуслойные.
Описаны две методики однослойной ЗР [17, 18, 20, 23]. Одна из них предусматривает наложение швов между рассеченной мышечно-фасциальной пластинкой (рабдосфинктером) позади мочеиспускательного канала и пересеченным краем фасции Денонвилье, расположенной на полпути между мочевым пузырем и уретрой, в то время как другая методика включает фиксацию между пересеченной мышечно-фасциальной пластинкой (рабдосфинктером) и задней стенкой мочевого пузыря. С другой стороны, в оригинальной методике, предложенной Rocco et al., реконструкция выполняется в два слоя [11, 25, 30]. Первый слой создается путем сшивания пересеченной мышечно-фасциальной пластинки (рабдосфинктера) позади мочеиспускательного канала с пересеченным краем фасции Денонвилье, второй – путем сшивания рабдосфинктера чуть ниже мочеиспускательного канала с задней стенкой мочевого пузыря (дорсальная часть наружного слоя детрузора). Недавно был проведен ряд проспективных и ретроспективных исследований клинических исходов одно- и двухслойной ЗР после РАРПЭ, однако роль ЗР в послеоперационном восстановлении удержания мочи остается противоречивой [17–23]. Два ретроспективных исследования однослойной ЗР (с присоединением рабдосфинктера позади мочеиспускательного канала к переднему краю фасции Денонвилье) показали ее положительное влияние на раннее послеоперационное восстановление удержания мочи [18, 23], но два проспективных исследования не выявили существенного преимущества этой техники [17–20]. C. W. Jeong et al. [22] недавно опубликовали результаты рандомизированного контролируемого исследования (РКИ), показавшего, что новая однослойная одноэтапная методика ЗР с фиксацией рабдосфинктера к задней стенке мочевого пузыря имела незначительную пользу для раннего восстановления социально значимого удержания мочи. Gondo et al. [19], проведя однофакторный анализ, сообщили, что двухслойная двухэтапная ЗР значительно связана с ранним восстановлением удержания мочи через 1 мес. после удаления катетера [14]. Однако D. E. Sutherland et al. [21] в своем РКИ не нашли никаких преимуществ двухслойной двухэтапной ЗР.
Задняя мышечно-фасциальная пластина играет роль динамической опорной конструкции для простатическо-мембранозного отдела уретры [31, 32]. Эта опорная ткань, повышающая структурную прочность, простирается от брюшины позадипузырного пространства к мембране промежности и центральному сухожилию промежности [27, 31]. Простатэктомия сопровождается анатомическим и функциональным разрушением этой поддерживающей структуры, что может приводить к послеоперационному недержанию мочи [26]. Мы предположили, что многослойная реконструкция этой поддерживающей системы с помощью модифицированной методики потенциально может более эффективно восстанавливать анатомическую и функциональную целостность и обеспечивать более сильную заднюю опору для сфинктерного комплекс уретры. Сравнение со стандартной однослойной ЗР продемонстрировало, что уровень недержания мочи через 1 мес. после РАРПЭ был достоверно ниже в группе двухслойной ЗР, чем в группе стандартной ЗР, предположив, что методика двухслойной ЗР может способствовать предотвращению недержания мочи в послеоперационном периоде. Через 3 и 6 мес. после операции результаты в обеих группах статистически не различались.
Совокупный анализ сравнительных исследований показал, что стандартная ЗР способствует предотвращению недержания мочи в течение первых 30 дней после радикальной простатэктомии, в то время как на степень удержания мочи через 90 дней после операции использованный метод реконструкции не влияет [33]. Недавний систематический обзор, представленный Grasso et al., показал, что ЗР способствовала предотвращению недержания мочи через 3–7, 30 и 90 дней после удаления катетера [24].
Помимо того что модифицированная ЗР имеет положительное влияние на удержание мочи в послеоперационном периоде, следует отметить, что восстановление поврежденных тазовых нервов и мышц после операции также создает предпосылки к предотвращению недержания мочи. Этим можно объяснить, что через 3 и 6 мес. после РАРПЭ между двумя группами в этом исследовании статистически значимой разницы выявлено не было.
К ограничениям проведенного нами исследования следует отнести небольшое количество пациентов, отсутствие рандомизации по группам (распределение осуществлялось на основании решения хирурга).
Заключение. Данные, полученные в ходе настоящего сравнительного исследования, позволяют предположить, что двухслойная ЗР при РАРПЭ, являясь простым в исполнении методом, улучшает раннее (через 1 мес.) восстановление послеоперационного удержания мочи по сравнению со стандартной ЗР, однако для получения более достоверных данных необходимы крупные многоцентровые РКИ.



