Мочекаменная болезнь (МКБ), или уролитиаз, занимает одно из лидирующих мест в структуре обращаемости за ургентной урологической помощью и причин экстренной госпитализации в профильные отделения [1]. Распространенность МКБ в развитых странах в среднем составляет от 7 до 10%, возрастая в эндемических регионах до 20% и более [2–4]. Кроме того, повсеместно за последнее десятилетие отмечают прирост заболеваемости уролитиазом до 37% в странах Западной Европы и Северной Америки [5–7]; в России данный показатель за аналогичный период составил 29,1% [3, 8].
За сравнительно небольшой срок как в России, так и за рубежом мы пережили, наверное, революционные изменения в подходах к лечению нефролитиаза: от открытой хирургии через повсеместное увлечение дистанционной ударно-волновой литотрипсией к перкутанному и ретроградному доступам [9–11]. Последние на настоящий момент максимально востребованы и обеспечивают оптимальное соотношение радикальности удаления конкрементов и минимальной инвазивности и риска осложнений [12]. Перкутанный доступ в качестве первой линии лечения рекомендован при нефролитиазе, особенно пациентам с крупными конкрементами, и может быть реализован в положениях пациента как на животе, так и на спине [12, 13].
Перкутанная хирургия уролитиаза, как любой хирургический метод, ассоциирована с рядом специфических и неспецифических осложнений. По частоте встречаемости доминируют геморрагические и воспалительные осложнения [14]. А вот повреждения органов брюшной полости, включая толстую кишку, довольно редки и, по данным Европейской урологической ассоциации, составляют не более 1,7% [12, 14]. Обзоры, ориентированные именно на повреждения ободочной кишки, сообщают о еще меньшем риске развития подобных осложнений – 0,3–0,4% [15–17].
AslZare Mohammad и соавт. [17], анализируя собственный 18-летний опыт перкутанной хирургии уролитиаза, сообщили о 11 повреждениях ободочной кишки на 5039 процедур чрескожной нефролитотомии, что составило 0,2%. Среди факторов риска авторы выделили следующие: левосторонний доступ, пункцию нижней чашечки, пожилой возраст пациентов и наличие подковообразной почки. Примечательно, что интраоперационно диагноз был установлен лишь трети пациентов. Также у трети пациентов осложнение манифестировало толстокишечно-кожным свищом, у 2 (18%) пациентов развилась клиника калового перитонита [17]. В. А. Малхасян и соавт. [18], опираясь на публикации по проблеме повреждения ободочной кишки, к предрасполагающим факторам относят следующие: пункция латеральнее задней подмышечной линии, худые женщины с неразвитой забрюшинной жировой клетчаткой, мобильная почка, кифосколиоз, аномалии развития почек. По их мнению, вышеперечисленные предрасполагающие факторы увеличивают риск наличия так называемой ретроренальной ободочной кишки (рис. 1).
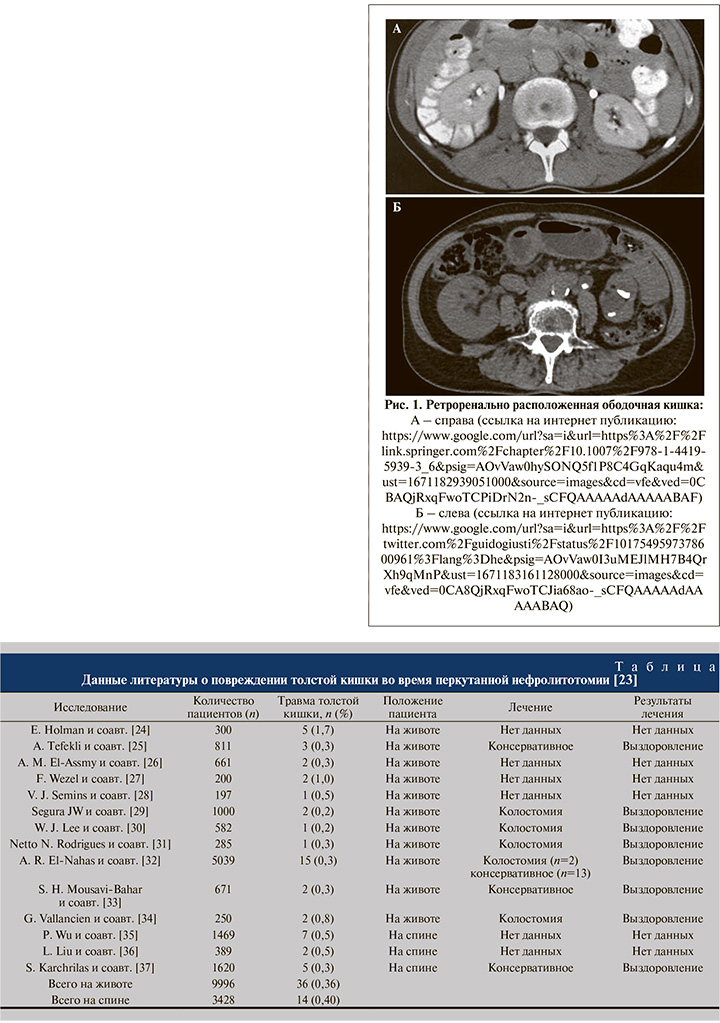
Анализ томограмм пациентов с выраженным сколиозом выявил более чем семикратное увеличение частоты встречаемости ретроренальной ободочной кишки по сравнению с пациентами без сколиоза (р<0,001) [19]. В публикации, рассматривающей рентгенологическую диагностику ретроренального расположения ободочной кишки, основанную на результатах спиральной компьютерной томографии (СКТ), авторы показали выраженные различия в зависимости от положения пациента [20]. Так, ретроренальная ободочная кишка среди 500 пациентов в положении лежа на спине выявлена у 1,9%, тогда как среди 90 пациентов в положении на животе этот показатель достиг 10%, что авторы связывают с дислокацией как почки под действием силы гравитации, так и собственно ободочной кишки вследствие повышения внутрибрюшинного давления в prone-позиции [20]. Подобные тенденции были отмечены и в других менее масштабных обзорах рентгенологических данных. Однако ретроренальная ободочная кишка в положении на спине диагностирована в 12–15,7%, на животе – в 24,5–28% [21, 22]. Казалось бы, существенный довод для выбора доступа для перкутанной хирургии.
При этом литературный анализ хирургических осложнений при перкутанной нефролитотомии, опубликованный Hakan Öztürk [23], не выявил различий в частоте повреждений ободочной кишки в зависимости от положения пациента (на спине или на животе). Более того, в стандартной позиции на животе процент повреждений был статистически незначимо ниже и составил 0,36 и 0,4 для 9996 и 3428 пациентов соответственно (р>0,05, см. таблицу) [23]. Обращает на себя внимание отсутствие данных о выборе метода лечения и его эффективности в 6 (42,9%) из 14 публикаций, включенных в данный обзор. Также отсутствовали указания на методику первичной пункции как возможного фактора риска повреждения ободочной кишки и четкая определенность в отношении колостомии в тех публикациях, где метод лечения был указан в качестве тактики лечения пациентов. По результатам анализа 50 наблюдений ранения ободочной кишки можно заключить следующее: частота использования колостомии была достоверно ниже консервативного ведения – 8 (16%) против 23 (46%) (p<0,05), однако способы лечения, а тем более их результат у оставшихся 19 (38%) представлены не были (см. таблицу).
К ранним клинико-инструментальным симптомам стоит отнести звук спускающегося воздуха (шипение) при пункции чашечно-лоханочной системы (ЧЛС) и подозрительный, напоминающий кишечные гаустры затек при антеградном или ретроградном контрастировании ЧЛС [18]. Однако стоит отметить, что интраоперационное обнаружение такого осложнения не превышает трети случаев, а в остальных наблюдениях имеет место запоздалая диагностика травмы ободочной кишки [23]. Клиническими проявлениями на этом этапе выступают крепитация в зоне нефростомы, пневматурия, вздутие живота, диарея, неприятный запах мочи, наличие кишечного кожного свища и симптомы перитонита [18].
С целью диагностики травмы ободочной кишки во время чрескожной нефролитотомии многие авторы рекомендуют СКТ в нативном режиме и с экскреторной фазой, которая может быть дополнена при необходимости антеградной уретеропиелографией (фистулографией) или ретроградной уретеропиелографией.
Перед тем как приступить к презентации клинического наблюдения, мы хотели бы ретроспективно оценить риски повреждения ободочной кишки у данного пациента на основании представленного обзора литературы и по результатам спиральной компьютерной томографии, выполненной после травмы, перед вмешательством с контралатеральной стороны. Так как при первичном обращении мы располагали только данными УЗИ и экскреторной урографии.
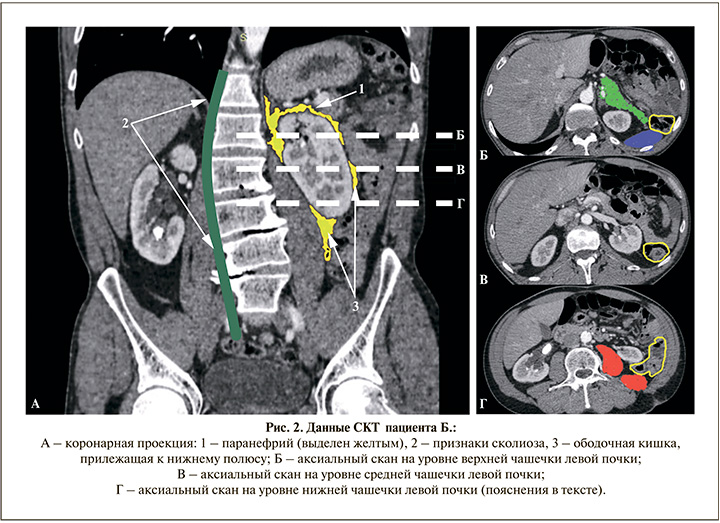
К очевидным факторам риска ранения ободочной кишки стоит отнести левосторонний доступ, наличие сколиоза и небольшое количество паранефральной жировой клетчатки (рис. 2а, 1-3). Более детально разберем синтопию на уровне верхней (рис. 2а-b), средней (рис. 2а-с) и нижней (рис. 2а-d) групп чашечек. Аксиальный срез на уровне верхней группы чашечек (рис. 2b): ободочная кишка (желтый контур) вне зоны интереса, тогда как по дорсальной поверхности почка интерпозирована селезенкой (закрашена синим), а по переднелатеральной поверхности – хвостом и телом поджелудочной железы. Риск повреждения последних достаточно высок при выборе данного доступа, и такие наблюдения описаны в литературе. Зона средней группы чашечек: на аксиальном скане (рис. 2с) видно, что до 50% пункционного окна уже занято ободочной кишкой (желтый контур). Уровень нижней группы чашечек характеризуется тем, что дорсальная поверхность и медиальный край почки экранированы mm. psoas major и iliacus sin. (закрашены красным), к оставшейся дорсолатеральной поверхности прилежит ободочная кишка (желтый контур). Нужно принять во внимание, что СКТ выполнено в положении на спине, а перкутанное вмешательство мы проводили в pron-позиции, что, как отмечено выше, повышает вероятность ретроренальной ободочной кишки [19]. Таким образом, пункция через ободочную кишку у данного пациента была предопределена, а ввиду достаточной редкости такого осложнения (это первое более чем на 1693 перкутанные нефролитотомии, что без учета перкутанных нефростомий составило около 0,6‰) мы вряд ли смогли бы актуализировать приведенные выше факторы риска и при наличии СКТ на дооперационном этапе.
Пациент Б. 46 лет поступил с клиникой рецидивирующей почечной колики слева, по результатам методов визуализации (УЗИ и экскреторная урография) поставлен диагноз: МКБ. Билатеральный оксалатный нефролитиаз. Гидронефроз слева. Лабораторно отсутствовали лейкоцитоз и урокультура. С учетом клинической картины и распространенности уролитиаза пациенту выполнена стандартная перкутанная нефролитотомия, диаметр кожуха Аmplatz – 30 Сh (рис. 3а). Продолжительность операции вместе с этапом катетеризации почки – 25 мин, почка дренирована баллонным нефростомическим дренажем 22 Сh, баллон которого спущен на 1-е сутки, а сам дренаж удален на 2-е сутки. Нужно также отметить отсутствие латерализации перкутанного доступа, что можно было бы рассматривать как техническую погрешность операции. На рис. 3b показана проекционная скелетотопия левой почки, из которой видно, что перкутанный доступ локализуется медиальнее обычного, практически по лопаточной линии.
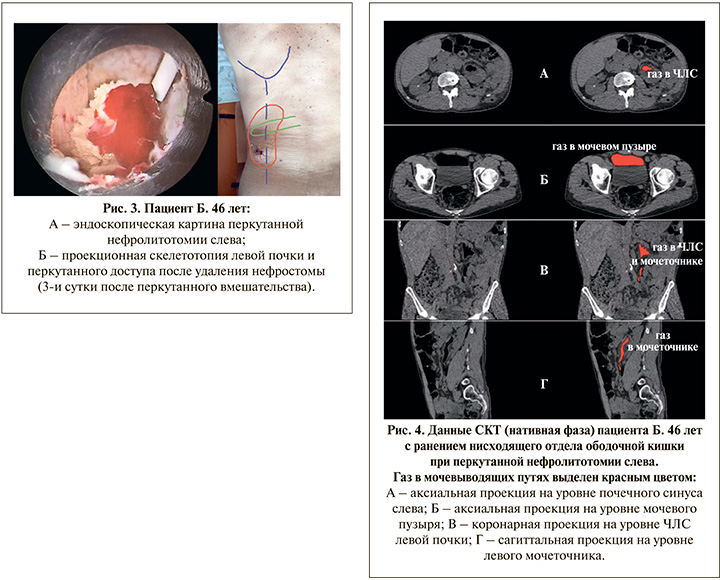
Перед планируемой выпиской на 3-и сутки пациент предъявил жалобы на интенсивную пневматурию. Отсутствовали лихорадка и лейкоцитоз, парез кишечника и перитонеальные симптомы. Выполненная в экстренном порядке сонография не выявила признаков уростаза и жидкостных образований паранефрально на стороне операции, также отсутствовала свободная жидкость в брюшной полости. Однако при проведении СКТ с болюсным контрастированием выявлены скопления газа в верхних мочевыводящих путях слева и мочевом пузыре (рис. 4), в экскреторную фазу визуализировался свищевой ход и поступление контраста в ободочную кишку (рис. 5). Таким образом, была верифицирована травма ободочной кишки с наличием внутреннего толстокишечно-почечного свища. Кишечное отделяемое или моча в области перкутанного доступа, как и признаки локального воспаления, отсутствовали (рис. 3b).
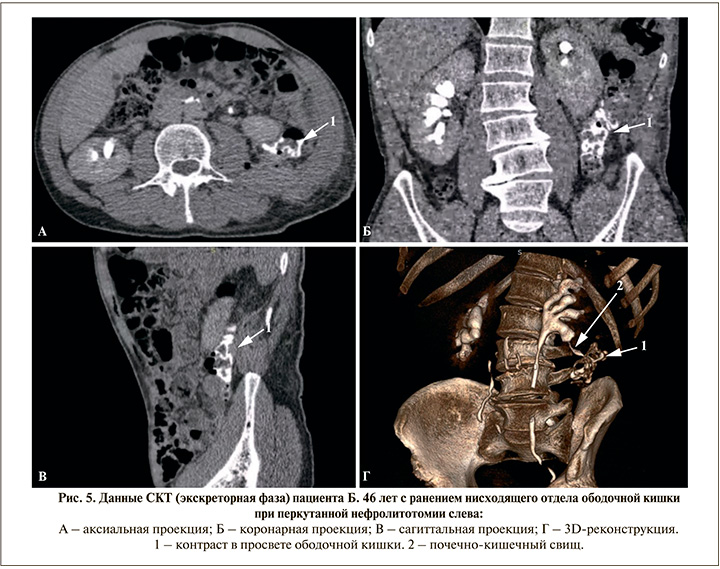
Наиболее трудным в тактическом плане стал вопрос о характере последующего лечения, и сторонники активной хирургической тактики были в подавляющем большинстве. С учетом отсутствия жизнеугрожающих инфекционных осложнений, а также четких клинических рекомендаций о необходимости хирургического подхода и имеющихся в литературе указаний на эффективность консервативного лечения коллегиально было принято решение остановиться на последнем.
С целью снижения риска гнойно-деструктивных поражений забрюшинного пространства, «облегчения» формирования наружного свища нами выполнена «марсупитализация» свищевого хода. Под местной инфильтрационной анестезией разрез расширен до 5 см, вворачивающими швами кожа фиксирована к широчайшей мышце спины, мышечный канал тупо разведен до 4 см, куда был установлен дренаж (рис. 6). Ни визуальную, ни пальцевую ревизию паранефрия, кишки и почки не выполняли. Возможно, это стало излишним лечением, так как мы не зафиксировали ни кишечного отделяемого, ни мочи. Дренаж и вворачивающие швы сняли на 10-е сутки после данной манипуляции по мере купирования пневматурии. Кожная рана закрылась самостоятельно без необходимости наложения вторичных швов еще через 4 сут., т.е. на 17-е сутки от перкутанного вмешательства.
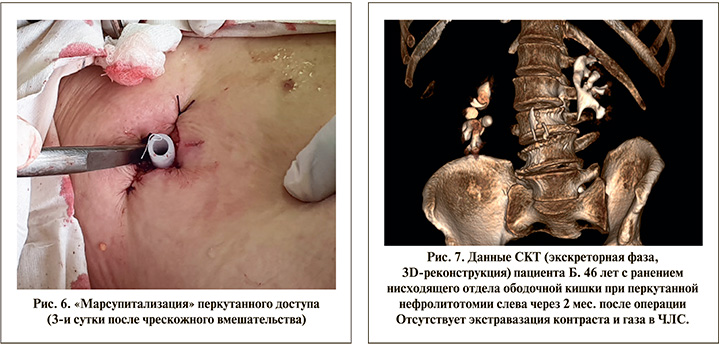
Пациент был выписан на амбулаторное лечение с рекомендациями по контралатеральной перкутанной нефролитотомии через 2 мес. Перед последней была выполнена контрольная СКТ, которая констатировала закрытие толстокишечно-почечного свища (рис. 7). Операция справа прошла без осложнений, пациент выписан на 4-е сутки без нефростомического дренажа.
Обсуждение. Ранение ободочной кишки – довольно редкое осложнение перкутанных вмешательств, которое также редко диагностируется интраоперационно. Несмотря на это, накоплен достаточный клинический опыт и определены факторы риска, позволяющие прогнозировать вероятность подобных осложнений, что делает особо актуальным владение данной информацией. С ориентацией на увеличение частоты выявления ретроренальной ободочной кишки в prone-позиции, видимо, целесообразно выполнять СКТ в том положении, в котором предполагается перкутанное вмешательство, чтобы актуализировать анатомические взаимоотношения. Ввиду ограниченности опубликованных в литературе наблюдений не сформирована четкая тактика ведения этой группы пациентов. Активная хирургическая тактика с колостомией, ревизией и дренированием забрюшинного пространства, безусловно, показана пациентам с клиникой перитонита, забрюшинной флегмоны и синдрома системной воспалительной реакции. При отсутствии вышеперечисленных осложнений возможно рассматривать консервативное ведение пациента, тем более что данный подход оказался эффективеным не менее чем в 46% представленных в публикациях наблюдений.
Заключение. Знание факторов риска повреждения ободочной кишки может снижать вероятность развития подобных осложнений, а ранняя их диагностика, возможно, позволит избегать объемных, травматичных и этапных хирургических вмешательств. У определенной группы таких пациентов можно рассматривать консервативное ведение.



