Актуальность. В течение последних 5 лет только в Москве выполнено более 150 тыс. ПЭТ/КТ всего тела человека по поводу органических и функциональных заболеваний различной локализации. На электронном носителе пациенты получили ответ на один конкретный вопрос направившего врача, все остальное просканированное тело, а точнее состояние его жизнеспособности, осталось без внимания стандартной процедуры этого наукоемкого и высокотехнологичного исследования. Однако еще в 2010 г. на страницах Оксфордского академического медицинского журнала в разделе «Визуализации в нефрологии» опубликована одна из первых научных работ, указавших на потенциальные возможности ПЭТ/КТ-технологии в качестве альтернативы нефробиопсии [1]. В 2014 г. C. R. Christopher et al. одни из первых высказали мнение, согласно которому ретроспективное изучение результатов ПЭТ/КТ у молодых людей может увеличивать выявляемость бессимптомно протекающей патологии [2].
Хроническая болезнь почек (ХБП), по данным ВОЗ, занимает одно из ведущих мест среди причин инвалидности и смертности трудоспособного населения. Она характеризуется наличием поражения или снижения функции почек в течение минимум 3 мес. независимо от причины [3]. Поражение почек обычно проявляется патологическими изменениями в паренхиме, установленными с помощью визуализации, биопсии или на основании лабораторных маркеров, таких как проявление мочевого синдрома с повышенной альбуминурией и прогрессирующим снижением скорости клубочковой фильтрации [4]. Данных визуализирующих, инструментальных методов или прижизненного морфологического исследования, выполненных даже однократно, может хватить для диагностики ХБП и постановки диагноза, если оно недвусмысленно указывает на необратимые структурные изменения органа. При этом маркерами повреждения почек могут быть изменения, которые можно выявить при клиническом обследовании, показывающем наличие патологических процессов в почечной ткани [5]. Понятие ХБП не отменяет нозологического подхода к диагностике заболеваний почек. Оно является универсальным инструментом для определения степени нарушения функции почек при разных нозологических формах, отражающих наличие факта возникновения и прогрессирования нефропатий. В зависимости от клинической ситуации диагностика ХБП может базироваться на выявлении любых морфологических или клинических маркеров почечного повреждения [6].
Изучение жизнеспособности тканей на молекулярно-клеточном уровне методом совмещенной позитронно-эмиссионной и КТ (ПЭТ/КТ) в режиме реального времени в течение 10 лет широко используется в онкологии, клинической кардиологии, функциональных исследованиях и в последние годы в нефроурологии [7–9]. Анализ состояния липидного метаболизма проводится с помощью изотопа 11С-холина, который является предшественником мембранных фосфолипидов и составляет до 60% их массы. Содержание ведущих фракций мембранного бислоя (лизолецитина, фосфатидилхолина, сфингомиелина) обеспечивает достаточную физиологическую текучесть мембран для обеспечения коммуникации клетки. При обеднении бислоя за счет уменьшения содержания холиносодержащих фосфолипидов мембраны становятся жесткими, биохимизм клетки нарушается, включается механизм апоптоза с последующим замещением региона рубцовой тканью. И не важно, по какой причине снижается процесс регенерации липидного бислоя, будь то действие бактериальных токсинов, иммунных комплексов или токсичных медикаментов, ПЭТ/КТ-томография визуализирует эти регионы и позволяет рассчитывать уровень снижения их жизнеспособности. Меченые биомолекулы излучают протонный импульс, по которому определяется их визуальное и количественное стереохимическое положение, что обеспечивает высокоточную навигацию [10–14].
В основу ПЭТ/КТ-диагностики болезней положен принцип анализа тропности жизненно важных меченых биомолекул к структурам энергично функционирующих клеток. При этом визуально цветовой анализ от высоконасыщенного белого до сниженного белого или желто-оранжевого и количественный расчет импульса в g/ml используются в качестве объективных показателей, отражающих жизнеспособность изучаемых тканей с чувствительностью 90% и специфичностью до 85% [15–19].
По данным ВОЗ, до 20% населения планеты имеют различно выраженные клинико-лабораторные проявления ХБП, однако в доступной литературе мы не нашли информации о возможности выявления ХБП на молекулярно-клеточном уровне по результатам ретроспективного изучения ПЭТ/КТ-томограмм людей, уже прошедших этот вид обследования, что определило цель нашего пилотного исследования.
Цель исследования: изучить возможность применения ретроспективного анализа результатов ПЭТ/КТ всего тела человек в качестве инструмента для диспансеризации населения на предмет выявления субклинических проявлений хронической болезни почек.
Материалы и методы. Для достижения поставленной цели на основе случайно-выборочного метода ретроспективно изучены результаты ПЭТ/КТ всего тела человека с 11С-холином на предмет выявления ХБП у 100 жителей Тюменского региона, прошедших исследование в радиологическом центре ГАУЗ ТО МК МЦ «Медицинский город» Тюмени в 2016–2020 гг. по поводу различных заболеваний вне органов мочеполовой системы. Это были 52 мужчины и 48 женщин с медианой возраста 44,6 (42;55) года, не имевших анамнестических и клинико-лабораторных проявлений почечной патологии. ПЭТ/КТ-исследования выполнялись по стандартной методике на аппарате (Biograph) фирмы Siemens. Анализ полученных данных проводился визуальным методом с 3D-реконструкцией изображения.
В работе изучались функциональные изменения в паренхиме почек, которые анализировались по ее тропности к изотопу 11С-холина. Визуальный контроль дополнялся количественной оценкой этого процесса. Зоны метаболизма анализировались в автоматическом режиме по уровню захвата изотопа 11С-холина (SUVmax в g/ml). Исследование начиналось через 10 мин после введения препарата из расчета 3 МКб на 1 кг массы тела пациентов. Изотоп готовился в радиологическом центре на компактном циклотроне шведской фирмы «Scanditronix».
Статистическая обработка материала проводилась согласно международным требованиям, предъявляемым к обработке данных научных исследований, при помощи программы для персональных компьютеров Statistica for Windows (версия 11.5). Непрерывные переменные представлены в виде M±m. (Среднее±стандартная ошибка среднего). Достоверность выявленных различий оценивалась по t-критерию Стьюдента.
Результаты. Всего в Тюменском радиологическом центре за последние 5 лет проведено более 10 тыс. подобных ПЭТ/КТ-исследований. После прохождения профильного специализированного лечения пациенты, находясь в состоянии стойкой ремиссии основного заболевания, включая безрецидивный период онкологической патологии, направлялись для дальнейшего лечения и наблюдения в поликлиники по месту жительства, имея на руках электронный носитель с исчерпывающей информацией о состоянии жизнеспособности всех внутренних органов, расположенных от уровня щитовидной железы до вертлужных впадин. В рамках настоящего исследования нами проведена ретроспективная ПЭТ/КТ-диспансеризация 100 пациентов, прошедших исследование всего тела с изотопом 11С-холина на предмет возможного выявления у них на молекулярно-клеточном уровне ранних проявлений ХБП. Изучая данные направления на ядерное исследование, которые в обязательном порядке содержали анамнестическую и параклиническую информацию о всех сопутствовавших заболеваниях, в этой группе не оказалось лиц, достоверно страдавших патологией почек.
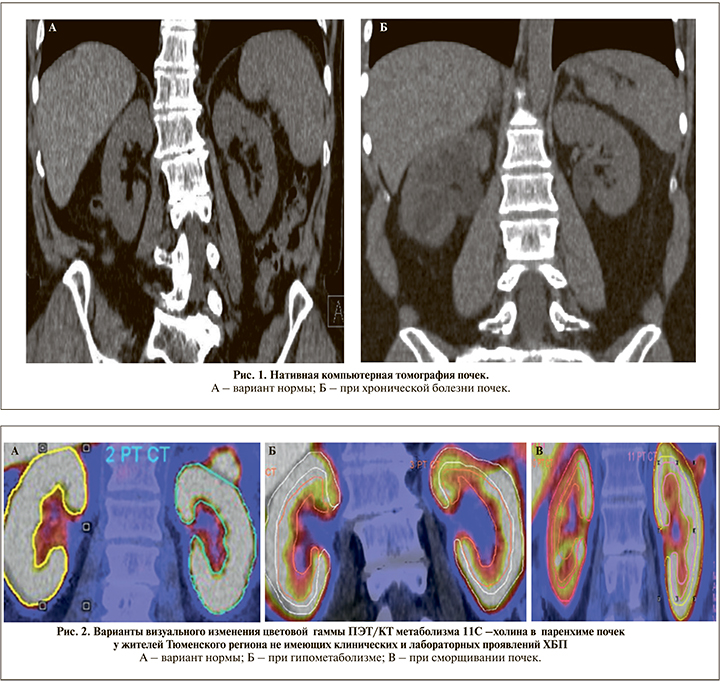
Проведенный анализ показал, что независимо от основного заболевания, послужившего поводом для проведения ПЭТ/КТ всего тела, у 22 пациентов имели место различно выраженные проявления гипометаболизма 11С-холина, указывающие на снижение жизнеспособности паренхимы этих регионов (рис. 1, 2). В той группе у 14 пациентов наблюдалось локальное снижение тропности к изотопу 11С-холина (SUVmax), которое не сопровождалось визуальными рентгенологическими признаками поражения почек и у 8 пациентов имело место тотальное снижение его метаболизма, которое совпадало с появлением КТ-признаков их сморщивания (искривление контура, деформация чашечно-лоханочной системы и уменьшение размеров), что позволило расценивать это в качестве достоверных маркеров поражения паренхимы.
В таблице представлены цифровые данные ПЭТ/КТ-метаболизма 11С-холина, отразившие состояние жизнеспособности паренхимы почек, из которых видно, что снижение тропности паренхимы почек к 11С-холину до 20% относительно показателей структурно и функционально состоятельной паренхимы, не сопровождались визуальными КТ-проявлениям деформации контура почек. В то время как снижение тропности паренхимы более чем на 30% визуально совпадало с появлением рентгенологических признаков, характерных для необратимых изменений в паренхиме почек (искривление контура, деформация чашечно-лоханочной системы, уменьшение размеров) (рис. 3).

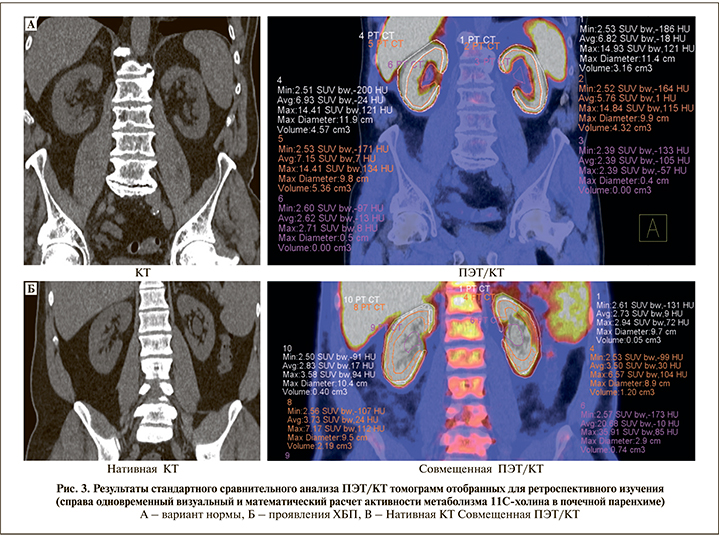
По результатам сравнительного визуального и математического анализов представленных томограмм можно заключить, что у пациента Б., как и у пациента А., не имевших на момент обследования анамнестических и клинико-лабораторных проявлений ХБП, имело место снижение метаболизма меченых биомолекул в проекции коркового и мозгового слоев обеих почек более чем на 40% относительно условно рассчитанной нормы (SUVmax 11,6±1,0 g/ml), что сопровождалось уменьшением диаметра анализируемой почечной паренхимы на 10%.
Все пациенты с выявленными в процессе ПЭТ/КТ-диспасеризации молекулярно-клеточными проявлениями ХБП направлены к нефрологу для дальнейшего уточнения причин поражения почечной паренхимы.
Обсуждение. Проведенное в рамках настоящей работы пилотное ретроспективное изучение результатов ПЭТ/КТ всего тела с 11С-холином у 100 жителей Тюменского региона, не имевших анамнестических и клинико-лабораторных проявлений ХБП, позволило визуально выявить и количественно рассчитать процесс снижения жизнеспособности паренхимы почек у 22% прошедших исследование и в 8% эти изменения носили необратимые рентгенологические признаки поражения почек.
Выводы. Возможность ранней ядерной молекулярно-клеточной верификации нефропатии не исключает более широкого применения ретроспективной ПЭТ/КТ-диспансеризации в качестве одного из высокоэффективных методов раннего выявления ХБП, что нуждается в дальнейших исследованиях и уточнении.



