 Введение. Эпидемическая ситуация по туберкулезу в РФ, несмотря на положительную динамику в течение последних 5 лет, остается напряженной и неоднородной [1]. Успехи, достигнутые в борьбе с легочным процессом, не отразились за последние десятилетия в динамике заболеваемости экстрапульмональными локализациями, не превышающими 2–4 на 100 тыс. населения [2]. Известно, что лидирующей формой внелегочного туберкулеза (ВЛТ) в большинстве регионов России является мочеполовая, доля которой превышает 50% [3–6]. При туберкулезе почек вовлечение нижележащих отделов мочевого тракта с формированием его рубцовых сужений и деформаций имеет место в 54,0–84,7% случаев [7–9], а в структуре причин образования стриктур мочеточника доля туберкулеза достигает 9,0–12,3% [10, 11]. Частота его множественных и протяженных сужений вследствие туберкулезного поражения достигает 16,7% [12–14]. Развивающийся при этом уретерогидронефроз – неизбежное и грозное патологическое состояние, неуклонно вызывающее компрессию паренхимы почки, вторичный пиелонефрит и гибель органа [15–17]. В этих случаях методом выбора является замещение мочеточника лоскутами мочевого пузыря или кишечника. В мировой литературе публикации, посвященные энтероуретеропластике для больных туберкулезом, носят единичный характер. Эффективность и безопасность этих операций изучены недостаточно.
Введение. Эпидемическая ситуация по туберкулезу в РФ, несмотря на положительную динамику в течение последних 5 лет, остается напряженной и неоднородной [1]. Успехи, достигнутые в борьбе с легочным процессом, не отразились за последние десятилетия в динамике заболеваемости экстрапульмональными локализациями, не превышающими 2–4 на 100 тыс. населения [2]. Известно, что лидирующей формой внелегочного туберкулеза (ВЛТ) в большинстве регионов России является мочеполовая, доля которой превышает 50% [3–6]. При туберкулезе почек вовлечение нижележащих отделов мочевого тракта с формированием его рубцовых сужений и деформаций имеет место в 54,0–84,7% случаев [7–9], а в структуре причин образования стриктур мочеточника доля туберкулеза достигает 9,0–12,3% [10, 11]. Частота его множественных и протяженных сужений вследствие туберкулезного поражения достигает 16,7% [12–14]. Развивающийся при этом уретерогидронефроз – неизбежное и грозное патологическое состояние, неуклонно вызывающее компрессию паренхимы почки, вторичный пиелонефрит и гибель органа [15–17]. В этих случаях методом выбора является замещение мочеточника лоскутами мочевого пузыря или кишечника. В мировой литературе публикации, посвященные энтероуретеропластике для больных туберкулезом, носят единичный характер. Эффективность и безопасность этих операций изучены недостаточно.
Цель исследования: повышение эффективности хирургического лечения туберкулеза почки с тотальным поражением мочеточника на основе использования органуносящих и органзамещающих технологий.
Материалы и методы. Материалом настоящего исследования послужило изучение клинического течения и результатов хирургического лечения 48 больных с протяженными или множественными стриктурами мочеточников специфического (n=36) и неспецифического (n=12) происхождения в возрасте от 35 до 69 (51,0±0,6) лет, которым выполнена уретеропластика с использованием кишечных аутотрансплантатов. Больные оперированы в урологических клиниках Московского городского научно-практического центра борьбы с туберкулезом, Уральского и Санкт-Петербургского НИИ фтизиопульмонологии в 2005–2013 гг. Критерием включения в исследование служило наличие специфического поражения мочевыделительной системы и/или тотального поражения мочеточника.
 Наблюдаемые пациенты подвергнуты общепринятым для фтизиоурологического стационара клиническим и лабораторным, а также рентгенологическим, ультразвуковым, инструментальным и эндоскопическим методам исследования. Резервные возможности почек и верхних мочевых путей (ВМП) определяли до и после декомпрессии почек с помощью раздельной пробы Реберга после декомпрессии почки с помощью чрескожной пиелонефростомии (ЧПНС). На основании полученных данных решали вопрос о целесообразности сохранения почки и определяли уровень резекции патологически измененного мочеточника.
Наблюдаемые пациенты подвергнуты общепринятым для фтизиоурологического стационара клиническим и лабораторным, а также рентгенологическим, ультразвуковым, инструментальным и эндоскопическим методам исследования. Резервные возможности почек и верхних мочевых путей (ВМП) определяли до и после декомпрессии почек с помощью раздельной пробы Реберга после декомпрессии почки с помощью чрескожной пиелонефростомии (ЧПНС). На основании полученных данных решали вопрос о целесообразности сохранения почки и определяли уровень резекции патологически измененного мочеточника.
Показаниями к кишечной пластике мочеточника считали:
- Необратимое тотальное или субтотальное поражение мочеточника общей протяженностью более 10 см различной этиологии с вовлечением или без в патологический процесс мочевого пузыря (МП).
- Уменьшение емкости мочевого пузыря, не позволяющее выполнять операцию Боари.
- Высокий и неоправданный риск аутотрансплантации почки (единственная почка, снижение функции контрлатеральной почки, пиелонефрит, ХПН и др.).
Противопоказаниями к кишечной пластике мочеточника стали:
- Инфравезикальная обструкция.
- ХПН (клубочковая фильтрация менее 40 мл/мин).
- Терминальный уретерогидронефроз.
Связанное со здоровьем КЖ пациентов оценено в баллах с использованием опросника SF-36. Противотуберкулезная терапия проведена 4–5 основными противотуберкулезными препаратами согласно действующим нормативным документам (Приказ № 109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерации» от 21.03.2003). Патогенетическое лечение включило применение антиоксидантов и физиоэнзимотерапию на область поражения мочеточника.

Статистическую обработку полученных результатов осуществляли с использованием методов параметрической и непараметрической статистики. Для описания средних групповых значений признаков рассчитывали средние арифметические и их стандартные ошибки, в ряде случаев и 95% доверительные интервалы. Для анализа межгрупповых различий применяли t-критерий Стьюдента. Критический уровень достоверности нулевой статистической гипотезы (об отсутствии различий) принимали равным 0,05.
Статистический анализ выполнен в среде Windows XP с использованием программ Statistica for Windows 5.0 и Graph PadIn Stat tm, 1994.
 Результаты исследования и их обсуждение. Для изучения функциональных резервов почки и целесообразности ее сохранения 35 больным нефротуберкулезом выполнена ЧПНС с последующей оценкой КФ путем осуществления раздельной пробы Реберга. С этой целью суточную мочу из дренированной почки и выпущенную самостоятельно собирали раздельно. Пробу ставили на следующие, 7–9-е и 14–16-е сутки после отведения мочи.
Результаты исследования и их обсуждение. Для изучения функциональных резервов почки и целесообразности ее сохранения 35 больным нефротуберкулезом выполнена ЧПНС с последующей оценкой КФ путем осуществления раздельной пробы Реберга. С этой целью суточную мочу из дренированной почки и выпущенную самостоятельно собирали раздельно. Пробу ставили на следующие, 7–9-е и 14–16-е сутки после отведения мочи.
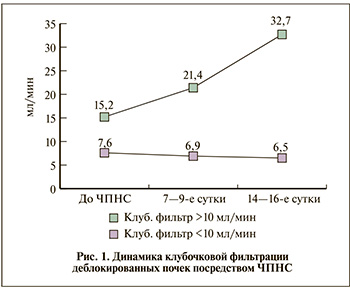
Установлено, что после ЧПНС в 15 (42,9%) почечно-мочеточниковых единицах (ПМЕ) парциальная составляющая КФ составила от 2,5 до 9,0 мл/мин, в среднем – 7,6±1,0 мл/мин. При контрольном исследовании отмечена ее убыль в среднем на 0,5±0,2 на 7–9-е сутки и 1,1±0,4 мл/мин – на 14–16-е сутки (p>0,05). При колебаниях КФ от 11,2±2,3 до 19,1±2,0 (15,2±2,1) мл/мин зарегистрирован прирост этого показателя на 6,2±1,3 и 17,5±3,1 мл/мин соответственно (p<0,05). Данные о динамике клубочковой фильтрации дренированных почечно-мочеточниковых единиц (ПМЕ) представлены на рис. 1.
Показано, что при исходном уровне КФ менее 10 мл/мин резервные возможности почки при уретерогидронефрозе туберкулезной этиологии исчерпаны. Когда клиренс креатинина превышает эту величину, происходит восстановление функции деблокированной почки. В первом случае показана нефрэктомия или нефроуретерэктомия, во втором – реконструктивное вмешательство на мочеточнике.
Этиология протяженных стриктур мочеточников, подвергнутых заместительной пластике, представлена в табл. 1. Большинство (36 – 75,0%) больных оперировали по поводу туберкулеза, реже (12 – 25,0%) – в связи с иными заболеваниями. Ятрогенные повреждения мочеточника (4–8,3%) возникли вследствие иссечения натечного абсцесса (1), уретеролитотомии в средней трети (1), операции Боари (1), экстирпации матки (1). Шести (12,5%) больным операции осуществлены по поводу нейромышечной дисплазии мочеточников и болезни Ормонда, 2 (4,2%) – в связи с лучевыми стриктурами и облитерациями.
Виды реконструкций верхних мочевыводящих путей показаны в табл. 2. В отношении 45 больных использовали подвздошную кишку, 3 – червеобразный отросток. Двадцати шести (54,2%) пациентам замещали только мочеточник, 22 (45,8%) – мочеточник и мочевой пузырь. Замещение сегментом кишки одного мочеточника произведено 43 пациентам, двух – 5. У 12 больных патологический процесс локализовался только в тазовом отделе мочеточника. Из них 10 больным потребовалась замена дистальной части одного и 2 – двух мочеточников. При этом длина пораженного дистального участка составила не менее 10 см и зона повреждения у всех пациентов распространялась выше подвздошных сосудов. Двум пациентам выполнена аппендикопластика средней трети (с/3) мочеточника, а 1 из них в сочетании с замещением поясничного отдела лоскутом мочевого пузыря по Боари. У 1 пациентки червеобразный отросток успешно использован для замещения нижней трети (н/3) правого мочеточника. Для выяснения локализации патологического процесса, уточнения функционального состояния почки и мочеточника под ультразвуковым и рентгенотелевизионным контролем им произведена ЧПНС с антеградной пиелоуретерографией. В результате рентгенологического обследования выявлены протяженные дефекты в н/3 и с/3 мочеточника, не позволившие выполнить типичные реконструктивные операции. Для иллюстрации эффективности аппендикоуретеропластики приводим одно их клинических наблюдений.
 Больная И.О.С. 1965 г.р. (47 лет) находилась на обследовании и лечении с 11.02.13. по 11.04.13. в урологическом отделении № 1 Московского НПЦ борьбы с туберкулезом. Поступила с жалобами на наличие нефростомического дренажа справа.
Больная И.О.С. 1965 г.р. (47 лет) находилась на обследовании и лечении с 11.02.13. по 11.04.13. в урологическом отделении № 1 Московского НПЦ борьбы с туберкулезом. Поступила с жалобами на наличие нефростомического дренажа справа.
Из анамнеза известно, что диссеминированный туберкулез легких в фазе инфильтрации и обсеменения, МБТ(+), выявлен в июне 2012 г. Начато лечение в туберкулезной клинической больнице № 3 Москвы, в ходе обследования выявлен правосторонний уретерогидронефроз. В условиях урологического отделения № 1 Московского НПЦ борьбы с туберкулезом в октябре 2012 г. выполнена пункционная нефростомия справа. В ходе обследования выявлена высокодифференцированная аденокарцинома матки. в Московском областном онкологическом диспансере 16.01.13 произведена пангистерэктомия, интраоперационно выявлены рубцовые сращения правого мочеточника в н/3, не позволившие исключить туберкулезное поражение. Гистологически верифицирован первично-множественный синхронный рак эндометрия рТ1аNxM0 и шейки матки in situ pTisNxM0.
Диагноз при поступлении: МКБ, конкремент правой почки. Правосторонний уретерогидронефроз. ЧПНС справа в октябре 2012 г. Вторичный хронический пиелонефрит, ремиссия. Туберкулез мочеполовых органов? Инфильтративный туберкулез верхней доли левого легкого. МБТ (-).
При поступлении состояние удовлетворительное. Кожные покровы чистые, отеков нет, температура тела нормальная. Пульс – 78 в 1 мин, ритмичный. Артериальное давление – 110/70 мм рт. ст. Тоны сердца приглушены. Частота дыхания 17 в 1 мин. При аускультации выслушивается жесткое дыхание. Живот мягкий, безболезненный при пальпации. Печень, селезенка, почки не пальпируются. Пальпация и поколачивание в проекции почек безболезненны с обеих сторон. Физиологические отправления в норме.
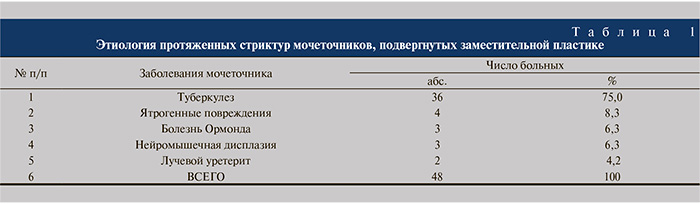
Нефростомический дренаж переустановлен. Продолжено противотуберкулезное лечение по фазе продолжения согласно рекомендациям фтизиатров. Выполнена антеградная пиелоуретерография справа, выявлено препятствие в н/3 мочеточника (рис. 2). Скорость КФ по данным пробы Реберга в деблокированной правой почке превышает20 мл/мин, уровень креатинина крови соответствует нормальным показателям. По лабораторным данным зарегистрировано снижение гемоглобина крови до 97 г/л, гематокрита до 26,6%, лейкоцитурия до 35 в поле зрения, эритроцитурия до 20.
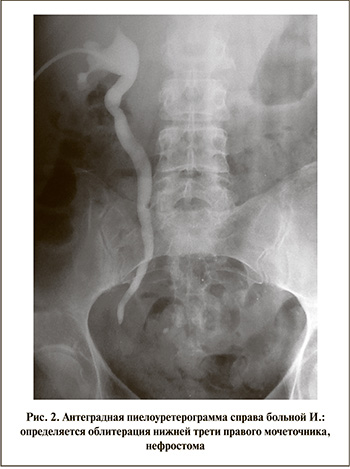
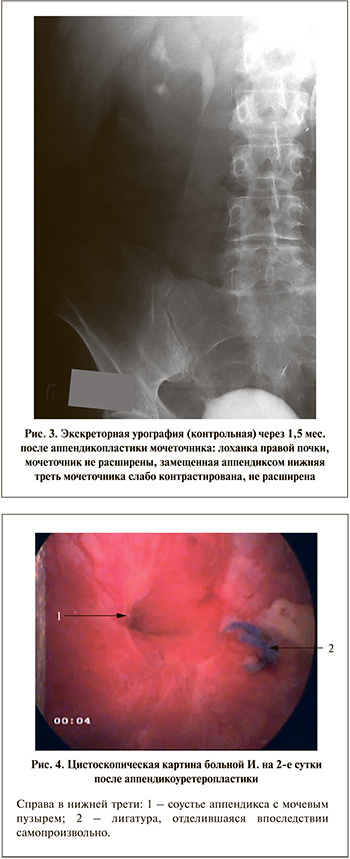
Для восстановления проходимости правого мочеточника 07.03.13 выполнена его пластика в н/3 червеобразным отростком. Послеоперационный период протекал без осложнений, последовательно удалены дренажи: 21.03.13 – на 14-е сутки нефростома, 03.04.13 – на 26-е сутки стент из правой почки. Эхографически расширения чашечно-лоханочной системы почки не отмечено. Гистологическое исследование ткани удаленного мочеточника выявило картину хронического уретерита, наличие гранулем. Методом полимеразной цепной реакции обнаружена ДНК МБТ. Установлен диагноз: туберкулезный папиллит правой почки, туберкулез правого мочеточника, МБТ(-). Продолжено лечение двумя противотуберкулезными препаратами, а также проведена энзимофизиотерапия на область правого мочеточника. По данным внутривенной урографии от 10.04.13 пассаж контрастного вещества по верхним мочевыводящим путям справа не нарушен (рис. 3). При цистоскопии определяется соустье аппендикса с мочевым пузырем, напоминающее естественное устье мочеточника (рис. 4). Выписана для продолжения лечения по месту жительства.
Диагноз при выписке: Туберкулез множественных локализаций: туберкулез мочеполовых органов: туберкулезный папиллит правой почки, туберкулезный уретерит справа. МБТ (-). Инфильтративный туберкулез верхней доли левого легкого, МБТ(-). Пластика н/3 правого мочеточника червеобразным отростком 07.03.13 по поводу стриктуры мочеточника. Нефростомия в октябре 2012 г. в связи с уретерогидронефрозом справа. Сопутствующие заболевания: Первично-множественный синхронный рак: рак эндометрия рТ1аNxM0. Рак шейки матки in situ pTisNxM0. Пангистерэктомия 16.01.13 ХОБЛ. Хронический бронхит курильщика, ремиссия. ДН 2-й ст. Хронический панкреатит, ремиссия.
Ранние осложнения оперативного вмешательства зарегистрированы у 2 (4,1%) больных, включая 1 (2,1%) некроз трансплантата и 1 (2,1%) несостоятельность межкишечного анастомоза. В первом наблюдении потребовалось удаление кишечного трансплантата и наружное дренирование почки, во втором – ревизия органов брюшной полости, межкишечный реанастомоз и интубация кишечника зондом Эббота. После некроза трансплантата удалось восстановить естественный пассаж мочи, выполнив повторную уретероилеопластику, а во втором – справиться с перитонитом и парезом кишечника. Отдаленные результаты лечения в сроки от 0,5 до 8 лет изучены у 31 (64,6%) пациента, осложнения отмечены у 4 (8,3%) больных. Пузырно-кишечно-мочеточниковый рефлюкс при ретроградной цистографии выявлен только у 2 больных после замещения правого мочеточника кишечным сегментом длиной 10 см. Они получали консервативное лечение. Острый пиелонефрит выявлен у 2 больных. Нарастание уровня креатинина в крови имело место у 1 больной после тотального замещения обоих мочеточников и мочевого пузыря с одновременной цистоуретеропластикой.
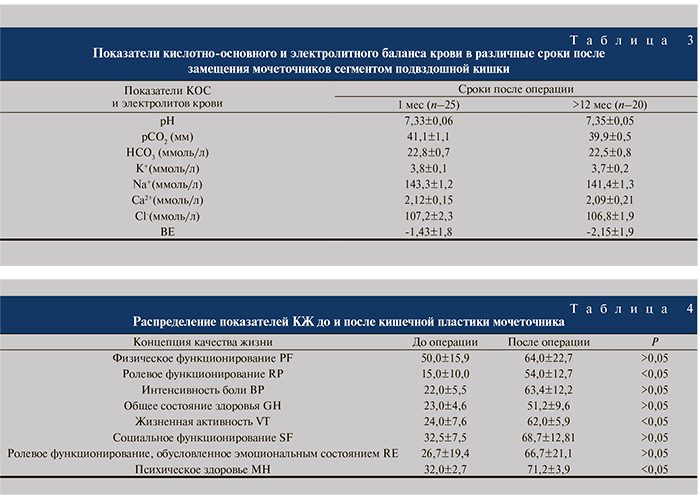
При использовании подвздошной кишки для замещения мочевыводящих путей в результате резорбции электролитов может развиваться гиперхлоремический метаболический ацидоз, который наиболее часто появляется при ХПН. Поэтому нами изучены средние показатели кислотноосновного (КОС) и электролитного баланса крови в раннем послеоперационном периоде у 25 пациентов и через 6–12 месяцев у 21 больного после илеоуретеропластики (табл. 3).
В течение первого месяца после илеоуретеропластики среднее значение уровня калия в сыворотке крови составило 3,8±0,1 ммоль/л; хлора – 107,2±2,3; дефицит оснований (ВЕ) – -1,43±1,8 ммоль/л. Через 6–12 месяцев после операции эти показатели оставались стабильными. Концентрация калия была 3,7±0,2 ммоль/л; хлора – 106,8±1,9, недостаток оснований (ВЕ) – 2,15±1,9 ммоль/л. Таким образом, использование для замещения мочеточника подвздошной кишки длиной не более 25 см не приводило к серьезным метаболическим и электролитным нарушениям. Благодаря широкому пузырно-кишечному анастомозу не происходит застаивания мочи в кишечном трансплантате, уменьшается время ее контакта с кишечным эпителием. В таких условиях резорбция мочи и, следовательно, развитие метаболического ацидоза сводятся к минимуму.
Для изучения качества жизни (КЖ) выполнено анкетирование с помощью общего опросника SF-36 23 больных, перенесших кишечные реконструкции мочеточников, до операции и через 4–6 месяцев после (табл. 4). Установлено, что пациенты с протяженными стриктурами мочеточников имеют низкие показатели КЖ. Изучая отдаленные результаты, отмечено существенное улучшение КЖ по всем показателям, особенно психического компонента здоровья, жизненной активности и ролевого функционирования, стойкое снижение интенсивности болевого симптома (p<0,05).
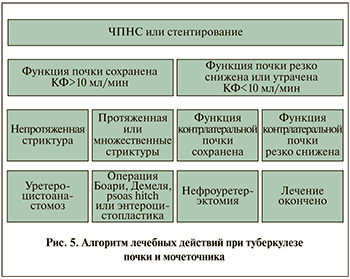
Таким образом, кишечная пластика мочеточников при их протяженных сужениях туберкулезного и другого генеза является эффективным способом восстановления уродинамики при невозможности использования тканей мочевого тракта. Данные операции позволяют избавлять пациентов от пожизненного наружного дренирования почек, сохраняя их функцию и существенно улучшая связанное со здоровьем качество жизни пациентов по всем показателям. Все вышеизложенное позволило представить алгоритм лечебных действий в отношении больных туберкулезом почки и мочеточника (рис. 5).
Заключение. Изучение клубочковой фильтрации деблокированной путем ЧПНС почки позволяет определять хирургическую тактику: при ее величине менее 10 мл/мин избрать органоуносящее вмешательство, при превышении этого показателя – органосохраняющее (реконструктивно-восстановительное).
Протяженные поражения мочеточников при невозможности восстановления тканями мочевого тракта являются показанием к выполнению реконструктивно-восстановительных операций с использованием участка тонкой кишки. Выполнение данных операций позволяет избавлять пациентов от пожизненного наружного дренирования почек в 92,0% наблюдений, тем самым существенно улучшая качество жизни. Последнее исходно имеет низкие показатели, которые в результате кишечной реконструкции мочеточников в отдаленном послеоперационном периоде значительно улучшаются (p<0,05).
При множественных и протяженных стриктурах мочеточника туберкулезной и иной этиологии оптимальным методом его реконструкции является илеоуретеропластика. При невозможности использования подвздошной кишки альтернативой является аппендикоуретеропластика, если червеобразный отросток по своим анатомическим параметрам соответствует пораженному отделу мочеточника.


