Введение. В 1985 г. американский изобретатель Ч. Халл запатентовал процесс «стереолитографии» и основал компанию «3D-Systems», положившую начало виртуальным технологиям. Однако развитие трехмерных технологий было бы невозможным без компьютерной томографии – метода рентгенов-ской визуализации органов и тканей, предложенного в 1972 г. американским физиком А. Кормиком и английским инженером-физиком Г. Хаунсфилдом. В 1979 г. ученые были удостоены Нобелевской премии в области физиологии и медицины. В последние десятилетия компьютерные технологии прочно вошли во все сферы деятельности человека, в том числе в медицину, в особенности в хирургию. Первая лапароскопическая операция с использованием метода виртуальной реальности была произведена в 1989 г. В России наибольшим опытом использования виртуальных технологий в хирургии обладает Институт хирургии им. А. В. Вишневского. В частности, в 2003 г. среди 349 пациентов с различными заболеваниями органов брюшной полости у 16 операции были выполнены по поводу опухоли почки [1]. Урологи и онкоурологи стали использовать трехмерное моделирование с целью планирования операций в последние 5–7 лет [2–6].
В настоящей работе мы хотели бы продемонстрировать актуальность трехмерного моделирования в урологической практике как в целом, так и на примере опыта клиники урологии Первого МГМУ им. И. М. Сеченова.
Материалы и методы. За 2014 г. в клинике урологии Первого ММУ им. И. М. Сеченова прооперированы 206 пациентов с опухолями почки, которым проводились лапароскопические (n=133) и открытые (n=71) вмешательства. У двух пациентов группы лапароскопического пособия почка была един-ственной. При этом у пациентов с функционально или анатомически единственной почкой, а также тех больных, у которых однозначно определить локализацию опухолевого узла не представлялось возможным, было выполнено трехмерное компьютерное моделирование (n=118).
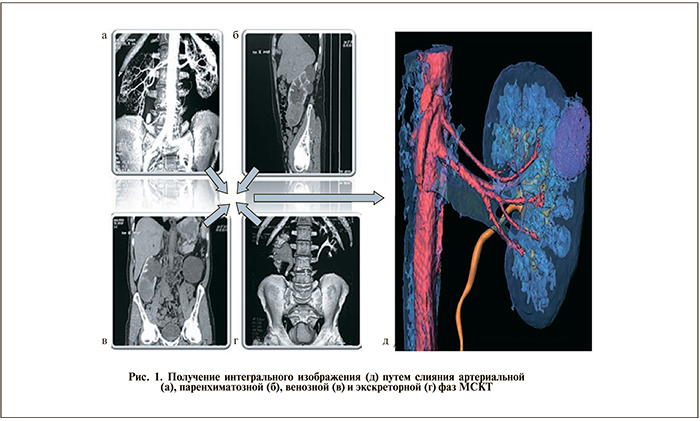
 Интегральное объемное изображение получали путем совмещения четырех основных фаз контра-стного усиления мультиспиральной компьютерной томографии (МСКТ): артериальной, паренхиматозной, венозной и экскреторной (рис. 1).
Интегральное объемное изображение получали путем совмещения четырех основных фаз контра-стного усиления мультиспиральной компьютерной томографии (МСКТ): артериальной, паренхиматозной, венозной и экскреторной (рис. 1).
Полученное интегральное изображение тщательно анализируют и на основании полученных данных делают вывод о возможности оперативного вмешательства как такового, оценивают вероятность проведения органосохраняющего пособия и выбирают оптимальный доступ и тип операции.
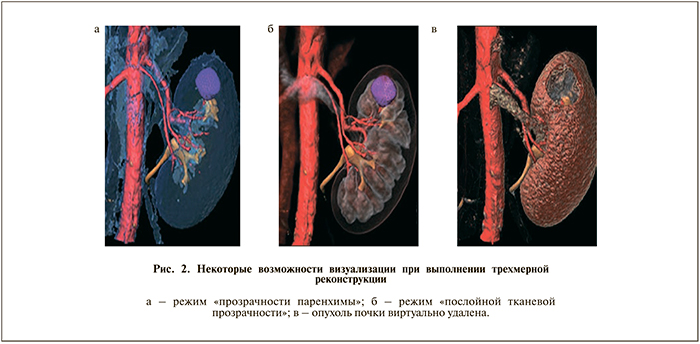
Рассмотрим анализ трехмерных моделей патологического процесса более детально. Благодаря специальному программному обеспечению существует возможность загружать данные в формате Dicom/Dacs, в результате чего получаются 3D-изображения виртуальной реальности. После построения объемной модели рентгенолог, хирург и программист отбирают необходимые изображения, располагают их в соответствующем порядке и положении, производят вычитание и соединение отдельных фрагментов. Самым простым вариантом виртуальной хирургии является околоопухолевая резекция или энуклеация, которые можно выполнить благодаря возможности подробнейшего изучения трехмерной модели в различных проекциях, в статичном и динамичном режимах. Все это позволяет оценить индивидуальные особенности как внеорганного, так и интраренального почечного кровоснабжения с учетом взаимоотношений с элементами чашечно-лоханочной системы. Для получения возможно полной информации трехмерную анатомическую реконструкцию необходимо изучать в различных режимах: прозрачности (интраренальные структуры в «стеклянном стакане» – паренхима виртуально удалена), полупрозрачности (интраорганные структуры определяются внутри передней или задней фронтальной поверхности почки (рис. 2)), выполняя тот или иной вид виртуальной операции.
Полученная из разных ракурсов максимально подробная визуальная картина является основой для следующего процесса – непосредственного выполнения виртуальной операции, которая может быть многократно исполнена с тем, чтобы оценить результат каждого из вариантов и определить наиболее подходящий. Например, «сечение» паренхимы путем общепринятой плоскостной резекции почки у конкретного пациента может быть сопряжено с высоким риском повреждения чашечки, а «клиновидная» резекция паренхимы к подобному осложнению не приведет, поэтому выбор должен быть сделан в пользу последнего варианта.
Изучение раневой поверхности после того или иного вида резекции позволяет спланировать наиболее рациональный из них. Возможность виртуального сечения в любой плоскости представляет широчайшие возможности для планирования оптимальной, но уже реальной операции.
Результаты. Лапароскопическая нефрэктомия при раке почки была проведена у 60 больных, резекция – у 73 (в том числе у 8 ретроперитонеоскопически). Открытые нефрэктомии по поводу рака почки выполнены 60 пациентам, открытые резекции – 11 больным. Средний возраст пациентов, которым выполнялось лапароскопическое органосохраняющее пособие, составил 55,7 года, органоуносящее – 59,8 года, открытые нефрэктомии и резекции – 72 года и 65 лет соответственно.
В группе больных, которым было выполнено лапароскопическое пособие, у 73 пациентов проведена органосохраняющая операция, из них у 59 (80,8%) заболевание соответствовало стадии pT1a, у 7 (9,6%) – pT1b и у 7 (9,6%) – pT3a. У 60 больных ввиду неблагоприятного анатомического расположения опухолевого узла или тяжелой сопутствующей патологии выполнена лапароскопическая нефрэктомия, из них у 7 (11,66%) диагностирована стадия pT1a, у 19 (31,66%) – pT1b, у 10 (16,66%) – pT2a, у 3 (5%) – pT2b, у 21 (35%) – pT3a.
 В группе открытых оперативных пособий нефрэктомия проведена у 1 (1,6%) больного с опухолью стадии pT1a, у 4 (6,7%) – pT1b, у 41 (68,3%) – pT3a, у 7 (11,7%) – pT3b и у 7 (11,7%) – pT4. Резекция почки выполнена 7 (63,6%) пациентам со стадией pT1b и 4 (36,4%) – pT3a.
В группе открытых оперативных пособий нефрэктомия проведена у 1 (1,6%) больного с опухолью стадии pT1a, у 4 (6,7%) – pT1b, у 41 (68,3%) – pT3a, у 7 (11,7%) – pT3b и у 7 (11,7%) – pT4. Резекция почки выполнена 7 (63,6%) пациентам со стадией pT1b и 4 (36,4%) – pT3a.
Средняя продолжительность лапароскопической резекции почки составила 140 мин, открытой резекции – 180 мин. Аналогичный показатель при органоуносящих пособиях был равен 159 и 183 мин соответственно.
Время тепловой ишемии почки при лапароскопической резекции составило в среднем 15 мин, при открытой – 14 мин.
Как уже было сказано выше, для получения максимально достоверной информации о локализации опухолевого узла, особенностях его кровоснабжения и вариантах клинической анатомии элементов почечной ножки использовали МСКТ с трехмерной реконструкцией изображений. Подробный анализ трехмерных реконструкций позволял не только выбрать оптимальный вид операции для данного пациента, но и в целом решить вопрос об операбельности или иноперабельности при местно-распространенном процессе, а также резектабельности при локальном процессе.
Трудно переоценить возможности трехмерного моделирования в решении вопросов, касающихся технического исполнения расширенной операции при опухоли почки с резекцией соседнего органа. Для иллюстрации данного утверждения приводим клиническое наблюдение.
Б о л ь н о й К. 59 лет поступил в клинику урологии с опухолью правой почки стадии Т4N0M0 (инвазия в печень), а также кистой той же почки. Очевидно, что у данного пациента вопрос об органоуносящем оперативном пособии был решен однозначно, а вот об объеме операции на печени оставался открытым. На основании данных различных методов визуализации сказать однозначно, имела ли место инвазия опухоли в VI–VIII сегменты печени, какова глубина инвазии и, соответственно, каков объем предстоящего оперативного пособия, было невозможно. Однако детальный анализ трехмерных реконструкций патологического процесса позволил дать ответы на все указанные вопросы. У данного пациента опухоль почки проникала в вещество печени на 3,7 см в области только VII сегмента органа. Кроме того, на объемной модели удалось предельно точно рассчитать расстояние от края опухолевого узла до крупной артериальной ветви печени (рис. 3). Таким образом, именно виртуальная технология указала на возможность выполнения наряду с нефрэктомией реальной резекции печени у больного, ранее признанного в другом лечебном учреждении иноперабельным (рис. 4).
В некоторых ситуациях изучение трехмерных моделей позволило избежать оперативного пособия, которое могло неблагоприятно закончиться для больного.
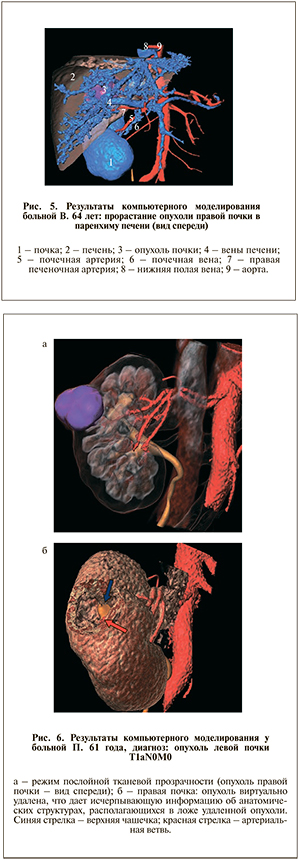
Убедительным примером может послужить история болезни п а ц и е н т к и В. 64 лет с четвертой стадией опухоли правой почки, инвазией в печень. При анализе трехмерной реконструкции патологического процесса у данной пациентки было установлено, что опухолевый узел расположен в непосредственной близости от крупных вен печени, а потому выполнение резекции органа невозможно, поскольку сопряжено с риском повреждения крупных сосудов (рис. 5).
С целью попытки продления жизни больной было решено на первом этапе лечения прибегнуть к пункционной биопсии опухоли почки с последующим выполнением эмболизации почечных сосудов справа. Далее провести курс таргетной химиотерапии, после чего вновь рассмотреть вопрос о возможности выполнения органоуносящего оперативного пособия.
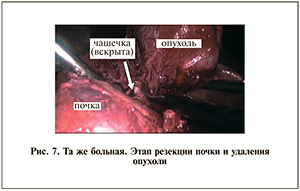 Широкое внедрение органосохраняющих операций при локализованной опухоли почки заставляет проводить анализ так называемой резектабельности опухоли. Тенденция сохранить почку, удалив новообразование методом резекции органа или энуклеации опухоли с использованием всех технически осуществимых пособий, в том числе у пациентов со здоровой противоположной почкой, заставляет на основании предоперационной информации отвечать на вопрос: выполнима ли реально органосохраняющая операция? Логично, если этот ответ будет базироваться на данных виртуально выполненной операции с подробным анализом возможных вариантов, то есть не на субъективной оценке, а на объективных данных. Виртуальная операция становится жизненно необходимой при опухоли единственной почки. Всесторонний анализ топографо-анатомических нюансов, планирование безишемической резекции почки, обеспечение гемостаза из раны почки, сохранение или восстановление целостности внутрипочечных мочевых путей, ревизия глубинной раны почки после удаления опухоли – эти и другие вопросы требуют максимально достоверной информации на дооперационном этапе. Именно виртуальное планирование и выполнение оперативного пособия позволяют снять данные вопросы еще на дооперационном этапе. Такой всесторонний анализ виртуальной операции позволит осуществлять реальную операцию у каждого конкретного пациента, ориентируясь на изображение на экране персонального компьютера непосредственно в операционной. Перечисленные моменты в подходе к планированию операции у больной раком правой почки представлены на рис. 6, 7.
Широкое внедрение органосохраняющих операций при локализованной опухоли почки заставляет проводить анализ так называемой резектабельности опухоли. Тенденция сохранить почку, удалив новообразование методом резекции органа или энуклеации опухоли с использованием всех технически осуществимых пособий, в том числе у пациентов со здоровой противоположной почкой, заставляет на основании предоперационной информации отвечать на вопрос: выполнима ли реально органосохраняющая операция? Логично, если этот ответ будет базироваться на данных виртуально выполненной операции с подробным анализом возможных вариантов, то есть не на субъективной оценке, а на объективных данных. Виртуальная операция становится жизненно необходимой при опухоли единственной почки. Всесторонний анализ топографо-анатомических нюансов, планирование безишемической резекции почки, обеспечение гемостаза из раны почки, сохранение или восстановление целостности внутрипочечных мочевых путей, ревизия глубинной раны почки после удаления опухоли – эти и другие вопросы требуют максимально достоверной информации на дооперационном этапе. Именно виртуальное планирование и выполнение оперативного пособия позволяют снять данные вопросы еще на дооперационном этапе. Такой всесторонний анализ виртуальной операции позволит осуществлять реальную операцию у каждого конкретного пациента, ориентируясь на изображение на экране персонального компьютера непосредственно в операционной. Перечисленные моменты в подходе к планированию операции у больной раком правой почки представлены на рис. 6, 7.
Заключение. В настоящей работе мы попытались продемонстрировать, насколько необходима и жизненно важна для пациента трехмерная реформация анатомических структур и «виртуальная репетиция» показанного реального оперативного пособия.
В ситуации, когда хирург неоднократно выполнит операцию в различных вариантах и выяснит, что оперативное вмешательство сопряжено с риском для жизни пациента, никто не осудит его, если он все-таки откажется от операции, ссылаясь на ее сложность и рискованность. В то же время, признавая больного иноперабельным, хирург возлагает на себя огромную ответственность, т.к. наиболее эффективным методом лечения больных раком почки остается оперативный, а отказ от операции практически лишает пациента надежд на выздоровление или хотя бы на продление жизни. Если же все-таки хирург принимает решение об операции, несмотря на ее высокий риск, ему необходимы доводы в пользу такого решения. И более весомого довода, чем виртуальное осуществление операции в разных вариантах, вряд ли можно привести. В последнее время появились сообщения о 3D-принтинге макета почки с опухолью у конкретного больного. Напечатанная на основании виртуальной трехмерной модели почка утеряла свою абстрактность (по выражению одного из соавторов, «она была вырвана из виртуальных лап»), имела материальную структуру (специальный прозрачный материал), поддавалась воздействию хирургических инструментов. Наблюдение было представлено на конгрессе EAU в Стокгольме в 2014 г. Несмотря на то что напечатанная 3D-принтинговая копия почки не является функциональной, возможность получить манипуляционные ощущения и выполнить рациональное «виртуально-мануально-реальное» пособие при опухоли почки открывает новые перспективы в решении проблемы инжиниринга органов и заставляет задуматься о смысле фразы известного философа Р. Юнга «Если Вам не лень, то будущее уже наступило». Глубокий смысл фразы может восприниматься по-разному, неоднозначно, призывает достойно оценить достигнутое, творчески подойти к выполнению намеченного, а применительно к тематике операции на почке – заставляет хирурга, it-технолога и рентгенолога совместно создавать трехмерное изображение почки и патологического процесса, творчески спланировать и осуществить виртуальную операцию и оценить результаты своего «творчества».


