Введение. Экстрофия мочевого пузыря — довольно редкая врожденная аномалия, встречающаяся с частотой 1/10 000–1/50 000 новорожденных [1]. Поскольку таких пациентов, как правило, оперируют в раннем детстве, взрослые с подобными аномалиями встречаются крайне редко. Вследствие недостаточной информированности родителей или недоступности адекватной медицинской помощи, например. в отдаленных районах эту аномалию в отдельных случаях оперируют у взрослых. Еще одну немногочисленную группу составляют взрослые после неудачных операций, выполненных в детстве. Так или иначе, при выполнении реконструктивных операций взрослым восстановление брюшной стенки, особенно без остеотомии, остается серьезной проблемой.
Представляем описание методики реконструкции и результаты лечения экстрофии–эписпадии у взрослого пациента.
Б о л ь н о й М. 33 лет поступил в нашу клинику 15.09.07 с диагнозом «экстрофия мочевого пузыря, эписпадия». Из анамнеза известно, что пациенту дважды, в возрасте 10 и 23 лет, производились попытки оперативного лечения врожденной аномалии, не увенчавшиеся успехом. При осмотре обращала на себя внимание везикальная площадка с резко измененной гипертрофированной слизистой и выраженной кератинизацией по краям. Размеры дефекта передней брюшной стенки составляли около 10х10 см, диастаз между лонными костями – около 11 см. При ультразвуковом и рент- генологическом исследовании расширения верхних мочевых путей не отмечено. Основные биохимические показатели крови были в пределах нормы. Обращали на себя внимание выраженные психологические изменения, низкие самооценка и уровень социальной коммуникабельности. Пациент отмечал эрекции при сексуальной стимуляции. 21.09.07 пациенту была выполнена операция: цистпростатэктомия, формирование гетеротопического континентного резервуара, пла- стика передней брюшной стенки.
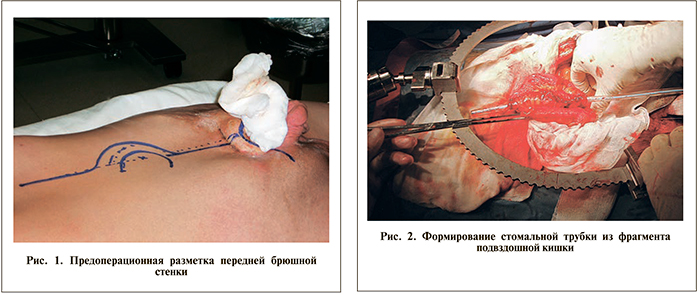
Методика операции. Выполнили срединную лапаротомию (рис. 1). При этом везикальную пластину вместе с прилегающей измененной кожей отсекли от окружающих тканей. После вскрытия париетальной брюшины по линии Тольдта с обеих сторон правый мочеточник выделили на протяжении примерно нижней трети, левый – нижней половины. Пузырные артерии, мочеточники и семявыносящие протоки лигировали и пересекли с обеих сторон. Дистальные концы лигатур использовали в качестве держалок. После выделения семенных пузырьков и протоков, рассечения фасции Денонвилье заднюю стенку мочевого пузыря преимущественно тупым путем отсепаровали от прямой кишки. После вскрытия внутритазовой фасции и пересечения пубопростатических связок лигировали и пересекли дорсальный венозный комплекс. Мочевой пузырь удалили единым комплексом с предстательной железой и семенными пузырьками.
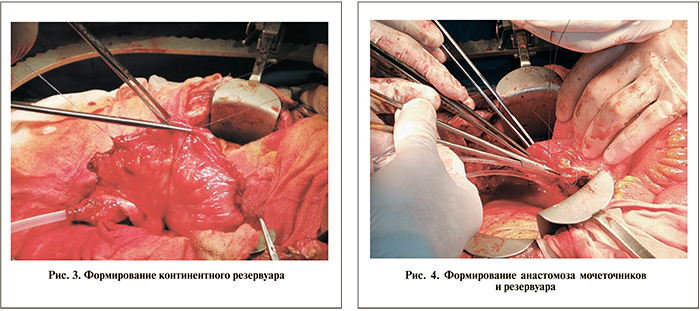
Выполнили аппендэктомию. На 15 см проксимальнее илеоцекального угла последовательно выделили и отсекли на брыжейке два фрагмента подвздошной кишки длиной 10 и 45 см соответ- ственно. Целостность подвздошной кишки восстановили путем анастомоза «конец в конец» однорядным швом. Из короткого фрагмента кишки на дренаже 24 Ch сформировали эфферентный сегмент для наложения наружной стомы после отсечения избытка стенки кишки (рис. 2). Длинный сегмент кишки уложили S-образно и детубуляризировали на всем протяжении. После реконфигурации сформировали резервуар непрерывным монофиломентным швом (рис. 3). Левый мочеточник провели под корнем брыжейки. Выполнили анастомоз между медиальными краями спатулированных на протяжении 3 см мочеточников. После проведения интубаторов сформировали мочеточниково-резервуарный анасто- моз (рис. 4). Ранее сформированный эфферентный подвздошно-кишечный сегмент анастомозировали с резервуаром после погружения в экстрамуральный серо-серозный тоннель на протяжении 4 см, сформированный отдельными швами через «окна» в брыжейке. Наружный конец стомальной трубки вывели через отверстие в передней брюшной стенке и фиксировали к апоневрозу и коже отдельными швами. Мочеточниковые интубаторы и цистостомический дренаж вывели через отдельные проколы наружу. Резервуар фиксировали к передней брюшной стенке. Через континентную стому в резервуар провели силиконовый катетер 22 Ch.
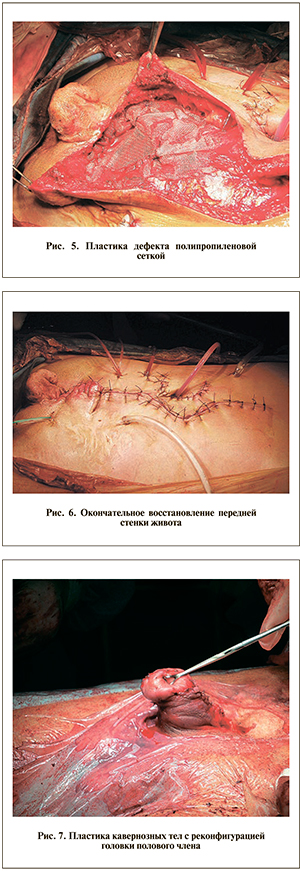 При ушивании раны заместить мышечно-апоневротический дефект размером 10х10 см местными тканями путем транспозиции не представлялось возможным. После низведения сальника область дефекта закрыли полипропиленовой сеткой размером 15х16 см. Последнюю фиксировали к окружающим тканям отдельными швами (рис. 5). Кожу и подкожную клетчатку ушили над сеткой, оставив дополнительный активный дренаж (рис. 6).
При ушивании раны заместить мышечно-апоневротический дефект размером 10х10 см местными тканями путем транспозиции не представлялось возможным. После низведения сальника область дефекта закрыли полипропиленовой сеткой размером 15х16 см. Последнюю фиксировали к окружающим тканям отдельными швами (рис. 5). Кожу и подкожную клетчатку ушили над сеткой, оставив дополнительный активный дренаж (рис. 6).
Антибиотики пациент получал внутривенно в течение 15 дней. Признаков раневой инфекции отмечено не было. Дренажи удалены последовательно через 5–7 дней после операции, мочеточниковые интубаторы – на 10-й и 12-й день, резервуаростомический дренаж – на 15-й день, катетер континентной стомы – на 21-е сутки. Пациент выписан из клиники через 4 недели после операции.
При обследовании через 5 лет после операции состояние пациента удовлетворительное, континенция хорошая, емкость резервуара при резервуарографии составляла около 500 мл, форма резервуара эллипсоидная. Пациент опорожнял резервуар 4–6 раз в сутки, используя катетер 14 Ch. Подтекания мочи пациент не отмечал ни в дневное, ни в ночное время. Проблем с самокатетеризацией в течение всего периода наблюдения не возникло. Редкие эпизоды мочевой инфекции купировались пероральным приемом уросептиков. При УЗИ почки и верхние мочевые пути без особенностей, конкрементов не обнаружено. Все основные биохимические параметры крови в пределах нормы, включая креатинин плазмы – 110 мкмоль/л. Пациент выразил большую удовлетворенность изменением своего тела, улучшение социальной адаптации и степени самооценки по результатам заполнения опросника, используемого в нашем центре. Эректильная функция оказалась достаточной для ведения половой жизни. В связи с этим 15.10.12 пациенту выполнена пластика кавернозных тел с реконфигурацией головки полового члена (рис. 7). Через 2 мес косметический эффект операции пациент оценил как хороший.
В настоящее время значительные усилия направлены на улучшение пренатальной диагностики экст- рофии мочевого пузыря [2]. Тем не менее все еще встречаются случаи обращений взрослых пациентов по поводу экстрофии. Безусловно, подобные случаи вызывают одновременно большое удивление и клинический интерес, так как имеющиеся явные анатомические изменения, сопровождающиеся по- стоянным истечением мочи, не могут быть незамеченными до такого возраста и являются причиной особого образа жизни таких пациентов. В частности, у нашего пациента отмечались выраженные психологические изменения. В связи с редкостью подобных случаев, вариабельностью вторичных изменений и присоединяющихся осложнений до настоящего времени не существует единого подхода к реконструктивным вмешательствам при экстрофии у взрослых.
В 1987 г. T. Matsuda и соавт. [3] описали лечение экстрофии мочевого пузыря у 24-летней женщины путем формирования континентного резервуара по Коку. Успешное использование континентного илеум-резервуара позволило не только радикально улучшить физиологическое качество жизни, но и сущест- венно повлиять на ее ментальность. С тех пор было опубликовано еще несколько случаев коррекции подобных аномалий у взрослых [4–7]. Возможность выполнения реконструкции с сохранением мочевого пузыря ограничена выраженными многолетними вторичными изменениями слизистой и высоким риском малигнизации [4, 8, 9]. N. Smeulders и соавт. [9], обследовав 103 пациентов с классическим аномальным комплексом экстрофии–гипоспадии, обнаружили, что частота возникновения карциномы пузыря у таких пациентов в 700 раз превышала частоту заболевания в общей популяции с учетом возраста.
В связи с выраженными изменениями слизистой и рубцовыми изменениями прилежащих тканей после ранее перенесенных оперативных вмешательств единственным реальным методом отведения мочи мы сочли формирование континентного резервуара из подвздошной кишки. Для обеспечения удерживающего механизма был создан экстрамуральный серо-серозный тоннель. Последующее наблюдение продемонстрировало хорошую континентную функцию стомы и удовлетворенность пациента косметическим эффектом. Все это позволило достичь высокой степени физической и социальной адаптации. О надежности этой относительно простой методики свидетельствует отсутствие стенозирования и трудностей при катетеризации в течение более 5 лет. В течение этого периода не отмечено тенденции к снижению функции почек.
Одной из главных проблем при операциях по поводу экстрофии у взрослых является выраженный дефект передней брюшной стенки. Использование того или иного метода с целью его закрытия во многом определяется степенью «дефицита» местных тканей, выраженностью склероза и воспалительных изменений. H. Pathak и соавт. [7] успешно использовали транспозицию мышечных лоскутов. При относительной сохранности мышечной стенки пузырной пластины A. Mansour и соавт. [10] предложили использовать ее для укрепления передней брюшной стенки после предварительного иссечения слизистой. Использование тазовой остеотомии для уменьшения диастаза сопровождается высоким риском развития остеомиелита, септического артрита, повреждения бедренного нерва, асимметрии таза [10].
В связи со значительным дефицитом тканей, обусловленным как самой аномалией, так и послед- ствиями выполненных ранее операций, в описанном наблюдении не представлялось возможным обойтись транспозицией мышечных лоскутов для восстановления и укрепления передней стенки. Учитывая возраст пациента и существенный риск развития «костных» осложнений, мы воздержались от выполнения остеотомии, а для реконструкции и укрепления стенки живота с успехом использовали полипропиленовую сетку. Последняя была изолирована от органов брюшной полости низведенным сальником, а от внешней среды – подкожной жировой клетчаткой и кожей. Для предотвращения скопления жидкости и развития раневых осложнений брюшная полость и подкожная клетчатка дренировались в течение первой недели до полного прекращения экссудации, а пациент получал системно антибиотики в течение двух недель после операции. Несмотря на риск развития местных осложнений на фоне хронической мочевой инфекции, рана зажила первичным натяжением. В дальнейшем за счет склероза вокруг полипропиленовой сетки нижняя часть передней стенки живота при пальпации представлялась достаточно монолитным образованием без ощущения «грыжевых ворот».
Заключение. Коррекция экстрофии мочевого пузыря у взрослых представляет технически довольно сложную задачу, состоящую из двух основных аспектов: способа отведения мочи и метода реконструкции брюшной стенки. Формирование континентного резервуара из подвздошной кишки позволяет получить хорошие функциональные и косметические результаты, не сопровождается снижением выделительной функции почек. Удаление везикальной пластины оправданно в связи с выраженными многолетними изменениями слизистой и окружающей кожи, а также высоким риском малигнизации. Использование полипропиленовой сетки значительно облегчает реконструкцию передней брюшной стенки и обеспечивает достаточную степень ее укрепления.



