Введение. В связи с увеличением продолжительности жизни населения и ростом числа пожилых и старых людей одним из важных научно-практических направлений улучшения качества их жизни является разработка методологии хирургической тактики при выполнении изолированных и симультанных операций в гериатрической урологии [1–3]. Речь идет о выборе рационального объема и характера операции c учетом полиморбидного фона пожилого пациента, риска послеоперационных осложнений, существенно влияющих на качество жизни этих больных. Однако многие вопросы, связанные с выполнением изолированных и симультанных операций пациентам старших возрастных групп с аденомой простаты (АП) остаются недостаточно изученными.
Новые возможности в решении этой проблемы открылись в условиях полноценного предоперационного обследования больных пожилого и старческого возраста, определяющих четкие показания и противопоказания к изолированным и симультанным операциям, а также в связи с внедрением в гериатрическую практику малоинвазивных хирургических технологий, успехами современной анестезиологии и реаниматологии, эффективной профилактикой послеоперационных осложнений, оптимальным сопровождением послеоперационной реабилитации [3–9].
Цель исследования: разработать научно обоснованную систему лечения больных старших возрастных групп с АП, направленную на снижение частоты и тяжести осложнений и летальности после изолированных и симультанных операций.
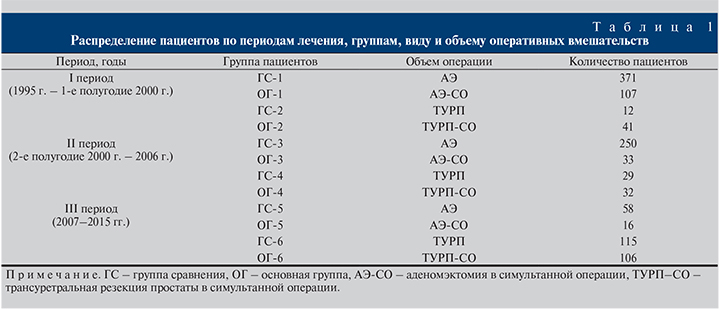
Материалы и методы. В основу работы положены результаты обследования и лечения 1170 больных пожилого и старческого возраста с АП, которым выполняли изолированную аденомэктомию (АЭ), трансуретральную резекцию простаты (ТУРП) или симультанную операцию в условиях Самарского областного клинического госпиталя ветеранов войн с 1995 по 2015 г. Симультанные операции были проведены в 335 (28,6%) наблюдениях (табл. 1).
Возраст пациентов варьировался от 60 до 89 лет; в возрасте от 60 до 75 лет было 41,3% больных, от 75 до 89 лет – 58,7%. По возрасту, основной и сопутствующей патологии и длительности заболевания все группы были репрезентативными.
При обследовании и хирургическом лечении пациентов учитывали как клинические рекомендации Российского общества урологов и Ассоциации медицинских обществ по качеству [12], так и рекомендации ведущих отечественных специалистов [1, 6–9]. При этом изучали жалобы, анамнез заболевания, физикальные и лабораторные данные (включая концентрацию простатспецифического антигена), проводили ЭКГ, ЭхоКГ, урофлоуметрию, УЗИ органов брюшной полости и забрюшинного пространства, по показаниям – КТ, рентгенографию органов грудной клетки. Больные консультированы терапевтом, неврологом, хирургом, анестезиологом, а при необходимости – и другими специалистами. У каждого больного было выявлено от 2 до 6 сопутствующих заболеваний, которые требовали предоперационной коррекции.
 Группы различались по объему обследования, характеру интраоперационной анестезии и выполненных оперативных вмешательств.
Группы различались по объему обследования, характеру интраоперационной анестезии и выполненных оперативных вмешательств.
Так, в I периоде для прогнозирования и профилактики ранних послеоперационных эзофагогастродуоденальных кровотечений (РПЭГДК) перед операцией больным выполняли ЭГДС лишь при наличии в анамнезе язвенной болезни желудка или двенадцатиперстной кишки. Выбор объема операции (изолированные АЭ, ТУРП или СО) осуществляли по существовавшим на тот момент показаниям и противопоказаниям. Операции выполняли под эндотрахеальным наркозом (63,1% пациентов), внутривенной анестезией (17,2%), под спинальной анестезией (19,7%).
Во II периоде для прогнозирования и профилактики РПЭГДК всем пациентам выполняли ЭГДС с одновременной пристеночной рН-метрией четырех функциональных зон (пищевод, тело и антрум желудка, луковица двенадцатиперстной кишки) в 11 точках. Для этого использовали отечественный аппарат АГМ-03 и гастроскопы фирмы «Olympus» (Япония). Оценку результатов эндоскопической пристеночной рН-метрии выполняли по методу, разработанному Т. К. Дубинской и соавт. [10]. У пациентов с повышенной желудочной кислотностью определяли риск развития РПЭГДК и проводили их профилактику Н2-блокаторами и ингибиторами протонной помпы (удостоверение на рационализаторское предложение № 008 от 15.10.2012). Выбор объема операции (изолированные АЭ, ТУРП или СО) осуществляли как и в I периоде. Операции выполняли под эндотрахеальным наркозом (44,1%), внутривенной анестезией (16%), спинальной анестезией (39,9%).
В III периоде всем больным выполняли ЭГДС и хромогастроскопию с использованием витального красителя конго-рот [11]. Это позволяло точнее определить уровень желудочной кислотности и более эффективно проводить профилактику РПЭГДК ингибиторами протонной помпы больным с повышенной кислотностью (удостоверение на рационализаторские предложения № 038 и 044 от 3.08.2015).
В III периоде мы существенно изменили хирургическую тактику в отношении выбора объема операции, отдавая предпочтение ТУРП как при изолированной, так и при симультанной операции. При этом значительно возросло количество больных с массой простаты более 60 г, ретротригональным ее ростом, а также больных выраженными сопутствующими интеркуррентными заболеваниями. Все эти пациенты в течение 1–2 сут проходили предоперационную подготовку в условиях отделения реанимации и интенсивной терапии (ОРИТ). У больных с ненадежным гемостазом в области ложа предстательной железы использовали устройство для гемостаза в области ложа предстательной железы (патент на полезную модель РФ № 161164 / Лещенко И. Г., Шатохина И. В., Лазарев И. Ю.; заявитель и патентообладатель – частное учреждение: образовательная организация высшего образования «Медицинский университет “Реавиз”» (RU), № 2015149195; заяв.16.11.2015; опубл. 10.04.2016. Бюлл. № 10) [3].
В зависимости от выявленных сопутствующих заболеваний пациентам проводили тщательную предоперационную подготовку с применением всего арсенала медикаментозных и немедикаментозных средств [1–3, 12].
Для определения степени операционно-анестезиологического риска для пожилых больных нами была использована методика, рекомендованная Московским научным обществом анестезиологов-реаниматологов [2, 5].
Оперативное лечение по поводу АП всем больным выполняли урологи первой и высшей категорий. Операция включила вазорезекцию с двух сторон и чреспузырную АЭ – одномоментно или в два этапа, ТУРП выполняли согласно Федеральным рекомендациям [12]. При симультанном варианте дополнительно выполняли одно или два оперативных вмешательства на наружных половых органах или по поводу вентральных грыж.
При выполнении СО по поводу сопутствующих хирургических заболеваний в операционную бригаду вводили хирурга. При этом в ходе вмешательств, выполненных с 2001 г., использовали ненатяжные методы герниопластики.
В работе использованы статистические методы описательной статистики, определение статистической значимости различий между данными разных групп пациентов на основе расчета критерия Стьюдента.

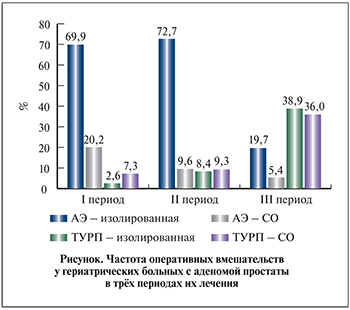
Результаты. При оценке частоты выполнения АЭ и ТУРП, как изолированных, так и в составе СО, в динамике отмечено существенное увеличение доли больных, которым выполняли малоинвазивные операции – ТУРП изолированную или в составе СО (см. рисунок).
Так, если в I периоде подавляющее большинство составили пациенты, которым была проведена АЭ, – 91,1%, то в III периоде приоритет принадлежал ТУРП – 74,9%.
Анализ показателей послеоперационных осложнений и летальности позволил установить определенные закономерности, указывающие на улучшение результатов лечения наших больных в связи с оптимизацией лечебно-диагностического процесса и хирургической тактики в III периоде по отношению ко II и особенно к I периодам (табл. 1–3).
При сравнительной оценке общего числа местных и общих осложнений при изолированной АЭ у пациентов ГС-1 отмечен более высокий их уровень по отношению к ГС-3 (р<0,05) и ГС-5 (р<0,01). Аналогичная ситуация определена для таких осложнений, как кровотечение из ложа простаты (соответственно 6,2; 5,1 и 1,7%), РПЭГДК (4,3; 2,4 и 0%). Показатели летальности среди пациентов ГС-1 и ГС-3 существенно не различались – 3,5 и 4,5% соответственно (р>0,05), но были статистически значимо ниже, чем в ГС-5 (8,5%, р<0,05).
Сопоставив результаты лечения пациентов ГС-1, ГС-3 и ГС-5 после изолированной АЭ с таковыми лечения пациентов ОГ-1, ОГ-3 и ОГ-5 после СО по местным и общим послеоперационным осложнениям, установлено (см. табл. 1–3), что выполнение СО не привело к увеличению частоты этих осложнений.
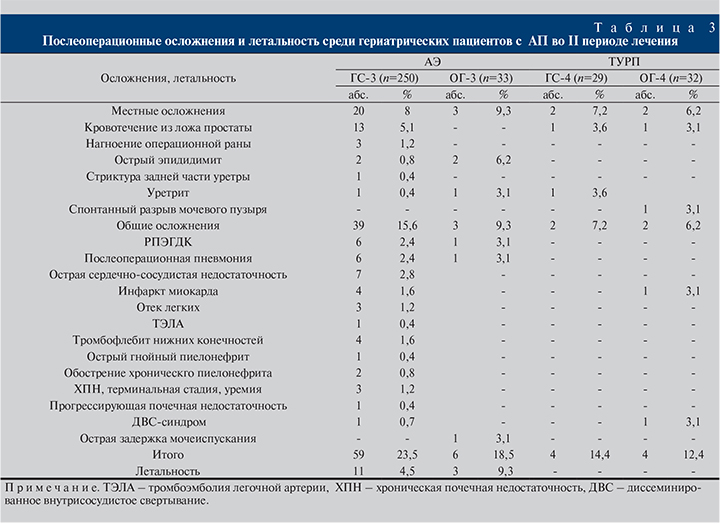
Самые хорошие результаты были получены от больных, которым выполнена изолированная ТУРП или ТУРП в составе СО. У этих пациентов по сравнению с аналогичными группами сравнения в каждом периоде показатели, отражавшие частоту местных и общих послеоперационных осложнений, были статистически значимо ниже, а летальные исходы во II и III периодах отсутствовали. С другой стороны, выполнение СО этим пациентам не сопровождалось повышением уровня этих показателей по отношению к тем, кому выполнена изолированная ТУРП.
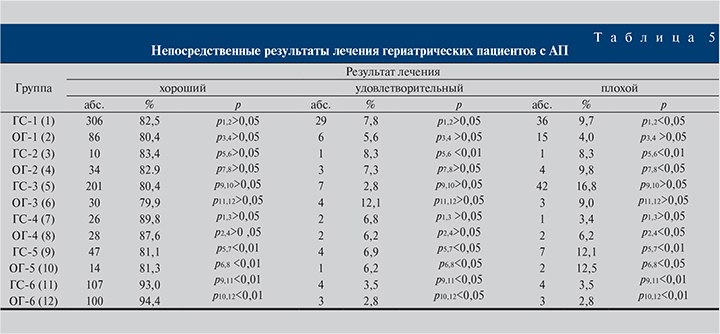
Непосредственные результаты лечения пациентов в группах оценивали в соответствии со следующей градацией: хороший результат – лечение проведено без осложнений, удовлетворительный результат – возникающие осложнения удавалось довольно быстро купировать, а пациента выписывали в удовлетворительном состоянии. К плохим результатам отнесены летальные исходы и тяжелые послеоперационные осложнения (инфаркт миокарда, послеоперационная пневмония и др.).
Анализ непосредственных результатов лечения приведен в табл. 5.
Этот анализ показал, что чаще всего хорошие результаты констатировали во II и III периодах у пациентов, которым выполнена изолированная ТУРП или ТУРП в СО: ГС-4 (89,8%), ОГ-4 (87,6%), ГС-6 (93%), ОГ-6 (94,4%).
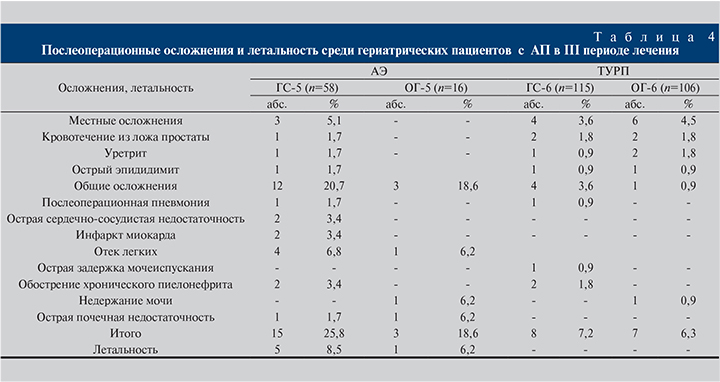
Наиболее высокий процент плохих непосредственных результатов лечения (от 9 до 16,8%) был во всех трех периодах у больных с выполненной АЭ, изолированной или в СО (кроме ОГ-1 – 4%). В то же время лишь у больных ОГ-2 в I периоде, которым выполнена ТУРП в СО, доля плохих результатов составила 9,8%.
Таким образом, в целом можно отметить, что непосредственные результаты лечения оказались значительно лучше у больных, которым выполнена изолированная ТУРП и ТУРП в составе СО, чем у больных, которым произведена изолированная АЭ или АЭ в составе СО.
Обсуждение. Научно-практическое обоснование нашего системного подхода базировалось на результатах сравнительной оценки ранних послеоперационных осложнений, летальности и непосредственных результатах лечения гериатрических пациентов с АП.
В доступной отечественной и зарубежной литературе мы обнаружили лишь единичные сообщения об аналогичном подходе к такой оценке больных АП, но без разграничения на возрастные группы. Причем они посвящены лишь сравнительной оценке результатов лечения изолированной АЭ или ТУРП. С другой стороны, практически отсутствуют сообщения о симультанных вмешательствах у этой категории больных.
В работе [1] представлены сравнительные результаты хирургического лечения больных АП без возрастной дифференциации, которым выполнена изолированная АЭ или ТУРП. Частота послеоперационных осложнений после изолированной АЭ составила 23%, данных о летальности не представлено. У наших пациентов в III периоде общее число послеоперационных осложнений составило 25,8 % (р>0,05), летальность – 8,5%.
После изолированной ТУРП, по данным тех же авторов [1], общее число местных осложнений составило 41,2%. Показатели общих осложнений и летальности также не указаны. В нашем исследовании после изолированной ТУРП число местных осложнений в I периоде составило 8,3% (р<0,01), летальность – 8,3%, во II и III периодах – 3,6% (р<0,01), летальных исходов не было.
В работе В. Е. Марченкова [13] приведен анализ лечения 277 больных пожилого и старческого возраста с АП. Симультанные операции выполнены 75 пациентам. Чреспузырная АЭ проведена в 145 наблюдениях, ТУРП – в 132. Автор не приводит раздельных данных о результатах лечения при изолированных операциях и СО. Общее число ранних послеоперационных местных и общих осложнений после АЭ составило 72%, летальность – 2%, после ТУРП – соответственно 34% (р<0,01) и 0,75% (р<0,01).
Сопоставив эти данные с нашими, следует отметить, что в I периоде у наших пациентов после АЭ частота общих и местных послеоперационных осложнений составила 22,9% (р<0,01), летальность была выше – 8,3% (р<0,05), во II периоде соответствующие показатели составили 23,5 (р<0,01) и 4,5% (р>0,05), в III – 25,8 (р<0,01) и 8,5% (р<0,05).
После изолированной ТУРП у наших пациентов в I периоде частота общих и местных послеоперационных осложнений составила 16,6% (р<0,01), летальность – 8,3% (р<0,05), во II и III периодах общие и местные послеоперационные осложнения диагностировали в 7,2% наблюдений (р<0,01), летальных исходов не было.
Наши данные подтверждают общую закономерность лучших результатов лечения гериатрических пациентов с АП, отмеченную другими исследователями [6–9], при выполнении ТУРП по отношению к АЭ. Полученные данные подтверждают отмеченную другими авторами [6–9] тенденцию достижения лучших результатов при выполнении ТУРП по сравнению с АЭ.
Заключение. Улучшение результатов лечения гериатрических пациентов с АП от I до III периодов произошло за счет разработанного нами нового системного подхода, определяющими положениями которого стали:
- увеличение числа пожилых пациентов с массой АП более 60 г при выполнении как изолированной ТУРП, так и ТУРП в составе СО от I (10,1%) до III периода (74,8%; p<0,01);
- разработанный, а затем усовершенствованный метод прогнозирования риска и профилактики РПЭГДК, позволивший снизить частоту этого тяжелого послеоперационного осложнения с 4,3% (I период) и 2,4% (II период) до 0% в III периоде (p<0,01);
- перевод больных тяжелыми интеркуррентными заболеваниями на несколько суток из урологического отделения в ОРИТ для более эффективной предоперационной подготовки. В I периоде доля таких пациентов составила 3,7%, в III – 8,1% (p<0,05).
- увеличение числа больных с применением спинномозговой анестезии от I периода (19,7%) к III (81,4%) (p<0,01);
- использование разработанного устройства для гемостаза в III периоде (в 1-е сутки после АЭ) в отношении пациентов с ненадежным гемостазом в области ложа предстательной железы, что позволило полностью избежать кровотечения из ложа простаты. В I периоде это осложнение возникло у 6,9% больных, во II – у 4,6%.


