Инфекции мочевыводящих путей (ИМП) представляют собой одну из наиболее актуальных проблем современной медицины. Это связано как с их широкой распространенностью, так и с наличием нерешенных проблем при проведении рациональной антимикробной терапии (АМТ). Данные многочисленных исследований свидетельствуют о широкой распространенности ИПМ среди как амбулаторных, так и госпитализированных пациентов [1–3]. Инфекция мочевыводящих путей – вторая по частоте бактериальная инфекция человека после пневмонии, поражающая население земного шара с момента появления человека [4]. В амбулаторной практике наиболее распространенными формами ИМП являются острый цистит и острый пиелонефрит. Установлено, что один эпизод неосложненной ИМП в течение жизни переносит каждая вторая женщина, при этом у 30% из них заболевание имеет рецидивирующее течение [5, 6]. В США ИМП составляют 0,7±0,1% от числа всех обращений пациентов за амбулаторной помощью. При проведении анкетирования в США установлено, что 10,8% женщин отмечали развитие эпизода ИМП в течение 12 мес, предшествовавших анкетированию [7]. К возрасту 32 лет 50% женщин сообщают о развитии по крайней мере одного эпизода, а в течение жизни 50–70% переносят один эпизод ИМП [4]. В многоцентровом исследовании, включившем молодых (19,2 года) женщин из России, Республики Беларусь, Казахстана, Киргизии, нами были исследованы некоторые показатели распространенности ИМП. Установлено, что клинические проявления, характерные для ИМП, развиваются в течение года у 17,8% опрошенных, в 50,6% случаев ИМП рецидивируют [8].
Среди инфекций, связанных с оказанием медицинской помощи (включая нозокомиальные инфекции), ИМП также занимают лидирующие позиции. Известно, что до 45% всех нозокомиальных инфекций являются ИМП, большинство (около 80%) из них развивается на фоне катетеризации мочевыводящих путей [7, 9–11]. У 2–4% пациентов нозокомиальные ИМП осложняются развитием уросепсиса [11]. В урологических стационарах России, ряда стран Европы и Азии частота нозокомиальных ИМП составляет не менее 11%, при этом наиболее распространенными формами ИМП являются бессимптомная бактериурия (29%), цистит (26%), пиелонефрит (21%) и уросепсис (12%) [12].
На сегодняшний день очевидно, что проблема диагностики и терапии ИМП выходит за рамки одной специальности и ее решение требует совместных усилий ученых, а также клиницистов разных направлений – урологов, терапевтов, акушеров-гинекологов, микробиологов, фармакологов и др. Назначение антибиотиков при ИМП в большинстве случаев является обязательным компонентом терапии. При этом выбор антимикробного препарата (АМП) определяется многими факторами – клинической эффективностью препарата, его переносимостью, безопасностью, стоимостью и др. Однако в настоящее время помимо вышеперечисленных факторов отечественными и зарубежными учеными в качестве одного из наиболее значимых критериев выбора препарата для антибиотикотерапии ИМП рассматривается антибиотикорезистентность предполагаемого или идентифицированного уропатогена [5, 13, 14].
Необходимо подчеркнуть, что при всей кажущейся простоте и наглядности данных по чувствительности уропатогенов их использование для обоснования рациональной АМТ связано с многочисленными нюансами, которые могут существенно исказить их объективную оценку.
В настоящей публикации мы постарались обсудить некоторые сложные моменты использования в клинической практике данных по чувствительности уропатогенов.
Прежде всего важно разделять использование термина «антибиотикорезистентность» применительно к конкретному штамму или к некоей популяции пациентов (исследуемых) – популяционная резистентность. В настоящее время существует несколько методов определения чувствительности микроорганизмов к АМП, которые делятся на две основные группы: диффузионные (диски с антибиотиками, Е-тесты) и методы разведения (разведение в агаре или бульоне) [15]. Наряду с этим сегодня все чаще используют методы амплификации нуклеиновых кислот, позволяющие выявлять у бактерии наличие генов, отвечающих за развитие антибиотикорезистентности, а также аппаратные методы [15].

На основании полученных количественных данных, например значений минимальной подавляющей концентрации (МПК) антибиотика или зоны задержки роста микроорганизма, выделенный штамм может быть отнесен к категориям «чувствительный» (Ч, S), «умеренно резистентный» (У/Р, I) и «резистентный» (Р, R) [16]. Для интерпретации полученных данных и стратификации микроорганизма к одной из перечисленных категорий наиболее часто используются Стандарты Института клинических и лабораторных стандартов США (Clinical and Laboratory Standards Institution – CLSI) [17] или критерии, разработанные Европейским комитетом по определению чувствительности к антибиотикам (European Committee for Antimicrobial Susceptibility Testing – EUCAST) [18].
Следует отметить, что приведенные выше документы, во-первых, регулярно обновляются, в связи с чем даже в отсутствие изменений МПК может изменяться как стратификация штамма в одну из групп (S, или I, или R), так и доля резистентных штаммов в популяции в зависимости от использованных критериев. Например, штамм E. coli с величиной МПК ципрофлоксацина 2 мг/л, согласно критериям EUCAST [18], является резистентным, в то же время, согласно критериям CLSI [17], он относится к категории «чувствительный». Таким образом, стратификация штамма S-I-R по степени чувствительности к АМП является в определенной мере условной и зависит от выбранной системы координат – критериев интерпретации и методики определения чувствительности. Эта особенность стратификации штаммов довольно наглядно отображена в исследовании P. D. Tamma и соавт. [19]. Так, в учреждениях, использовавших «старые» критерии CLSI (действовали до 2011 г.), доля штаммов E. coli, чувствительных к цефазолину, достигала 90% (S≤8 мкг/мл), тогда как в учреждениях, которые придерживались «новых» критериев (действовали после 2011 г.) (S≤2 мкг/мл), к категории «чувствительные» были отнесены лишь 47% штаммов E. coli (табл. 1).
Помимо различий, присутствующих в современных стандартах по оценке результатов определения чувствительности (критериев интерпретации), существует еще одна важная проблема. Так, до настоящего момента не решен вопрос о клинической значимости стратификации штамма в одну из категорий – S, I, R. Типичным заблуждением многих клиницистов является оценка клинической ситуации при выделении резистентного штамма как гарантированной неэффективности применения АМП. Такая оценка результатов определения чувствительности микроорганизмов in vitro выявлена нами при проведении анкетирования клиницистов. На вопрос: по вашему мнению, насколько снижается эффективность антибиотика, если инфекция вызвана резистентным к нему микроорганизмом, большинство врачей дали ответ – на 90%. Таким образом, большинство практических врачей ставят знак равенства между резистентностью штамма in vitro и клинической неэффективностью АМП, что далеко не всегда верно.

Изучение чувствительности микроорганизмов in vitro является крайне упрощенной моделью инфекционного процесса, происходящего в организме человека. Основной целью использования подобной модели служит прогнозирование клинической эффективности антимикробной терапии. В настоящее время очевидно несовершенство данной модели, обусловленной значительным количеством факторов, некоторые из которых перечислены в табл. 2 [20–22].
С практической точки зрения очень важно знать: какова вероятность достижения клинического успеха или неэффективности АМТ при назначении того или иного АМП при разных значениях чувствительности штамма in vitro? Однако в подавляющем большинстве случаев такая информация отсутствует. В последние годы эту проблему пытается устранить упомянутый выше комитет EUCAST, используя при разработке критериев интерпретации чувствительности микроорганизмов методы, основанные на оценке фармакодинамики и фармакокинетики (PK/PD) АМП, – так называемые клинические пограничные значения (сlinical breakpoints) [23]. Однако даже в этом случае верификация корреляции между клиническими исходами и данными о чувствительности штамма in vitro выполняется далеко не всегда.
Почему же данные о чувствительности штамма к антибиотику in vitro не всегда коррелируют с результатами лечения? Этот факт объясняется тем, что критерии интерпретации чувствительности для представителей семейства Enterobacteriaceae (наиболее частые возбудители ИМП) к антибиотикам, разработанные CLSI, ориентированы прежде всего на лечение системных инфекций (сепсис, бактериемия) [17]. Таким образом, критерии оценки МПК штамма и его отнесение к категории «резистентный» или «чувствительный» основываются в основном на сывороточных концентрациях препарата. Исключения здесь составляют «уросептики», прежде всего нитрофурантоин и фосфомицин, которые используются практически только для терапии цистита и бактериурии. В то же время многие антибиотики, например цефалоспорины, создают в моче концентрации, в десятки и сотни раз превышающие сывороточные, что может объяснять эффективность указанных антибиотиков даже при резистентности штамма in vitro. Более точным прогностическим показателем эффективности фторхинолонов в отношении грамотрицательных возбудителей является соотношение максимальной концентрации антибиотика к минимальной подавляющей концентрации (Cmax/МПК). Высокий уровень эффективности отмечается при показателе, превышающем 10 [24]. Для β-лактамов используется показатель T>МПК (время, в течение которого концентрация антибиотика превышает МПК возбудителя), при этом при лечении неосложненных ИМП суммарный показатель T>МПК, превышающий 30 ч в течение курса приема препарата, обеспечивает микробиологическую эффективность терапии 80–90% [25].
Следует отметить, что за последние 2–3 года и CLSI, и EUCAST были разработаны отдельные критерии для интерпретации чувствительности уропатогенов, выделенных от пациентов с неосложненными ИМП, к некоторым АМП. Так, в октябре 2013 г. EUCAST опубликовали пересмотренные критерии для амоксициллина/клавуланата, согласно которым представители семейства Enterobacteriaceae относятся к категории «чувствительные», если МПК антибиотика ≤32 мг/л [26]. При этом в случае системных инфекций, вызванных представителями Enterobacteriaceae, критерии для амоксициллина/клавуланата остались прежними – чувствительными считаются штаммы с МПК ≤8 мг/л [26].
Необходимость пересмотра критериев EUCAST для неосложненных ИМП была обусловлена рядом факторов. Во-первых, амоксициллин/клавуланат создает высокие концентрации в моче. Так, концентрация амоксициллина в моче после приема препарата в дозе 500 мг достигает 1100 мг/л, при этом клавулановая кислота на 30% выводится в неизменном виде и ее средняя концентрация в течение 4 ч после приема поддерживается на уровне 400 мг/л [26]. Таким образом, концентрации амоксициллина/клавуланата, создаваемые в моче, превышают сывороточные в несколько раз. Наряду с этим в исследованиях на животных было показано, что предиктором эффективности большинства β-лактамов при неосложненных ИМП является концентрация антибиотика в моче, а не в плазме крови или паренхиме почек [26]. Во-вторых, результаты клинических исследований свидетельствуют о том, что высокая клиническая эффективность амоксициллина/клавуланата при лечении ИМП наблюдалась в случаях, когда МПК антибиотика для уропатогенов не превышала 32 мг/л [27, 28]. Следует отметить, что при использовании обновленных критериев доля чувствительных к амоксициллину/клавуланату штаммов E. coli, выделенных от пациентов с неосложненными ИМП в Европе (более 56 тыс. штаммов), возросла с 79,6 до 97,4% [26].
Однако далеко не во всех микробиологических исследованиях последних лет учитывается необходимость использовать отдельные критерии интерпретации для штаммов, вызывающих неосложненные ИМП. Это может приводить к заниженной оценке активности амоксициллина/клавуланата и цефалоспоринов.
Критерии CLSI были обновлены несколько позднее – в 2014 г. Нововведением стало использование данных по чувствительности уропатогенов семейства Enterobacteriaceae, полученных от пациентов с неосложненными ИМП, к цефазолину в качестве предиктора чувствительности к пероральным цефалоспоринам [29]. В соответствии с данными критериями штаммы уропатогенов чувствительны, если МПК цефазолина для них не превышает 16 мг/л [29].
В классическом определении резистентной бактерии сказано, что при лечении инфекций, вызванных резистентными бактериями, даже применение максимальных доз антибиотика не дает эффекта [15]. Однако сейчас накоплены данные, которые свидетельствует о том, что при лечении инфекций, вызванных устойчивыми in vitro штаммами (здесь и далее по тексту речь идет о приобретенной устойчивости), клиническая эффективность терапии может снижаться, но вовсе не до нуля, наряду с этим в ситуации, когда инфекция вызвана чувствительным штаммом, клиническая эффективность лечения не всегда достигает 100% [22, 30, 31].
Это утверждение наглядно иллюстрируется эмпирическим правилом, которое получило название «90–60». Согласно этому правилу, если инфекция вызвана чувствительным in vitro штаммом, вероятность достижения клинического успеха составляет ~90%, в случае резистентного изолята эффективность снижается до ~60% [31].
Нередко при анализе назначений АМТ можно столкнуться с другой крайностью в оценке микробиологических данных – полным игнорированием данных по чувствительности микроорганизмов in vitro при выборе антибиотика. Такие ошибки при выборе АМТ базируются на ошибочном мнении, будто резистентность микроорганизма in vitro не влияет на эффективность АМТ. На сегодняшний день понятно, что такая корреляция существует, но степень этого влияния зависит от конкретного АМП, локализации и тяжести инфекции, используемых критериев интерпретации чувствительности и других факторов [30].
Одним из первых препаратов, для которых была установлена количественная связь между резистентностью уропатогенов in vitro и клинической неэффективностью АМТ, явился ко-тримоксазол. Показано, что применение ко-тримоксазола пациентами с внебольничными ИМП, вызванными ко-тримоксазолрезистентными уропатогенами, клиническая эффективность терапии снижается до 50% [32], а частота эрадикации возбудителя уменьшается в 1,81 раза по сравнению с ИМП, вызванными чувствительными штаммами [33]. Следует отметить, что данная закономерность правомочна только для ко-тримоксазола и переносить ее на другие АМП и другие нозологии необоснованно.
Менее выраженное влияние резистентности на эффективность терапии ИМП было продемонстрировано для фторхинолонов. В работе [34] установлено, что при лечении ОЦ клиническая эффективность 3-дневного курса гатифлоксацина в дозировке 200 мг 1 раз в сутки внутрь при наличии у возбудителя устойчивости in vitro была довольно высокой – 75%, в случае чувствительного штамма клиническая эффективность терапии составляла 94,7%.
 Можно привести и противоположный пример, когда данные по чувствительности антимикробного препарата in vitro нередко приводят к переоценке его ожидаемой клинической эффективности. Весьма показательна история изучения и применения препарата фосфомицин при ИМП. Этот антибиотик был разработан в Испании в 1969 г. Первые исследования, проведенные до середины 1970-х гг. по изучению активности препарата в отношении грамотрицательных бактерий, установили умеренную активность фосфомицина в отношении основных уропатогенов, в основном E. coli (МПК90 – 32–64 мкг/мл), а частота выделения при ИМП резистентных штаммов E. coli достигала 10–12% [35, 36]. «Поворотным моментом» в истории изучения фосфомицина стало наблюдение, показывающее, что добавление глюкозо-6-фосфата (Г6Ф) в питательную среду или в состав диска для определения чувствительности приводит к снижению МПК фосфомицина (т.е. повышения его активности in vitro) в несколько десятков раз. Например, для штаммов E. coli снижение МПК фосфомицина отмечено в 16–64 раза [35, 37]. Не совсем понятно, по какой причине с начала 1980-х гг. использование Г6Ф является стандартом при определении чувствительности к фосфомицину in vitro, хотя никакого обоснования данная рекомендация не получила [38].
Можно привести и противоположный пример, когда данные по чувствительности антимикробного препарата in vitro нередко приводят к переоценке его ожидаемой клинической эффективности. Весьма показательна история изучения и применения препарата фосфомицин при ИМП. Этот антибиотик был разработан в Испании в 1969 г. Первые исследования, проведенные до середины 1970-х гг. по изучению активности препарата в отношении грамотрицательных бактерий, установили умеренную активность фосфомицина в отношении основных уропатогенов, в основном E. coli (МПК90 – 32–64 мкг/мл), а частота выделения при ИМП резистентных штаммов E. coli достигала 10–12% [35, 36]. «Поворотным моментом» в истории изучения фосфомицина стало наблюдение, показывающее, что добавление глюкозо-6-фосфата (Г6Ф) в питательную среду или в состав диска для определения чувствительности приводит к снижению МПК фосфомицина (т.е. повышения его активности in vitro) в несколько десятков раз. Например, для штаммов E. coli снижение МПК фосфомицина отмечено в 16–64 раза [35, 37]. Не совсем понятно, по какой причине с начала 1980-х гг. использование Г6Ф является стандартом при определении чувствительности к фосфомицину in vitro, хотя никакого обоснования данная рекомендация не получила [38].
Известно, что глюкоза, поступающая в клетки органов и тканей, фосфорилируется с использованием АТФ, превращаясь в Г6Ф. Фосфорилирование глюкозы – практически необратимая реакция, образование Г6Ф в клетке – это своеобразная «ловушка» для глюкозы, так как мембрана клетки не проницаема для фосфорилированной глюкозы. Таким образом, Г6Ф находится только в цитозоле клеток, а в сыворотке может появляться в следовых концентрациях на короткий срок и быстро разрушается [37, 39]. Исходя из оценки объема распределения фосфомицина, который составляет 0,1–0,15 л/кг, можно сделать вывод, согласно которому препарат в клетки практически не поступает [40, 41]. Этот вывод подтверждается низкой активностью фосфомицина в отношении внутриклеточно расположенных возбудителей [41]. Таким образом, нет никаких теоретических предпосылок для определения чувствительности бактерий к фосфомицину с добавлением Г6Ф.
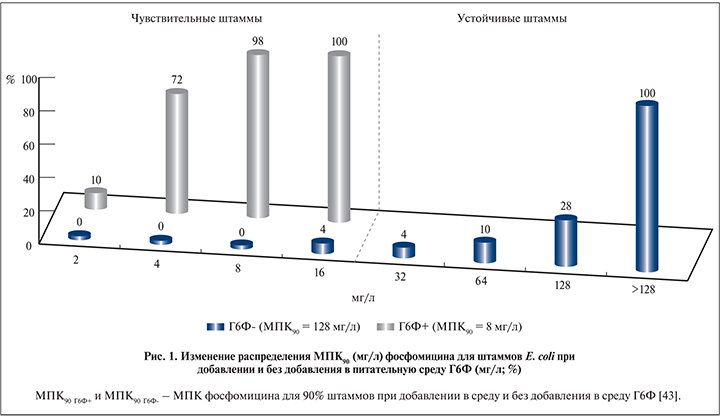
Подтверждением неадекватности использования Г6Ф при определении чувствительности бактерий к фосфомицину является тот факт, что в исследованиях, в которых вместо питательной среды с Г6Ф используются биологические жидкости, например моча или спинномозговая жидкость, чувствительность микроорганизмов к фосфомицину снижается в 8–16 раз, т.е. по сути соответствует цифрам, которые получаются в случае определения чувствительности без использования Г6Ф [42] (рис. 1). Определение чувствительности с использованием мочи, а не питательной среды приводит к повышению МПК90 фосфомицина, т.е. снижению чувствительности в 13 раз! Для E. coli c 12,3 мг/л до >162 мг/л, а для Klebsiella spp. в 3 раза – c 46,5 мг/л до >162 мг/л.
Крайне важно, что описанные выше особенности определения чувствительности фосфомицина in vitro имеют непосредственное значение для клинической практики, прежде всего потому, что, по данным текущих микробиологических исследований, резистентность к фосфомицину низкая – от 0 до 2% [44]. В то же время клиническая эффективность фосфомицина не превышает 80% и уступает таковой ко-тримоксазола, ципрофлоксацина, нитрофурантоина [45–47].
Под термином «популяционная резистентность» в настоящее время понимают долю резистентных штаммов, выделенных при исследовании той или иной популяции. Данные популяционной резистентности публикуются после проведения эпидемиологических микробиологических исследований и широко используются при разработке клинических рекомендаций в качестве критерия выбора АМП [5]. Для этого данные популяционной резистентности сравнивают с так называемыми отсекающими значениями (cut-off). Например, рекомендуется использовать фторхинолоны, нитрофураны и фосфомицин в качестве препаратов выбора при уровне резистентности E. coli к ко-тримоксазолу, превышающем 20% [5, 48]. При этом фторхинолоны не рекомендуется использовать для эмпирической терапии ИМП, если уровень резистентности к ним в популяции превышает 10% [5].
Следует учитывать, что популяционная резистентность – это показатель, который изменяется со временем, с одной стороны, и является характерным для определенной популяции и/или территории, с другой. Это создает существенные сложности при выборе рациональной антимикробной терапии (АМТ), так как требует от клинициста постоянного мониторинга состояния чувствительности основных уропатогенов. Причем использование устарелых данных или данных других регионов может приводить к серьезным ошибкам. Например, еще относительно недавно наблюдался довольно низкий уровень популяционной резистентности уропатогенной E. coli к ко-тримоксазолу и данный антибиотик рассматривался в качестве препарата выбора для эмпирической терапии ИМП во многих странах мира. Однако в настоящее время в большинстве стран уровень резистентности уропатогенов к нему превышает 20%, что, согласно современным рекомендациям по лечению ИМП, не позволяет использовать его для эмпирической антибиотикотерапии данных инфекций [5, 49–51].
Наряду с ко-тримоксазолом в последние 5–10 лет наблюдается значительный рост уровня антибиотикорезистентности E. coli и к фторхинолонам, которые до середины прошлого десятилетия являлись «золотым» стандартом в лечении ИМП. Так, в России, по данным исследований UTIAP-I и UTIAP-II (2004), к фторхинолонам были чувствительны более 95% штаммов уропатогенной E. coli [52]. По прошествии 8 лет были опубликованы результаты многоцентрового исследования ДАРМИС, согласно которым средняя частота выделения фторхинолонрезистентной E. coli, полученной от взрослых пациентов с внебольничными ИМП, в России достигает 20% [51]. Высокий уровень резистентности уропатогенной E. coli, выделенной от пациентов с внебольничными ИМП (более 26%), к фторхинолонам был подтвержден в исследовании О. Ю. Филимоновой и соавт. [53]. Аналогичная ситуация с ростом резистентности уропатогенов к фторхинолонам наблюдается в США, странах Европы и Азии [54–57].
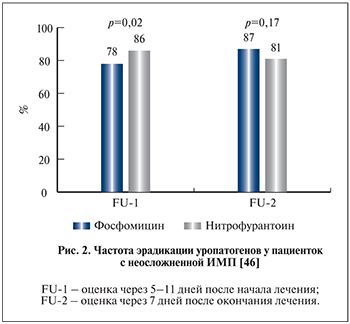
Еще одной потенциальной ошибкой, связанной с некорректным использованием данных популяционной резистентности, является использование этого показателя для сравнения эффективности нескольких АМП. При этом ошибочно предполагается, что если показатели популяционной резистентности АМП ниже, то его ожидаемая клиническая и/или микробиологическая эффективность будет выше. Это предположение справедливо далеко не во всех случаях. Например, в многоцентровом плацебо-контролируемом исследовании [46] сравнивалась эффективность фосфомицина 3 г однократно внутрь и 7-дневного курса нитрофурантоина у женщин с неосложненной ИМП. Было установлено, что уропатогены, выделенные до начала лечения, в 94% случаев были чувствительны к фосфомицину, а в 83% – к нитрофурантоину. Несмотря на это, микробиологическая эффективность фосфомицина через 5–11 дней после начала лечения была статистически значимо ниже, чем у нитрофурантоина (рис. 2).
Еще один пример ограниченной возможности использования показателя популяционной резистентности был получен при сравнении эффективности левофлоксацина и дорипенема у пациентов с осложненными ИМП.
В ходе исследования были установлены уровни популяционной резистентности E. coli для дорипенема и левофлоксацина, которые составили 0 и 10,5% соответственно.
В то же время клиническая эффективность сравниваемых препаратов не различалась, а для подгруппы пациентов с острым пиелонефритом левофлоксацин оказался более эффективным [58].
Помимо отсутствия достаточного количества данных, показывающих наличие взаимосвязи между уровнем популяционной резистентности и клинической эффективностью для многих классов АМП (например, фторхинолоны, β-лактамы, нитрофурантоин, фосфомицин и т.д.), также необходимо учитывать и тот факт, что одни и те же данные по чувствительности уропатогенов могут быть интерпретированы по-разному, в связи с чем уровень популяционной резистентности может варьироваться в широких пределах. С этой точки зрения довольно интересны данные, которые приводятся в работе ученых из Турции, опубликованной в 2015 г. [59]. В своей работе они использовали 298 штаммов E. coli, полученных от пациентов с неосложненными ИМП. Чувствительность выделенных штаммов к АМП определялась дискодиффузионным методом, для интерпретации полученных результатов использовали критерии CLSI (2014) и EUCAST (2014). Необходимо отметить, что полное совпадение полученных результатов было выявлено лишь для амикацина (100% чувствительных штаммов) и ко-тримоксазола (63,09% чувствительных штаммов). Наряду с этим для ряда препаратов были обнаружены статистически значимые различия в уровне популяционной резистентности. Так, согласно стандартам CLSI, к гентамицину, цефуроксиму аксетилу и левофлоксацину были чувствительны 91,95, 20,13 и 73,83% выделенных штаммов соответственно, тогда как при использовании критериев EUCAST доля чувствительных к данным АМП штаммов составляла 84,56; 77,18 и 67,11% соответственно. Таким образом, в зависимости от выбранных критериев различия в уровне популяционной резистентности могут достигать 50% и более [59].
В связи со сказанным выше уровень популяционной резистентности, несмотря на свою популярность и кажущуюся простоту интерпретации, должен использоваться крайне аккуратно.
Инфекция мочевыводящих путей – одна из наиболее распространенных форм инфекций и одна из самых частых причин назначения АМП как в амбулаторной практике, так и в стационаре. На сегодняшний день во всем мире антибиотикорезистентность уропатогенов рассматривается в качестве одного из основных критериев выбора АМП. Однако использование данных по чувствительности уропатогенов при выборе АМТ требует взвешенного подхода и сопоставления микробиологических, клинических данных, особенностей фармакодинамики и фармакокинетики АМП.
Сложности в клинической оценке данных чувствительности микроорганизмов заключаются прежде всего в том, что до сих пор степень корреляции данных in vitro с клинической эффективностью терапии ИМП установлена только для отдельных АМП. Было показано, что ряд препаратов сохраняет эффективность при лечении неосложненных ИМП даже при устойчивости к ним штамма in vitro, другие же АМП, такие как фосфомицин, могут быть недостаточно эффективными при практически 100%-ной активности препарата in vitro.
Эти особенности могут быть объяснены как несовершенством критериев интерпретации чувствительности, так и особенностями фармакокинетики и фармакодинамики самих препаратов.



