Введение. Экстракорпоральные и эндоскопические методики в лечении нефролитиаза детально разработаны и высокоэффективны. При камнях размером до 10–15 мм, как правило, выполняют дистанционную литотрипсию (ДЛТ) (дискутабельное исключение – камни нижней группы чашечек) [1–3]. При камнях размером более 15–20 мм предпочтительным считаются чрескожная нефролитотрипсия (ЧНЛТ) и ее разновидности [4, 5]. Интенсивно развивается ретроградная интраренальная хирургия, в том числе с использованием гибкого эндоскопического инструментария (возможности методики существенно лимитированы при камнях, превышающих 15–20 мм) [6–8].
Тем не менее существуют клинические ситуации, когда, казалось бы, забытая уже пиелолитотомия оказывается менее травматичной, опасной и более эффективной. В основном это предположение относится к больным с «гигантскими» камнями внепочечных лоханок, аномалиями развития почек (что затрудняет чрескожный доступ) [9–11], а также к пациентам с высоким риском септических осложнений традиционной ЧНЛТ. Поскольку открытая хирургия нефролитиаза в ведущих центрах индустриально развитых стран становится исключением, речь идет о лапароскопическом доступе [12]. Лапароскопическая пиелолитотомия может быть успешно дополнена трансабдоминальной гибкой пиелокаликоскопией, что при отработанной хирургической технике и по мере накопления опыта позволяет добиваться крайне высоких показателей «stone-free» [13, 14].

Цель исследования: определить место лапароскопической пиелолитотомии в структуре методов хирургического лечения нефролитиаза.
Материалы и методы. Проанализировано 16 лапароскопических пиелолитотомий, выполненных в клинике за последние несколько лет. Возраст пациентов варьировался от 39 до 72 лет (средний возраст – 51±8 лет). Средняя плотность камней составила 1012 (160–1483) HU.
Показаниями к лапароскопическому доступу являлись следующие:
1. Крупные и коралловидные камни аномалийных почек (n=8); подковообразная почка (n=6), поясничная и тазовая дистопия (по 1). Выбор обосновывали сравнительной доступностью технологии, удобным внеорганным, фронтальным расположением лоханки, а также особенностями строения чашечно-лоханочной системы (ЧЛС), затрудняющими полноценную чрескожную нефроскопию.
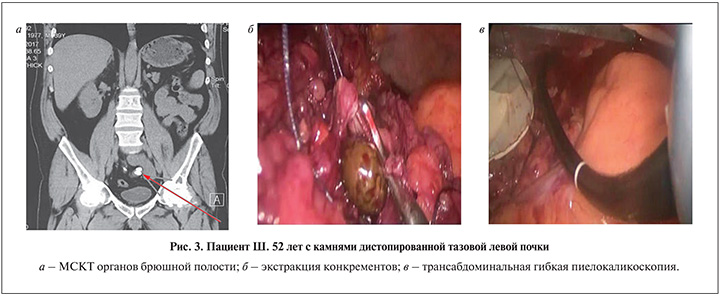
В 2 наблюдениях единичные камни объемом 20 и 25 см³ локализовывались в лоханках. В 6 наблюдениях камни были крупные коралловидные и множественные (рис. 1–3).
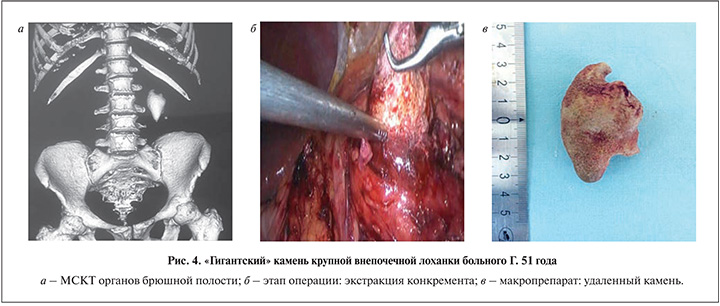
2. «Гигантские» (более 30–40 см³) монолитные камни крупных внепочечных лоханок (n=3). Выбор обосновывали сравнительной оперативностью пособия и снижением рисков длительной интраренальной чрескожной эндоскопии. Размеры камней составляли от 5×3×3,5 до 11×4,5×4,8 см (рис. 4);
 3. Множественные камни ЧЛС, суммарный объем которых (≥ 40 см³) не позволял производить чрескожное пособие в «условно» рекомендованные временные интервалы (n=2). Камни размером от 3 мм до 3 см локализовывались во всех отделах ЧЛС.
3. Множественные камни ЧЛС, суммарный объем которых (≥ 40 см³) не позволял производить чрескожное пособие в «условно» рекомендованные временные интервалы (n=2). Камни размером от 3 мм до 3 см локализовывались во всех отделах ЧЛС.
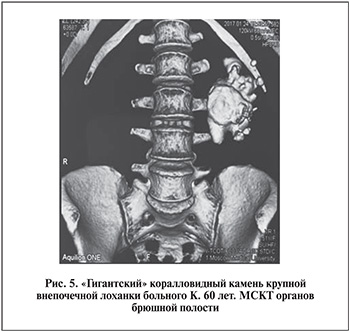
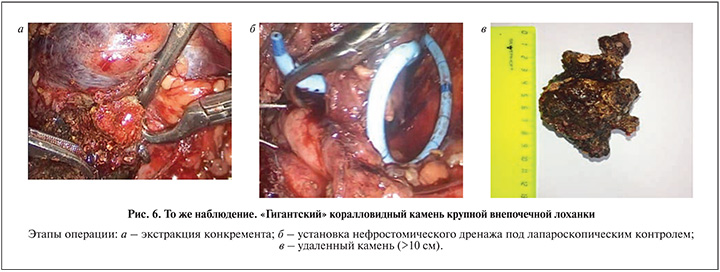
4. Крупные рецидивные (после ЧНЛТ) камни почек у больных с риском бактериотоксических осложнений чрескожной нефроскопии (n=3). Выбор был продиктован особенностью течения нефролитиаза: инфицированные камни, упорное течение пиелонефрита, стойкая бактериурия, гнойно-септические осложнения чрескожных вмешательств в анамнезе (рис. 5 и 6).
Помимо традиционных диагностических процедур большинству пациентов выполнили мультиспиральную компьютерную томографию (МСКТ) с контрастом до и через 30–180 дней после операции (исключение – больной с тазовой дистопией почки ввиду наличия аллергии к йодсодержащим контрастным препаратам). Пациентам с коралловидными камнями и аномалийными почками МСКТ дополняли разработанным в нашей клинике 3D-моделированием патологического процесса.
Особенности пособий. В 15 наблюдениях осуществлен традиционный лапароскопический доступ к почке и верхним мочевым путям (ВМП) с мобилизацией восходящего/нисходящего (в зависимости от стороны операции) отдела толстого кишечника по линии Тольда. Одному больному операцию выполнили трансмезентериально.
Пиелотомию осуществляли по передней поверхности. Разрез предполагал косое или U-образное направление, преследуя цель создать максимально масштабный доступ к полостям и камням ЧЛС без ущерба для последующего восстановления уродинамики. Видимые через разрез лоханки конкременты удаляли атравматическими лапароскопическими экстракторами и помещали в контейнер-эвакуатор. При необходимости выполняли контрольную трансабдоминальную гибкую пиелокаликоскопию. Для этого по одному из 10 мм троакаров в брюшную полость проводили гибкий нефроскоп, который через разрез лоханки под эндоскопическим контролем заводили в ЧЛС и выполняли ревизию лоханки и всех групп чашечек. В качестве вещества, расправляющего стенки ЧЛС, использовали газ (CO2) или физиологический раствор, а также их комбинации. Для выполнения газовой пиелокаликоскопии CO2, который первоначально использовали для создания пневмоперетонеума, подавали через ирригационный канал гибкого эндоскопа. Данный этап операции требовал синхронной работы хирургов, а также наличия лапароскопической и эндоурологической стоек (рис. 7).
Экстракцию конкрементов выполняли при помощи специальных чашечковых корзинок-экстракторов.
Эндоскопическую ревизию ЧЛС завершали антеградным стентированием ВМП (n=15). У пациента с тазовой дистопией почки стент установили ретроградно до операции (n=1). У одной больной с выявленными в ходе операции некротическими изменениями ЧЛС на фоне длительного нахождения гигантского камня мы осуществили комбинированное дренирование ВМП (стент+нефростома). В 13 наблюдениях размер стента составил 8 Ch, в 3–7 Ch. Рану лоханки ушивали непрерывным швом викрила 4-0 и 5-0.
 Фасцию Герота восстанавливали непрерывным герметичным швом с применением нити с однонаправленными насечками с предварительным дренированием паранефрального клетчаточного пространства активным дренажом. Дополнительный дренаж устанавливали в брюшную полость к зоне вмешательства.
Фасцию Герота восстанавливали непрерывным герметичным швом с применением нити с однонаправленными насечками с предварительным дренированием паранефрального клетчаточного пространства активным дренажом. Дополнительный дренаж устанавливали в брюшную полость к зоне вмешательства.
Среднее время лапароскопической пиелолитотомии составило 137 (96–255) мин, гибкой трансабдоминальной пиелокаликоскопии – 31,2 (12–110) мин.
Стент удаляли на 25–40-е сутки после операции. Из осложнений отмечена тампонада ЧЛС и большая паранефральная гематома у больной после удаления «гигантского» камня лоханки, что потребовало установки чрескожной пункционной нефростомии (ЧПНС) и консервативного гемостатического лечения. Ни в одном наблюдении активизации воспалительного процесса не отмечено. Дооперационный койко-день составил 1 день, послеоперационный – от 2 до 18 (в среднем 6).
Результаты. Все лапароскопические пиелолитотомии протекали без конверсий. Существенная длительность операций (более 3–4 часов) у некоторых больных обусловлена комплексом причин. Основное время занимала гибкая нефроскопия у пациентов со «сложным» древовидным строением чашечно-лоханочных систем и у больных с аномальными почками. Частые атаки пиелонефрита у больных с крупными конкрементами сопровождались значительным «пендукулитом», периуретеритом и продуктивным паранефритом. Это также затрудняло и удлиняло время мобилизации мочевых путей. Большая длительность операций отмечена на этапе освоения методики. Сокращению длительности хирургического вмешательства с накоплением опыта способствовало наличие двух дублирующих эндоскопических стоек, необходимого арсенала гибких чашечковых экстракторов различного размера. Гибкая трансабдоминальная пиелокаликоскопия является сравнительно сложной прецизионной манипуляцией с длительной кривой обучения, необходимой для хорошего объемного восприятия эндоскопической картины ЧЛС.
Более рациональному планированию этапа гибкой нефроскопии способствуют выполнение до операции и проанализированное 3D-моделирование ЧЛС с находящимися внутри конкрементами. С накоплением опыта и оптимизацией синхронной работы хирургической бригады двумя эндоскопами манипуляция становится вполне доступной и высокоэффективной.
Современное инструментальное сопровождение лапароскопических операций по поводу камней почек позволяет добиваться высокой эффективности этих пособий. Показатель «stone free» в нашем исследовании составил 87%. Резидуальные, клинически незначимые камни выявлены у 2 (13%) больных с коралловидными конкрементами подковообразных почек и сложными чашечно-лоханочными системами. Добиться 100%-ного результата с накоплением достаточного хирургического опыта, по всей видимости, возможно при наличии С-дуги с возможностями полипозиционной съемки в пределах лапароскопической операционной.
Лапароскопическая пиелолитотомия обладает довольно низкой морбидностью, не сопровождается рисками геморрагических осложнений. Интраоперационная кровопотеря не превышала 50–100 мл.
Результаты контрольных УЗИ и МСКТ через 3 мес после операции свидетельствовали о восстановлении или существенном улучшении уродинамики ВМП, что заключалось в восстановлении проходимости лоханочно- мочеточникового сегмента и верхней трети мочеточника, а также в сокращении и уменьшении в размерах не только лоханки после удаления из нее крупных конкрементов, но и чашечек.
К 3-му месяцу после операции существенно снижалась степень бактериурии и лейкоцитурии. Наблюдение за пациентами продолжается.
Обсуждение. Коллектив нашей клиники обладает разносторонним богатым опытом хирургического лечения нефролитиаза. Методика ЧНЛТ обладает хорошими результатами, небольшим количеством осложнений и возможностями неоднократного повторения, что безусловно характеризует ее как приоритетную при удалении камней почек. Тем не менее наш опыт лапароскопической хирургии нефролитиаза свидетельствует о том, что методика не только имеет право на существование, но и по достоинству займет определенную нишу в лечении больных мочекаменной болезнью в ближайшее время.
Лапароскопическую пиелолитотомию, дополненную трансабдоминальной гибкой пиелокаликоскопией, считаем возможным рекомендовать для хирургического лечения больных с «гигантскими» множественными и инфицированными камнями почек, длительность чрескожного удаления которых выходит за рекомендованные временные интервалы и сопровождается повышенным риском гнойно-септических осложнений. Кроме того, лапароскопический доступ вполне приемлем для больных мочекаменной болезнью с указанными выше аномалиями развития почек.
Из недостатков лапароскопического доступа следует отметить: 1) возможность его использования, как правило, исключительно при экстраренально расположенных лоханках; 2) высокую техническую сложность и необходимость дублирующих эндоскопических стоек при сочетании с гибкой трансабдоминальной пиелокаликоскопией; 3) сравнительную сложность или невозможность повторных трансабдоминальных вмешательств при рецидивирующем нефролитиазе.
Заключение. Лапароскопическая пиелолитотомия является прекрасным дополнением современного арсенала хирургических методик при лечении больных нефролитиазом. Метод характеризуется высоким показателем «stone free», низкой частотой осложнений. Начиная развивать лапароскопическую хирургию нефролитиаза, необходимо оснастить операционную гибкими эндоскопами, что позволит оказывать эффективную квалифицированную помощь больным практически вне зависимости от локализации конкрементов и строения ЧЛС.



