Введение. Хронический абактериальный простатит с воспалительным компонентом (ХАПВК) – одно из наиболее распространенных и упорно рецидивирующих заболеваний органов мочеполовой системы. Несмотря на многочисленные исследования, посвященные его этиологии, диагностике и лечению, добиться снижения заболеваемости ХАПВК пока не удается [1]. Переохлаждения, персистирование инфекции, снижение физической активности, психосексуальные дисгармонии и дизритмии в половой жизни, ведущие к нарушению прокреативных и рекреативных функций мужчины, обусловливают частые обострения ХАПВК [2]. Длительное течение ХАПВК, как правило, сопровождается нарушением внутрисемейных отношений, что еще больше осложняет проявления заболевания и приводит к психологической инвалидизации мужчины [3]. Социально-экономический урон обществу от увеличения заболеваемости ХАПВК не вызывает сомнений.
В работах российских [4, 5] и зарубежных [6, 7] ученых показано, что частота ХАПВК может достигать 30% у мужчин молодого возраста, а доля таких пациентов занимать до 20% общего амбулаторного приема уролога [8, 9]. Тем не менее эти цифры не всегда отражают истинное положение вещей, так как при вскрытии трупов мужчин, погибших от случайных причин, даже в молодом возрасте выявляются изменения в простате, характерные для хронического воспаления [10, 11].
Многообразие субъективных и объективных симптомов, обусловленных воспалением простаты, затрудняет диагностику, а общепринятые клинические и лабораторные методы не всегда позволяют подтвердить наличие воспалительного процесса в органе [12]. По-прежнему дискутируется вопрос об инфекционных агентах, поражающих простату и ведущих к хроническому простатиту, и их роли в детерминации воспалительного процесса [13]. Хронический абактериальный простатит характеризуется длительным течением с периодами ремиссий и обострений, приводящих при неквалифицированном лечении к ухудшению функции простаты. Бесконтрольное применение антибиотиков способствует повышению резистентности патогенных микроорганизмов и создает значительные трудности в этиотропном лечении. Традиционные методы терапии без учета этиологии и патогенеза ХАПВК не обеспечивают существенного и стойкого улучшения состояния больных, что, несомненно, требует поиска новых способов диагностики и лечения [14]. В свете последнего приказа Правительства РФ № 1673н от 29.12.2012, направленного на диагностику, лечение и профилактику хронического простатита, утверждается стандарт первичной медико-санитарной помощи, чтобы заболеваемость хроническим простатитом из чисто медицинской не трансформировалась в глубоко социальную проблему.

Цель настоящего исследования – изучить течение ХАПВК у молодых мужчин на фоне комплексного лечения с применением общей и локальной озонотерапии. Представленная работа является первым этапом нашего исследования ХАПВК. На втором этапе, результаты которого будут представлены в следующей статье, мы проанализируем индивидуально-типологические особенности течения заболевания на фоне лечения в зависимости от соматического типа молодых мужчин.
Материалы и методы. Объектом исследования были 306 мужчин-европеоидов первого периода зрелого возраста, страдавших ХАПВК. Использование схемы возрастной периодизации было выбрано не случайно, так как в соответствии с современными представлениями о физиологии репродуктивной системы мужчины простата окончательно формируется к 20–22 годам, а к 35–37 годам уже прослеживается тенденция к пролиферации и физиологической инволюции ее ткани [15].
Все мужчины находились на стационарном или амбулаторном лечении в андрологическом отделении Городской клинической больницы №4 Красноярска. Комплексная диагностическая программа включила сбор анамнеза, клинических данных; анализ 4-стаканной пробы Meares–Stamey, пальцевое ректальное исследование (ПРИ); заполнение анкет суммарной оценки симптомов хронического абактериального простатита с воспалительным компонентом (СОС-ХАПВК) и формулы сексуальной мужской функции (СМФ) [17]; оценку соматопсихического состояния; бактериоскопическое, бактериологическое и молекулярно-биологическое исследования отделяемого уретры и секрета простаты с определением T. vaginalis, G. vaginalis, U. urealiticum, M. hominis, M. genitalium и C. trachomatis; общий анализ мочи, общий и биохимический анализы крови; урофлоуметрию (аппарат PICOFLOW); трансректальное УЗИ простаты с проведением цветного допплеровского картирования (ЦДК) и допплерографии уретральных и капсулярных артерий; исследование микроциркуляции слизистой простатического отдела уретры и кожи в точке проекции простаты методом лазерной допплеровской флоуметрии. Регистрацию перечисленных параметров производили до лечения и через 20 дней после лечения.
На выделения из уретры жаловались 167 (54,6%) пациентов. При объективном обследовании у 107 (35%) мужчин губки уретры были отечными, у 211 (69%) – гиперемированными, у 122 (39,9%) – вывернутыми. Лабораторное исследование уретрального отделяемого и секрета простаты микроскопическим, бактериологическим и геномным методами выявило у всех больных инфекции, передаваемые половым путем (ИППП; табл. 1). Чаще всего обнаруживались трихомонады, хламидии и уреаплазмы.
Длительность заболевания ХАПВК колебалась от 3 мес до 12 лет и в среднем составила 3,27±0,43 года. Продолжительность заболевания до года имела место у 89 (29,1%) мужчин, от года до 3 лет – у 120 (39,2%), от 3 до 5 лет – у 71 (23,2%), более 5 лет – у 26 (8,5%) мужчин. По социальному статусу распределение пациентов было следующим: частные предприниматели – 100 (32,7%) человек, служащие – 94 (30,7%), рабочие – 33 (10,8%), студенты – 10 (3,3%), полицейские – 12 (3,9%), неработающие – 49 (16%), медицинские работники – 8 (2,6%). Из них 188 (61,4%) были женатыми. Одного ребенка имели 83 (27,1%) мужчины, двоих – 29 (9,5%).
Всем обратившимся проведена стандартная терапия ХАПВК, включившая антибиотик (левофлоксацин по 500 мг 1 раз в сутки, 28 дней), простатопротекторы (свечи ректальные «Витапрост» по 1 свече на ночь, 20 дней; раствор «Простакор» по 1 мл внутримышечно 1 раз в сутки, 20 дней), α-адреноблокатор (тамсулозина гидрохлорид по 0,4 мг 1 раз в сутки, 30 дней), НПВС (нимесулид по 10 мг 1 раз в сутки, 10 дней), противопротозойный препарат (при выявлении T. vaginalis; орнидазол по 500 мг 2 раза в сутки, 10 дней), вазоактивные препараты и витамины. Левофлоксацин способен создавать высокие тканевые концентрации в предстательной железе. Кроме того, используя один антибактериальный препарат, в том числе и у пациентов с M. genitalium и C. trachomatis, мы попытались максимально оптимизировавать (унифицировать) наше исследование.
Кроме того, в комплекс лечебных мероприятий ХАПВК было включено два наиболее эффективных метода озонотерапии. Для приготовления озонсодержащих растворов использовали озонтерапевтическую установку УОТА-60-01 «Медозон». Физиологический раствор в объеме 400 мл предварительно озонировали, пропуская через него озонокислородную смесь до достижения концентрации озона в жидкости 4–6 мкг/мл, после чего ее вводили внутривенно пациенту, на курс – 7 вливаний. Помимо этого местно (в прямую кишку) назначали аппликации специально приготовленного озонированного масла в сочетании с массажем простаты (10 процедур).
Описательные статистики представлены в зависимости от типа учетных признаков и функции распределения полученных данных.
В случае нормального распределения количественных величин описание представлено средним значением (M) и среднеквадратическим отклонением (±) или доверительным интервалом (ДИ 95%). Для количественных признаков представлены абсолютные значения, процентные доли (Р), стандартная ошибка для долей (±m) и доверительные интервалы (ДИ 95%). В ряде случаев при разделении выборки на подгруппы для уточнения диапазона доверия применялся метод Бутстрепа. Определение нормального распределения при проведении статистического анализа осуществлено с помощью критериев Колмогорова–Смирнова и Шапиро–Уилкса.
Статистическая значимость различий определена с помощью критерия χ2 и точного критерия Фишера. Для исследования статистической значимости различий в независимых непараметрических выборках использован критерий Манна–Уитни (U). Оценка согласованности мнения экспертов проведена с помощью критерия Кендала (W). Критический уровень значимости (p) при проверке статистических гипотез в исследовании принят равным 0,05.
Результаты. При диагностике ХАПВК у большинства мужчин выделяют три группы симптомов: болевой, дизурический и сексуальный. В то же время жалобы этих пациентов характеризуются неопределенностью, разнообразием и психоэмоциональной зависимостью. Именно поэтому в клинической практике для объективизации и количественного выражения показателей, характеризующих состояние пациента, а также для адекватной оценки проводимого лечения ХАПВК целесообразно применение количественных шкал: СМФ и СОС-ХАПВК [16, 17].
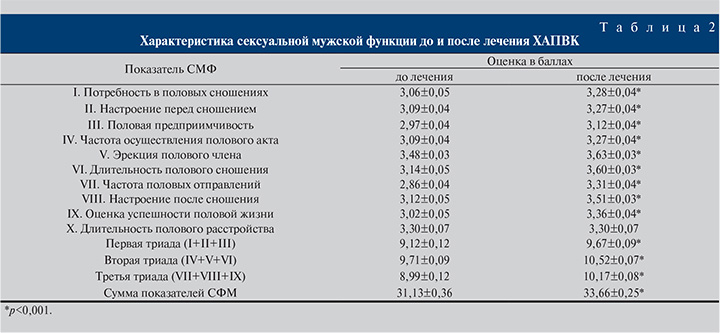
Характеристика мужской копулятивной функции до и после лечения отражена в табл. 2, из которой видно, что после лечения в соответствии с балльной оценкой сексуальная функция у обследуемых мужчин статистически значимо улучшилась и стала соответствовать средней статистической норме [17].
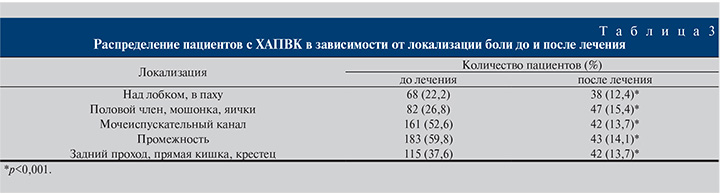
До лечения наиболее часто боль локализовывалась в мочеиспускательном канале 161 (52,6%) и промежности – 183 (59,8%). В то же время после окончания терапии ХАПВК типичных мест локализации болевых ощущений выявлено не было (табл. 3).
Анкета СОС-ХАПВК позволила упростить выявление и анализ жалоб больных ХАПВК, оценить симптомы заболевания, получить объективную характеристику всего многообразия клинических проявлений у конкретного мужчины.
После заполнения все полученные анкетные показатели СОС-ХАПВК были подвергнуты статистической обработке. В первую очередь подсчитывали баллы, характеризующие болевые ощущения симптомов, дизурии, простатореи (выделение секрета простаты в конце мочеиспускания или дефекации) и качества жизни (КЖ).
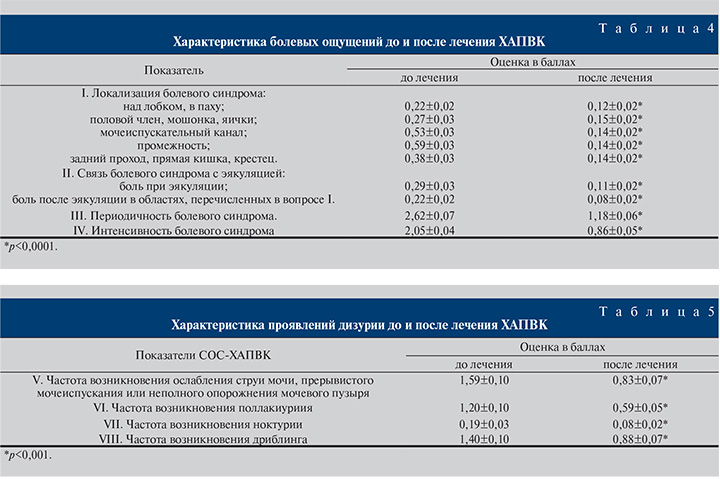
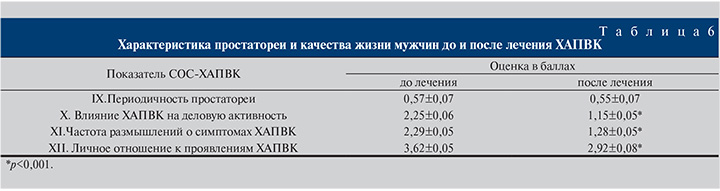
Согласно данным, приведенным в табл. 4–6, результатом лечения стало статистически значимое (р<0,001) уменьшение выраженности болевых ощущений и дизурии, повышение качества жизни. Периодичность простатореи, свидетельствующее об атонии простаты, в течение лечения ХАПВК не изменилась.
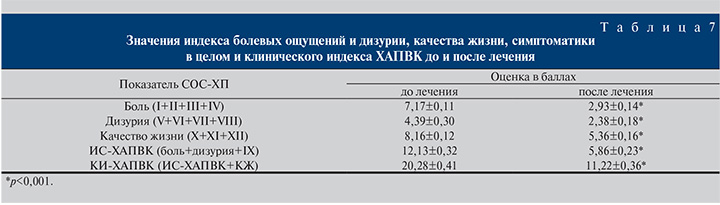
Следующим этапом определен индекс симптоматики (ИС)-ХАПВК, характеризующий суммарную оценку баллов болевых ощущений, дизурии и простатореи (табл. 7). Последним рассчитывали клинический индекс (КИ)-ХАПВК, который помимо количественной отражал качественную характеристику заболевания.
В зависимости от степени выраженности клинических проявлений ХАПВК подразделяется на незначительный (0–10 баллов), умеренный (11–25 баллов) или значительный (26–50 баллов). Согласно полученным данным, средние показатели КИ-ХАПВК статистически значимо уменьшились во время лечения практически в 2 раза, что, по принятой градации, соответствует нижней границе умеренной степени ХАПВК (табл. 7).
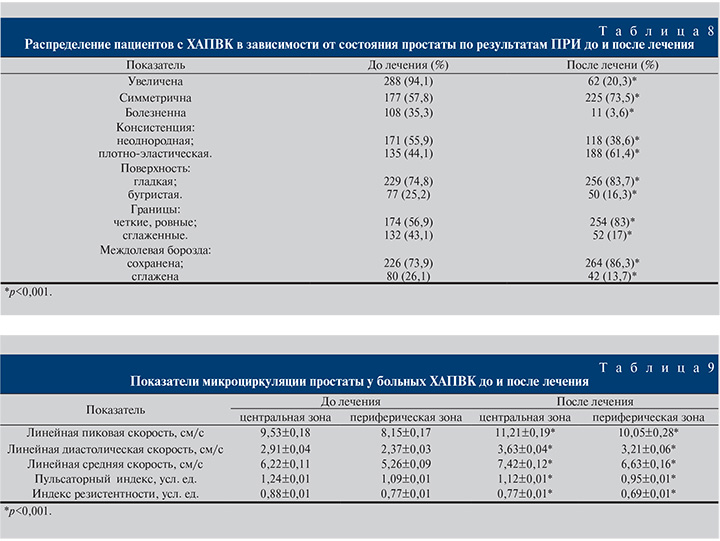
У большинства мужчин после лечения ХАПВК в ходе ПРИ простата была уменьшена в размерах, безболезненна, симметрична, плотно-эластической консистенции, с четкими, ровными границами, гладкой поверхностью и сохраненной междолевой бороздой (табл. 8).
При микроскопическом исследовании секрета простаты на фоне лечения обнаружено уменьшение числа лейкоцитов с 29,29±0,67 до 4,75±0,15 (р<0,001), а также увеличение количества лецитиновых зерен (р<0,001). До лечения умеренное количество лецитиновых зерен в секрете простаты наблюдалось у 98 (32%) мужчин, небольшое количество – у 150 (49%), а единичные лецитиновые зерна определялись у 58 (19%) человек. После лечения у 127 (41,5%) мужчин выявлена большое количество лецитиновых зерен, у 119 (38,9%) – умеренное, у 60 (19,6%) – небольшое.
Одним из основных инструментальных методов мониторинга при ХАПВК является УЗИ простаты. Оно позволяет оценить размеры и объем простаты, ее эхоструктуру, а в сочетании с ЦДК – состояние гемодинамики.
У обследованных нами пациентов выявлено статистически значимое (р<0,001) уменьшение всех размеров простаты: высоты (верхненижний размер) с 40,99±0,22 до 39,13±0,21 мм, ширины (поперечный размер) с 41,94±0,21 до 39,94±0,22 мм, толщины (переднезадний размер) с 30,52±0,20 до 29,15±0,18 мм.
Объем простаты также уменьшился с 27,78±0,42 до 24,10±0,36 см (р<0,001).
При оценке состояния микроциркуляции у всех наблюдаемых нами пациентов до лечения отмечено диффузное обеднение сосудистого рисунка в центральной и периферической зонах простаты, что выражалось в уменьшении количества сосудов на площади изображения соответствующего участка.
Как видно из табл. 9, проведенная терапия ХАПВК способствовала существенному (р<0,001) улучшению показателей микроциркуляции.
При исследовании базального кровотока в точке проекции простаты после лечения было выявлено умеренное повышение тканевой перфузии – с 7,80±0,07 до 8,65±0,08 перф. ед. (р<0,001).
Показатели базального кровотока простатического отдела мочеиспускательного канала на фоне лечения также повысились – с 40,08±0,21 до 42,42±0,23 перф. ед. (р<0,001), что может свидетельствовать об улучшении гемодинамики как в уретре, так и в простате в целом.
С учетом частоты и клинического значения нарушений акта мочеиспускания урофлоуметрия является обязательным методом исследования больных хроническим простатитом, позволяющим выявлять инфравезикальную обструкцию, а также осуществлять динамическое наблюдение за пациентом в процессе лечения [18]. Проведенное нами обследование выявило увеличение средней объемной скорости мочеиспускания с 8,96±0,15 до 11,82±0,15 мл/с (р<0,001).
Таким образом, после комплексного лечения ХАПВК с применением общей и местной озонотерапии удалось добиться симптоматического улучшения, а именно снизить интенсивность болевых ощущений, уменьшить выраженность дизурии, улучшить сексуальную функцию и качество жизни мужчины. Кроме этого у больных было отмечено повышение кровотока в артериях и венах простаты, уменьшение размеров органа и его объема. Однако полученные данные недостаточно отражают индивидуально-типологическую характеристику течения заболевания.
В связи с этим нами продолжается изучение особенностей течения ХАПВК в зависимости от особенностей фенотипа мужчины.



