Введение. Мочекаменная болезнь занимает одно из ведущих мест среди всех урологических заболеваний и продолжает оставаться одной из самых актуальных проблем современной медицины, подтверждением чего служит неуклонный рост ее распространенности. Ежегодная заболеваемость мочекаменной болезнью в мире варьируется от 0,5 до 5,3% [1]. По данным официальной статистики Министерства здравоохранения РФ, за период 2002–2010 гг. заболеваемость выросла с 440,5 до 535,7 на 100 тыс. взрослого населения. В абсолютных числах рост зарегистрированных больных составил с 629 453 до 760 237 [2].
 Наиболее тяжелой формой мочекаменной болезни является коралловидный нефролитиаз (КН), вопросы диагностики, выбора тактики и способа лечения которого остаются одними из наиболее обсуждаемых и противоречивых [3].
Наиболее тяжелой формой мочекаменной болезни является коралловидный нефролитиаз (КН), вопросы диагностики, выбора тактики и способа лечения которого остаются одними из наиболее обсуждаемых и противоречивых [3].
Факторами, определяющими выбор тактики лечения, служат не только форма коралловидного камня, индивидуальная стереоанатомия чашечно-лоханочной системы (ЧЛС) и ангиоархитектоники нормально развитой почки, но и их пространственные взаимоотношения [4]. Кроме того, необходимо помнить об альтернативных вариантах строения, аномалиях развития почек и сопутствующих заболеваниях [5].
Стремление хирурга улучшить результаты операции толкает его на поиск новых технологий в сфере диагностики и лечения. Как правило, диагностика нефролитиаза строится вокруг ультразвукового и рентгенологического методов исследования. Однако, несмотря на их объективность и информативность, при определении тактики лечения и характера предстоящей операции данные, получаемые с помощью этих методов, не всегда позволяют полностью и правильно ответить на поставленные вопросы. Очевидно, что только при комплексном анализе ситуации можно рассчитывать на качественный результат лечения. Неоценимую помощь в этом оказывают современные методы компьютерной визуализации – мультиспиральная компьютерная томография с трехмерной реконструкцией, 3D-компьютерное моделирование, позволяющие получать детальное представление об индивидуальных особенностях строения органа и течении заболевания [6, 7].
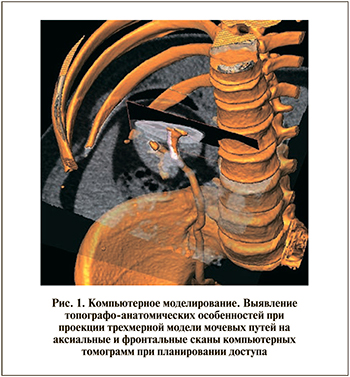
В недавнем прошлом планирование лечения имело место только в сознании уролога, где формировались представления топографо-анатомических взаимоотношений, течение патологического процесса и прогноза эффективности предстоящего лечения. Сегодня же новые технологии компьютерной графики позволяют не только подтвердить свои предположения, но и предварительно оценить эффективность и безопасность планируемой операции [8]. Важной особенностью применения компьютерного моделирования перед стандартными методами обследования считается возможность выполнения виртуального планирования манипуляции с учетом индивидуальных топографо-анатомических особенностей строения органа в совокупности с патологическим процессом (рис. 1).
Созданная компьютерная модель почки позволяет хирургу в виртуальном режиме детально проанализировать форму строения ЧЛС и тип ротации чашечек, что играет важную роль при оценке технических аспектов предстоящего пособия и прогнозировании эффективности лечения коралловидного нефролитиаза (рис. 2).

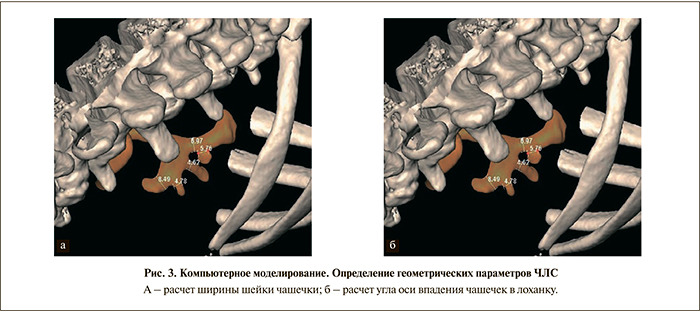
К другой отличительной особенности компьютерного моделирования относится возможность проведения анализа эффективности перкутанного вмешательства из выбранного хирургом доступа. Владение информацией о стереоанатомии чашечно-лоханочной системы позволяет хирургу во время виртуальной операции оценить возможность интраренальных манипуляций ригидным инструментом и визуализации всей ЧЛС из планируемого доступа для достижения ее полной элиминации от камня (рис. 3).
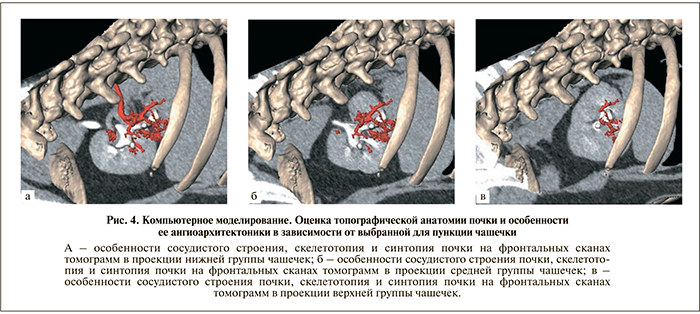
Также важной особенностью компьютерного моделирования служит возможность оценки сосудистого строения почки при создании пункционного доступа на виртуальной модели в планировании предстоящего лечения (рис. 4). Полученная информация – решающий фактор в профилактике интраоперационных кровотечений.
Таким образом, целью исследования стало изучение роли компьютерного моделирования в улучшении результатов лечения коралловидного нефролитиаза.
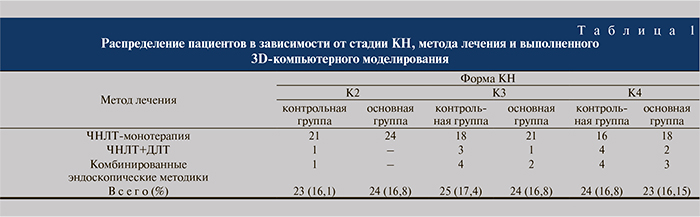
Материалы и методы. В рамках исследования проведен анализ результатов обследования и лечения 143 пациентов с К2–К4-стадиями КН. С учетом отсутствия серьезных затруднений при выборе тактики и способа лечения при К1-форме КН, а также высокой эффективности различных оперативных методик эта группа пациентов не включалась в исследование. Оценка эффективности лечения КН проведена на основании анализа результатов оперативных вмешательств в отношении пациентов, которым выполнялась чрескожная нефролитотрипсия (ЧНЛТ) в качестве монотерапии, «sandwich»-терапии – чрескожная нефролитотрипсия в сочетании с дистанционной литотрипсией (ЧНЛТ+ДЛТ) и ЧНЛТ в комбинации с дополнительным эндоскопическими методиками – second-look nephroscopy или mini-perc technique. ЧНЛТ в режиме монотерапии была осуществлена 118 (82,52%) пациентам, ЧНЛТ в сочетании с ДЛТ 11 (7,69%), ЧНЛТ в комбинации с дополнительным эндоскопическими методиками выполнена 14 (9,79%) пациентам. Повторное оперативное лечение в отдаленном послеоперационном периоде по поводу резидуальных камней более 4 мм потребовалось 5 пациентам.
Среди пациентов были 71 (49,65%) мужчина и 72 (50,35%) женщины. Средний возраст пациентов составил 49 лет. Форма К2 диагностирована 47 (32,87%) пациентам, К3 – 49 (34,26%), К4 – 47(32,87%). Корраловидные камни 120 (83,9%) пациентов носили одиночный характер, 23 (16,1%) – множественный.
Все пациенты были разделены на две группы. В контрольной группе предоперационное обследование проведено без использования 3D-компьютерного моделирования, в основной – с 3D-моделированием (табл. 1). Все группы отвечали аналогичным критериям отбора. Критерием эффективности лечения стала полная элиминация камней из ЧЛС или наличие резидуальных камней до 4 мм.
Тип строения ЧЛС оценивали согласно классификации, предложенной F. Sampaio, в соответствии с которой выделяют две основные группы в зависимости от варианта слияния собирательной системы почки в лоханку. В обеих группах чашечки верхнего и нижнего сегментов сливаются в крупные верхнюю и нижнюю чашечки. Вариабелен лишь путь дренирования среднего сегмента почки. При типе А средний сегмент дренируется через одну или обе полярные чашки. Чашечно-лоханочная система типа А имеет два подтипа: при подтипе АI чашечки среднего сегмента впадают в одну или обе полярные чашки так, что бассейны паренхимы вокруг верхней и нижней чашечек не пересекаются, при подтипе АII две чашечки среднего сегмента пересекаются во фронтальной плоскости. При типе В средний сегмент дренируется самостоятельно – через третью, среднюю, чашку (подтип ВI) или же путем непосредственного впадения чашечек среднего сегмента в лоханку (подтип ВII).
Варианты ротации чашечек распределены по принадлежности к Броделевскому или Ходсоновскому типу. Разделение по типу ротации определяется углом, формируемым чашечками передней и задней групп между своими осями и фронтальной плоскостью почки. При варианте ротации, предложенной Броделем, угол между осью задних чашечек и фронтальной плоскостью почки составляет около 20°, в то время как для чашечек передней группы этот угол составляет около 70°. Ходсон описал зеркально противоположный тип строения ЧЛС, при котором чашечки передней группы отклонялись от фронтальной плоскости на 20° и проецировались латеральнее чашечек задней группы, отходящих под углом 70° к фронтальной плоскости почек (табл. 2) [9, 10].
Для оценки роли компьютерного моделирования в предоперационном планировании ретроспективно проведен анализ частоты интраоперационных осложнений.
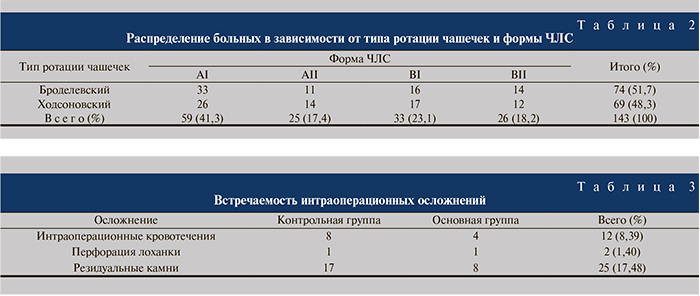
Результаты и обсуждение. Эффективность лечения КН в целом составила 96,5%, эффективность ЧНЛТ монотерапии – 82,52%, осложнения регистрировали в 27,27% наблюдений (табл. 3).
При анализе структуры методов лечения в зависимости от применения компьютерного моделирования патологического процесса установлено, что ЧНЛТ в качестве монотерапии в группе с моделированием выполняли на 12,34% чаше, чем в контрольной. Это обусловлено достижением лучших показателей элиминации ЧЛС от камней в этой группе и как следствие – снижением необходимости проведения комбинированного лечения для избавления от резидуальных камней.
Ведущее место среди всех осложнений – 39 (27,27%) случаев – занимали резидуальные камни. Повторное оперативное лечение потребовалось 25 (17,48%) пациентам. Основными причинами резидуальных камней послужили миграция фрагментов в труднодоступную чашечку, неправильно выбранный доступ и интраоперационное кровотечение. Применение компьютерного моделирования патологического процесса позволило сократить встречаемость резидуальных камней на 12,34% (р<0,5).
Интраоперационное кровотечение развилось у 12 (8,39%) пациентов. В зависимости от формы ЧЛС наиболее часто кровотечения встречались в группе пациентов с формами AII (41,7%) и BII (33,3%). Все осложнения купированы консервативным путем и не потребовали дополнительных вмешательств. Использование компьютерного моделирования позволило сократить количество случаев интраоперационных кровотечений на 5,48% (р<0,5).
Заключение. Залогом успеха лечения КН наряду с неотъемлемыми составляющими, такими как квалификация хирурга, его опыт и оснащение урологического стационара, остается адекватная оценка патологического процесса, особенностей индивидуального строения органа, планирование лечения, а главное – прогнозирование результата. Влияние внутреннего строения почки на эффективность лечения КН определяет целесообразность применения компьютерного моделирования для оптимизации выбора тактики и улучшения результатов лечения, а также с целью снижения риска развития интраоперационных осложнений.



