 Мочекаменная болезнь, туберкулез, ретроперитонеальный фиброз, воспалительные или лучевые поражения, ятрогенные (чаще эндоскопические) повреждения могут приводить к облитерации мочеточников, в том числе и протяженной. Восстановление проходимости верхних мочевыводящих путей при значительных дефектах остается одной из самых сложных проблем оперативной урологии. Невозможность восстановления естественного пассажа мочи при использовании неизмененных тканей мочевого тракта, техническая сложность замены мочеточника другими материалами часто ставят выбор между нефрэктомией и постоянным мочевым дренажом (при единственной почке или двустороннем поражении), снижая качество жизни пациента [1–4].
Мочекаменная болезнь, туберкулез, ретроперитонеальный фиброз, воспалительные или лучевые поражения, ятрогенные (чаще эндоскопические) повреждения могут приводить к облитерации мочеточников, в том числе и протяженной. Восстановление проходимости верхних мочевыводящих путей при значительных дефектах остается одной из самых сложных проблем оперативной урологии. Невозможность восстановления естественного пассажа мочи при использовании неизмененных тканей мочевого тракта, техническая сложность замены мочеточника другими материалами часто ставят выбор между нефрэктомией и постоянным мочевым дренажом (при единственной почке или двустороннем поражении), снижая качество жизни пациента [1–4].
В настоящее время существует множество методик реконструктивных восстановительных операций на мочеточнике [3, 4]. Установлено, что для замещения протяженных повреждений одной из наиболее эффективных и физиологически оптимальных операций является тонкокишечная (в некоторых случаях аппендикулярная) пластика мочеточника [4–7]. Несмотря на большую техническую сложность исполнения, по частоте ранних и поздних осложнений данный вид восстановления естественного пассажа мочи статистически сопоставим с другими методами [8, 9].
Приводим собственное клиническое наблюдение.
Б о л ь н а я К. 44 лет. Диагноз: основной – мочекаменная болезнь: камень верхней трети левого мочеточника. Осложнение: протяженная стриктура левого мочеточника, гидроуретеронефроз слева, вторичный хронический пиелонефрит слева, латентная фаза с исходом в нефросклероз.
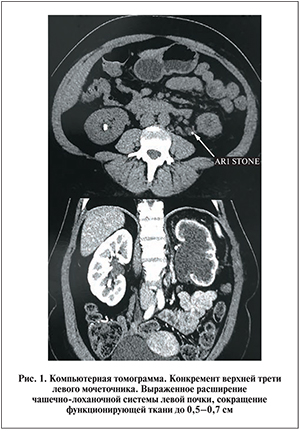
Из анамнеза: в июле 2012 г. выполнено 2 сеанса дистанционной литотрипсии длительно стоящего камня верхней трети левого мочеточника (рис. 1) без эффекта. При уретероскопии выявлено выраженное сужение просвета мочеточника (провести уретероскоп и выполнить контактную уретеролитотрипсию невозможно). В октябре 2012 г. выполнена операция: удаление конкремента из верхней трети левого мочеточника, пластика лоханочно-мочеточникового сегмента и верхней трети мочеточника лоскутом из лоханки (операция Culp-DeWeerd) с восстановлением естественного пассажа мочи в послеоперационном периоде. В ноябре 2013 г. пациентка поступила в урологическое отделение с обострением пиелонефрита слева. При обследовании выявлено выраженное расширение полостной системы оперированной почки до верхней трети мочеточника, выполнена чрескожная пункционная нефростомия; явления воспаления купированы. В дальнейшем при попытках восстановления естественного пассажа мочи отмечены обострения пиелонефрита.
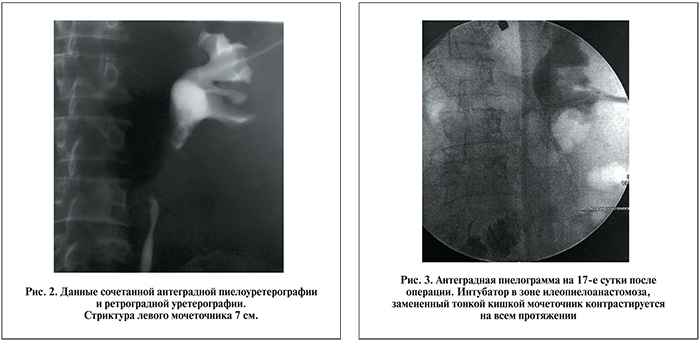
В сентябре 2014 г. больная поступила в урологическое отделение ГБУЗ ЯО «Областная клиническая больница» для оперативного лечения. При обследовании: по нефростомическому дренажу до 700 мл мочи в сутки; суммарная функция почек в норме: креатинин 69 мкмоль/л, мочевина 4,1 ммоль/л, СКФ 119,7 мл/мин. По данным УЗИ, правая почка не увеличена, толщина паренхимы 2,1 см, чашечно-лоханочная система (ЧЛС) не расширена, определяются три солитарные кисты размером от 1,1 до 2,1 см, в нижней чашечке – конкремент 0,9х1,0 см, в верхней чашечке – конкремент 0,5 см; левая почка не увеличена, толщина паренхимы – 1 см, чашечки до 0,7 см, лоханка – 1,5 см, дренирована нефростомой, конкрементов нет. На обзорной и внутривенных урограммах функция правой почки сохранена, теней, подозрительных на конкременты, четко не определяется; слева эвакуаторная функция нарушена на уровне верхней трети мочеточника. Результаты антеградной пиелографии: стриктура верхней трети мочеточника, контраст за препятствие не проходит; при одновременном антеградном и ретроградном введении контрастного вещества определяется протяженная (более 7 см) стриктура левого мочеточника (рис. 2). По данным ангионефросцинтиграфии констатирован 90%-ный дефицит функции левой почки.
 6.10.14 выполнена операция: пластика левого мочеточника сегментом подвздошной кишки (iliоpyelocystoa-nastomosis).
6.10.14 выполнена операция: пластика левого мочеточника сегментом подвздошной кишки (iliоpyelocystoa-nastomosis).
Произведена верхняя срединная лапаротомия. При ревизии периуретеральной клетчатки выявлен выраженный рубцовый процесс с границы средней трети мочеточника до прилоханочной зоны. После мобилизации от рубцов мочеточник на протяжении 9–10 см представлен шнуровидным образованием до зоны лоханочно-мочеточникового сегмента, лоханка расширена, напряжена, спереди по лоханке проходят дополнительные артерия и вена. Пальпаторно определяется неравномерное истончение паренхимы. Учитывая категорический отказ пациентки от нефрэктомии и желание избавиться от нефростомы, молодой возраст, а также наличие кист и конкрементов в контралатеральной почке, несмотря на недостаточный объем функционирующей паренхимы оперируемой почки, решено выполнить тонкокишечную пластику мочеточника. Из подвздошной кишки, отступя 20 см от илеоцекального угла, на сосудистой ножке выкроен сегмент протяженностью 25 см. Проходимость тонкой кишки восстановлена путем создания анастомоза по типу «конец в конец» двухрядным кишечным швом нитью ПГА 3/0. Мочеточник пересечен в пределах здоровых тканей, изолированный сегмент кишки сориентирован изоперистальтически, на интубаторе сформирован анастомоз между лоханкой и проксимальным краем кишки по типу «конец в бок». Дистальный конец сегмента анастомозирован с мочевым пузырем атравматическими иглами с нитью ПГА 2/0 «конец в бок» без «антирефлюксной защиты». Герметичность анастомоза удовлетворительная. Мочевой пузырь перитонизирован у линии анастомоза, дренирован через уретру катетером Фолея. Брюшная полость дренирована у зон анастомозов и ушита.
Первые сутки наблюдения: диурез адекватный (по катетеру Фолея 2 л, по нефростоме до 150 мл), снижения общей азотвыделительной функции почек не было: креатинин крови 89,9 мкмоль/л, мочевина 2,8 ммоль/л, натрий 143 ммоль/л, калий 3,9 ммоль/л, СКФ 91,9 мл/мин.
Страховочные дренажи удалены на 5-е сутки послеоперационного периода. При этом суточный диурез по нефростоме увеличился до 700 мл. На 9-е сутки после операции отмечена атака пиелонефрита. Пациентке проведена консервативная дезинтоксикационная, противовоспалительная, антибактериальная терапия до полного купирования клинических симптомов. Катетер Фолея удален на 15-е сутки послеоперационного периода. Для контроля состоятельности анастомозов выполнены: МРТ (на 16-е сутки после операции) – левая почка 76х36 мм с неровными контурами, паренхима 5,5–8 мм, кортикомедуллярная дифференцировка нарушена, подшитый фрагмент тонкой кишки визуализируется на всем протяжении, паранефральная клетчатка не изменена; антеградная пиелограмма (на 17-е сутки после операции) — мочеточник контрастируется на всем протяжении, затеков контрастного вещества не определено (рис. 3), выполнена диспозиция интубатора в лоханку. После проведения контрольной антеградной пиелографии на 20-е сутки послеоперационного периода (рис. 4) нефростомический дренаж удален. Для контроля состояния оперированной почки на 23-е сутки после операции выполнено УЗИ: справа почка – без динамики, левая почка 9х3,9 см с мелковолнистым контуром, толщина паренхимы 0,9–1,0 см повышенной эхогенности, лоханка 1,2 см. Больная выписана в удовлетворительном состоянии на 25-е сутки для амбулаторного наблюдения. Контрольный осмотр через 3 мес: лабораторные показатели в пределах нормальных значений, при УЗИ (рис. 5) в оперированной почке ЧЛС не расширена, паренхима повышенной эхогенности толщиной от 8 до 10 мм.
По результатам МРТ (рис. 6) по сравнению с послеоперационными данными отмечается уменьшение размеров ЧЛС с 44х30 до 24х29 мм, размеры почки и паренхимы без динамики, мочеточник контрастируется, анастомозы состоятельны.
Заключение. В настоящее время опыт полной замены мочеточника и в России и за рубежом невелик. Это может быть связано как с редко возникающей клинической необходимостью, так и с технической сложностью выполнения оперативного пособия. В представленном клиническом наблюдении пациентке проведена органосохраняющая операция путем формирования мочеточника из тонкой кишки. Мы получили удовлетворительные результаты в раннем послеоперационном периоде: заживление раны первичным натяжением, полное восстановление пассажа мочи естественным путем, отсутствие нарушения почечной функции, развития свищей и несостоятельности анастомоза. Положительный опыт проведения такой реконструктивной операции позволит нам более активно применять данный вид лечения в нашей практике при клинической необходимости.


