Общепринятого определения анатомо-функциональной несостоятельности мочеиспускательного канала у женщин вследствие его повреждения различного генеза не существует. Для описания данного состояния в отечественной и зарубежной литературе чаще используется термин «деструкция уретры». Таким образом, деструкция уретры – это результат тяжелого повреждения мочеиспускательного канала, клиническими проявлениями которого являются укорочение или отсутствие мочеиспускательного канала, выявляемое при обследовании, хроническая мочевая инфекция и недержание мочи. Деструкция уретры у женщин в настоящее время достаточно редкая патология, что может затруднять диагностику и выбор метода лечения. При проведении анализа русскоязычной и зарубежной литературы мы встретили лишь небольшое количество работ по данной проблеме. Статистической информации о распространенности деструкции уретры у женщин в Российской Федерации также не представлено. К основным этиологическим факторам деструкции уретры относятся различные повреждения уретры: акушерская травма, часто вследствие длительных родов, при клинически узком тазе, при использовании акушерских щипцов, в развивающихся странах такие повреждения описаны при проведении симфизиотомии в родах [1]; ятрогенные травмы при оперативном лечении парауретральных кист, дивертикулов уретры, передней кольпоррафии, а также при использовании синтетических имплантов при лечении недержания мочи; лучевая терапия при опухолях шейки матки, влагалища [2, 3]; пролежни уретры как отдаленное следствие длительной уретральной катетеризации у женщин с нейрогенными дисфункциями нижних мочевыводящих путей, а также при длительном нахождении в палате реанимации (в особенности в коматозном состоянии) [4]; переломы тазового кольца, в том числе взрывные ранения [5, 6]; сексуальные травмы: при насильственных половых актах, при мастурбации с использованием различных предметов [7].
Основной жалобой женщины при деструкции уретры считается непроизвольное выделение мочи, что вызывает значительные физические и моральные страдания, ведет к утрате трудоспособности и в конечном итоге – к серьезным клиническим, социальным и экономическим последствиям.

В настоящее время в российской клинической практике используется классификация, предложенная в 1989 г. профессором О.Б. Лораном (табл. 1). В ее основу положен принцип единства структурных и функциональных нарушений, что и определяет подходы к терапии [8]. Лечение деструкции уретры, как правило, оперативное. Проблема выбора метода оперативного лечения деструкции уретры до сих пор остается актуальной и нерешенной. При этом требуется проведение такого вмешательства, которое будет направлено не только на формирование неоуретры (табл. 2), но и на коррекцию недержания мочи [9, 10], что считается не менее сложной хирургической задачей.

Цель статьи – описание конкретных клинических наблюдений, позволяющих оценить сложность выбора и особенности индивидуального подхода к лечению пациенток с деструкцией уретры. В Центре урологии и гинекологии линики НИИТО с 2013 по 2018 г. наблюдались две пациентки с деструкцией уретры.
Клиническое наблюдение 1
Пациентка 46 лет в анамнезе перенесла многочисленные операции на уретре по поводу недержания мочи, в ряде случаев с инфекционными осложнениями, потребовавшими удаления имплантатов, что в итоге привело к формированию свищей и безуспешным попыткам фистулопластик. В результате пациентка обратилась в клинику с жалобами на тотальное недержание мочи. При обследовании выявлена деструкция мочеиспускательного канала 4-й степени: на фоне выраженных рубцовых изменений передней стенки влагалища полностью отсутствует задняя стенка уретры, передняя представлена рубцами, задняя полуокружность шейки мочевого пузыря разрушена, шейка зияет, имеется прямое сообщение с полостью мочевого пузыря, вследствие чего и тотальное недержание мочи.
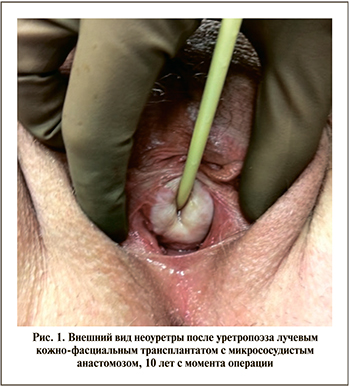 Сложность коррекции заключалась в том, что выполнение уретропоэза местными тканями было технически невозможным вследствие выраженного их дефицита, а также массивных рубцовых изменений влагалища. Что потребовало формирования неоуретры с использованием трансплантата. Для этой цели был выбран лучевой кожно-фасциальный трансплантат, из которого была сформирована неоуретра, а с использованием микрохирургической техники и микрососудистых анастомозов пересажена в типичное место. Был получен хороший результат уретропоэза (рис. 1), сформированная неоуретра имеет достаточную длину (до 4 см) и проходимость. Однако впоследствии мы столкнулись с проблемой камнеобразования на волосах трансплантата, что потребовало неоднократных контактных уретролитотрипсий.
Сложность коррекции заключалась в том, что выполнение уретропоэза местными тканями было технически невозможным вследствие выраженного их дефицита, а также массивных рубцовых изменений влагалища. Что потребовало формирования неоуретры с использованием трансплантата. Для этой цели был выбран лучевой кожно-фасциальный трансплантат, из которого была сформирована неоуретра, а с использованием микрохирургической техники и микрососудистых анастомозов пересажена в типичное место. Был получен хороший результат уретропоэза (рис. 1), сформированная неоуретра имеет достаточную длину (до 4 см) и проходимость. Однако впоследствии мы столкнулись с проблемой камнеобразования на волосах трансплантата, что потребовало неоднократных контактных уретролитотрипсий.
В течение 2 лет рост волос и камнеобразование прекратились.
Наличие неоуретры как таковой не привело к полному восстановлению мочеиспускания. Что, естественно, связано с необратимым повреждением сфинктера, отсутствием подвешивающего и связочного аппарата у сформированной уретры и как следствие – ее удерживающей функции. У пациентки сохранялась тотальная утечка мочи в ортостазе. В последующем потребовалось несколько оперативных вмешательств, направленных на коррекцию инконтиненции. Сначала была предпринята попытка коррекции путем выполнения слинговой операции трансобтураторным доступом с использованием сетчатого имплантата (синтетической ленты), как наименее рискованной, однако никакого эффекта получено не было. Интраоперациоонно создать натяжение ленты, необходимого для коаптации неоуретры, не удалось. По всей видимости, это можно объяснить тем, что при трансобтураторной установке лента расположена горизонтально и в условиях грубых периуретральных рубцово-спаечных изменений не обеспечивает необходимого смыкания стенок уретры и удержания мочи.
Спустя 3 мес. был выполнена позадилонная уретропексия синтетической лентой. При позадилонной установке концы ленты располагаются вертикально, однако при наличии местного рубцово-спаечного процесса без натяжения и фиксации слинга данный метод также не позволяет добиваться необходимой коаптации уретры и прекращения утечки мочи. В отсутствие фиксации лента после прекращении усилия, создающего натяжение, смещается обратно за счет периуретральных рубцовых изменений, не сохраняя ранее созданное натяжение. Таким образом, применение свободного от натяжения слинга не дало эффекта.
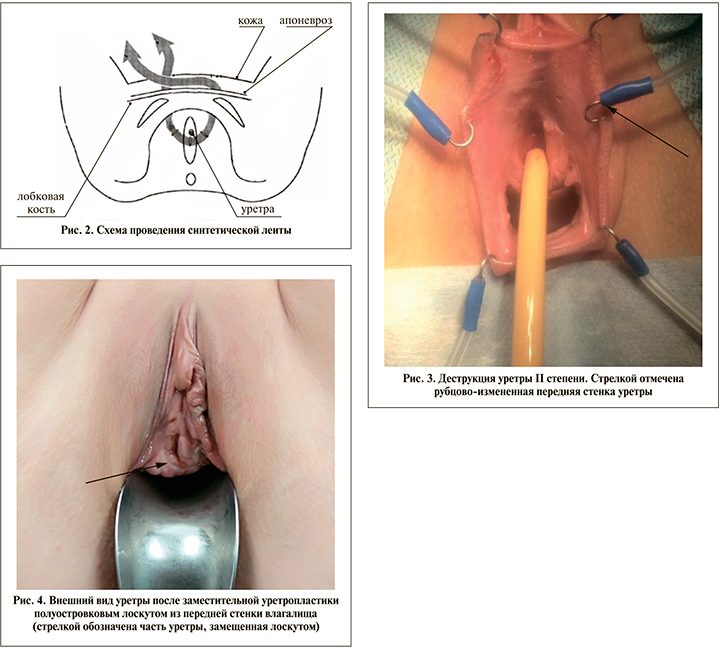
Поэтому для коррекции недержания мочи в условиях периуретрального фиброза разработана методика фиксации слинга (синтетической ленты) в состоянии натяжения. Этот способ лечения включает разрез передней стенки влагалища в области средней трети уретры длиной 0,5–1 см, мобилизацию парауретральных пространств по внутренней поверхности лобковых костей, латеральнее уретры протяженностью 1–2 см по направлению к надлобковой области. В разрез стенки влагалища с помощью игл-перфораторов лента проводится в разрезы в надлобковой области, затем один из концов ленты проводится подкожно по направлению к противоположному и через него выводится наружу. Таким образом, оба конца ленты оказываются выведенными через один разрез в надлобковой области (рис. 2). После чего концы ленты соединяют и завязывают между собой над апоневрозом передней брюшной стенки подкожно с сохранением ранее созданного натяжения (патент РФ № 2566925. Способ лечения недержания мочи III типа у ранее оперированных пациенток).
С помощью данной методики было исключено обратное смещение ленты, что обеспечило достаточное ее натяжение и коаптацию уретры, а наличие рубцовых изменений периуретральных тканей в этой ситуации предотвращает формирование пролежня. В настоящее время срок наблюдения после операции – 7 лет. У пациентки полностью восстановлено мочеиспускание и удержание мочи.
Клиническое наблюдение 2
Пациентка 31 года обратилась в клинику с жалобами на недержание мочи при напряжении и частые рецидивы мочевой инфекции. Описанные жалобы возникли после неоднократного оперативного лечения парауретральной кисты. В динамике степень выраженности недержания мочи при напряжении усугублялась. Пациентка стала отмечать утечку мочи при минимальных физических нагрузках, сексуальных контактах. Присоединилась часто рецидивирующая мочевая инфекция.
При осмотре обнаружены небольшие рубцовые изменения в области передней стенки уретры, задняя стенка частично отсутствует, просвет уретры зияет, при разведении ее стенок определяется шейка мочевого пузыря, кашлевая проба резко положительна (рис. 3). Стенки влагалища без выраженных рубцовых изменений и дефицита тканей. При уретроцистоскопии протяженность уретры не превышает 1 см, имеются минимальные признаки хронического цистита.
Установлен клинический диагноз «деструкция уретры 2-й степени. Недержание мочи 3-го типа средней степени тяжести. Хронический цистит, часто рецидивирующее течение». С учетом отсутствия выраженных рубцовых изменений и дефицита тканей влагалища первым этапом оперативного лечения выполнена заместительная уретропластика полуостровковым лоскутом из передней стенки влагалища, сфинктеропластика бульбокавернозными мышцами. При этом мы не рассчитывали на устранение недержания мочи, а использовали бульбокавернозные мышцы для укрытия швов неоуреты и формирования площадки для последующей установки синтетической ленты. В послеоперационном периоде отмечалось удовлетворительное заживление тканей в области вмешательства, при контрольном обследовании длина уретры составляла 3 см (рис. 4). Однако, как и предполагалось, недержание мочи при напряжении средней степени тяжести сохранялось.
С целью коррекции недержания мочи через 4 мес. пациентке выполнен второй этап оперативного лечения. Поскольку трансобтураторно установленная лента при сфинктерной недостаточности и умеренном периуретральном фиброзе с высокой вероятностью не обеспечила бы необходимой коаптации уретры, выбран вариант позадилонной уретропексии синтетической лентой. Во время операции произведен разрез стенки влагалища в проекции средней трети уретры, визаулизирован слой бульбокавернозных мышц, использованных для сфинктероспластики, далее мобилизованы парауретральные пространства по внутренней поверхности лобковых костей, латеральнее уретры, протяженностью 1–2 см по направлению к надлобковой области. В разрез стенки влагалища с помощью игл-перфораторов лента проведена в надлобковую область. В средней трети уртеры лента уложена на бульбокавернозные мышцы, создано необходимое натяжение ленты, избытки ленты отсечены, раны ушиты.
После проведения второго этапа оперативного лечения недержание мочи было полностью устранено, восстановлено адекватное мочеиспускание. При сроке наблюдения свыше 5 лет отсутствуют рецидивы инфекции нижних мочевыводящих путей, удержание мочи полностью сохранено.
Основным клиническим проявлением деструкции уретры является недержание мочи, выраженность его зависит от степени вовлечения в деструктивный процесс проксимальных отделов уретры и шейки мочевого пузыря, как следствие – недостаточность внутреннего сфинктера. Реконструктивная операция (уретропластика или уретропоэз) не решает проблемы недержания мочи, в связи с чем большинству пациенток через 3–6 мес. требуется проведение второго этапа оперативного лечения. Для этого используются различные слинговые операции. При этом очень важно во время выполнения первого этапа оперативного лечения планировать второй и заранее подготовить площадку для последующего расположения ленты, препятстующую развитию пролежня в последующем. Для этого можно использовать сфинктеропластику бульбокавернозными мышцами.
По нашему опыту, при втором этапе оперативного лечения большей эффективностью обладает позадилонная петлевая уретропексия по сравнению с трансобтураторной, что связано с вертикальным расположением синтетической ленты, обеспечивающим достаточное натяжение и коаптацию уретры при сфинктерной недостаточности. В условиях выраженного периуретрального фиброза дополнительно может потребоваться создание постоянного натяжения ленты, что можно достичь путем фиксации концов ленты между собой с сохранением ранее созданного натяжения.
Таким образом, для выбора корректной тактики оперативного лечения пациенток с деструкцией уретры всегда требуется индивидуальный подход. Реконструктивные операции на уретре, а в особенности последующая имплантация слинга при сформированной неоуретре – крайне сложные вмешательства, поэтому требуют большого хирургического опыта.


