Введение. Очевиден тот факт, что широкое внедрение симультанных операций (СО) в повседневную хирургическую практику станет одним из важнейших достижений медицины; вехой на пути совершенствования здравоохранения; фактором, в значительной степени облегчающим процесс исцеления пациентов, страдающих не одним, а двумя и более заболеваниями хирургического урологического профиля.
Однако реалии настоящего времени таковы, что, несмотря на высокую потребность в СО (согласно данным Всемирной организации здравоохранения [ВОЗ], опубликованным в 1995 г., сочетанные заболевания, требующие оперативного лечения, регистрируют у 25–30% пациентов, обратившихся за хирургической помощью; по данным А. Т. Байгазакова (2015), у 2,8–63%), последние выполняются только в 1,5–6,0% случаев от необходимого по показаниям числа [1–6].
Отказ от СО в недавнем прошлом – примерно до 1980– 1990-х гг. – многие исследователи связывают с доминированием открытых вмешательств, проводимых в условиях использования менее совершенного, чем сейчас, анестезиологического пособия и хирургического оснащения. В таких ситуациях реализация «в один операционный сеанс» [7] двух хирургических технологий закономерно сопровождалась увеличением травматичности доступа и риска развития анестезиологических осложнений, в частности в случаях продолжительности наркоза более 3 ч [7–9]. В настоящее время использование высокоточных малоинвазивных лапароскопических методик позволяет значительно уменьшать травматичность доступов, объемы кровопотери, вероятность инфицирования и др. [4, 10–13]. Однако многие специалисты считают неоправданным проведение лапароскопических СО пациентам, объективный статус которых соответствует ASA-II или ASAIII, т.к. велика доля пожилых людей, относящихся к этим группам, в связи с увеличением продолжительности жизни населения. При этом у данной категории пациентов часто имеются физиологические и патологические изменения, которые происходят во всех системах организма. Функция органов ухудшается, что приводит к снижению способности преодолевать хирургический стресс. В результате пациенты пожилого возраста после перенесенных оперативных вмешательств имеют более высокие показатели периоперационной заболеваемости и смертности [3, 14].
К факторам, ограничивающим применение СО, относят также необходимость длительного поддержания карбоксиперитонеума при лапароскопических операциях (при этом повышается вероятность развития тромбофлебита вен нижних конечностей, гиповентиляции легких ввиду нефизиологичного механизма дыхания, тромбоэмболических осложнений из-за снижения скорости кровотока, нарушений механизмов регуляции сердечного ритма и др.) [15–16], увеличение продолжительности хирургического вмешательства [17–18].
Несмотря на существование объективных сложностей при выполнении СО, большинство исследователей согласны с тем, что « …СО являются перспективным направлением современной хирургии…» [19–23, 14].
Позитивные результаты СО: безопасное устранение всех нарушений (повреждений) в процессе только одного вмешательства с сокращением сроков лечения и исключением вероятности обострения сопутствующего заболевания в дальнейшем, снижением необходимости повторной операции с очередным предоперационным обследованием, анестезиологической нагрузкой, эмоциональными переживаниями пациента и др., получены при хирургическом лечении различных сочетанных заболеваний органов брюшной полости, забрюшинного пространства и полости малого таза. Среди них: симультанные вмешательства у 36 человек по поводу синхронного рака желудка и ободочной кишки (n=36) [24]; симультанное удаление новообразований надпочечников (n=22) [25]; успешно выполненные СО по поводу желчнокаменной болезни и кисты почки (n=10), паховой грыжи и варикоцеле слева (n=10), паховой грыжи и врожденного крипторхизма (n=6) [14]; одновременная радикальная позадилонная простатэктомия и пластика паховой грыжи (n=32) [26] и др.
Исследователями отмечается малочисленность публикаций, посвященных симультанным вмешательствам, и недостаточная разработанность проблемы СО в целом, подтверждается необходимость дальнейших изысканий [19–22, 6, 14].
Целью настоящей работы стало изучение в сравнении периоперационных результатов симультанных вмешательств и соответствующих изолированных операций на органах мочеполовой системы.
Материалы и методы. Проведен ретроспективный сравнительный анализ периоперационных результатов плановых СО (табл. 1) и соответствующих моноопераций (МО; табл. 2), выполненных в урологических отделениях № 1 и 2 Санкт-Петербургского государственного бюджетного учреждения здравоохранения (СПбГБУЗ), Клинической больнице Святителя Луки (Городском центре эндоурологии и новых технологий) с 01.09.2018 по 30.12.2019.
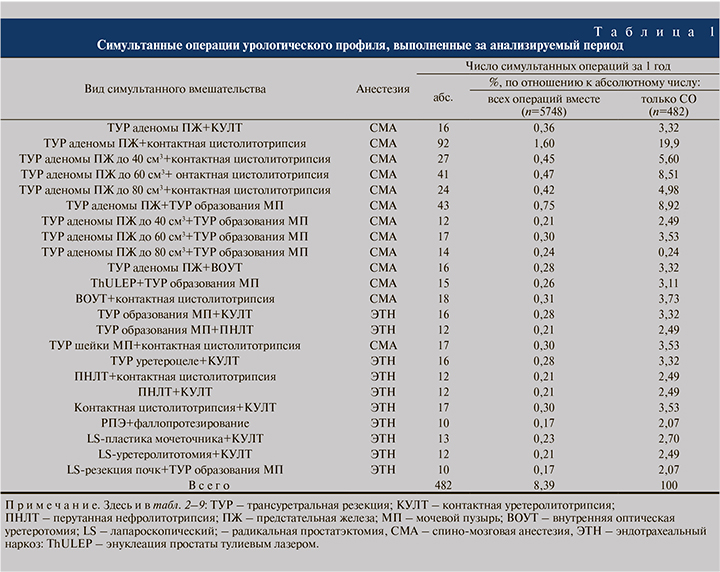

Как видно из абсолютное число всех хирургических вмешательств в целом, всех СО и соответствующих раздельно проведенных МО, выполненных в плановом порядке за рассматриваемый период, составило 5748, 482 и 5266 соответственно, т.е. доля СО от всех вмешательств, проведенных за тот период, составила 8,39%, доля моноопераций – 91,61%.
Критерии включения в исследование для пациентов с необходимостью проведения ТУР аденомы ПЖ: объем ПЖ до 80 см3, при выполнении КУЛТ – камни нижней трети мочеточников до 1 см, при выполнении ПНЛТ – камни почек до 2 см; для пациентов с необходимостью ТУР образования МП – новообразование до 2 см, с необходимостью ВОУТ – непротяженные стриктуры уретры до 1 см, при выполнении лапароскопической резекции почки – экзофитное образование до 4 см, для лиц, нуждающихся в РПЭ, – локализованные формы РПЖ (для всех случаев СО рассматривалось выполнение РПЭ без невросбережения и тазовой лимфодиссекции). Также критерием включения в исследование стало отсутствие активного воспалительного процесса мочевыделительной системы.
В каждом конкретном случае анализировали следующие периоперационные показатели: продолжительность операции, объем интраоперационной кровопотери (ИОК); продолжительность дренирования МП уретральным катетером, частоту встречаемости инфекционно-воспалительных осложнений (ИВО) со стороны органов мочеполовой системы в ближайшем послеоперационном периоде, продолжительность пребывания в стационаре в послеоперационном периоде, продолжительность индукции СМА и ЭТН, продолжительность пробуждения пациентов (этот показатель рассматривали только в тех случаях, когда симультанные и моновмешательства выполнялись в условиях ЭТН).
Статистический анализ полученных данных выполнен посредством применения двувыборочного двустороннего t-теста (пакет компьютерных прикладных программ Statistica, 10.0). Различия считали значимыми при р≤0,05. Статистическую обработку выполняли посредством использования программы «IBM® SPSS® Statistics» (версия 23, русскоязычная) с применением функции «Сравнение средних» (анализ→сравнение средних→T-критерий для парных выборок).
Результаты исследования. В табл. 3 представлены данные о продолжительности выполнения симультанных вмешательств по сравнению с таковой при соответствующих монооперациях. Учитывалась только непосредственная продолжительность СО и МО от момента начала манипуляций для получения хирургического доступа до момента ушивания раны (продолжительность индукции анестезии при спинальной анестезии [СМА] и интубационном [эндотрахеальным] наркозом [ЭТН] и время пробуждения пациента [при ЭТН] рассмотрены ниже).
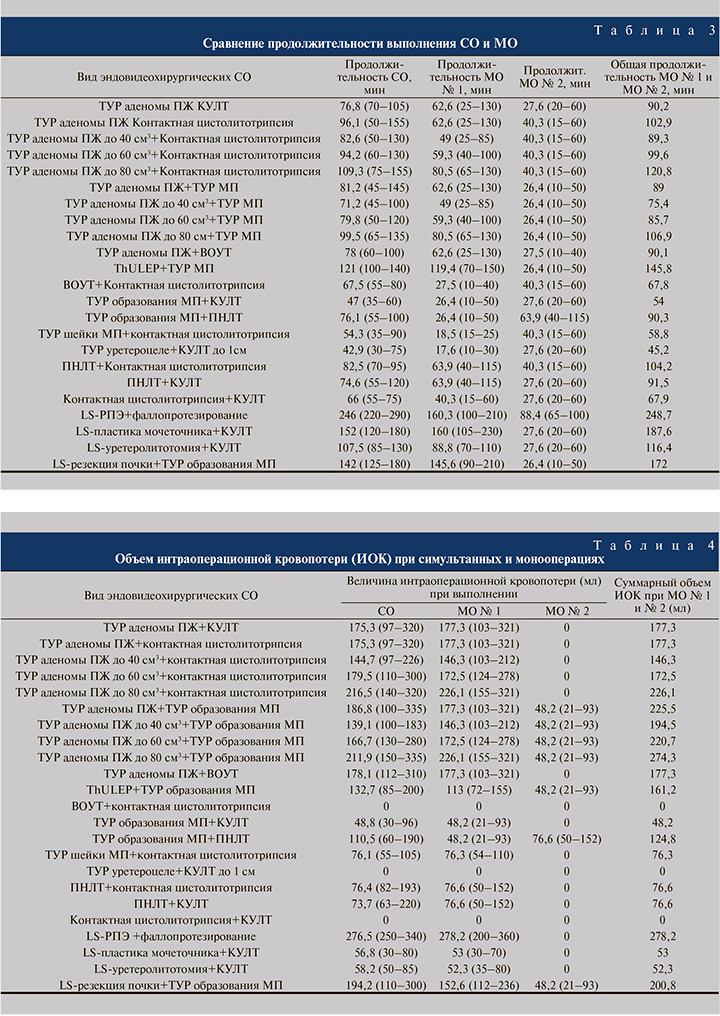
Как видно из представленных данных, продолжительность СО во всех случаях была меньше, чем суммарная продолжительность аналогичных, но отдельно выполненных оперативных пособий. Так, например, при симультанном выполнении ПНЛТ и контактной цистолитотрипсии (n=12) вмешательство продолжалось в среднем 82,5 (70–95) мин, тогда как раздельное проведение ПНЛТ (n=252) и контактной цистолитотрипсии (n=1056) потребовало в среднем 63,9 (40–115) и 40,3 (15–60) мин соответственно. Таким образом, суммарная продолжительность ПНЛТ и контактной цистолитотрипсии, выполненных раздельно, составила 104,2 (55– 175) мин, что на 20,8% дольше продолжительности соответствующей симультанной операции (р=0,0415). Сокращение времени, потраченного на выполнение двух хирургических вмешательств за счет проведения их в один «операционный сеанс», наблюдалось во всех случаях, анализированных в данном исследовании. Длительность СО была короче, чем суммарная продолжительность соответствовавших МО, при симультанном выполнении лапароскопической пластики мочеточника и КУЛТ (на 18,98%), ПНЛТ и КУЛТ (на 18,48%), лапароскопической резекции почки и ТУРобразования МП (на 17,44%), ТУР аденомы ПЖ и ВОУТ (на 13,43%), ТУР-образования МП и ПНЛТ (на 15,73%).
Группа пациентов, которым проводилась ТУР аденомы ПЖ совместно с ТУР-образованием МП или контактной цистолитотрипсией, дополнительно разделена на подгруппы в зависимости от размера оперируемой ПЖ. При симультанных ТУР аденомы ПЖ и контактной цистолитотрипсии продолжительность СО сократилась по сравнению с суммарной длительностью этих моноопераций на 7,50, 5,42 и 9,52% при объеме ПЖ до 40, 60 и 80 см3 соответственно. Аналогичные результаты получены в случаях симультанного выполнения ТУР аденомы ПЖ и ТУР опухоли МП: продолжительность вмешательств уменьшилась на 5,57, 6,88 и 9,22% при объеме ПЖ, не превысившем 40, 60 и 80 см3 соответственно.
Продолжительность симультанных ВОУТ и контактной цистолитотрипсии, РПЭ и фаллопротезирования, контактной цистолитотрипсии и КУЛТ была короче, чем суммарная продолжительность соответствовавших моновмешательств, на 0,44, 1,09 и 2,79% соответственно.
Как видно из данных, представленных в табл. 4, меньшие объемы ИОК во время выполнения СО по сравнению с таковыми в случаях МО отмечались для следующих разновидностей СО: 1) ТУР аденомы ПЖ и ТУР опухоли мочевого пузыря (МП), при выполнении которых «в один операционный сеанс», величина кровопотери была меньше, чем при раздельных МО, на 28,48, 24,4 и 22,75 % в зависимости от предоперационного объема ПЖ (до 40 см3, до 60 см3 и до 80 см3 соответственно); 2) ThULEP и ТУР опухоли МП, где получены аналогичные результаты; 3) ТУР опухоли МП и ПНЛТ, при симультанном проведении которых объем ИОК на 11,46 % меньше, чем при выполнении моноопераций.
Для ряда эндоскопических оперативных моновмешательств, таких как КУЛТ, ВОУТ, контактная цистолитотрипсия, фаллопротезирование, объем кровопотери установить не возможно ввиду слишком низкой концентрации гемоглобина в промывных водах (принимался за 0). Наибольшие различия в объеме кровопотери (4,25 %) выявлены при выполнении в один сеанс ТУР аденомы ПЖ и контактной цистолитотрипсии, наименьшие (0,26 %) – при симультанных ПНЛТ и контактной цистолитотрипсии. При выполнении всех рассматриваемых вмешательств, как симультанных, так и отдельно проводимых, всем пациентам устанавливался уретральный катетер. Во всех без исключения случаях СО наблюдалось значительное сокращение сроков дренирования МП (табл. 5). Так, например, у лиц, которым в составе СО проводилась ТУР аденомы ПЖ или опухоли МП, продолжительность дренирования МП становилась короче на 45,9% при ТУР ДГПЖ и ТУР опухоли МП (n=43), на 38,7% – при ТУР ДГПЖ и контактной цистолитотрипсии (n=92), на 47,9% – при ТУР ДГПЖ и КУЛТ (n=16), на 47,4% – при ThULEP и ТУР опухоли МП (n=15), на 53,8% – при ТУР опухоли МП и КУЛТ (n=16), на 55,8% – при ТУР опухоли МП и ПНЛТ (n=12).

Несколько в меньшей степени сокращался этот период при симультанном выполнении ТУР аденомы ПЖ и ВОУТ (n=16) – на 30,38%; ВОУТ и контактной цистолитотрипсии (n=18) на 28,68%; лапароскопической РПЭ и фаллопротезирования (n=13) на 23,71%.
Стоит обратить внимание на продолжительность дренирования МП при ТУР аденомы ПЖ, выполненной симультанно с контактной цистолитотрипсией (n=92) или с ТУР опухоли МП (n=43). Независимо от предоперационного объема ПЖ (до 40, 60 или 80 см3) в каждом из указанных случаев укорочение данного показателя произошло на 38,7 и на 45,9% соответственно. Частота ИВО со стороны органов мочеполовой системы в ближайшем периоде после симультанных и моноопераций показана в табл. 6.

Как видно из представленных данных, симультанные вмешательства не сопровождались инфекционными осложнениями по сравнению с монооперациями. Например, при выполнении «в один сеанс» лапароскопической РПЭ и фаллопротезирования (n=10) или в другом варианте – ТУР уретероцеле и КУЛТ (n=16), тогда как у лиц, перенесших только РПЭ или только КУЛТ, ИВО развивались в 5,5 и 11,2% случаев соответственно.
При симультанном проведении ТУР аденомы ПЖ и ВОУТ (n=16), ВОУТ и контактной цистолитотрипсии (n=18), ТУР образования МП и ПНЛТ (n=12), ПНЛТ и контактной цистолитотрипсии (n=12), контактной цистолитотрипсии и КУЛТ (n=17), лапароскопической пластики мочеточника и КУЛТ (n=13), ТУР аденомы ПЖ и КУЛТ (n=16); ThULEP и ТУР опухоли МП (n=15), ТУР опухоли МП и КУЛТ (n=16), ТУР шейки МП и контактной цистолитотрипсии (n=17), ПНЛТ и КУЛТ (n=12), лапароскопической уретеролитотомии и КУЛТ (n=12), а также других СО встречаемость ИВО в ближайшем периоде после операции была меньше, чем суммарная частота ИВО после соответствовавших раздельных вмешательств.
Различия в числе койко-дней после СО и соответствующих моноопераций (табл. 7) в среднем составили 1,04 койко-дня в пользу симультанных вмешательств. В большей степени сокращение койко-дня отмечено у пациентов, перенесших одновременно ТУР уретероцеле и КУЛТ (n=16), на 54,55%, ТУР аденомы ПЖ (с предоперационным объемом ПЖ не более 40 см3) и ТУР опухоли МП (n=12) на 32%; ТУР опухоли МП и ПНЛТ (n=12) на 50%; ПНЛТ и контактную цистолитотрипсию (=12) на 40 %. В меньшей степени эти изменения касались ТУР аденомы ПЖ (с предоперационным объемом органа не более 60 см3) и ТУР образования МП (n=17) на 16 %.
При проведении рассматриваемых хирургических вмешательств, как симультанных, так и раздельных, использовали два вида анестезиологического пособия: СМА и ЭТН. Как показано в табл. 8, у всех пациентов, перенесших СО в условиях СМА (n=352), продолжительность периода индукции анестезии составила в среднем 12,0 (6,9–17,7) мин, т.е. была примерно в 2 раза меньше, чем при соответствующих раздельных вмешательствах, – 24,3 (15,4–41,5) мин.
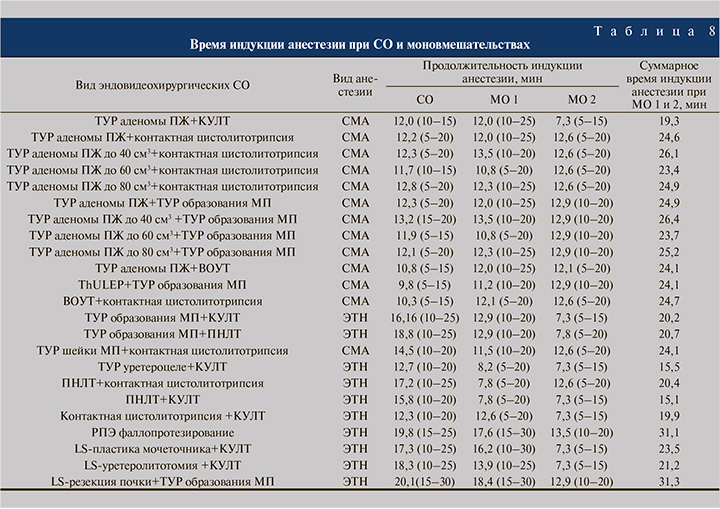
В большей степени данный показатель снизился при симультанном выполнении ThULEP и ТУР опухоли МП (на 59,34%, n=15) и ВОУТ в сочетании с контактной цистолитотрипсией (на 58,30%, n=18), в меньшей – при одновременном проведении ТУР шейки МП и контактной цистолитотрипсии (на 39,83%, n=17), а также ТУР аденомы ПЖ и КУЛТ (на 37,82%, n=16).
Эндотрахеальный наркоз использовался при проведении СО (ТУР образования МП и КУЛТ, ТУР МП и ПНЛТ, РПЭ и фаллопротезирование, лапароскопическая резекция почки и ТУР опухоли МП и др.) 130 пациентам. Из них у 118 (90,77%) человек отмечен более короткий период индукции анестезии по сравнению с вариантами раздельного оперирования. Различия в значениях показателей для СО и моновмешательств составили 35,78% при выполнении лапароскопической резекции почки и ТУР опухоли МП (n=10), 36,33% для РПЭ и фаллопротезирования (==10), 38,19 % при контактной цистолитотрипсии и КУЛТ (n=17), 20% для ТУР опухоли МП и КУЛТ, 26,38% для лапароскопической пластики мочеточника и КУЛТ (n=13), 9% для ТУР опухоли МП и ПНЛТ (n=12), 15,7% ПНЛТ и контактной цистолитотрипсии (n=12); 13,7% при лапароскопической уретеролитотомии и КУЛТ (n=12) и 18% при ТУР уретероцеле и КУЛТ (n=16). При симультанном проведении ПНЛТ и КУЛТ (n=12) продолжительность периода индукции анестезии практически не отличалась от таковой при монооперациях.
У всех больных, которым симультанные вмешательства выполнялись в условиях ЭТН (сь130), продолжительность периода пробуждения (выведения из анестезии) варьировала от 10,5 до 21,3 мин (5–35 мин) и в каждом случае была статистически значимо короче, чем при монооперациях (табл. 9).

Так, например, различия в пользу СО между значениями рассматриваемых показателей при симультанном и двухэтапном выполнениях РПЭ и фаллопротезирования (n=10), ТУР опухоли МП и КУЛТ (n=16), ТУР уретероцеле и КУЛТ (n=16), лапароскопической уретеролитотомии и КУЛТ (n=12) составили 37,54, 35,98, 33,53 и 33,48% соответственно. Этапы выведения пациентов из наркоза после сочетанных ТУР МП и ПНЛТ (n=12), ПНЛТ и КУЛТ (n=12) были короче, чем суммарное время пробуждения после раздельных ТУР МП и ПНЛТ; ПНЛТ и КУЛТ на 30,81 и 29,56% соответственно. Длительность периода пробуждения после симультанных ПНЛТ и контактной цистолитотрипсии (n=12), лапароскопической пластики мочеточника и КУЛТ (n=13), лапароскопической резекции почки и ТУР опухоли МП (n=10) также сократилась по сравнению со временем пробуждения после МО (хотя и в меньшей степени) на 20,86, 17,39 и 13,41% соответственно.
Таким образом, при плановом оперативном лечении сочетанных заболеваний почек и мочевыводящих путей (одновременном и раздельном) в случаях с применением СО регистрировались лучшие периоперационные результаты, чем у лиц, перенесших двухэтапное хирургическое лечение.
Это выражалось:
- в ме́ньшей продолжительности СО у всех пациентов;
- в меньшем (до 32%) объеме интраоперационной кровопотери у 64,3% больных;
- в сокращении срока дренирования МП уретральным катетером в 100% случаев;
- в ме́ньшей частоте встречаемости ранних ИВО со стороны органов мочеполовой системы у 100% пациентов (при этом после симультанного выполнения ТУР уретероцеле и КУЛТ, а также РПЭ и фаллопротезирования ИВО не было зарегистрировано вовсе);
- в сокращении числа послеоперационных койко-дней у всех пациентов;
- в уменьшении продолжительности периода индукции СМА в 2 раза у 100% пациентов;
- в уменьшении периода времени введения в ЭТН в 90,77% случаев и сокращении срока выведения из ЭТН.
Очевидно, что отмеченные преимущества СО перед соответствовавшими монооперациями служат важным фактором повышения качества хирургической помощи за счет снижения периоперационной травмы и негативного психоэмоционального перенапряжения пациентов, ме́ньшего риска развития анестезиологических и послеоперационных инфекционно-воспалительных осложнений, более раннего возврата больных к активному образу жизни, уменьшения финансовых затрат со стороны как пациентов, так и лечебных учреждений.
Заключение. Результаты проведенного исследования подтверждают факт целесообразности, правомерности и необходимости более широкого использования симультанных вмешательств при плановом хирургическом лечении сочетанных заболеваний урологического профиля.


