Согласно опубликованным в 2023 г. данным Всемирной организации здравоохранения (ВОЗ), бесплодие – это широко распространенная проблема, с которой в течение жизни в среднем сталкиваются 17,5% жителей Земли – мужчин и женщин, проживающих на разных континентах, в странах с различными уровнями развития экономики и доступности медицинской помощи [1]. За последние годы появились публикации, свидетельствующие о снижении числа и концентрации сперматозоидов в эякуляте мужчин в большинстве стран мира, включая РФ [2 3], а также о негативном влиянии неблагоприятных факторов окружающей среды и образа жизни мужчин на параметры эякулята и функциональные характеристики сперматозоидов [4]. Принимая во внимание сокращение численности населения и снижение рождаемости в нашей стране, а также с учетом увеличения числа бесплодных мужчин, негативные социальные последствия проблемы бесплодия для пары задача сохранения и восстановления репродуктивного здоровья является актуальной и с учетом выявленных тенденций требующей безотлагательного решения [5].
Исследования последних лет существенно расширили представления о многообразии механизмов, обеспечивающих реализацию репродуктивной функции на организменном, клеточном и молекулярном уровнях. Установлено, что вероятность наступления беременности зависит от множества мужских и женских факторов, определяющих сексуальную активность и созревание гамет, продвижение сперматозоидов и их взаимодействие с яйцеклеткой в женских половых путях, образование зиготы, а также последующее развитие эмбриона и его имплантацию в эндометрий. В связи с этим для получения полноценного представления о состоянии репродуктивного здоровья столкнувшихся с проблемой бесплодия пациентов и поиска способов коррекции обнаруженных нарушений требуется разработка и внедрение методов диагностики, позволяющих выявлять не только состояние органов и систем организма, но и функциональные характеристики половых клеток, особенности структуры молекул ДНК, а для преодоления проблемы бесплодия – междисциплинарного подхода с привлечением профессиональных компетенций врачей разных специальностей: урологов, акушеров-гинекологов, генетиков, эндокринологов, гематологов, терапевтов, врачей лабораторной диагностики, биологов и др.
С целью объединения усилий специалистов разного профиля и стандартизации подходов к проблеме бесплодия у мужчин по инициативе Российского общества урологов и главного внештатного уролога МЗ РФ академика Д. Ю. Пушкаря была сформирована наша междисциплинарная рабочая группа, которая разработала российские клинические рекомендации (КР) по мужскому бесплодию, они были одобрены Научно-практическим советом МЗ РФ, размещены на сайте-рубрикаторе и действуют с 1 января 2022 г. по настоящее время [6].Так как база медицинских знаний постоянно обновляется, приказом МЗ РФ определена необходимость пересмотра действующих положений КР и уровней их убедительности на регулярной основе – не реже 1 раза в 3 года с учетом достоверности полученных новых данных. В связи с этим по инициативе членов группы в программы научно-образовательных мероприятий федерального и регионального уровней неоднократно были включены доклады и дискуссии по вопросам профилактики и диагностики нарушений репродуктивной функции, лечения мужчин при бесплодии в паре, а также использования терминов и определений. Фрагменты этих обсуждений представлены в настоящей статье с целью привлечения внимания к актуальным вопросам репродуктивной медицины и поиску возможных путей их решения.
Определение бесплодия. Кодирование бесплодия согласно Международной классификации болезней (МКБ).
Эксперты российских профессиональных сообществ урологов и акушеров-гинекологов разместили в КР по мужскому и женскому бесплодию [6, 7] разработанное в 2017 г. международной группой специалистов научно-обоснованное определение бесплодия: «заболевания, характеризующегося невозможностью достичь клинической беременности после 12 мес. регулярной половой жизни без контрацепции вследствие нарушения способности субъекта к репродукции, либо индивидуальной, либо совместно с его/ее партнером» [8]. Его неоспоримым достоинством является формирование представлений о паре мужчина–женщина как о единице репродуктивного здоровья, необходимости проведения их одновременного обследования и согласованного междисциплинарного взаимодействия при составлении плана лечения, направленного на рождение здорового ребенка. К его недостаткам можно отнести невозможность использования для обозначения основного диагноза (в том числе и ввиду отсутствия соответствующего бесплодию у пары кода МКБ-10) у обратившихся за консультацией мужчин, а также дихотомичность распределения значений (есть бесплодие или нет бесплодия) в границах заданного интервала времени, не позволяющую обозначить вариабельность различных и рекомендованных к количественной оценке показателей репродуктивной функции. Принимая во внимание приоритет профилактической медицины в вопросах сохранения репродуктивного здоровья, а также с учетом включения в программу государственных гарантий бесплатного оказания медицинской помощи диспансеризации мужчин по оценке репродуктивного здоровья представляется целесообразным дополнить КР фрагментами, позволяющими отразить тактику действий врача, направленных на выявление и устранение возможных нарушений репродуктивной функции до того, как пара столкнется с бесплодием.
Термин «репродуктивная функция» давно и широко используется в биологии и медицине для обозначения совокупности всех биологических процессов организма, приводящих к появлению новых организмов. Состояние этой функции может быть оценено путем измерения ряда клинических показателей, снижение которых можно обозначить как «недостаточность репродуктивной функции», или «репродуктивная дисфункция». МКБ-10 позволяет кодировать обращения к врачу с целью получения заключения о состоянии репродуктивной функции или проведения преконцепционной подготовки (Z31.6 «Общее консультирование и советы по восстановлению детородной функции»), в клиническом диагнозе также необходимо воспользоваться формулировкой «бесплодие в паре» для обоснования планов последующего обследования и лечения.
Из практики ведения бесплодных пар известно, что мужчины впоследствии могут добиться реализации репродуктивной функции как в существующих, так и в других отношениях, поэтому причисление всех мужчин, которым при попытках зачатия в течение 12 мес. не удалось добиться наступления беременности, к бесплодным представляется избыточной диагностикой. Помимо возможного искажения статистических данных и несоответствия требований к качеству оказанной медицинской помощи [9] такая гипердиагностика несет риски, связанные со здоровьем и даже жизнью пациентов. Так, было установлено, что распространенность депрессии среди мужчин с диагнозом «бесплодие» варьируется от 14 до 24%, что в свою очередь угнетает выработку тестостерона, нарушает сексуальную функцию и приводит к снижению показателей эякулята, замыкая таким образом в проблеме бесплодия порочный круг. Более того, у 1–2% считающих себя бесплодными мужчин отмечается суицидальная идеация [10–13].
Бесплодие у пары может быть вызвано абсолютным бесплодием (стерильностью) мужчины и/или женщины, однако чаще всего наблюдается относительное бесплодие, при котором имеется недостаточность репродуктивной функции мужчины и женщины по отношению друг к другу. Анализ КР, разработанных специалистами по репродуктивной медицине в разных странах мира, показал, что формулировка диагноза «мужское бесплодие» в них либо отсутствует, либо сведена к перечислению снижающих репродуктивную функцию и имеющих собственные коды в МКБ состояний в условиях отсутствия женской репродуктивной дисфункции [8]. Такие формулировки не получили широкого распространения, так как при описанных состояниях мужчина может оставаться фертильным, к тому же практически невозможно достоверно определить недостаточность репродуктивной функции мужчины по отношению к состоянию репродуктивного здоровья женщины. Международная группа экспертов ВОЗ предложила считать мужским бесплодием «любое заболевание репродуктивной системы мужчин, характеризующееся дисфункцией выброса спермы или отсутствием измеримого числа сперматозоидов в эякуляте» [14]. Так как это определение фактически соответствует понятию стерильности, т.е. абсолютного бесплодия, преимущества его практического применения очевидны – поставленный на основании таких критериев клинический диагноз легко обосновать как при информировании пациента, так и при подготовке ответов на официальные запросы. Оно также поможет избегать ненужных переживаний у мужчин с ненулевыми значениями репродуктивной функции, так как врач, вместо того чтобы называть их бесплодными, будет использовать понятия «недостаточность репродуктивной функции», или «репродуктивная дисфункция», которые способствовали появлению проблемы бесплодия у пары. При этом упоминание словосочетания «бесплодие в паре» в клиническом диагнозе позволит обосновать использование в отношении таких пациентов всего арсенала диагностических методов и лечебных мероприятий, описанных в КР «Мужское бесплодие». В истории урологии похожие решения об изменении терминологии уже принимали ранее по отношению к практике оказания медицинской помощи мужчинам с нарушениями эрекции, отказавшись при этом от использования термина «импотенция», оказывавшего негативное влияние на мужчин.
Однако предложенное экспертами ВОЗ определение мужского бесплодия также не лишено недостатков, так как не может быть применено в тех случаях, когда у всех обнаруженных сперматозоидов в эякуляте выявляются не позволяющие эффективно взаимодействовать с яйцеклеткой структурные или функциональные дефекты, например при 100%-ной некро-, астено- или глобулозооспермии, синдроме ацефалических сперматозоидов и др. В связи с этим члены рабочей группы начали обсуждение возможности дополнения определения, рекомендованного ВОЗ, формулировками, позволяющими расширить представление о формах мужского бесплодия [15].
Лабораторные методы исследования эякулята
Многие столкнувшиеся с проблемой бесплодия мужчины предъявляют результаты исследования эякулята уже при первичном визите к урологу. Этому в значительной степени способствуют появление доступной для пациентов информации по методам оценки репродуктивной функции в сети Интернета, а также появление КР по женскому бесплодию, согласно которым необходимо направлять партнера обратившейся женщины на проведение спермограммы и обследование врачом-урологом так, чтобы диагностика по поводу бесплодия началась у супругов одновременно.
Лабораторные методы исследования эякулята широко применяются в урологической практике, определение его параметров дает возможность получать важные для оценки репродуктивного здоровья мужчины сведения о функции яичек и добавочных половых желез, расстройствах семяизвержения, воспалительных заболеваниях половых органов и инфекций, передаваемых половым путем и др. [16]. Стандартизацией подходов к проведению исследований и обработке эякулята человека на протяжении многих лет занимаются эксперты ВОЗ [17], а в 2023 г. был разработан отечественный стандарт «Исследование качества спермы базовое». В дополнение к описанию методик лабораторной диагностики в последних изданиях руководства ВОЗ были представлены сведения о минимальных референсных значениях (5-й процентиль и 95%-й доверительный интервал) базовых показателей спермы, полученной в когорте фертильных мужчин [18]. Изучение региональных особенностей распределения и референсных показателей тестов, входящих в базовое исследование эякулята российских мужчин, было проведено в многоцентровом исследовании под руководством проф. В. А. Божедомова [15].
В связи с тем что вероятность зачатия связана с количеством, жизнеспособностью, подвижностью и морфологией сперматозоидов, всем мужчинам, обратившимся по поводу бесплодия, должно быть рекомендовано базовое исследование эякулята. Исследуемые показатели у мужчин в норме варьируются в широких пределах в зависимости от разнообразных причин, однако часто анализа одной порции спермы оказывается достаточно для составления общего представления о состоянии репродуктивной функции и необходимости проведения дальнейшего обследования или лечения [19–21]. В опубликованном в 2010 г. 5-м издании руководства ВОЗ были даны разъяснения о том, что параметры эякулята, лежащие в пределах 95% доверительного интервала, не гарантируют фертильности, а мужчины, чьи семиологические характеристики оказываются ниже минимальных референсных значений, не должны быть отнесены к категории бесплодных. Систематический обзор работ, авторы которого поставили перед собой цель определить характеристики эякулята, свидетельствующие о бесплодии, пришли к выводу о том, что к ним можно отнести лишь азооспермию и 100%-ную некро- и глобулозооспермию [22]. К сожалению, ложное представление о том, что несоответствие критериям нормозооспермии следует рассматривать как патологическое состояние или «мужской фактор бесплодия», получило широкое распространение. В связи с этим экспертной группой, в которую вошли российские специалисты – член-корреспондент РАН О. И. Аполихин и С. С. Красняк, было принято решение удалить из руководства ВОЗ издания 2021 г. фрагмент с терминами для описания различных видов патозооспермии и, отказавшись от написания лабораторных заключений, основанных на сопоставлении результатов тестов с референсными значениями, предложить интерпретировать полученные показатели клиницистам.
Несмотря на то что отдельные параметры спермы не позволяют отличать бесплодных мужчин от фертильных, совокупная оценка результатов тестов, входящих в базовое исследование эякулята, может предоставлять клинически полезную информацию. Российские и зарубежные исследователи выяснили, что наиболее информативными в отношении прогнозирования возможности зачатия естественным путем оказались расчетные показатели, отражавшие число подвижных сперматозоидов: вероятность наступления беременности от мужчин, имевших менее 1 млн и от 1 до 5 млн подвижных сперматозоидов в эякуляте, оказалась ниже по сравнению с теми, у кого этот показатель превышал значение в 5 млн (отношения шансов составили 0,371 (0,215–0,64) и 0,505 (0,307–0,832 соответственно) [15, 23, 24]. Кроме того, полученные при базовом исследовании эякулята значения могут оказаться ниже пороговых величин, определяющих необходимость проведения лабораторной и аппаратной диагностики, а также дальнейшую маршрутизацию мужчин, обратившихся по поводу бесплодия.
Исследования последних лет показали, что способность мужчины к воспроизведению потомства может снижаться под действием неблагоприятных химических и физических факторов окружающей среды, образа жизни, а также сопутствующих заболеваний. Оказалось, что одним из патогенетических механизмов снижения репродуктивной функции в таких случаях является оксидативный стресс – избыточное формирование активных форм кислорода (АФК), вызывающих повреждение клеточных структур, в частности фрагментацию ДНК сперматозоидов (ФДС), что в итоге приводит к нарушению функции сперматозоидов, а также повышает риски невынашивания беременности и развития наследственных дефектов у плода [25–28]. В связи с тем, что при отсутствии установленной причины бесплодия признаки оксидативного стресса выявляют у 80% мужчин, как и у 30–40% мужчин с нормозооспермией, международная группа экспертов в 2019 г. предложила дополнить классификацию новой категорией – «Мужское бесплодие, обусловленное оксидативным стрессом».
В настоящее время усилия исследователей направлены на разработку методов его диагностики, позволяющих получать точные и воспроизводимые результаты, а также способов лечения, основанных на принципах доказательной медицины [29–31].
Полученные данные обусловливают необходимость более широкого внедрения методов исследования функциональных характеристик сперматозоидов. При разработке руководства эксперты ВОЗ в 2021 г. к расширенным методам анализа отнесли расчеты индексов множественных дефектов сперматозоидов, тесты на фрагментацию ДНК и анеуплоидию сперматозоидов, определение содержания антиспермальных антител и незрелых сперматогенных клеток, измерение числа лейкоцитов, CD45 и цитокинов в сперме, биохимические тесты для оценки функции добавочных половых желез (измерение содержания цинка, фруктозы, альфа-гликозидазы), а также исследование последовательно выделившихся порций эякулята. К методам углубленного анализа были отнесены тесты на определение оксидативного стресса и АФК, оценку состояния акросом и акросомальных реакций, хроматина, трансмембранных ионных токов и ионного транспорта, а также компьютерный анализ эякулята. Представления о клиническом значении этих тестов все еще формируются, и по ряду вопросов эксперты профессиональных сообществ не сходятся во мнениях и дают противоречивые комментарии [32–34]. Законодательство некоторых стран позволяет при наличии информированного согласия использовать при обследовании пациентов не рекомендованные к применению в клинической практике тесты, которые в соответствии с мнением лечащего врача могут предоставлять необходимую для оказания медицинской помощи информацию. В РФ оказание медицинской помощи в соответствии с КР, одобренными Научно-практическим советом Минздрава, является ведущим критерием, определяющим качество и безопасность медицинской деятельности, поэтому они содержат только те диагностические тесты, которые ранее были утверждены в номенклатуре медицинских услуг. Из перечня, представленного руководством ВОЗ, в нее были включены спермограмма, тест «смешанная антиглобулиновая реакция сперматозоидов» и оценка фрагментации ДНК сперматозоидов. Над решением задачи по включению в номенклатуру остальных указанных в руководстве ВОЗ тестов работают эксперты под руководством главного внештатного специалиста Минздрава по репродуктивному здоровью мужчин члена-корреспондента РАН О. И. Аполихина.
Тест «смешанная антиглобулиновая реакция» или MAR-тест на наличие антиспермальных антител в сперме относятся к категории иммунологических, позволяют судить о наличии на поверхности сперматозоидов иммуноглобулинов IgA и IgG, снижающих фертильность. Продолжается дискуссия о том, какое значение теста следует считать достаточным для постановки диагноза иммунологического мужского бесплодия. Результаты недавно проведенного ретроспективного анализа данных более 10 тыс. пациентов показали, что мужчины, имевшие 50% сперматозоидов, покрытых антиспермальными антителами, не могли добиться зачатия только при наличии других снижающих репродуктивную функцию факторов, в то время как значение MAR-теста, равное 100%, могло быть единственной причиной бесплодия [35].
Оценка уровня ФДС позволяет получать представление о доле сперматозоидов в эякуляте, имеющих разрывы молекул ДНК. Для его проведения применяется несколько методов, наибольшее распространение получили TUNEL-тест (Terminal deoxynucleotidyl transferase dUTP nick end labelling), окраска акридиновым оранжевым и SCSA (sperm chromatin structure assay), Comet-анализ, тест на дисперсию хроматина и метод ник-трансляции. Отсутствие стандартизации выполнения этих исследований, различия мнений специалистов о пороговых значениях по каждому из них и различия значений, полученных при применении разных тестов для анализа одного и того же образца спермы, а также недостаток работ, позволяющих получить представление о том, как использовать полученный результат при составлении плана лечения пациентов, привели к появлению противоречий в КР, разработанных профессиональными сообществами.
Большинство экспертов не поддерживают назначение этого теста при первичном обследовании мужчин по поводу бесплодия, при этом результаты мета-анализов указывают на целесообразность оценки ФДС при необъяснимом бесплодии и привычном выкидыше [36, 33] и недостаточно доказанную ценность для прогнозирования успеха лечения с применением вспомогательных репродуктивных технологий (ВРТ) [37, 38]. Следуя указаниям ВОЗ, каждой лаборатории необходимо установить собственные референсные интервалы значений уровня ФДС в зависимости от применяемой методики и величин показателей прогностической ценности, рассчитанных по значениям теста пролеченных больных с учетом результатов этого лечения.
Лечение
Мужчинам, у которых по результатам проведенного обследования были выявлены признаки, свидетельствующие о возможности улучшения репродуктивной функции и устранения бесплодия, необходимо назначить лечение. Важным условием для начала лечения, целью которого является обеспечение последующего зачатия естественным путем, является согласование его плана с гинекологом. С этой целью при первичной консультации мужчины по поводу бесплодия урологу следует рекомендовать направить его партнершу на консультацию и обследование у гинеколога с целью оценки состояния и функции органов женской репродуктивной системы. В тех случаях, когда возникает необходимость проведения лечения с применением ВРТ, задачей для уролога становится составление плана мероприятий по обеспечению наилучшего состояния репродуктивной функции мужчины к началу протокола – преконцепционная подготовка, персонифицированная с учетом всех имеющихся факторов образа жизни, среды обитания и заболеваний и др. Она нередко требует междисциплинарного взаимодействия с терапевтами, эндокринологами, генетиками и согласования с гинекологом с учетом плана лечения женщины.
Анализ результатов обследования мужчин, обратившихся за медицинской помощью в связи с невозможностью зачатия естественным путем, показал, что чаще всего встречается бесплодие, причины которого остались невыясненными. В связи с тем что несоответствие результатов тестов при базовом исследовании эякулята референсным значениям, предложенным в руководствах ВОЗ, не свидетельствует о мужском бесплодии, формулировки определений идиопатического бесплодия (бесплодие, при котором после обследования причины снижения показателей эякулята остаются нераспознанными) и необъяснимого бесплодия (бесплодие у мужчин с нормозооспермией при отсутствии женских факторов бесплодия) представляются устаревшими. Этим близким между собой понятиям, вероятно, можно дать общее определение как бесплодия, причины которого остаются нераспознанными после проведенного обследования.
В арсенале врача имеется большой выбор препаратов для эмпирической терапии у таких пациентов, к ним относятся антиэстрогены, гонадотропины, витамины, минеральные добавки, метаболические средства – аминокислоты и их производные, а также пептидные препараты. Исследования, проведенные в России и за рубежом, показали, что они способствуют улучшению количественных и качественных показателей спермы, повышению частоты наступления беременности и рождения ребенка. Однако научная доказательность их эффективности в настоящее время не позволяет точно ответить на вопросы: что делать, кому делать и с какой целью делать, с целью формулировки КР. Чаще всего эти работы лишь свидетельствуют о достоверности различий показателей в группе пролеченных больных при сравнении с группой, получавшей плацебо. Так как на основании российских КР формируются стандарты оказания медицинской помощи, необходимо продолжение работ в этом направлении для получения представлений о типовых моделях нуждающихся в терапии пациентов и о том, какая доля получивших лекарство, может достигнуть конечной цели лечения – рождения ребенка [39–43]. Кроме того, при оценке возможности включения в план лечения этих лекарственных средств с целью улучшения репродуктивной функции мужчин необходимо учитывать, что принятая в некоторых медицинских организациях практика согласования их применения в соответствии с показателями (характеристиками), не указанными в инструкции по применению, нелегитимными решениями врачебной комиссии не устраняет риски, имеющиеся у лечащего врача.
Для повышения репродуктивного потенциала мужчин с варикоцеле может применяться оперативное лечение с целью как обеспечения зачатия естественным путем, так и повышения вероятности успеха применения ВРТ. Большинство исследователей подтверждают, что хирургическая коррекция клинически значимого варикоцеле может приводить к повышению числа, подвижности, доли нормальных форм сперматозоидов и снижению фрагментации содержащихся в них молекул ДНК. При этом выводы авторов о преимуществах такого лечения для повышения вероятности зачатия или рождения ребенка противоречивы [44–49].
Развитие представлений о роли оксидативного стресса в реализации снижающего репродуктивную функцию эффекта варикоцеле привело к появлению консервативных подходов к лечению варикоцеле в расчете на подавление патогенетических механизмов угнетения сперматогенеза, снижения влияния АФК и повышения репродуктивного потенциала. Отечественным авторам удалось продемонстрировать заметные преимущества лечения пациентов с варикоцеле антиоксидантами без операции в достижении показателя рождения ребенка [50]. С учетом противоречивости мнений специалистов и данных, полученных разными исследовательскими группами, возможно, что решение о целесообразности проведения лечения по поводу варикоцеле у мужчины при бесплодии следует рекомендовать принимать индивидуально с учетом клинической значимости варикоцеле, принимая во внимание все аспекты состояния репродуктивной функции обоих супругов и личный опыт врача.
К показаниям к хирургическому получению сперматозоидов относятся необструктивная и обструктивная азооспермии; расстройства эякуляции (аспермия, ретроградная эякуляция), 100%-ная некрозооспермия. Врачам-урологам предоставлена возможность выбора оптимального для каждого пациента способа получения сперматозоидов для последующего использования в программах ВРТ (чрескожных и открытых биопсий), в том числе и с применением 6–25-кратного оптического увеличения и микрохирургической техники [51–53]. Также появились предложения в связи с меньшей ФДС применять для ИКСИ (ICSI – Intra Cytoplasmic Sperm Injection) сперматозоиды, полученные из яичек мужчин с повторными неудачными протоколами ВРТ и повышенным значением этого показателя. Несмотря на то что этот подход до сих пор считается экспериментальным и доказательность его использования в рутинной клинической практике еще не достаточна, целесообразно предложить возможность применения такого лечения у отобранных пациентов по решению врачебной комиссии [54, 55].
Другим вопросом для дискуссии с коллегами-специалистами по применению ВРТ может быть дополнение перечня ограничений для проведения женщине программы экстракорпорального оплодотворения (ЭКО) некоторыми клиническими признаками мужчин – их супругов или партнеров, например азооспермией, аспермией, 100%-ной некроспермией до их устранения путем получения сперматозоидов хирургическим путем или применения донорской спермы. Это, в частности, позволит поставить перед парой вопрос о необходимости получить информированное добровольное согласие на применение донорской спермы до начала лечения и при отрицательных результатах биопсий яичек и позволит избегать нерационального использования средств обязательного медицинского страхования (ОМС) в парах, не согласных на ее применение.
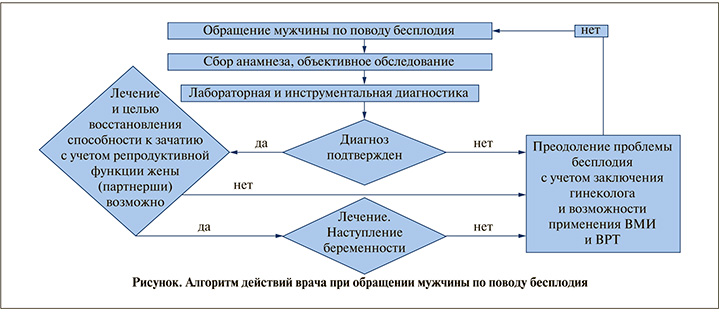
Кроме того, в связи с тем что не только при естественном зачатии, но и при применении лечения с использованием ВРТ, от состояния репродуктивной функции мужчин непосредственно зависят результаты оплодотворения ооцитов, развитие эмбриона, вероятность наступления и вынашивания беременности, представляется целесообразным закрепить в КР по мужскому и женскому бесплодию, а также привычному выкидышу положения, указывающие на целесообразность консультации мужчин врачом-урологом как во всех случаях выявления бесплодия, так и после неудачных протоколов ЭКО, доля которых, к сожалению, на протяжении последних лет остается стабильно высокой. Такая консультация может быть полезной для уточнения причин неудач и назначения преконцепционной подготовки с целью повышения вероятности успеха последующего лечения [56, 57]. Дополненный этими предложениями алгоритм действий врача при обращении мужчины по поводу бесплодия представлен на рисунке. Следуя алгоритму, после постановки клинического диагноза, обоснованного результатами проведенного обследования, необходимо назначать лечение по поводу выявленных заболеваний и оценивать вероятные перспективы и сроки восстановления репродуктивной функции и последующего зачатия естественным путем. Их необходимо сопоставлять с возможностью сохранения в течение этого времени репродуктивной функции жены (партнерши) с учетом результатов ее обследования врачом-гинекологом, и при наличии показаний принять решение о преодолении бесплодия у пары с применением ВРТ.
В завершение хотелось бы выразить надежду, что совместными усилиями представителей различных профессиональных сообществ по итогам коллегиального междисциплинарного обсуждения специалистами по репродуктивной медицине мы сможем на основе клинических рекомендаций и используя персонифицированные подходы к лечению постоянно совершенствовать медицинскую помощь парам, стремящимся к рождению здорового ребенка. Мы предлагаем читателям журнала «Урология» принять участие в обсуждении представленных в этой статье дискуссионных вопросов, присылать свои комментарии и предложения в адрес Российского общества урологов: mail@ooorou.ru



