Введение. Хронический простатит (ХП) – наиболее распространенное урологическое заболевание среди мужчин в возрасте от 20 до 40 лет [1–4].
Согласно классификации Национального института здоровья США [5], выделяют четыре категории простатита:
- категория I: острый простатит – острая инфекция предстательной железы;
- категория II: хронический бактериальный простатит (ХБП);
- категория III: хронический абактериальный простатит/синдром хронической тазовой боли:
- категория IIIА: воспалительный синдром хронической тазовой боли;
- категория IIIВ: невоспалительный синдром хронической тазовой боли;
- категория IV: бессимптомный простатит.
Частота отдельных форм простатита в популяции различна. Так, острый бактериальный простатит (ОБП) встречается в 5–10% случаев, ХБП – в 5–10%, хронический абактериальный простатит/синдром хронической тазовой боли – в 80–90% [6].
Наиболее часто возбудителями ХБП являются представители семейства Enterobacteriaceae. Штаммы E. coli вызывают ХБП в 65–80% наблюдений, различные виды Serratia, Klebsiella, Proteus, Enterobacter, Acinetobacter – в 10–15%. Большинство исследователей считают, что на долю Enterococcus faecalis приходится от 5 до 10% подтвержденных инфекций простаты [5]. По данным М. И. Когана и соавт. [7], в этиологической структуре ХБП доминировали неклостридиальные анаэробы, которые обнаруживали у 100% больных; коагулазонегативные стафилококки выделяли из секрета предстательной железы у 88% пациентов, коринеформные бактерии – у 65%. Доля представителей семейства Enterobacteriaceae, которые, по данным отечественных и зарубежных исследователей, признаны ведущим этиологическим фактором бактериального простатита, была незначительной (10%) [7, 8].
Диагностический алгоритм лабораторных исследований при ХП включает оценку анамнестических данных, объективных и субъективных симптомов, пальцевое ректальное исследование предстательной железы, общий анализ мочи, бактериологический анализ средней порции мочи, исключение атипичной внутриклеточной инфекции методами полимеразной цепной реакции, микроскопию секрета простаты, бактериологическое исследование трех порций мочи и секрета (тест, предложенный Meares-Stamey в 1968 г.) [9]. Тест Meares-Stamey считается трудным к применению в урологической практике и, по мнению ряда авторов, может быть заменен на двустаканную пробу [10]. Для больных старше 45 лет целесообразно определение уровня общего простатического специфического антигена (ПСА) сыворотки крови с целью ранней диагностики рака предстательной железы.
 Перспективным методом диагностики является также иммуногистохимическое исследование, позволяющее выявлять тип тканевой реакции и определять стадию воспалительного процесса, которые коррелируют с категориями хронического простатита. Оно позволяет оценивать степень агрессивности воспалительного процесса, что имеет важное прогностическое значение. Кроме того, с помощью иммуногистохимического исследования определяются изменения местного иммунитета, способствующие поддержанию воспалительного процесса [11].
Перспективным методом диагностики является также иммуногистохимическое исследование, позволяющее выявлять тип тканевой реакции и определять стадию воспалительного процесса, которые коррелируют с категориями хронического простатита. Оно позволяет оценивать степень агрессивности воспалительного процесса, что имеет важное прогностическое значение. Кроме того, с помощью иммуногистохимического исследования определяются изменения местного иммунитета, способствующие поддержанию воспалительного процесса [11].
Антимикробные препараты группы фторхинолонов на сегодняшний день являются средством выбора для лечения ХБП. Согласно Российским национальным рекомендациям по антимикробной терапии и профилактике инфекций почек, мочевыводящих путей и мужских половых органов, опубликованным в 2013 г., препаратами выбора для лечения ХБП являются левофлоксацин, офлоксацин и ципрофлоксацин [12]. При ХБП левофлоксацин назначают по 500 мг 1 раз в сутки, а офлоксацин и ципрофлоксацин – по 400 мг 2 раза и по 500 мг 2 раза в сутки соответственно в течение 3–4 нед.
Между тем изолированная антибактериальная терапия нередко оказывается малоэффективной при лечении ХБП. При выявлении микроорганизма, являющегося причиной бактериального простатита, нередко приходится использовать несколько лекарственных препаратов, действующих на разные звенья патогенеза заболевания: уменьшающих отек тканей предстательной железы, нормализующих кровообращение в ней, устраняющих спазм ее гладкомышечных элементов и нормализующих иммунные реакции.
В числе препаратов животного происхождения, обладающих этими свойствами, – витапрост®, витапрост® форте, в состав которых входит комплекс водорастворимых биологически активных пептидов, выделенных из предстательной железы ткани простаты быков и бычков, достигших половой зрелости. Было доказано, что эти препараты оказывают органотропное действие, т.е. влияют на процессы дифференцировки в популяции клеток, из которых они выделены. Кроме того, они обладают противовоспалительными и иммуномодулирующим эффектами, усиливают синтез антигистаминовых и антисеротониновых антител, улучшают микроциркуляцию в пораженном органе.
В течение продолжительного времени лекарственные средства при лечении больных ХБП применяют в различных сочетаниях. Как правило, основной целью при этом остается повышение эффективности лечения, а в ряде случаев – и улучшение его переносимости. В настоящее время существует масса готовых комбинированных и комплексных лекарственных препаратов, в том числе и антимикробных. Данные препараты призваны оптимизировать фармакотерапию и расширять ее границы [13]. Так или иначе, при каждом новом появлении на отечественном рынке такого препарата возлагаются надежды на его высокую клиническую и бактериологическую эффективность, на благоприятный профиль безопасности его компонентов, обеспечивающих долгосрочное успешное применение в клинической практике. В связи с вышеизложенным в контексте проблемы лечения ХБП особый интерес представляет успешно применяющийся в отечественной практике препарат, проявляющий антибактериальную активность и позволяющий воздействовать на различные звенья патогенеза, в виде ректальных суппозиториев – витапрост® плюс. Один суппозиторий содержит: простаты экстракт – 100 мг (в пересчете на водорастворимые пептиды – 20 мг), ломефлоксацина гидрохлорид – 400 мг и вспомогательное вещество – основу для суппозиториев (витепсол) – достаточное количество для получения суппозитория массой 2,25 г.
Доклиническое изучение сочетания простаты экстракта и ломефлоксацина подтвердило целесообразность разработки данной ректальной формы.
В исследовании, выполненном в ГУ НИИ фармакологии им. В. В. Закусова РАМН лабораторией фармакокинетики в 2005 г., изучали сравнительную фармакокинетику и относительную биодоступность ломефлоксацина после однократного введения кроликам витапроста® плюс, суппозитории ректальные и ломефлоксацин, таблетки, покрытые оболочкой. Установлено, что после однократного введения ломефлоксацина кроликам в виде ректальных суппозиториев препарат достигает системного кровотока. Уровни максимальных концентраций ломефлоксацина в плазме крови животных после орального и ректального введения были сопоставимыми – 5,65±2,11 и 4,75±1,86 мкг/мл соответственно. По скорости всасывания между изучаемыми лекарственными формами ломефлоксацина достоверных различий не обнаружено. Время достижения максимальной концентрации препарата в плазме крови для ломефлоксацина, таблеток, составило 3,6±1,2 ч, для суппозиториев витапрост® плюс – 3,9±1,0 ч. Относительная биодоступность витапроста® плюс по отношению к ломефлоксацину в таблетках в среднем составила 68,7% [14].
В открытом сравнительном рандомизированном клиническом исследовании эффективности и безопасности препарата витапрост® плюс, суппозитории ректальные (ОАО «Нижфарм»), по сравнению с препаратом ломефлоксацин, таблетки, покрытые пленочной оболочкой, больным ХБП показано, что применение комбинированного лекарственного средства витапрост® плюс приводит к уменьшению интенсивности воспалительного процесса в предстательной железе, что проявляется более выраженным по сравнению с изолированной антимикробной терапией ломефлоксацином снижением количества лейкоцитов в секрете ПЖ [15].
Как в основной, так и в контрольной группе 27 (72,97%) пациентами была достигнута эрадикация чувствительных к ломефлоксацину микроорганизмов. Однако после курса лечения витапростом® плюс число больных персистируюшей инфекцией оказалось ниже, чем в контрольной группе, – 4 (10,81%) и 7 (18,92%) соответственно. Применение витапроста® плюс способствовало также более выраженному уменьшению симптомов ХП в целом и болевого симптома в частности, выявленных при анкетировании с помощью шкалы NIH-CPSI; повышало клиническую эффективность лечения, что подтверждено комплексной оценкой терапии как врачом, так и самими пациентами [15].
Целью настоящего исследования являлась оценка эффективности и безопасности лекарственного препарата витапрост® плюс, суппозитории ректальные, в лечении пациентов с ХБП, проведенная в условиях реальной клинической практики.
Материалы и методы. Работа выполнена в 2012 г. на базе Окружного урологического отделения ГБУЗ ГП № 69 ДЗМ. В исследовании приняли участие 60 пациентов с ХП II типа.
Диагноз был установлен на основании данных анамнеза, жалоб, осмотра, анкетирования пациентов с помощью шкалы NIH-CPSI, в том числе и оценки качества жизни. Микробиологическое исследование секрета ПЖ проведено перед началом и после его окончания. Этиологическая роль выделенного возбудителя считалась доказанной, если в секрете простаты выявляли уропатогенные бактерии в титре 103 КОЕ/мл или более. Обязательным условием для включения пациента в исследование была чувствительность выявленной культуры к ломефлоксацину.
Всем пациентам было проведено цитоиммуногистохимическое исследование секрета предстательной железы, при котором выявлены изменения, характерные для ХБП. Также выполняли трансректальное УЗИ простаты с допплерографией, урофлоуметрию до и после лечения. Проводили исследование мазка из уретры на наличие Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum методом ПЦР, клинические и биохимические лабораторные исследования крови и мочи. У всех пациентов старше 45 лет для исключения рака простаты однократно определяли уровень общего ПСА в сыворотке крови.
Пациенты были рандомизированы на две сопоставимые группы по 30 человек. Пациенты основной группы (средний возраст – 39,3±11,5 года) получали витапрост® плюс, суппозитории ректальные, по 1 суппозиторию 1 раз в сутки в течение 30 дней, пациенты контрольной группы (средний возраст – 45,5±16,3 года) – ломфлокс, таблетки, покрытые оболочкой, по 400 мг 1 раз в сутки в течение 30 дней.
Клиническую эффективность проводимого лечения оценивали по динамике выраженности симптомов ХП на основании данных шкалы-опросника NIH-CPSI, состоящей из 9 вопросов, разделенных на 3 домена: боль (1–4-й вопросы); расстройства мочеиспускания (5-й и 6-й вопросы); качество жизни (7–9-й вопросы). При этом оценивали как отдельные домены, так и общую сумму баллов.
Статистическую обработку данных проводили с помощью программного обеспечения BioStat 2009. Использовали непараметрические методы статистики: тест Уилкоксона для зависимых выборок и тест Манна–Уитни для независимых выборок.
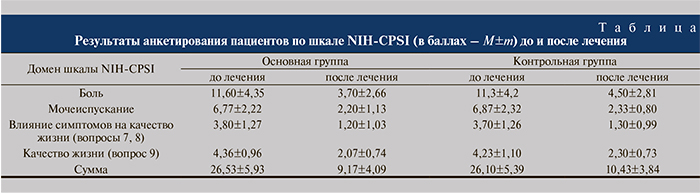
Результаты и обсуждение. Статистически значимое (p<0,05) снижение баллов после терапии зарегистрировано по каждому домену опросника и по результатам суммарной оценки в обеих группах (см. таблицу). Отмечено более выраженное снижение болей и улучшение качества жизни пациентов основной группы. Так, выраженность болей уменьшилась в основной группе с 11,6±4,35 до 3,7±2,66 балла, в контрольной – с 11,3±4,2 до 4,5±2,81 балла. Улучшение качества жизни было более выраженно в первой группе (уменьшение показателя с 4,36±0,96 до 2,07±0,74) по сравнению с контрольной группой (с 4,23±1,1 до 2,3±0,73 балла). Таким образом, применение витапроста® плюс привело к более выраженному уменьшению симптоматики ХП в целом и болевого симптома в частности, а также к улучшению качества жизни, выявленному при анкетировании с помощью шкалы симптомов ХП NIH-CPSI.
Выраженность противовоспалительного эффекта препарата оценивали на основании результатов микроскопического исследования секрета предстательной железы.
Среднее количество лейкоцитов в поле зрения больных основной группы до лечения составило 22,23±18,44, контрольной – 21,97±16,48. Таким образом, до лечения группы по данному показателю статистически значимо не различались.
В результате проведенного лечения в обеих группах произошло достоверное снижение количества лейкоцитов: в основной группе – до 8,32 ± 7,8, в контрольной – до 13,1±11,8 (p<0,01) в поле зрения. При этом в основной группе отмечено более существенное уменьшение количества лейкоцитов (p<0,05). Таким образом, более выраженный противовоспалительный эффект был достигнут на фоне применения витапроста® плюс.
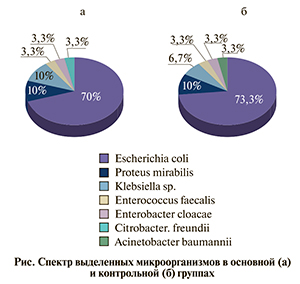
Данные о спектре выделенных микроорганизмов по результатам микробиологического исследования представлены на рисунке. В основной группе эрадикация возбудителей достигнута 22 (73,3%) больными, в контрольной – 21 (70%).
Цитоиммуногистохимическое исследование секрета предстательной железы выполнялось до и после лечения. До лечения в обеих группах выявлены изменения, характерные для ХП II типа: повышенная концентрация поли- и мононуклеаров, выраженная экссудативная реакция, провоспалительная ориентация воспалительной реакции со сниженной стимуляцией пролиферации эпителиальных и лимфоидных клеток. После лечения в основной группе отмечен ряд сдвигов, которые могут быть отнесены к положительным реакциям. Существенно снизился лейкоцитоз (количество полиморфноядерных лейкоцитов). Этот параметр в ситуации бактериального простатита является объективным показателем снижения выраженности альтернативных изменений в ткани простаты. Снизились показатели агрессивности инфильтрата (концентрация CD8 и CD16 – т.е. мононуклеаров, обладающих киллерными потенциями). Повысилась концентрация мононуклеаров, стимулирующих апоптоз и влияющих на процесс репаративной регенерации (процесс заживления). Отмечена тенденция к стимуляции пролиферативной активности (фактически тенденция к усилению репаративной регенерации) мононуклеаров, эпителиоцитов, а также усиление стимуляции их дифференцировки. В контрольной группе изменения были статистически значимо менее выражены и могут быть связаны с естественными репаративными процессами.
Статистически значимых изменений объема предстательной железы по данным трансректального УЗИ, показателей гемодинамики в предстательной железе (пиковая систолическая скорость, индекс резистентности) по данным допплерографии в обеих группах выявлено не было.
Оценка безопасности терапии в обеих группах проведена по показателям общих клинических анализов мочи и крови, биохимического анализа крови (общий белок, креатинин, мочевина, билирубин, щелочная фосфатаза, АСТ, АЛТ, глюкоза). Ни в основной, ни в контрольной группах до и после лечения данные показатели не выходили за пределы референсных значений, что свидетельствует о хорошей переносимости и безопасности препарата.
Заключение. В настоящее время витапрост® плюс, представляющий собой сочетание простаты экстракта и антимикробного препарата ломефлоксацина, является эффективным лекарственным средством терапии ХБП.
Несомненные достоинства препарата, такие как пролонгированное действие, способность проникать через гематопростатический барьер, воздействовать на грамотрицательные бактерии-уропатогены, а также хорошая переносимость, позволяют с успехом использовать его для лечения больных ХБП.


