Введение. Трансректальная биопсия простаты и уретроцистоскопия – часто проводимые урологические процедуры, что обусловлено актуальностью ранней диагностики наиболее распространенных онкоурологических заболеваний у мужчин: рака предстательной железы и мочевого пузыря. Оба вмешательства инвазивные. Частота инфекционно-воспалительных осложнений после указанных процедур колеблется в пределах от 2 до 10% [1–3]. Наряду с этим от 5 до 20% пациентов длительное время отмечают дизурию, боли в малом тазу и в мошонке, гематурию, гемоспермию, различные нарушения половой функции. Безусловно, наличие подобных случаев вызывает дополнительные сомнения, страхи и боязнь у пациентов, которым предстоит выполнение данных манипуляций. В стандартных случаях после биопсии и уретроцистоскопии назначают кратковременный курс антибактериальной терапии и противовоспалительное лечение [1–3]. Однако нередко после подобных диагностических процедур пациенты отмечают снижение качества жизни, что чаще всего связано с неадекватной реабилитацией.
Препарат Витапрост® положительно зарекомендовал себя при использовании для профилактики и лечения хронического простатита, а также терапии расстройств мочеиспускания после перенесенной трансуретральной резекции простаты [4–6]. Для усиления терапевтического эффекта было решено использовать сочетание различных фармацевтических форм (суппозитории ректальные+таблетки) для улучшения реабилитации пациентов, достижения максимального терапевтического эффекта и комплаентности после выполненных диагностических урологических процедур (биопсия простаты, уретроцистоскопия).
Обоснованием выбранного исследования служит благоприятное действие, оказываемое препаратом Витапрост® на ткани простаты, что усиливает противовоспалительный эффект, препятствует развитию фиброза, ускоряет регенерацию тканей и способствует восстановлению кровотока в поврежденных зонах простаты (после биопсии простаты). Кроме того, препарат оказывает благоприятное влияние на ткани предстательной железы.
Целью исследования стала оценка эффективности и безопасности назначения Витапроста (суппозитории и таблетки) в сочетании со стандартной противовоспалительной терапией для реабилитации пациентов, перенесших биопсию простаты и уретроцистоскопию с биопсией мочевого пузыря.
Материалы и методы. С января по июль 2015 г. в ГКБ № 57 под наблюдением находились 90 мужчин, которым были проведены инвазивные урологические диагностические вмешательства (биопсия простаты, уретроцистоскопия). Для исследования были отобраны пациенты в возрасте от 50 до 70 лет с сохранной половой функцией, без признаков инфекций мочеполовых путей до процедуры, готовые следовать указаниям врача и проходить контрольные обследования.
У 63 пациентов уровень простатспецифического антигена (ПСА) был выше 4 нг/мл, и 27 мужчин ранее перенесли трансуретральную резекцию мочевого пузыря по поводу мышечно-неинвазивного рака мочевого пузыря. Критерии исключения: инсулинозависимый сахарный диабет и активный гепатит С. Пациенты, которые не явились на контрольные обследования, также были исключены из исследования.

Перед включением в исследование пациенты подписывали информированное согласие.
После проверки соответствия критериям включения пациенты были рандомизированы на две группы. В основную группу вошли 28 больных после биопсии простаты и 12 – после цистоскопии с биопсией мочевого пузыря, в контрольную – 35 и 15 соответственно. Всем пациентам в течение первых 5 дней после процедуры проведена стандартная антибактериальная (ципрофлоксацин 250 мг 2 раза в сутки перорально), противовоспалительная (свечи с индометацином 50 мг, 1 свеча 2 раза в день) и гемостатическая терапия. Пациентам основной группы дополнительно назначали Витапрост® форте первые 10 дней в виде ректальных суппозиториев с последующим переходом на таблетированную форму Витапроста на аналогичный срок. Больные контрольной группы получали только вышеописанную стандартную терапию.
Шестидесяти трем пациентам была проведена трансректальная пункционная биопсия простаты по стандартной методике по 6 биоптатов из каждой доли, в ходе которой осуществлено также пальцевое ректальное исследование. Вмешательство выполнено под трансректальным ультразвуковым контролем (ультразвуковой аппарат Aloka с биплановым ректальным датчиком с частотой 5–7,5 MГц) биопсийным пистолетом «ProMag 2.5» с иглами 18-го калибра и глубиной вкола 20–22 мм.
Двадцати семи пациентам была проведена уретроцистоскопия с биопсией мочевого пузыря. Перед введением цистоскопа осуществлена внутриуретральная инстилляция геля-любриканта и смазан тубус ригидного цистоскопа для снижения риска травмы уретры и предстательной железы. Во всех случаях использовали ригидный цистоскоп фирмы «Karl Storz» № 22 Fr. Осмотр мочевого пузыря проведен с использованием 12° и 30° оптики, биопсия — «холодными» щипцами по стандартной методике из подозрительных участков.
На 5-й день после вмешательства проведен мониторинг субъективных (I-PSS, QoL, ИЭФ, оценка болевого синдрома по визуальной аналоговой шкале [ВАШ], наличие гемоспермии после биопсии простаты) и объективных (уровень лейкоцитурии и эритроцитурии в общем анализе мочи, объем простаты и максимальная объемная скорость мочеиспускания [Qmax]) показателей. Через 1 мес. после проведения биопсии простаты или мочевого пузыря было проведено контрольное обследование для оценки параметров эффективности (вышеуказанные субъективные и объективные показатели) и безопасности (развитие нежелательных явлений, отклонения в лабораторных показателях крови и мочи) проведенного лечения.
Полученные результаты занесены в базу данных Microsoft Excel и с помощью встроенных статистических формул произведен расчет среднего значения, стандартного отклонения. Значимость межгрупповых отличий оценена с помощью критерия Стьюдента, достоверным считалось р<0,05.
Результаты. Как видно из табл. 1, по клинико-лабораторным показателям группы были сопоставимыми. В группе пациентов, которым проведена биопсия простаты, симптоматика нижних мочевыводящих путей была легкой или средней степени. Показатели ВАШ общего самочувствия в обеих группах свидетельствовали об исходном хорошем самочувствии пациентов. Объем простаты в обеих группах практически не отличался, показатели максимальной объемной скорости были выше 13 мл/с. Уровень ПСА в группах варьировался от 4 до 5,2 нг/мл.
Данные, представленные в табл. 2, свидетельствуют о негативном влиянии биопсии простаты и биопсии мочевого пузыря на субъективные и объективные показатели пациентов. На 5-е сутки после проведения биопсии отмечено увеличение показателя I-PSS, более выраженное в контрольной группе. Аналогичная тенденция имела место и в отношении качества, а также общего самочувствия (см. табл. 2). Показатель короткого варианта шкалы МИЭФ на этапе промежуточного контроля мы не использовали в связи с небольшим сроком после проведения биопсии. При оценке объективных показателей на 5-е сутки после биопсии в обеих группах было отмечено снижение Qmax и увеличение объема простаты (на 14,5 и 47% в основной и контрольной группах соответственно) за счет ее отека.
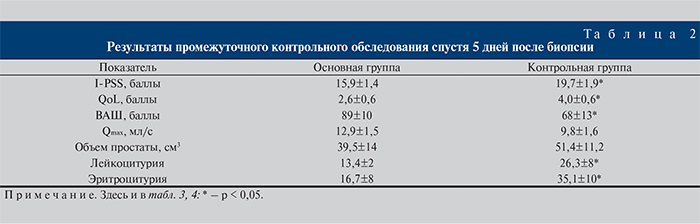
Изменения в общем анализе мочи отражают воспалительные изменения, характерные для пациентов, перенесших инвазивное вмешательство на нижних мочевыводящих путях. По сравнению с исходными данными в обеих группах наблюдалось увеличение количества лейкоцитов и эритроцитов, причем в контрольной группе эти показатели были в 2 раза больше, чем в основной.
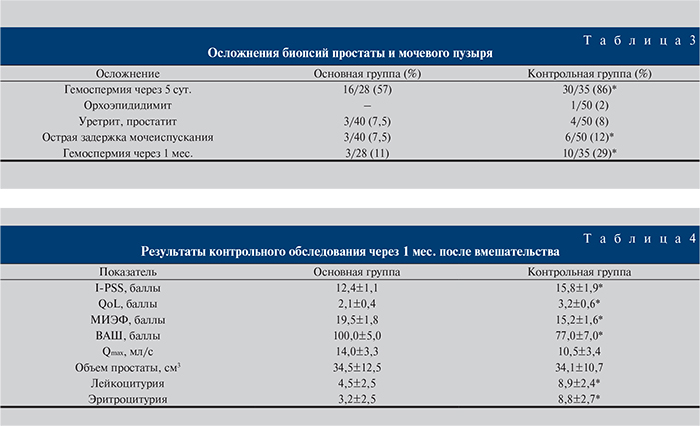
Общая частота осложнений оказалась невысокой и не превысила 10% в обеих группах (табл. 3).
Обращает на себя внимание меньшая частота гемоспермии (57 против 86%) и острой задержки мочеиспускания (7,5 против 12%) в основной группе по сравнению с контрольной.
Как видно из табл. 4, через 1 мес. после выполненного вмешательства практически по всем анализируемым показателям статистически значимое преимущество продемонстрировали пациенты основной группы.
Не было отмечено случаев нежелательных явлений, связанных с применением препарата Витапрост. Кроме того, прием Витапроста не сопровождался отклонениями лабораторных показателей.
Обсуждение. Разработка и последующее внедрение в клиническую практику последних технических усовершенствований (роботическая и лапароскопическая хирургия предстательной железы, биполярная и лазерная хирургия мочевого пузыря) определили актуальность своевременной диагностики рака мочевого пузыря и предстательной железы на ранних стадиях в связи с тем, что функциональные и онкологические результаты данных методов позволяют значительно улучшить не только онкологические результаты лечения, но и повысить качество жизни пациентов [1–3].
Биопсия простаты и уретроцистоскопия в сочетании с биопсией мочевого пузыря являются рутинным урологическим вмешательством. Качество выполнения последних зависит от технической оснащенности, навыков и опыта врача, выполняющего данные манипуляции, а также от оснащенности патоморфологической службы и опыта морфолога, консультирующего полученный гистологический материал.
Несмотря на кажущуюся малотравматичность, проведение данных манипуляций сопряжено с риском развития серьезных осложнений. Помимо геморрагических, нередко возникают инфекционно-воспалительные осложнения, такие как острый простатит, орхоэпидимит и даже бактериально-токсический шок, что служит существенным недостатком данных вмешательств. Многие пациенты, будучи информированными врачами о возможности их развития, воздерживаются от выполнения биопсии, что в некоторых случаях приводит к поздней диагностике онкоурологических заболеваний мочевого пузыря и простаты.
В ряде случаев последствием биопсии является усугубление хронического воспалительного процесса в предстательной железе. Ятрогенная травма предстательной железы обусловливает ее увеличение в размерах за счет воспалительного отека и участков геморрагии; впоследствии в данных зонах развивается рубцовая ткань, что в свою очередь усугубляет нарушение функции простаты. Одним из негативных последствий для пациентов, которым выполняется биопсия предстательной железы, помимо онкологической настороженности является боязнь попадания на операционный стол в связи с прогрессирующими симптомами нижних мочевыводящих путей. В отсутствие последующего надлежащего лечения биопсия простаты и мочевого пузыря может стать триггером к усугублению симптомов мочевыводящих путей. Вышеуказанные факты делают важным, с одной стороны, определение показаний к проведению инвазивных урологических вмешательств, с другой – разработку методов реабилитации предстательной железы после выполнения инвазивных вмешательств.
Результаты наших предыдущих работ, свидетельствующие об эффективности использования препарата Витапрост плюс®, суппозитории ректальные, после выполнения трансуретральной резекции предстательной железы [6], а также возрастающая популярность применения цитомединов в урологической практике [4, 5] послужили научно-практическим обоснованием для проведения настоящего исследования.
Компанией Нижфарм, входящей в холдинг STADA CIS, был разработан препарат Витапрост® форте, суппозитории ректальные. Один суппозиторий содержит 100 мг экстракта простаты. Витапрост® Форте оказывает органотропное действие на предстательную железу: уменьшает выраженность отека, лейкоцитарной инфильтрации, нормализует секреторную функцию эпителиальных клеток, увеличивает число лецитиновых зерен в секрете ацинусов, стимулирует мышечный тонус мочевого пузыря, а также улучшает микроциркуляцию за счет уменьшения тромбообразования, антиагрегантной активности, препятствует развитию тромбоза венул в предстательной железе. Кроме влияния на ткани предстательной железы препарат улучшает микроциркуляцию крови в стенке мочевого пузыря за счет вазодилатации неповрежденных сосудов и этим способствует восстановлению доставки кислорода в ткани, испытывающие гипоксию, что стимулирует физиологическую репарацию. Оказывает противовоспалительное действие за счет улучшения трофики стенки мочевого пузыря и стимуляции регенераторных процессов. Активация органного кровотока способствует повышению адаптационной и сократительной активности детрузора, увеличивая емкость мочевого пузыря. Витапрост® Форте способствует нормализации параметров предстательной железы и эякулята, уменьшает боль и дискомфорт, устраняет дизурию, улучшает половую жизнь [4, 5].
Поскольку основными показаниями к применению препарата Витапрост® служат хронические заболевания и состояния (хронический простатит, доброкачественная гиперплазия предстательной железы, синдром гиперактивного мочевого пузыря), для лечения которых требуются длительные и нередко повторные курсы терапии, для удобства пациентов была разработана другая лекарственная форма – Витапрост® таблетки.
Для реабилитации пациентов после выполнения инвазивных урологических вмешательств мы использовали следующую терапевтическую схему: в течение 10 дней применяли суппозитории с последующим переходом на таблетированную форму препарата также в течение 10 дней. Полученные результаты выявили статистически значимое уменьшение выраженности симптомов заболевания по шкале I-PSS, улучшение качества жизни, более выраженное снижение объема простаты и увеличение Qmax в группе пациентов, которым проводилась терапия препаратом Витапрост®. Кроме того, продемонстрировано достоверное преимущество в отношении снижения показателей эритроцитурии и лейкоцитурии как на 5-е сутки, так и спустя 1 мес. после вмешательства.
Немаловажным фактором служит комфортность применения препарата (однократный прием), что позволяет достигать высокой комплаентности у пациентов. Витапрост® в таблетках применялся пациентами дважды в день, однако ни один пациент не выбыл из исследования по причине пропуска приема препарата.
Заключение. Накопленный опыт позволяет нам рекомендовать суппозитории ректальные Витапрост® форте 10 дней и таблетки Витапрост® 10 дней в качестве реабилитационной схемы после проведения инвазивных урологических вмешательств.



